 图 1
nMg/nAl对催化剂活性的影响
Figure 1.
Effect of nMg/nAl on catalytic activity
图 1
nMg/nAl对催化剂活性的影响
Figure 1.
Effect of nMg/nAl on catalytic activity

Citation: LIU Shou-Qing, LI Xue-Mei, HE Xian-Wu, LIU Xiang-Yi, ZHENG Zhi-Feng. Synthesis and Characterization of Solid Base Catalyst Na2O/Al2O3-MgO with High Activity[J]. Chinese Journal of Inorganic Chemistry, 2017, 33(7): 1153-1160. doi: 10.11862/CJIC.2017.141

高活性固体碱Na2O/Al2O3-MgO的合成与表征
English
Synthesis and Characterization of Solid Base Catalyst Na2O/Al2O3-MgO with High Activity
-
由高温煅烧制备的镁铝双金属氧化物具有比表面积大、热稳定性好、机械强度高且同时具备酸碱活性中心等优点[1-2],成为重要的催化剂载体。其中,以其为载体制备的固体碱经常用作甲酯化反应[3]及Baeyer-Villiger氧化重排[4]反应的催化剂。但镁铝双金属氧化物的制备过程需以NaOH与Na2CO3配制的混合碱液[5-6]为沉淀剂,该混合碱液的配比及用量会对载体的结构产生较大影响,因此严格控制混合碱液的配比及体系pH值是开发高活性催化剂的关键。另外,镁铝双金属氧化物前驱体的制备过程往往产生大量的废酸废碱,由此导致的环境污染问题严重,若从绿色化学的角度分析,可以发现该制备工艺并非理想的生产过程,为此本研究提出了以氨水为沉淀剂,辅以碳酸钠浸渍、老化再焙烧处置的固体碱Na2O/Al2O3-MgO制备方法。为获得以该方法制备Na2O/Al2O3-MgO的较佳工艺,本研究选取蒜头果油为研究对象,将不同条件下所得固体碱用于蒜头果油的甲酯化过程,通过其甲酯化率评价催化剂的活性,并借助XRD、SEM、SEM-EDS、TG-DSC、N2吸附-脱附等手段对其结构性能进行表征,最终获得了该固体碱的较佳制备工艺,从而为以镁铝双金属氧化物为载体的高效催化剂的开发及制备提供新的研究思路。
1 实验部分
1.1 试剂与仪器
蒜头果油,购自云南省富宁县,采用乙醚索氏提取法提取,其中亚油酸含量1.9%、亚麻酸1.5%、棕榈酸0.8%、油酸32.2%、花生一烯酸2.5%、芥酸14.8%、神经酸46.2%。
Mg(NO3)2·6H2O、Al(NO3)3·9H2O、Na2CO3、氨水、甲醇、Na2SO4,以上试剂均为分析纯试剂;棕榈酸甲酯、油酸甲酯、亚油酸甲酯、亚麻酸甲酯、花生一烯酸甲酯、芥酸甲酯、神经酸甲酯、正庚烷,以上试剂均为色谱纯试剂。
7890A型气相色谱仪(安捷伦科技有限公司)、D40型电动搅拌机、电磁搅拌器、BS224S电子天平、HH-S型恒温水浴锅、DHG-9240A鼓风干燥箱、KSW马弗炉、Pyris 1TGA热重分析仪(美国Perkin-Elmer公司)、ASAP 2020物理吸附仪(美国Micromeritics公司)、KYKY-100B扫描电子显微镜(美国Tracor Northern公司)、日本D/max-2500X型X射线衍射仪。
1.2 实验过程
1.2.1 固体碱Na2O/Al2O3-MgO的制备
先将Mg(NO3)2·6H2O和Al(NO3)3·9H2O按一定物质的量之比配成溶液,然后滴加1:5(V/V)的氨水至pH值为9~10,静置4 h,过滤,继而将沉淀浸入15%的Na2CO3水溶液中,经老化(60℃),过滤、烘干、焙烧制得催化剂。
1.2.2 催化剂表征
采用X射线衍射仪对催化剂进行XRD表征,辐射源Cu Kα,波长0.154 06 nm,2θ扫描范围为5°~90°,步长0.02°,扫描速率为6°·min-1,管电流为120 mA,管电压为40 kV。采用扫描电子显微镜观察样品表面样貌,加速电压10 kV,样品采用喷金处理。采用热重分析仪对样品进行TG-DSC测定,升温速率为20 ℃·min-1,升温范围为40~900 ℃,N2气氛,流速20 mL·min-1,参比物为Al2O3。采用物理吸附仪进行N2吸附-脱附实验,样品先在150 ℃下脱气12 h,然后在-195.8 ℃下进行测定,以BET法计算催化剂的比表面积。
1.2.3 催化剂活性评价
催化剂活性以蒜头果油甲酯化转化率高低进行评价。转化率计算公式为:
其中m1为甲酯质量(g);ms为样品质量(g)。产物中脂肪酸甲酯含量采用外标法以气相色谱仪进行测定,准确称取0.1 g左右的甲酯化产物于10 mL容量瓶中,以正庚烷定容后进样,色谱条件为:色谱柱HP-INOWAX,30 m×0.32 mm×0.25 μm;FID检测器,检测器温度300 ℃;程序升温,初始温度170 ℃,保持1 min, 然后以10 ℃·min-1升温到230 ℃, 保持1 min, 再以2 ℃·min-1升温至250 ℃, 保持10 min;H2流量40 mL·min-1,空气流量400 mL·min-1,N2流量30 mL·min-1; 分流进样, 分流比10:1, 进样量1 μL。
1.2.4 甲酯化操作
按参考文献[7]进行实验, 其中醇油物质的量比为10:1,催化剂用量为油质量的2.5%,反应温度65 ℃, 反应时间4 h。
2 结果与讨论
2.1 镁铝离子物质的量之比对催化剂活性的影响
图 1为不同镁铝离子物质的量之比(以下以nMg/nAl表示)时所得催化剂对蒜头果油甲酯化的催化效果。由图 1可以看出,不同的nMg/nAl下所得催化剂的反应活性有较大差别,当nMg/nAl在3:1~1:3范围内,催化剂具有最高活性,此时蒜头果油甲酯转化率均超过了90%。
催化剂的活性与其活性中心含量及结构有直接关系。本研究所制催化剂是以氨水为沉淀剂先使Mg2+、Al3+形成共沉淀,再以Na2CO3溶液进行浸渍、老化处理,最终借助高温焙烧制得。由于氨水为弱碱,因此不会因过量而导致Al3+形成AlO2-流失,而以Na2CO3溶液进行浸渍、老化处理时,由于所得Mg-Al共沉淀为凝胶状细小颗粒,有利于CO32--在溶解-沉淀的动态平衡下逐渐进入Mg-Al共沉淀的内部,根据邓欣等[8, 10]对纳米晶镁铝水滑石形成机制的研究可以认为,当CO32--进入Mg-Al共沉淀的内部时,其将发挥柱撑离子的作用,使Mg-Al共沉淀形成类水滑石片层结构,而作为活性中心的Na+会作为电荷平衡离子被留存于前驱体中。恰当的nMg/nAl可有助于类水滑石片层结构的形成,根据Leont′eva等[11]的研究,当nMg/nAl=4:1~2:1时,可形成类水滑石的片层结构,而Paul等[12]则在nMg/nAl=1:1、1:3时,制备了镁铝水滑石,本研究亦选取了nMg/nAl=5:1、1:1、1:5的催化剂及其前驱体进行了SEM表征,结果见图 2。由图 2(a)~(c)可以看出,当nMg/nAl=1:1时,催化剂前驱体的确形成了较完美的片层结构,而其它2种离子比时,所得前驱体的形貌均为絮状结构;而图 2(d)~(f)为对应离子比下所得催化剂的SEM图,与图 2(a)~(c)比较可以发现,催化剂的基本形貌特征并未因焙烧处理而发生根本性变化,只是nMg/nAl=1:1的前驱体在经焙烧处理后,其原有较紧密的片层结构变的相对疏松,这主要是由于柱撑离子CO32--、层板羟基OH-在焙烧处理过程中会转变为CO2及水并从前驱体中逸出,导致原有紧密片层结构发生一定的崩解造成的。因此结合图 1可以认为,采用本研究所用方法制备Na2O/Al2O3-MgO催化剂时,nMg/nAl在1:3~3:1之间形成了类水滑石片层结构。
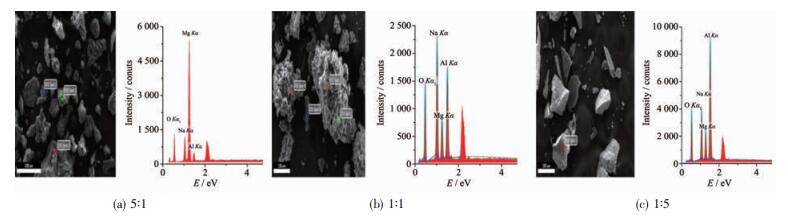
催化剂的微观结构会导致催化剂活性中心数量的变化,图 3为不同nMg/nAl下所得催化剂的SEM-EDS测定结果,而各元素的质量含量见表 1。由图 3及表 1可以看出,当nMg/nAl为5:1时,所得催化剂Na含量最低,仅有11.0%,而增大Al3+用量至nMg/nAl=1:1时,所得催化剂Na含量达到30.6%,继续增大Al3+用量,催化剂中Na含量又出现下降。在催化剂Na2O/Al2O3-MgO中,Na2O主要发挥活性中心的作用,Na含量的变化反映了催化剂活性中心的多少,当催化剂nMg/nAl=1:1时,催化剂活性中心最多,因此其催化活性最强。
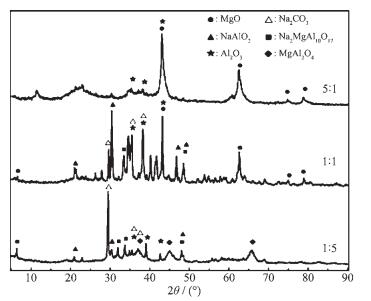
另外,nMg/nAl的变化还会引起催化剂物相组成的改变,进而影响到催化剂的活性。为对此进行验证,本研究选取nMg/nAl为5:1、1:1、1:5的催化剂进行了XRD分析,结果见图 4。由图 4可以看出,当nMg/nAl为5:1时,该物系主要存在MgO、Al2O3的衍射峰,而当nMg/nAl为1:1时,其XRD图除了存在明显的MgO、Al2O3衍射峰外,还存在NaAlO2、Na2Mg Al10O17及Na2CO3衍射峰,继续增加铝离子用量至nMg/nAl为1:5,其XRD图中除存在NaAlO2、Na2MgAl10O17及Na2CO3衍射峰外,还新形成了尖晶石相MgAl2O7,但MgO衍射峰消失。根据朱建华等[13]对负载型固体碱的研究发现,KNO3/ Al2O3及K2CO3/ Al2O3等催化剂之所以表现出强的碱性与K-Al氧化物的形成有直接关系,由此可以推断,nMg/nAl=1:1的催化剂表现岀较高催化活性的原因与形成Na-Al及Na-Mg-Al等氧化物有关。而nMg/nAl=1:5时,催化剂同样生成了Na-Al及Na-Mg-Al等氧化物,因此其反应活性明显高于nMg/nAl=5:1的催化剂,但由于此时还形成了尖晶石相MgAl2O7,该物相结构紧密,会使催化剂的比表面积有所下降,因此其活性比nMg/nAl=1:1时所得催化剂活性降低。
综上所述,制备Na2O/Al2O3-MgO催化剂的较佳nMg/nAl为3:1~1:3,此条件下催化剂具有较高催化活性。
2.3.2 老化时间对催化剂活性的影响
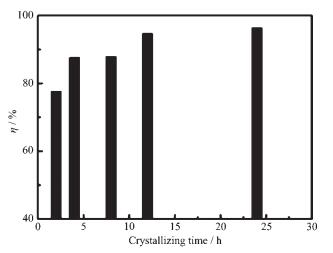
将Mg-Al氢氧化物共沉淀浸渍于Na2CO3溶液中进行老化处理时,CO32-会以柱撑离子形式进入Mg-Al共沉淀中,最终形成具有特定结构的前驱体,因此老化处理对制备Na2O/Al2O3-MgO催化剂至关重要。本研究以nMg/nAl为1:1的共沉淀为对象,在60 ℃老化温度下对其进行老化处理,考察老化时间为2、4、10、12、24 h下所得催化剂的催化活性,结果见图 5。由图 5可以看出,当老化时间小于12 h时,催化剂活性随老化时间延长而迅速升高,当达到12 h后,继续延长老化时间,催化剂的活性略有升高,但升高幅度较小。
图 6为老化时间分别为2、4、12 h时,nMg/nAl为1:1的催化剂前驱体SEM图,从图 6可以看出,老化2h时,Mg-Al氢氧化物共沉淀的表面开始出现部分的片层化,而随老化时间的延长,其片层化程度会向内部延伸,达到12 h后,前驱体的片层化程度已较高,结构亦较完美。综合图 5、图 6可以得出,较佳的老化时间为12 h。
2.3.3 焙烧温度对催化剂活性的影响
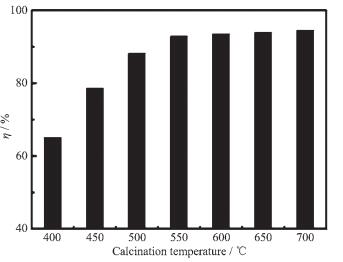
图 7为不同焙烧温度下,nMg/nAl为1:1时所得催化剂对蒜头果油甲酯化率的影响。由图 7可以看出,焙烧温度T < 550 ℃时,催化剂的活性随焙烧温度的升高迅速增加,超过550 ℃后,继续升高温度,催化剂的活性略有增加,但升高幅度较小。
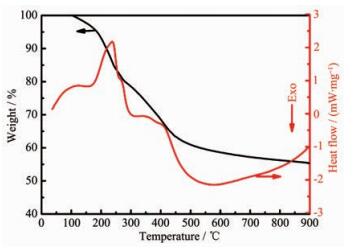
图 8为nMg/nAl=1:1时催化剂前驱体的TG-DSC曲线。由图 8 TG曲线可以看出,该前驱体在T < 200 ℃时,失重速率较慢,仅失重6%左右,当温度在200~500 ℃之间时,失重较快,失重率接近35%,继续升高温度,失重曲线近似出现一平台,催化剂分解完全。在200 ℃以内,前驱体的失重主要为表面残留的自由水、催化剂层间及内部的非结合水失去造成的;而继续升高温度,催化剂中Mg-Al氢氧化物、残留NaNO3开始大量分解产生H2O及NxOy,并与层板羟基[14]、柱撑离子CO32--分解产生的H2O、CO2等一起以气态形式快速逸出,造成质量迅速下降,失重率急剧升高;当超过500 ℃后,催化剂中可分解成分已基本分解完毕,此时继续升温,催化剂失重率不再明显增加。而由图 8 DSC曲线可以发现,在237 ℃左右,存在强吸热峰,主要可能是Mg-Al氢氧化物、NaNO3、柱撑CO32--分解吸收热量所致,超过550 ℃后,DSC曲线存在较宽的放热峰并呈现向吸热方向的斜坡,可能与催化剂中Na2MgAl10O17的形成有关。
焙烧温度会对催化剂的活性中心数目、物相组成、比表面积及结构等产生影响[15],结合图 8可以看出,焙烧温度过低,前驱体分解不完全,产生的活性中心不足,此时催化剂活性较低。而本研究仅对400~700 ℃的焙烧温度进行了考察,之所以未超过700 ℃,一方面是考虑到焙烧温度越高,能源消耗越大,会引起生产成本增加,另一方面,由图 4可知,催化剂中存在Al2O3,而较高的焙烧温度会导致Al2O3由γ型向比表面积相对较小的α型或β型转变[16],且过高的焙烧温度还会造成颗粒团聚、晶粒增大,反而不利于催化剂活性的提高。结合图 7可以看出,当焙烧温度为550~700 ℃时,催化剂具有较高的催化活性,表明此温度范围内,前驱体已能分解完全且尚未出现过度烧结,综合考虑催化剂的催化效率及能源节约两个方面,可以得出较佳的焙烧温度应控制在550 ℃左右。
2.3.4 焙烧时间对催化剂活性的影响
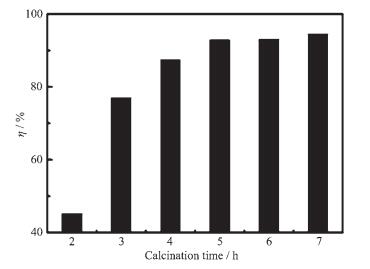
图 9为焙烧温度550 ℃时,焙烧时间对催化剂活性的影响,由图 9可以看出,焙烧时间超过5 h后,催化剂的活性基本不再随焙烧时间的延长而增加。催化剂中Mg-Al氢氧化物的分解及柱撑离子CO32--等的失去需要时间,当焙烧时间少于5 h时,其分解并不完全,活性中心不足,而焙烧时间达到5 h后,催化剂中各成分已分解完全,继续延长焙烧时间,催化剂的活性不会出现较大幅度升高。由此可见,较佳的焙烧时间为5 h。
2.3.5 验证实验
由上述单因素实验可以发现,采用氨水为沉淀剂并辅以Na2CO3浸渍,可以制备具有类水滑石结构的Na2O/Al2O3-MgO催化剂。其较佳工艺条件为:nMg/nAl=3:1~1:3、60 ℃下老化12 h、焙烧温度为550 ℃、焙烧5 h。
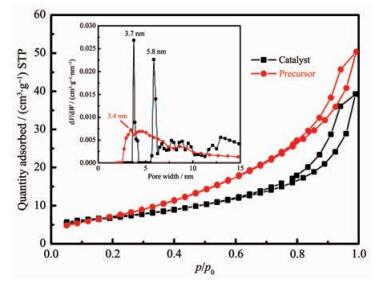
本研究分别按较佳制备工艺制备了nMg/nAl=3:1、1:1、1:3的催化剂及前驱体,并对其在-195.8 ℃下进行了N2的吸脱附等温线测定,所得性能参数见表 2,而nMg/nAl=1:1的等温线及孔径分布曲线见图 10。由表 2可以看出,3种离子比下所得催化剂前驱体经焙烧处理制成催化剂后,其比表面积及孔容均有所增大,而就孔径而言,除nMg/nAl=1:3时略有下降外,其余均有所增大,这可能与催化剂在焙烧处理时,OH-及柱撑离子CO32--等转化为CO2、H2O并逸出,导致催化剂结构变得疏松,并形成不规则孔洞有关。由图 10可以看出,前驱体及催化剂的吸脱附等温线在p/p0相对较高的区域出现滞后环,表明此工艺所得催化剂及前驱体属于介孔类材料,对照ICPAC标准物理吸附等温线的分类可以发现,此滞后环与H3型类似,因而可进一步证明该法所得催化剂及前驱体存在片层颗粒、片层间存在狭缝[17]。催化剂前驱体经焙烧处理后比表面积、孔容、孔径的增大使得反应物料更容易在催化剂内部扩散并与更多活性中心接触,有利于提高催化剂的催化活性。以nMg/nAl=1:1时制备的催化剂进行蒜头果油甲酯化实验,重复3次,蒜头果油甲酯化率均超过90%,最高达到96.4%。
 表 2
催化剂及前驱体的比表面积、总孔容及平均孔径
Table 2.
Specific surface area (SBET), total pore volume (VT) and average pore size (d) of catalyst and precursor
表 2
催化剂及前驱体的比表面积、总孔容及平均孔径
Table 2.
Specific surface area (SBET), total pore volume (VT) and average pore size (d) of catalyst and precursor

3 结论
采用氨水沉淀,再以Na2CO3进行浸渍、老化处理,可以获得具有类水滑石结构的催化剂前驱体,对其进行焙烧处理可以获得具有疏松片层结构的Na2O/Al2O3-MgO催化剂。通过XRD、SEM-EDS分析发现不同nMg/nAl会影响催化剂的物相组成及活性中心数量,具有较高催化活性的Na2O/Al2O3-MgO催化剂中形成了Na-Al及Na-Mg-Al氧化物,通过TG-DSC分析可以发现,前驱体的分解主要发生在200~500 ℃之间,其中在237 ℃时出现较强吸热峰,主要为Mg-Al氢氧化物及NaNO3大量分解、柱撑离子CO32--失去造成的,而超过550 ℃后,DSC曲线出现较宽的放热峰,可能与Na2MgAl10O17的形成有关。蒜头果油甲酯化的单因素实验表明,催化剂的较佳制备条件为:nMg/nAl=3:1~1:3、60 ℃下老化12 h、焙烧温度为550 ℃、焙烧5 h,此时催化剂具有较高的催化活性。选择nMg/nAl=1:1的催化剂进行验证实验,蒜头果油的甲酯化率最高达到96.4%。
-
-
[1]
Wang H, Duan W Z, Wu Y, et al. Inorg. Chim. Acta, 2014, 418:163-170 doi: 10.1016/j.ica.2014.04.031
-
[2]
李玉芹, 曾虹燕.工业催化, 2005, 13(12):37-42 doi: 10.3969/j.issn.1008-1143.2005.12.009LI Yu-Qin, ZENG Hong-Yan. Ind. Catal., 2005, 13(12):37-42 doi: 10.3969/j.issn.1008-1143.2005.12.009
-
[3]
Wang Y T, Fang Z, Zhang F, et al. Bioresour. Technol., 2015, 193:84-89 doi: 10.1016/j.biortech.2015.06.059
-
[4]
Jiménez-Sanchidrián C, Hidalgo J M, Llamas R, et al. Appl. Catal., A, 2006, 312(2/3):86-94
-
[5]
董金龙, 任跃红, 张跃文.应用化工, 2010, 39 (7):1058-1059DONG Jin-Long, REN Yue-Hong, ZHANG Yue-Wen. Appl. Chem. Ind., 2010, 39 (7):1058-1059
-
[6]
程月, 王泽青, 王程星, 等.应用化工, 2011, 40 (4):637-644CHENG Yue, WANG Ze-Qing, WANG Cheng -Xing, et al. Appl. Chem. Ind., 2011, 40 (4):637-644
-
[7]
刘守庆, 李雪梅, 赵雷修, 等.中国油脂, 2012, 37(7): 59-62LIU Shou-Qing, LI Xue-Mei, ZHAO Lei-Xiu, et al. China Oils Fats, 2012, 37(7): 59-62
-
[8]
吴玉秀, 李永丹, 张全忠, 等.石油化工, 2003, 32(9):800-804WU Yu-Xiu, LI Yong-Dan, ZHANG Quan-Zhong, et al. Petrochem. Technol., 2003, 32(9):800-804
-
[9]
邓欣, 曾虹燕, 冯震.功能材料, 2007, 38(6):965-967DENG Xin, ZENG Hong-Yan, FENG Zhen. J. Funct. Mater., 2007, 38(6):965-967
-
[10]
杨飘萍, 宿美平, 杨胥微, 等.无机化学学报, 2003, 19(5):485-490 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?flag=1&file_no=20030507&journal_id=wjhxxbcnYANG Piao-Ping, SU Mei-Ping, YANG Xu-Wei, et al. Chinese J. Inorg. Chem., 2003, 19(5):485-490 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?flag=1&file_no=20030507&journal_id=wjhxxbcn
-
[11]
Leont′eva N N, Cherepanova S V, Drozdov V A. J. Struct. Chem., 2014, 55(7):1326-1341 doi: 10.1134/S0022476614070142
-
[12]
Paul M, Pal N, Mondal J, et al. Chem. Eng. Sci., 2012, 71: 564-572 doi: 10.1016/j.ces.2011.11.038
-
[13]
朱建华, 王英, 淳远, 等.化学物理学报, 1998(2): 178-183ZHU Jian-Hua, WANG Ying, CHUN Yuan, et al. Chin. J. Chem. Phys., 1998(2): 178-183
-
[14]
王豪, 吴雁, 贾艳秋, 等.石油与天然气化工, 2010, 39(5): 406-410WANG Hao, WU Yan, JIA Yan-Qiu, et al. Chem. Eng. Oil Gas, 2010, 39(5): 406-410
-
[15]
连奕新, 王会芳, 张元华, 等.石油化工, 2009, 38(6):622-629LIAN Yi-Xin, WANG Hui-Fang, ZHANG Yuan-Hua, et al. Petrochem. Technol., 2009, 38(6):622-629
-
[16]
吴玉程, 宋振亚, 杨晔, 等.稀有金属, 2004, 28(6):1043-1048WU Yu-Cheng, SONG Zhen-Ya, YANG Ye, et al. Rare Met., 2004, 28(6):1043-1048
-
[17]
Othman M. Chem. Eng. Sci., 2009, 64(5):925-929
-
[1]
-
表 1 不同nMg/nAl时所得催化剂的元素含量
Table 1. Element content of catalysts prepared with different nMg/nAl

表 2 催化剂及前驱体的比表面积、总孔容及平均孔径
Table 2. Specific surface area (SBET), total pore volume (VT) and average pore size (d) of catalyst and precursor

-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 4
- 文章访问数: 574
- HTML全文浏览量: 102




 下载:
下载:









 下载:
下载:

