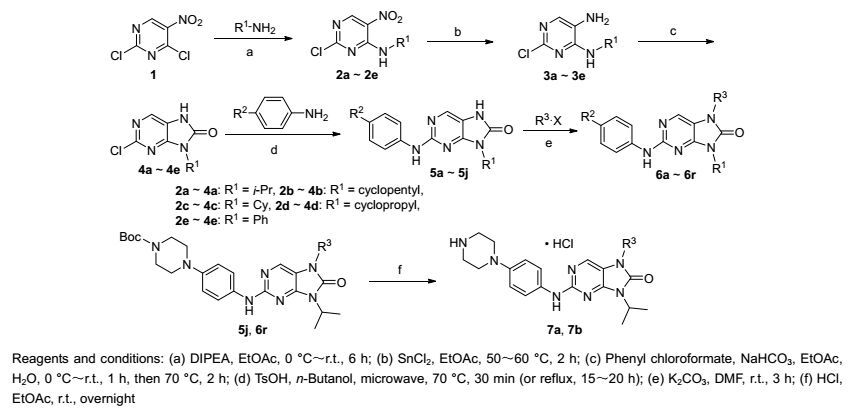
 图式 1
目标化合物的合成
Scheme1.
Synthetic route of the target compounds
图式 1
目标化合物的合成
Scheme1.
Synthetic route of the target compounds

Citation: Zhang Zipeng, Yang Xinying, Fang Hao. Synthesis and Antiproliferative Activity of Novel Purin-8-one Derivatives[J]. Chinese Journal of Organic Chemistry, 2017, 37(6): 1479-1486. doi: 10.6023/cjoc201611031

新型嘌呤-8-酮衍生物的合成及抗肿瘤活性研究
English
Synthesis and Antiproliferative Activity of Novel Purin-8-one Derivatives
-
Key words:
- purine derivatives
- / antitumor
- / synthesis
-
嘌呤是一种广泛存在于自然界中的氮杂环类物质, 许多重要生物分子都含有嘌呤环结构[1, 2].嘌呤类物质可参与有机体的核酸合成、能量转移以及多种生理过程[3, 4].无论是自然存在还是人工合成的嘌呤类物质都被发现有着广泛的生物活性, 已有许多报道证实了嘌呤类物质可用于治疗各种疾病.当然, 嘌呤骨架的研究也在抗肿瘤药物中获得了很大的成功, 如奈拉滨[5]、替莫唑胺[6]、巯嘌呤[7]、Idelalisib[8]和R-Roscovitine[9]等均具有较好的抗肿瘤作用.
本课题组在前期嘌呤类抗肿瘤活性化合物的研究中发现[10, 11], 嘌呤环C(2) 位引入取代芳胺有利于提高活性, C(6) 位以苄胺或环己基甲胺等取代对活性的提高影响很小; 而N(9) 位引入异丙基和环戊基等基团活性较好.为进一步提高先导化合物的抑制肿瘤细胞增殖的效果, 我们在保留C(2) 位不同取代芳胺结构的基础上, 去除对活性影响不大的C(6) 取代基团, 尝试在N(7) 位引入不同的片段(包括含有氢键受体或供体、疏水性或含π电子的结构), 以期增加目标化合物与靶组织的结合力.对于N(9) 位的改造, 除了保留异丙基和环戊基以外, 还考察了其他环状取代基以便分析立体效应对活性的影响.最后根据生物电子等排原理, 将嘌呤母核替换为嘌呤-8-酮骨架, 设计、合成了一系列结构新颖目标化合物.具体合成路线见Scheme 1.
1 结果与讨论
1.1 目标化合物的合成
参考文献[12]方法合成中间体4a~4e:以2, 4-二氯-5-硝基嘧啶为起始原料, 与不同取代伯胺(R1NH2)反应后制得硝基嘧啶胺类中间体2a~2e, 该中间体经二氯亚锡还原得到中间体3a~3e, 再与氯甲酸苯酯发生缩合和环合反应后生成嘌呤中间体4a~4e.随后分别与不同取代苯胺经过芳香亲核取代反应即可制得目标化合物5a~5j.所得目标化合物5a~5j与卤代物(R3-X)反应后制得目标化合物6a~6r.目标化合物7a和7b的制备是以5j和6r为原料, 在酸性条件下脱除Boc保护基后得到.所有目标化合物均经1H NMR、13C NMR和HRMS结构确认.
1.2 目标化合物的抗肿瘤细胞增殖活性
我们选用Hela和HCT116肿瘤细胞株, 应用四甲基偶氮唑盐(MTT)法测试了所有目标化合物在50 μmol•L-1浓度下对肿瘤细胞的抗增殖活性.该方法根据活细胞线粒体中的琥珀酸脱氢酶可将黄色MTT还原为不溶于水的蓝紫色结晶甲臜为原理, 测定肿瘤细胞存活率, 也是抗肿瘤药物研究中表型筛选的重要方法[12].初筛测试结果(图 1)表明:多数化合物对HCT116细胞株的抑制作用差, 对Hela细胞株的抑制作用较好; 分析目标化合物的结构与Hela细胞株的抑制活性可发现, 嘌呤-8-酮N(7) 位引入乙酸乙基片段(6a、6c~6e和6l~6n)、丙酮片段(6b、6f和6p)及乙酸片段(6g和6q)的活性较差, 而引入丙基(6h)、烯丙基(6i)、炔丙基(6j)及苄基(6k)的活性明显提高; 当嘌呤-8-酮的N(9) 位为环已基(5f)或苯基(5h和6o)取代时, 化合物的活性较好; 而苯环上引入羟基(5a)、Boc-哌嗪基(5j)或哌嗪基(7a和7b)时, 化合物的活性也明显提高.
以母核为嘌呤类Ⅱ期临床抗肿瘤药R-Roscovitine作为阳性对照, 选择初筛抑制率大于60%的目标化合物(5a、5h、5j、6h、6i和6j), 测试其对MOLT-4、Hela、K562和HCT116四株肿瘤细胞株的抗增殖活性(表 2).结果表明, 这6个目标化合物抑制Hela肿瘤细胞株的活性(IC50=5~20μmol•L-1)相当或优于阳性对照药R-Roscovitine (IC50=15.86±0.42 μmol•L-1); 化合物5h、6h、6i和6j抑制MOLT-4肿瘤细胞株的活性(IC50=5~9 μmol•L-1)优于阳性对照药R-Roscovitine (IC50=17.77±0.83 μmol•L-1); 化合物5h、6h、6i和6j抑制K562肿瘤细胞株的活性(IC50=12~48 μmol•L-1)相当或优于阳性对照药R-Roscovitine (IC50=41.76±5.04μmol•L-1); 但这六个化合物对HCT116肿瘤细胞株的抑制活性(IC50>39 μmol•L-1)则不如阳性对照药R-Roscovitine (IC50=17.16±3.77 μmol•L-1).分析它们对不同肿瘤细胞株的抗增殖作用可知, 它们对于MOLT-4和Hela肿瘤细胞株的抑制作用优于其它两株肿瘤细胞株K562和HCT116.分析它们的结构可知, 在嘌呤-8-酮的N(9) 位引入苯基(5h), 在N(7) 位引入丙基(6h)、烯丙基(6i)或炔丙基(6j)可显著提高化合物的抗肿瘤活性.
2 结论
通过对本课题组前期发现的嘌呤类抗肿瘤先导化合物进行了新的结构改造, 引入嘌呤-8-酮作为母核结构, 设计、合成了30个结构全新的目标化合物.所有目标化合物均经1H NMR、13C NMR和HRMS结构确认.在活性评价中, 有多个化合物在50 μmol•L-1浓度下对Hela细胞株有明显抑制作用.其中活性目标化合物5h、6h、6i和6j抑制Hela、MOLT-4和K562肿瘤细胞株的活性相当或优于阳性对照药R-Roscovitine.上述结果为今后研究新型嘌呤类抗肿瘤药物提供了新的思路.
3 实验部分
3.1 仪器与试剂
RY-1型熔点仪(天津天光光学仪器分公司); Bruker-300MHz和Bruker-400MHz核磁共振波谱仪; Agilent 6520型高分辨电喷雾电离质谱仪; Thermo Varioskan Flash全波长多功能酶标仪; Thermo Forma3111型二氧化碳恒温培养箱; Olympus CKX31双目倒置显微镜.
合成实验中所用的试剂均为市售的分析纯或化学纯试剂, 纯度为97%~99%, 未经纯化直接使用.人急性淋巴母细胞白血病细胞MOLT-4、人子宫颈癌细胞Hela、白血病细胞K562、人结肠癌细胞HCT116和改良型RPMI1640培养基(美国Hyclone公司); 10% (体积分数)胎牛血清(美国Hyclone公司); 2.5 g•L-1胰蛋白酶(美国Gibco公司); 阳性对照药R-Roscovitine购自MedChemExpress (MCE)中国分公司.
3.2 化合物的合成
3.3 抗肿瘤活性实验
对30个目标化合物采用四甲基偶氮唑盐(MTT)法测定它们的体外抗肿瘤细胞增殖活性.选取的肿瘤细胞株为MOLT-4、Hela、K562和HCT116.
将处于对数生长期的肿瘤细胞, 用含10%(体积分数)胚牛血清的RPMI1640培养液调整细胞数(MOLT-4调整为105 cell•mL-1的细胞悬液; K562调整为5×104 cell•mL-1的细胞悬液; 贴壁细胞Hela和HCT116先用2.5 g•mL-1的胰蛋白酶消化后调整为4×104 cell•mL-1的细胞悬液), 接种于96孔培养板中, 37 ℃、5% CO2条件下培养6~8 h后, 加入待测浓度目标化合物, 继续培养48 h, 然后每孔加入20 μL MTT (5 mg•mL-1), 再培养4 h后弃去液体, 每孔加入200 μL DMSO, 于37 ℃恒温振摇15 min, 检测570 nm波长处的OD值, 计算抑制率及IC50值.
辅助材料(Supporting Information) 所有化合物的1H-NMR、13C-NMR和HRMS谱图.这些材料可以免费从本刊网站(http://sioc-journal. cn/)上下载.
3.2.5 目标化合物7a和7b的合成
向化合物5j (0.45 g, 1 mmol)中加入HCl的饱和乙酸乙酯溶液10 mL, 密封, 室温搅拌过液.反应完毕, 过滤即得目标产物9-异丙基-2-(4-(哌嗪-1-基)苯氨基)-7, 9-二氢-8H-嘌呤-8-酮盐酸盐(7a), 白色固体0.23 g, 产率59%. m.p.>260 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 11.50 (s, 1H), 10.27 (s, 1H), 9.23 (s, 2H), 7.96 (s, 1H), 7.48 (d, J=8.9 Hz, 2H), 7.05 (d, J=8.9 Hz, 2H), 4.58~4.48 (m, 1H), 3.44~3.29 (m, 4H), 3.29~3.12 (m, 4H), 1.47 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6)δ: 155.0, 153.4, 150.8, 146.9, 130.4, 122.8, 122.1, 117.4, 115.5, 46.3, 45.3, 42.8, 20.0; HRMS (AP-ESI) calcd for C18H25ClN7O[M+H]+: 354.2017, found 354.2041.
7-(2-羟乙基)-9-异丙基-2-(4-(哌嗪-1-基)苯氨基)-7, 9-二氢-8H-嘌呤-8-酮盐酸盐(7b):黄色固体, 产率53.8%. m.p.>260 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 10.20 (s, 1H), 9.44 (s, 2H), 8.20 (s, 1H), 7.50 (d, J=8.9 Hz, 2H), 7.05 (d, J=8.9 Hz, 2H), 4.62~4.54 (m, 1H), 3.92~3.77 (m, 2H), 3.73~3.57 (m, 2H), 3.43~3.31 (m, 4H), 3.30~3.10 (m, 4H), 1.49 (d, J=6.8 Hz, 6H); 13C NMR (100 MHz, DMSO-d6)δ: 154.0, 153.4, 150.6, 147.8, 129.3, 124.0, 121.7, 117.5, 117.3, 58.8, 46.4, 46.2, 44.4, 43.1, 19.6; HRMS (AP-ESI) calcd for C20H29ClN7O2[M+H]+: 398.2299, found 398.2290.
3.2.3 目标化合物5a~5j的合成
将中间体4a (0.21 g, 1 mmol)、对氨基苯酚(0.16 g, 1.5 mmol)和对甲苯磺酸(0.52 g, 3 mmol)混合, 加入正丁醇20 mL, 微波170 ℃反应30 min(或加热回流15~20 h).反应完成后, 反应液冷却至室温, 加入过量饱和NaHCO3(约50 mL)剧烈搅拌15 min过滤, 滤饼通过柱层析纯化(也可用甲醇进行重结晶)得目标化合物9-异丙基-2-(4-羟基苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(5a), 白色固体0.07 g, 产率25%. m.p. 244~246 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 10.80 (s, 1H), 8.92 (s, 1H), 8.88 (s, 1H), 7.86 (s, 1H), 7.46 (d, J=8.9 Hz, 2H), 6.66 (d, J=8.9 Hz, 2H), 4.57~4.49 (m, 1H), 1.48 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6)δ: 155.6, 153.2, 152.1, 151.1, 134.1, 133.4, 120.7, 115.3, 114.7, 44.1, 20.2; HRMS (AP-ESI) calcd for C14H16N5O2 [M+H]+: 286.1299, found 286.1295.
以下化合物5b~5j的合成与5a的合成相同, 其中5j的后处理过程与5a的不同.
9-异丙基-2-(4-甲氧基苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(5b):白色固体, 产率31%. m.p. 262~264 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 11.06 (s, 1H), 9.39 (s, 1H), 7.91 (s, 1H), 7.58 (d, J=9.0 Hz, 2H), 6.89 (d, J=9.0 Hz, 2H), 4.60~4.49 (m, 1H), 3.73 (s, 3H), 1.49 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6) δ: 153.7, 153.3, 152.2, 151.0, 132.7, 130.2, 120.1, 114.0, 113.2, 54.6, 43.3, 19.1; HRMS (AP-ESI) calcd for C15H18N5O2 [M+H]+: 300.14554, found 300.1454.
9-环戊基-2-(4-甲氧基苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(5c):白色固体, 产率64%. m.p. 259~260 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 10.87 (s, 1H), 9.01 (s, 1H), 7.90 (s, 1H), 7.60 (d, J=9.1 Hz, 2H), 6.84 (d, J=9.1 Hz, 2H), 4.73~4.61 (m, 1H), 3.71 (s, 3H), 2.26~2.13 (m, 2H), 2.00~1.83 (m, 4H), 1.69~1.55 (m, 2H); 13C NMR (100 MHz, DMSO-d6)δ: 155.4, 154.1, 153.4, 151.1, 134.9, 134.2, 120.3, 115.0, 114.1, 55.6, 52.3, 29.2, 24.9; HRMS (AP-ESI) calcd for C17H20N5O2[M+H]+: 326.1612, found 326.1607.
9-异丙基-2-(4-(N, N-二甲氨基)苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(5d):白色固体, 产率54%. m.p. 262~264 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 10.79 (s, 1H), 8.85 (s, 1H), 7.86 (s, 1H), 7.52 (d, J=8.9 Hz, 2H), 6.70 (d, J=8.9 Hz, 2H), 4.61~4.48 (m, 1H), 2.82 (s, 6H), 1.50 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6) δ: 155.7, 153.2, 151.1, 146.2, 134.2, 132.0, 120.4, 114.6, 113.6, 44.1, 41.4, 20.3; HRMS (AP-ESI) calcd for C16H21N6O [M+H]+: 313.1771, found 313.1770.
9-环戊基-2-(4-(N, N-二甲氨基)苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(5e):黄绿色固体, 产率23%. m.p.>280 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 10.82 (s, 1H), 8.83 (s, 1H), 7.87 (s, 1H), 7.50 (d, J=9.0 Hz, 2H), 6.68 (d, J=9.0 Hz, 2H), 4.72~4.60 (m, 1H), 2.82 (s, 6H), 2.28~2.11 (m, 2H), 2.00~1.81 (m, 4H), 1.70~1.54 (m, 2H); 13C NMR (100 MHz, DMSO-d6)δ; 155.7, 153.4, 151.1, 146.2, 134.4, 131.9, 120.5, 114.6, 113.5, 52.3, 41.4, 29.2, 25.0; HRMS (AP-ESI) calcd for C18H23N6O [M+H]+: 339.1928, found 339.1923.
9-环已基-2-(4-(N, N-二甲氨基)苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(5f):黄绿色固体, 产率56%. m.p.>250 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 10.82 (s, 1H), 8.88 (s, 1H), 7.87 (s, 1H), 7.54 (d, J=9.0 Hz, 2H), 6.69 (d, J=9.1 Hz, 2H), 4.20~4.05 (m, 1H), 2.82 (s, 6H), 2.39~2.25 (m, 2H), 1.91~1.79 (m, 2H), 1.77~1.64 (m, 3H), 1.43~1.28 (m, 2H), 1.28~1.16 (m, 1H); 13C NMR (100 MHz, DMSO-d6)δ: 155.5, 153.4, 151.2, 146.1, 134.3, 132.0, 120.4, 114.8, 113.5, 51.6, 41.4, 29.7, 25.9, 25.5; HRMS (AP-ESI) calcd for C19H25N6O[M+H]+: 353.2084, found 353.2091.
9-环丙基-2-(4-(N, N-二甲氨基)苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(5g):黄绿色固体, 产率42%. m.p.>250 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 10.73 (s, 1H), 8.88 (s, 1H), 7.83 (s, 1H), 7.57 (d, J=9.1 Hz, 2H), 6.69 (d, J=9.1 Hz, 2H), 2.93~2.86 (m, 1H), 2.82 (s, 6H), 1.11~1.05 (m, 2H), 1.01~0.92 (m, 2H); 13C NMR (100 MHz, DMSO-d6)δ: 155.9, 154.0, 152.2, 146.1, 134.0, 132.1, 120.3, 114.5, 113.6, 41.4, 22.5, 5.8; HRMS (AP-ESI) calcd for C16H19N6O [M+H]+: 311.1615, found 311.1614.
9-苯基-2-(4-(N, N-二甲氨基)苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(5h):黄绿色固体, 产率43%. m.p.>250 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 11.10 (s, 1H), 8.91 (s, 1H), 7.99 (s, 1H), 7.65 (d, J=7.4 Hz, 2H), 7.55 (t, J=7.8 Hz, 2H), 7.49 (d, J=9.0 Hz, 2H), 7.43 (t, J=7.4 Hz, 1H), 6.64 (d, J=9.1 Hz, 2H), 2.80 (s, 6H); 13C NMR (100 MHz, DMSO-d6)δ: 156.0, 152.8, 151.4, 146.2, 134.9, 133.5, 131.8, 129.3, 128.1, 127.0, 120.5, 114.9, 113.5, 41.4; HRMS (AP-ESI) calcd for C19H19N6O[M+H]+: 347.1615, found 347.1610.
9-异丙基-2-(4-吗啉基苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(5i):白色固体, 产率42%. m.p.>270 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 10.83 (s, 1H), 8.99 (s, 1H), 7.89 (s, 1H), 7.59 (d, J=9.1 Hz, 2H), 6.87 (d, J=9.1 Hz, 2H), 4.61~4.48 (m, 1H), 3.86~3.62 (m, 4H), 3.14~2.91 (m, 4H), 1.50 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6)δ: 155.4, 153.2, 151.1, 146.0, 134.3, 134.2, 119.8, 116.2, 114.8, 66.7, 49.9, 44.1, 20.2; HRMS (AP-ESI) calcd for C18H23N6O2[M+H]+: 355.1877, found 355.1871.
4-(4-((9-异丙基-8-氧亚基-8, 9-二氢-7H-嘌呤-2-基)氨基)苯基)哌嗪-1-羧酸叔丁酯(5j)的合成:按上述步骤反应完成后, 蒸除溶液.加入20 mL二氯甲烷, 将含BOC-酸酐(0.44 g, 2 mmol)的二氯甲烷溶液10 mL缓慢滴入, 室温搅拌1 h.之后蒸除溶剂, 通过柱层析纯化后即得目标产物5j, 白色固体, 产率32%. m.p. 241~243 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 10.84 (s, 1H), 9.01 (s, 1H), 7.89 (s, 1H), 7.59 (d, J=9.0 Hz, 2H), 6.89 (d, J=9.0 Hz, 2H), 4.61~4.49 (m, 1H), 3.52~3.38 (m, 4H), 3.04~2.93 (m, 4H), 1.50 (d, J=6.9 Hz, 6H), 1.42 (s, 9H); 13C NMR (100 MHz, DMSO-d6)δ: 155.4, 154.3, 153.2, 151.1, 145.8, 134.7, 134.1, 119.7, 117.3, 114.9, 79.4, 50.0, 44.1, 28.5, 20.2; HRMS (AP-ESI) calcd for C23H32N7O3[M+H]+: 454.2561, found 454.2563.
3.2.4 目标化合物6a~6r的合成
将化合物5a (0.29 g, 1 mmol)溶于20 mL二甲基甲酰胺中, 向其中加入K2CO3 (0.28 g, 2 mmol).室温条件下, 向反应瓶中缓慢滴加含2-溴乙酸甲酯(0.18 g, 1.2 mmol)的二甲基甲酰胺10 mL, 反应3~4 h.反应完毕, 向体系中加入约120 mL水, 析出固体, 过滤.滤饼通过柱层析纯化后即得2-(9-异丙基-2-(4-羟基苯氨基)-8-氧亚基-8, 9-二氢-7H-嘌呤-7-基)乙酸甲酯(6a), 黄色固体0.17 g, 产率48%. m.p. 188~190 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 9.03 (s, 1H), 8.97 (s, 1H), 8.09 (s, 1H), 7.46 (d, J=8.8 Hz, 2H), 6.68 (d, J=8.8 Hz, 2H), 4.70 (s, 2H), 4.63~4.52 (m, 1H), 3.71 (s, 3H), 1.50 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6) δ: 168.9, 156.1, 152.4, 152.3, 150.0, 134.8, 133.1, 120.9, 115.7, 115.3, 52.8, 44.9, 42.4, 20.2; HRMS (AP-ESI) calcd for C17H20N5O4 [M+H]+: 358.1510, found 358.1510.
以下化合物6b~6r的合成与6a的合成相同, 其中6g和6q的后处理过程与6a的不同.合成中所用的卤代物R3X的种类不同, 其中制备目标化合物6b、6f、6p用氯代物, 合成目标化合物6c~6e、6g、6i~6o、6q、6r使用的为溴代物, 6h的制备则用碘代物.
7-(2-氧亚基丙基)-9-异丙基-2-(4-羟基苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(6b):白色固体, 产率36%. m.p. 130~133 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 9.00 (s, 1H), 8.96 (s, 1H), 7.96 (s, 1H), 7.46 (d, J=8.9 Hz, 2H), 6.67 (d, J=8.9 Hz, 2H), 4.77 (s, 2H), 4.63~4.51 (m, 1H), 2.22 (s, 3H), 1.50 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6) δ: 202.7, 156.0, 152.4, 152.2, 149.9, 134.6, 133.2, 120.8, 116.0, 115.3, 50.5, 44.8, 27.4, 20.3; HRMS (AP-ESI) calcd for C17H20N5O3 [M+H]+: 342.1561, found 342.1569.
2-(9-异丙基-2-(4-甲氧基苯氨基)-8-氧亚基-8, 9-二氢-7H-嘌呤-7-基)乙酸甲酯(6c):淡黄色固体, 产率46%. m.p. 128~130 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 9.18 (s, 1H), 8.12 (s, 1H), 7.62 (d, J=9.1 Hz, 2H), 6.86 (d, J=9.1 Hz, 2H), 4.71 (s, 2H), 4.66~4.54 (m, 1H), 3.76~3.66 (m, 6H), 1.51 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6) δ: 168.9, 155.9, 154.2, 152.4, 150.0, 134.8, 134.7, 120.3, 115.9, 114.2, 55.6, 52.8, 44.9, 42.4, 20.2; HRMS (AP-ESI) calcd for C18H22N5O4[M+H]+: 372.1666, found 372.1661.
2-(9-环戊基-2-(4-甲氧基苯氨基)-8-氧亚基-8, 9-二氢-7H-嘌呤-7-基)乙酸甲酯(6d):白色固体, 产率74%. m.p. 175~177 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 9.15 (s, 1H), 8.13 (s, 1H), 7.60 (d, J=9.1 Hz, 2H), 6.85 (d, J=9.1 Hz, 2H), 4.77~4.65 (m, 3H), 3.72 (s, 3H), 3.71 (s, 3H), 2.26~2.10 (m, 2H), 2.00~1.86 (m, 4H), 1.70~1.56 (m, 2H); 13C NMR (100 MHz, DMSO-d6) δ: 168.9, 155.9, 154.3, 152.6, 150.0, 134.9, 134.6, 120.5, 116.0, 114.1, 55.6, 53.0, 52.8, 42.5, 29.3, 24.9; HRMS (AP-ESI) calcd for C20H24N5O4[M+H]+: 398.1823, found 398.1824.
2-(9-异丙基-2-(4-(N, N-二甲氨基)苯氨基)-8-氧亚基-8, 9-二氢-7H-嘌呤-7-基)乙酸甲酯(6e):白色固体, 产率49%. m.p. 130~132 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 8.99 (s, 1H), 8.08 (s, 1H), 7.52 (d, J=9.1 Hz, 2H), 6.70 (d, J=9.1 Hz, 2H), 4.69 (s, 2H), 4.64~4.53 (m, 1H), 3.71 (s, 3H), 2.83 (s, 6H), 1.51 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6) δ 168.9, 156.2, 152.4, 150.1, 146.3, 134.9, 131.7, 120.5, 115.6, 113.6, 52.8, 44.9, 42.4, 41.3, 20.3; HRMS (AP-ESI) calcd for C19H25N6O3 [M+H]+: 385.1983, found 385.1975.
7-(2-氧亚基丙基)-9-异丙基-2-(4-(N, N-二甲氨基)苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(6f):淡黄色固体, 产率34%. m.p. 166~168 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 8.96 (s, 1H), 7.96 (s, 1H), 7.52 (d, J=8.9 Hz, 2H), 6.70 (d, J=8.9 Hz, 2H), 4.77 (s, 2H), 4.63~4.52 (m, 1H), 2.82 (s, 6H), 2.21 (s, 3H), 1.51 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6)δ: 202.6, 156.0, 152.5, 150.0, 146.2, 134.7, 131.8, 120.4, 115.9, 113.6, 50.5, 44.8, 41.3, 27.4, 20.3; HRMS (AP-ESI) calcd for C19H25N6O2[M+H]+: 369.2034, found 369.2035.
2-(9-异丙基-2-(4-(N, N-二甲氨基)苯氨基)-8-氧亚基-8, 9-二氢-7H-嘌呤-7-基)乙酸(6g):按上述步骤反应完后, 向反应体系中加入5 mol/L氢氧化钠4 mL, 室温搅拌3~4 h.向体系中加入水80 mL, 再用6 mol/L盐酸调pH=5~6, 析出固体, 过滤, 滤饼通过柱层析纯化即得目标化合物.黄色固体, 产率63%. m.p. 244~246 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 13.17 (br s, 1H), 8.98 (s, 1H), 8.08 (s, 1H), 7.52 (d, J=8.3 Hz, 2H), 6.71 (d, J=8.3 Hz, 2H), 4.68~4.44 (m, 3H), 2.83 (s, 6H), 1.51 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6) δ: 169.8, 156.0, 152.5, 150.0, 146.2, 134.7, 131.9, 120.5, 115.8, 113.6, 44.8, 42.5, 41.3, 20.3; HRMS (AP-ESI) calcd for C18H23N6O3 [M+H]+: 371.1826, found 371.1857.
7-丙基-9-异丙基-2-(4-(N, N-二甲氨基)苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(6h):白色固体, 产率62%. m.p. 114~116 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 8.93 (s, 1H), 8.10 (s, 1H), 7.53 (d, J=9.0 Hz, 2H), 6.70 (d, J=8.7 Hz, 2H), 4.65~4.51 (m, 1H), 3.73 (t, J=7.0 Hz, 2H), 2.83 (s, 6H), 1.73~1.60 (m, 2H), 1.50 (d, J=6.9 Hz, 6H), 0.86 (t, J=7.4 Hz, 3H); 13C NMR (100 MHz, DMSO-d6) δ: 155.9, 152.3, 150.0, 146.2, 134.1, 131.9, 120.4, 115.7, 113.6, 44.7, 42.6, 41.3, 21.7, 20.3, 11.5; HRMS (AP-ESI) calcd for C19H27N6O [M+H]+: 355.2241, found 355.2228.
7-烯丙基-9-异丙基-2-(4-(N, N-二甲氨基)苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(6i):淡黄色固体, 产率62%. m.p. 140~142 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 8.97 (s, 1H), 7.98 (s, 1H), 7.54 (d, J=9.0 Hz, 2H), 6.70 (d, J=8.5 Hz, 2H), 5.98~5.83 (m, 1H), 5.26~5.13 (m, 2H), 4.66~4.53 (m, 1H), 4.40 (d, J=5.3 Hz, 2H), 2.82 (s, 6H), 1.51 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6) δ: 156.0, 152.0, 150.1, 146.2, 134.3, 132.8, 131.8, 120.4, 117.9, 115.4, 113.5, 44.8, 43.2, 41.3, 20.3; HRMS (AP-ESI) calcd for C19H25N6O[M+H]+: 353.2084, found 353.2082.
7-炔丙基-9-异丙基-2-(4-(N, N-二甲氨基)苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(6j):淡黄色固体, 产率61%. m.p. 144~146 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 9.01 (s, 1H), 8.10 (s, 1H), 7.52 (d, J=9.0 Hz, 2H), 6.70 (d, J=9.1 Hz, 2H), 4.65 (d, J=2.4 Hz, 2H), 4.62~4.53 (m, 1H), 3.40 (t, J=2.4 Hz, 1H), 2.83 (s, 6H), 1.50 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6) δ: 156.2, 151.6, 150.2, 146.3, 134.6, 131.6, 120.6, 114.6, 113.5, 78.3, 76.0, 44.9, 41.3, 30.6, 20.2; HRMS (AP-ESI) calcd for C19H23N6O[M+H]+: 351.1928, found 351.1932.
7-苄基-9-异丙基-2-(4-(N, N-二甲氨基)苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(6k):白色固体, 产率55%. m.p. 150~152 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 8.95 (s, 1H), 7.94 (s, 1H), 7.50 (d, J=8.3 Hz, 2H), 7.41~7.23 (m, 5H), 6.69 (d, J=7.3 Hz, 2H), 4.98 (s, 2H), 4.65~4.56 (m, 1H), 2.82 (s, 6H), 1.52 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6) δ: 156.1, 152.4, 150.2, 146.3, 137.0, 134.3, 131.7, 129.2, 128.1, 128.1, 120.5, 115.3, 113.5, 44.9, 44.4, 41.3, 20.3; HRMS (AP-ESI) calcd for C23H27N6O[M+H]+: 403.2241, found 403.2239.
2-(9-环戊基-2-(4-(N, N-二甲氨基)苯氨基)-8-氧亚基-8, 9-二氢-7H-嘌呤-7-基)乙酸甲酯(6l):白色固体, 产率43%. m.p. 150~152 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 8.98 (s, 1H), 8.09 (s, 1H), 7.50 (d, J=9.0 Hz, 2H), 6.69 (d, J=9.1 Hz, 2H), 4.77~4.65 (m, 3H), 3.71 (s, 3H), 2.83 (s, 6H), 2.26~2.11 (m, 2H), 2.00~1.85 (m, 4H), 1.70~1.56 (m, 2H); 13C NMR (100 MHz, DMSO-d6) δ: 169.0, 156.2, 152.6, 150.0, 146.4, 135.0, 131.6, 120.7, 115.6, 113.5, 52.9, 52.8, 42.5, 41.3, 29.3, 25.0; HRMS (AP-ESI) calcd for C21H27N6O3[M+H]+: 411.2139, found 411.2133.
2-(9-环已基-2-(4-(N, N-二甲氨基)苯氨基)-8-氧亚基-8, 9-二氢-7H-嘌呤-7-基)乙酸甲酯(6m):灰白色固体, 产率40%. m.p. 150~152 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 8.99 (s, 1H), 8.08 (s, 1H), 7.53 (d, J=9.0 Hz, 2H), 6.70 (d, J=9.0 Hz, 2H), 4.69 (s, 2H), 4.22~4.10 (m, 1H), 3.70 (s, 3H), 2.83 (s, 6H), 2.38~2.24 (m, 2H), 1.91~1.80 (m, 2H), 1.78~1.66 (m, 3H), 1.44~1.30 (m, 2H), 1.29~1.16 (m, 1H); 13C NMR (100 MHz, DMSO-d6) δ: 168.9, 156.2, 152.5, 150.1, 146.3, 134.9, 131.7, 120.6, 115.6, 113.5, 52.8, 52.4, 42.5, 41.3, 29.8, 25.9, 25.4; HRMS (AP-ESI) calcd for C22H29N6O3[M+H]+: 425.2296, found 425.2299.
2-(9-环丙基-2-(4-(N, N-二甲氨基)苯氨基)-8-氧亚基-8, 9-二氢-7H-嘌呤-7-基)乙酸甲酯(6n):白色固体, 产率8%. m.p. 164~166 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 9.03 (s, 1H), 8.06 (s, 1H), 7.56 (d, J=9.1 Hz, 2H), 6.70 (d, J=9.1 Hz, 2H), 4.67 (s, 2H), 3.70 (s, 3H), 3.00~2.93 (m, 1H), 2.82 (s, 6H), 1.11~1.05 (m, 2H), 1.05~0.97 (m, 2H): 13C NMR (100 MHz, DMSO-d6) δ: 168.9, 156.4, 153.3, 151.1, 146.2, 134.7, 131.8, 120.5, 115.4, 113.6, 52.8, 42.4, 41.3, 22.8, 5.8; HRMS (AP-ESI) calcd for C19H23N6O3 [M+H]+: 383.1826, found 383.1826.
2-(9-苯基-2-(4-(N, N-二甲氨基)苯氨基)-8-氧亚基-8, 9-二氢-7H-嘌呤-7-基)乙酸甲酯(6o):黄色固体, 产率71%. m.p. 170~172 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 9.05 (s, 1H), 8.22 (s, 1H), 7.67 (d, J=8.2 Hz, 2H), 7.58 (t, J=7.8 Hz, 2H), 7.52~7.41 (m, 3H), 6.65 (d, J=9.1 Hz, 2H), 4.80 (s, 2H), 3.74 (s, 3H), 2.81 (s, 6H); 13C NMR (100 MHz, DMSO-d6) δ: 168.9, 156.5, 152.1, 150.2, 146.3, 135.6, 133.2, 131.5, 129.5, 128.5, 126.8, 120.6, 115.7, 113.5, 52.9, 42.7, 41.3; HRMS (AP-ESI) calcd for C22H23N6O3[M+H]+: 419.1826, found 419.1821.
7-(2-氧亚基丙基)-9-异丙基-2-(4-吗啉基苯氨基)-7, 9-二氢-8H-嘌呤-8-酮(6p):白色固体, 产率49%. m.p. 201~203 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 9.10 (s, 1H), 7.99 (s, 1H), 7.58 (d, J=9.0 Hz, 2H), 6.88 (d, J=9.1 Hz, 2H), 4.78 (s, 2H), 4.64~4.53 (m, 1H), 3.81~3.66 (m, 4H), 3.10~2.93 (m, 4H), 2.22 (s, 3H), 1.51 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6) δ: 202.6, 155.8, 152.5, 149.9, 146.1, 134.6, 134.2, 119.9, 116.2, 116.1, 66.7, 50.5, 49.9, 44.8, 27.4, 20.3; HRMS (AP-ESI) calcd for C21H27N6O3[M+H]+: 411.2139, found 411.2140.
2-(9-异丙基-2-(4-吗啉基苯氨基)-8-氧亚基-8, 9-二氢-7H-嘌呤-7-基)乙酸(6q):反应条件与化合物6g的相同.浅黄色固体, 产率9%. m.p.>260 ℃; 1H NMR (400 MHz, DMSO-d6)δ: 13.14 (br s, 1H), 9.10 (s, 1H), 8.10 (s, 1H), 7.59 (d, J=9.0 Hz, 2H), 6.88 (d, J=9.0 Hz, 2H), 4.67~4.50 (m, 3H), 3.79~3.66 (m, 4H), 3.08~2.96 (m, 4H), 1.51 (d, J=6.9 Hz, 6H); 13C NMR (100 MHz, DMSO-d6) δ: 169.8, 155.8, 152.5, 150.0, 146.1, 134.6, 134.1, 119.9, 116.2, 116.0, 66.7, 49.9, 44.9, 42.5, 20.3; HRMS (AP-ESI) calcd for C20H25N6O4 [M+H]+: 413.1932, found 413.1928.
4-(4-((7-(2-羟乙基)-9-异丙基-8-氧亚基-8, 9-二氢-7H-嘌呤-2-基)氨基)苯基)哌嗪-1-羧酸叔丁酯(6r):白色固体, 产率64.8%. m.p. 221~222 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 9.08 (s, 1H), 8.09 (s, 1H), 7.60 (d, J=9.0 Hz, 2H), 6.90 (d, J=9.0 Hz, 2H), 4.91 (t, J=5.6 Hz, 1H), 4.65~4.52 (m, 1H), 3.82 (t, J=5.2 Hz, 2H), 3.69~3.59 (m, 2H), 3.52~3.40 (m, 4H), 3.05~2.92 (m, 4H), 1.51 (d, J=6.9 Hz, 6H), 1.42 (s, 9H); 13C NMR (100 MHz, DMSO-d6) δ: 155.5, 154.3, 152.4, 149.9, 145.9, 134.6, 134.5, 119.7, 117.3, 116.6, 79.4, 59.4, 50.0, 44.6, 44.1, 28.5, 20.3; HRMS (AP-ESI) calcd for C25H36N7O4[M+ H]+: 498.2823, found 498.2828.
3.2.2 中间体4a~4e的合成
中间体4a~4e的合成参考相关文献[13].
9-异丙基-2-氯-7, 9-二氢-8H-嘌呤-8-酮(4a), 粉红色固体, 产率46%. m.p. 244~246 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 11.56 (br s, 1H), 8.12 (s, 1H), 4.63~4.49 (m, 1H), 1.47 (d, J=6.9 Hz, 6H).
9-环戊基-2-氯-7, 9-二氢-8H-嘌呤-8-酮(4b):粉色固体, 产率51%. m.p. 242~244 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 11.60 (s, 1H), 8.12 (s, 1H), 4.77~4.62 (m, 1H), 2.16~2.04 (m, 2H), 1.97~1.85 (m, 4H), 1.69~1.57 (m, 2H).
9-环已基-2-氯-7, 9-二氢-8H-嘌呤-8-酮(4c):灰白色固体, 产率60%. m.p.>260 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 11.59 (s, 1H), 8.12 (s, 1H), 4.23~4.06 (m, 1H), 2.27~2.08 (m, 2H), 1.90~1.60 (m, 5H), 1.45~1.28 (m, 2H), 1.27~1.12 (m, 1H).
9-环丙基-2-氯-7, 9-二氢-8H-嘌呤-8-酮(4d):紫色固体, 产率28%. m.p.>250 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 11.54 (s, 1H), 8.09 (s, 1H), 2.95~2.88 (m, 1H), 1.06~0.94 (m, 4H).
9-苯基-2-氯-7, 9-二氢-8H-嘌呤-8-酮(4e):淡红色固体, 产率49%. m.p.>250 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 11.99 (s, 1H), 8.26 (s, 1H), 7.63~7.54 (m, 4H), 7.52~7.46 (m, 1H).
3.2.1 中间体3a~3e的合成
中间体3a~3e参考相关文献[13]制得.
N4-异丙基-2-氯嘧啶-4, 5-二胺(3a), 紫色固体, 产率84%. m.p. 93~95 ℃; 1H NMR (400 MHz, CDCl3) δ: 7.58 (s, 1H), 5.03 (d, J=6.8 Hz, 1H), 4.38~4.27 (m, 1H), 3.01 (br s, 2H), 1.26 (d, J=6.5 Hz, 6H).
N4-环戊基-2-氯嘧啶-4, 5-二胺(3b):紫色固体, 产率95%. m.p. 126~128 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 7.36 (s, 1H), 6.65 (d, J=6.6 Hz, 1H), 4.94 (s, 2H), 4.29~4.19 (m, 1H), 2.02~1.91 (m, 2H), 1.75~1.63 (m, 2H), 1.63~1.51 (m, 2H), 1.51~1.39 (m, 2H).
N4-环已基-2-氯嘧啶-4, 5-二胺(3c):淡紫色固体, 产率98%. m.p. 142~144℃; 1H NMR (400 MHz, DMSO-d6) δ: 7.37 (s, 1H), 6.59 (d, J=7.4 Hz, 1H), 4.65 (br s, 2H), 3.90~3.76 (m, 1H), 1.97~1.85 (m, 2H), 1.79~1.69 (m, 2H), 1.66~1.56 (m, 1H), 1.40~1.10 (m, 5H).
N4-环丙基-2-氯嘧啶-4, 5-二胺(3d):深紫色粘稠液体, 粗品, 直接用于下一步反应.
N4-苯基-2-氯嘧啶-4, 5-二胺(3e):黄色固体, 产率20%. m.p. 136~137℃; 1H NMR (400 MHz, DMSO-d6) δ: 8.63 (s, 1H), 7.74~7.58 (m, 3H), 7.36 (t, J=7.9 Hz, 2H), 7.07 (t, J=7.4 Hz, 1H), 5.31 (s, 2H).
-
-
[1]
Legraverend, M.; Grierson, D. S. Bioorg. Med. Chem. 2006, 14, 3987. doi: 10.1016/j.bmc.2005.12.060
-
[2]
张京玉, 王清龙, 侯学会, 刘宏民, 有机化学, 2015, 35, 1022. http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract344726.shtmlZhang, J.-Y.; Wang, Q.-L.; Hou, X.-H.; Liu, H.-M. Chin. J. Org. Chem. 2015, 35, 1022 (in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract344726.shtml
-
[3]
Di Virgilio, F.; Adinolfi, E. Oncogene 2017, 36, 293. doi: 10.1038/onc.2016.206
-
[4]
Di Virgilio, F. Cancer Res. 2012, 72, 5441. doi: 10.1158/0008-5472.CAN-12-1600
-
[5]
Pui, C. H.; Jeha, S.; Kirkpatrick, P. Nat. Rev. Drug Discovery 2005, 4, 369. doi: 10.1038/nrd1724
-
[6]
Denny, B. J.; Wheelhouse, R. T.; Stevens, M. F. G.; Tsang, L. L. H.; Slack, J. A. Biochemistry 1994, 33, 9045. doi: 10.1021/bi00197a003
-
[7]
Parker, W. B. Chem. Rev. 2009, 109, 2880. doi: 10.1021/cr900028p
-
[8]
Sanford, D. S.; Wierda, W. G.; Burger, J. A.; Keating, M. J.; O'Brien, S. M. Clin. Lymphoma, Myeloma Leuk. 2015, 15, 385. doi: 10.1016/j.clml.2015.02.019
-
[9]
Asghar, U.; Witkiewicz, A. K.; Turner, N. C.; Knudsen, E. S. Nat. Rev. Drug Discovery 2015, 14, 130. doi: 10.1038/nrd4504
-
[10]
王军华, 王泉德, 顿艳艳, 方浩, 高等学校化学学报, 2014, 35, 1189. doi: 10.7503/cjcu20131048Wang J.-H.; Wang, Q.-D.; Dun Y.-Y.; Fang, H. Chem. J. Chin. Univ. 2014, 35, 1189 (in Chinese). doi: 10.7503/cjcu20131048
-
[11]
Wang, J.-H.; Wang, Q.-D.; Zhang, L.-R.; Fang, H. Chin. J. Chem. 2013, 31, 1181. doi: 10.1002/cjoc.201300420
-
[12]
Zheng, W.; Thorne, N.; McKew, J. C. Drug Discovery Today 2013, 18, 1067. doi: 10.1016/j.drudis.2013.07.001
-
[13]
Andrews, D. M.; Jones, C. D.; Simpson, I.; Ward, R. A. WO 2009024824, 2009[Chem. Abstr. 2009, 150, 283068].
-
[1]
-
表 1 化合物的结构
Table 1. The structure of the compounds

表 2 代表化合物的体外抗增殖活性
Table 2. Antiproliferative activities of representative compounds

-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 7
- 文章访问数: 1038
- HTML全文浏览量: 103



 下载:
下载:

 下载:
下载:

