 图 1
光催耦合生物阳极还原硝酸盐反应器
Figure 1.
Component of the reactor for photocatalytic reduction of nitrate using cathode combined with bio-anode
图 1
光催耦合生物阳极还原硝酸盐反应器
Figure 1.
Component of the reactor for photocatalytic reduction of nitrate using cathode combined with bio-anode

Citation: LI Liang, LIU Li-Fen, YANG Feng-Lin. Reduction of Nitrate by g-C3N4-TiO2 Photocatalyst on Electrode Coupled with Electricity Generating Bio-anode[J]. Chinese Journal of Inorganic Chemistry, 2017, 33(4): 637-643. doi: 10.11862/CJIC.2017.082

g-C3N4-TiO2光催化电极耦合生物产电阳极还原硝酸根
English
Reduction of Nitrate by g-C3N4-TiO2 Photocatalyst on Electrode Coupled with Electricity Generating Bio-anode
-
Key words:
- photocatalysis
- / biological anode
- / graphitic carbon nitride
- / titanium dioxide
- / nitrate
-
地下水作为重要的饮用水源,与人类健康息息相关。近年来,随着工农业废水的排放,部分地区地下水中硝酸盐含量超标。饮用水中硝酸盐超标会对人类的健康产生极大的危害,, 而常规水处理方法对硝酸盐去除效果不佳。近年来发展起来的光催化法对硝酸盐去除有很好的效果,其研究重点主要集中在新型催化剂的制备以及催化效率的提高,如Ru/TiO2[1]、Ag/TiO2[2]、Au/TiO2[3]等,在紫外光照射下都具有不错的还原效果。另一种新兴污染物降解技术微生物燃料电池 (microbial fuel cell,MFC) 通过微生物呼吸代谢氧化有机物产生电子,进而产生电流,是一种清洁的能源再生手段,对多种污水降解都有较好的效果[4-6]。随着两种污染物降解技术的发展,近年来有学者将光催化技术与MFC结合构建光催化型燃料电池[7-9],利用生物产电提高光催化效果,同时节约了成本。而对于光催化电极催化剂的选取以及电极对耦合体系的处理效果的提升还有待进一步研究。尚未见以g-C3N4-TiO2为电极耦合生物产电处理硝酸盐废水的研究。
1987年Kudo等[10]首次利用光催化将氨氮转化成硝酸盐,为脱氮指出了一条新道路。后来研究者多以二氧化钛或其与金属复合来实现硝酸盐还原[11-21]。这些以金属掺杂的TiO2光催化剂虽然提高了还原效率,但应用到实际水体的处理中时,存在金属浸出的风险。氮化碳g-C3N4具有热稳定性、化学稳定性好的优点,且具有可见光催化活性,其制备过程简单,原料廉价易得,因而受到研究者的青睐。为提高g-C3N4催化效率,研究者将TiO2与g-C3N4复合制备出可见光响应的复合光催化剂,具有较好的光催化性能。Yan等[22]采用热处理TiO2和g-C3N4混合物的方法制备了一种TiO2-g-C3N4光催化剂,用于光分解水制氢。Yang等[23]煅烧TiCl4乙醇溶液和g-C3N4制备出了N掺杂TiO2/g-C3N4光催化剂,提高了光催化效率。Fu等[24]以商业TiO2和尿素为前驱体一步固相合成了TiO2-g-C3N4光催化剂。
本研究采用简单的溶胶凝胶法制备了g-C3N4-TiO2光催化剂,并采用浸渍提拉的方法将其负载在碳纤维布上,制成催化电极,用于光催化还原硝酸盐的研究。为提高光催化还原硝酸盐的效率,我们提出了用生物阳极产电促进光催化阴极还原,有效地利用阳极产电菌代谢产生的电子和质子,不仅提高了还原效率,在反应过程中无需外加质子,节约了成本。
1 实验部分
1.1 催化剂及催化电极制备与表征
1.2 光催化阴极耦合生物阳极还原硝酸盐效果
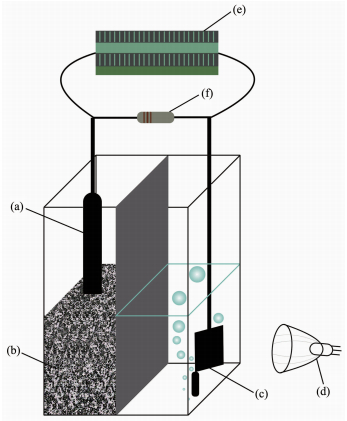
实验中采用双室石英反应器 (反应器结构如图 1),阳极室和阴极室容积均为300 mL,以50 W冷反射卤钨灯为光源,光源主要波长范围为380~820 nm,光源距电极为3 cm,阴极室底部装有曝气装置,反应中通入氮气,气体流量为100 mL·min-1。催化电极置于阴极室,作为阴极。阳极室装有100 g活性炭,其上负载有产电希瓦氏菌 (产电希瓦氏菌为购买的产电希瓦氏纯菌在实验室接种保持的,因在开放环境培养可能混有其他产电菌),阳极室溶液组成为蔗糖0.3 g·L-1,NaAc 0.381 3 g·L-1,NaNO3 0.121 4 g·L-1,K2HPO4 0.007 g·L-1,KH2PO4 0.002 4 g·L-1,MgSO4 0.005 g·L-1,CaCl2 0.005 g·L-1。阳极室密封保证其厌氧环境,阴阳极两室之间用质子交换膜隔开。反应开始后,在阴极室加入100 mL浓度为100 mg·L-1的硝酸盐溶液,在黑暗条件下吸附反应,通入氮气去除溶解氧,0.5 h后进行光照还原反应。每隔固定时间取样,反应结束后测定水样中硝氮、氨氮、亚硝氮的浓度,计算硝酸盐的去除率来表征催化反应效率,以副产物氨氮、亚硝酸盐的量来表示催化电极氮气选择性。
 图 1
光催耦合生物阳极还原硝酸盐反应器
Figure 1.
Component of the reactor for photocatalytic reduction of nitrate using cathode combined with bio-anode
图 1
光催耦合生物阳极还原硝酸盐反应器
Figure 1.
Component of the reactor for photocatalytic reduction of nitrate using cathode combined with bio-anode
1.1.3 g-C3N4-TiO2光催化剂的表征
催化剂X射线衍射表征仪器为Rigaku Dmax Ⅲ VC,测试使用Cu Kα(λ=0.154 2 nm) 靶射线为辐射源,扫描范围为10°~90°(2θ),加速电压为40 kV,工作电流为30 mA,扫描速度为6°·min-1。催化剂粉末形貌采用Nova NanoSEM 450扫描电子显微镜表征。催化剂光学吸收性质由Shimadzu-UV-2450紫外可见漫反射光谱仪测定,光谱扫描范围200~700 nm。
1.1.1 g-C3N4催化剂粉末制备
称取2 g三聚氰胺于坩埚中,于马弗炉中以5 ℃·min-1升温至530 ℃,煅烧4 h后冷却至室温,研磨过300目筛备用。
1.1.2 复合催化剂粉末及催化电极制备
分别量取27 mL钛酸四丁酯、23 mL乙醇于100 mL烧杯中,磁力搅拌下加入3.3 mL盐酸、2.7 mL去离子水。加入0.5 g g-C3N4,超声1 h,搅拌30 min后将10 cm×5 cm已清洗的碳纤维布浸入其中,取出后风干,反复浸入、烘干5次。将负载有催化剂的碳纤维布和凝胶状催化剂一同放入马弗炉中,以5 ℃·min-1升温至450 ℃,煅烧2 h,冷却至室温即制得光催化电极与粉末催化剂。粉末催化剂经研磨,过300目筛备用。
2 结果与讨论
2.1 g-C3N4-TiO2光催化剂的XRD分析
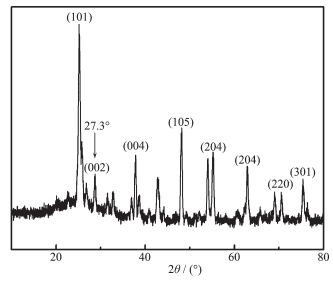
图 2为g-C3N4-TiO2粉末XRD图,由图中可以看出锐钛矿TiO2特征峰,即2θ=25.28°((101) 晶面)、38.0°((004) 晶面)、48.0°((105) 晶面)、54.8°((204) 晶面)。与锐钛矿TiO2标准卡片一致,说明复合催化剂中TiO2为锐钛矿型。在图中箭头所指位置2θ=27.3°左右出现的衍射峰为g-C3N4形成的 (002) 晶面衍射。相比TiO2,复合催化剂g-C3N4-TiO2衍射峰出现宽化,说明催化剂结晶度降低,2种催化剂实现有效复合。
2.2 g-C3N4-TiO2光催化剂的SEM分析
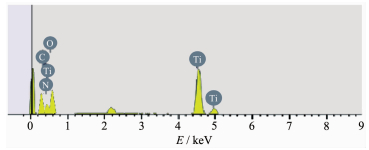
图 3为g-C3N4-TiO2光催化剂SEM图,A、B分别为放大5×104倍和2×105倍。可以看出TiO2为不规则球状颗粒,图中的片状结构为石墨碳g-C3N4,可以看到在g-C3N4片层上镶嵌有TiO2颗粒, 说明2种催化剂实现了复合。图 4为复合催化剂的EDS图,可以看出催化剂主要由C、N、Ti、O四种元素组成。
2.3 复合催化剂紫外可见吸收性能
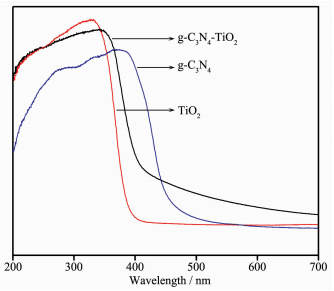
图 5为TiO2、g-C3N4、g-C3N4-TiO2的UV-Vis DRS谱图。从图中可以看出g-C3N4-TiO2复合催化剂在360~410 nm波长范围内光吸收相比于TiO2发生明显红移,说明g-C3N4的掺杂可提高TiO2的可见光吸收。在波长大于450 nm的可见光范围内g-C3N4-TiO2光催化剂的光吸收大于TiO2、g-C3N4,说明复合催化剂有更好的可见光吸收性能。这可能是复合催化剂中TiO2叠加了g-C3N4可见光响应。同时g-C3N4的带隙为2.7 eV,在可见光照射下,生成的光生电子转移到TiO2导带,使复合催化剂可见光响应范围变大。
2.4 光催化阴极耦合生物阳极体系硝酸盐去除效果
2.4.2 光照和微生物阳极对体系硝酸盐还原效率的提高
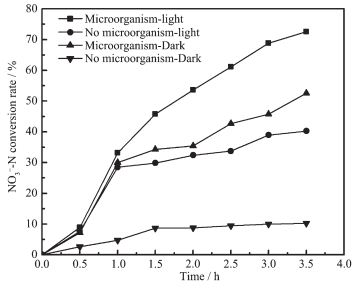
由图 7比较不同条件下硝酸盐还原效果可知,还原效果:有光有微生物 > 无光有微生物 > 有光无微生物 > 无光无微生物。这是由于光催化剂在光照条件下产生电子和空穴,电子在无氧条件下参与硝酸盐的还原。在有微生物作为阳极时,产电微生物产生电子,电子经由外电路到达阴极,在阴极催化剂作用下,进行硝酸盐还原,生物阳极电子的贡献可极大促进硝酸盐的还原。
2.4.7 硝酸盐还原机理分析
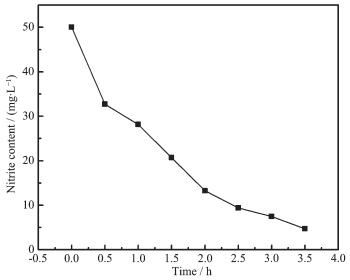
在整个反应过程中,硝酸盐含量一直在减小,且在开始迅速下降,之后缓慢降低,亚硝酸盐先升高后降低。为准确分析反应过程中亚硝酸盐变化规律,以100 mL亚硝酸盐浓度为50 mg·L-1溶液代替硝酸盐溶液,在相同条件下进行反应,反应过程中亚硝酸盐变化如图 12所示。反应过程中亚硝酸盐浓度一直下降,且没有检测到硝酸盐和氨氮的生成。说明在硝酸盐还原过程中,部分硝酸盐会被先转化为亚硝酸盐,再被进一步还原为N2,且在硝酸盐浓度较高时,转化为亚硝酸的量大于亚硝酸盐被还原的量,因此亚硝酸盐在初期呈上升趋势,在反应一段时间后,硝酸盐浓度降低,转化为亚硝酸盐的量减少,前期溶液中积累的亚硝酸盐逐渐被还原,亚硝酸盐浓度开始降低。在反应开始后,微生物通过代谢有机物产生电子,阴极基底为碳纤维布,故阳极微生物电势远低于阴极电势,阴阳极间存在的电势差促使阳极产生的电子能迅速地传递到阴极,参与阴极还原反应。通过对反应前后溶液pH值的检测,发现反应后pH值有明显的上升,说明反应过程中有H+参加反应。而H+的主要来源为阳极微生物代谢产生,通过质子交换膜从阳极传递到阴极,参与还原反应。通过以上实验分析得出,在耦合体系中,硝酸盐的还原机理可能为:
可能发生的反应有:
亚硝酸盐在催化剂作用下生成中间产物NOx,NOx相结合生成N-N键,形成N2。而在反应过程中未检测出气态NOx,说明在还原反应过程中大部分硝氮被直接还原为氮气,仅有小部分被还原产生中间副产物NOx,产生的少量NOx迅速反应生成N2,故未等气态NOx溢出便已反应生成N2气。
2.4.8 催化电极重复性实验
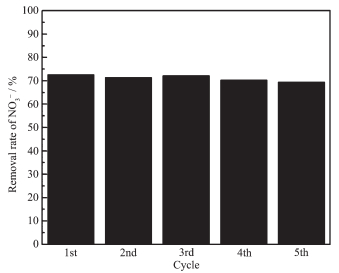
催化电极的重复性实验结果如图 13所示,连续进行5次实验后,硝酸盐的去除率由72.57%降到69.45%,下降幅度很小,说明催化电极可重复利用。对使用多次的电极进行观察,发现催化剂在载体上负载牢固,未有脱落现象。
2.4.1 耦合体系硝酸盐去除效率及降解产物
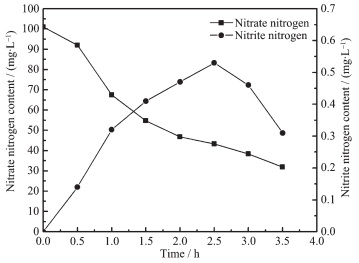
图 6为制备的g-C3N4-TiO2光催化电极在耦合生物阳极,可见光照射下硝酸盐浓度随时间变化曲线。可以看出反应开始后硝酸盐浓度迅速下降,反应3.5 h后,硝酸盐去除率达到72.57%, 转化效率高于纯TiO2[13]的28%、Au-TiO2[16]的46%以及部分金属掺杂TiO2的催化剂。随着反应的进行,副产物亚硝酸盐先逐渐增加, 在反应2.5 h后达到最大值,之后逐渐下降。3.5 h后降为0.31 mg·L-1,低于生活饮用水国家标准GB5749中亚硝酸盐指标 (1 mg·L-1)。在反应过程中未检出有氨氮生成。对反应过程中产生的气体进行收集,用氮氧化物测定仪检测,未检出氮氧化物,说明硝酸盐还原产物主要为氮气,整个体系氮气选择性为99.54%,其计算公式为:
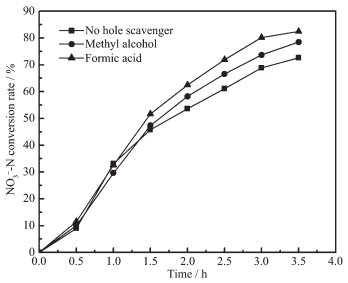
2.4.4 空穴清除剂与pH值对硝酸盐还原的影响
图 9为在加入甲醇、甲酸作为空穴清除剂后硝酸盐的还原效果变化曲线。空穴清除剂能够与空穴结合,抑制光生电子与空穴的复合,使更多的电子参与硝酸盐还原。而加入甲酸的还原效率要高于甲醇,这是因为甲酸的加入不仅能抑制电子与空穴的复合,还提供了还原反应所需的H+,因此还原效率更好。然而,加入空穴清除剂后对于硝酸盐还原效率的提高并不明显,这是由于生物阳极起到了积极的作用。生物阳极不断地向阴极传递电子,这些电子同样起到了光生电子的作用,这就为体系提供了充足的电子用于硝酸盐的还原。因此空穴清除剂不会成为影响体系硝酸盐还原效率的决定性因素。
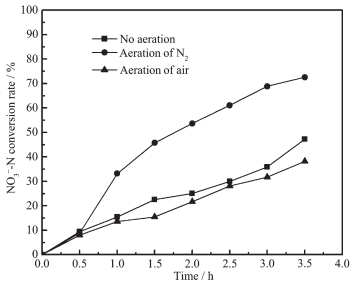
2.4.3 曝气对硝酸盐还原的影响
图 8为g-C3N4-TiO2光催化电极在不同曝气条件下硝酸盐的还原效率。还原效率从大到小依次为:曝氮气 > 不曝气 > 曝空气。这是由于溶液中的溶解氧会与硝酸盐竞争体系内的电子,而溶解氧更容易与电子结合,这便抑制了硝酸盐的还原。此外有氧气条件下,生成的亚硝酸盐会被氧化成硝酸盐,发生逆反应。因此通入氮气可有效提高催化效率。
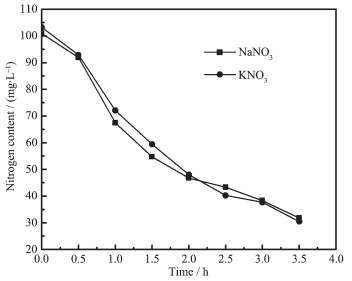
2.4.5 金属阳离子对硝酸盐还原的影响
图 10为相同浓度的硝酸钠与硝酸钾溶液在光照下的还原效果。从图中可以看出,在相同时间内硝酸钠溶液和硝酸钾溶液的硝酸根还原效率几乎相同。因此,不参与还原反应的金属阳离子对于硝酸盐还原几乎没有影响。
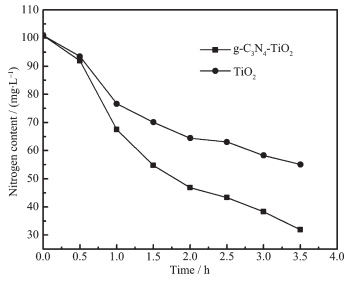
2.4.6 复合催化剂与纯TiO2的硝酸盐还原效果对比
图 11为复合催化剂与纯TiO2硝酸盐还原效果对比图。可以看出,在可见光照射下复合催化剂还原效果远高于纯TiO2,这是由于复合催化剂的可见光响应远高于纯TiO2催化剂。
2.4.9 还原体系产电性能分析
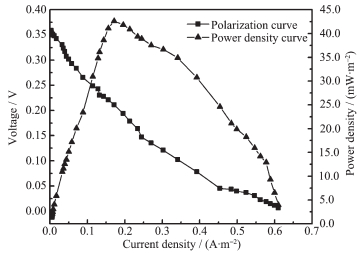
图 14、15为此耦合体系产电效果图。反应过程中,随着反应的进行电池电势先迅速下降后缓慢降低。联系硝酸盐去除率曲线发现,电池电势与硝酸盐浓度呈正相关,在反应开始时,硝酸盐去除较快,电池电势迅速下降;在硝酸盐浓度降低后,阴极电子受体减少,电子消耗速率减慢,电池电势也随之缓慢变化。由极化曲线斜率算出体系内阻为600 Ω,最大功率密度为33 mW·m-2,与以氧气为受体的微生物燃料电池功率密度相当。
3 结论
g-C3N4-TiO2负载在碳纤维布上做为光催化阴极,同时利用生物阳极产电促进硝酸盐还原,水中硝酸盐浓度为100 mg·L-1时,反应3.5 h,硝酸盐去除效率达到72.57%,还原产物氮气选择性达到99.54%。在采用微生物作为阳极时,硝酸盐还原效率从40.00%提高到72.57%,生物阳极极大地提高了硝酸盐的还原效率。该体系巧妙地利用了微生物代谢产生的电子与质子,在还原过程中无需外加空穴清除剂与质子,极大地降低了成本。在本实验中同步实现污水生物降解、产电以及硝酸盐还原,且都取得了较好的效果,反应条件温和,催化剂制备简单,无金属掺杂,安全无污染,具有很大的实际应用价值。
-
-
[1]
Zang F X, Jin R C, Chen J X, et al. Chin. J. Catal., 2005, 232:424-429 doi: 10.1016/j.jcat.2005.04.014
-
[2]
Anderson J A. Catal. Today, 2011, 175:316-321 doi: 10.1016/j.cattod.2011.04.009
-
[3]
Wen Q, Wu Y, Zhao L X, et al. Fuel, 2010, 89:1381-1385 doi: 10.1016/j.fuel.2009.11.004
-
[4]
Krishnaraj R N, Karthikeyan R, Berchmans S, et al. Electro-chim. Acta, 2013, 112:465-472 doi: 10.1016/j.electacta.2013.08.180
-
[5]
Mansoorian H J, Mahvi A H, Jafari A J, et al. Enzyme Microb. Technol., 2013, 52:352-357 doi: 10.1016/j.enzmictec.2013.03.004
-
[6]
Lu X F, Wang Q L, Cui D L. J. Mater. Sci. Technol., 2010, 26:925-930 http://www.cnki.com.cn/Article/CJFDTotal-CLKJ201010013.htm
-
[7]
Jassby D, Budarz J F, Wiesner M. Environ. Sci. Technol., 2012, 46:6934-6941 doi: 10.1021/es202009h
-
[8]
Ding H R, Li Y, Lu A H, et al. Bioresour. Technol., 2010, 101:3500-3505 doi: 10.1016/j.biortech.2009.11.107
-
[9]
Ranjit K T, Krishnamoorthy R, Viswanathan B. J. Photochem. Photobiol. A, 1994, 81:55-58 doi: 10.1016/1010-6030(93)03772-9
-
[10]
Kudo A, Domen K, Maruya K, et al. Chem. Lett., 1987:1019-1022 doi: 10.1246/cl.1987.1019
-
[11]
Li Y X, Wasgestian F. J. Photochem. Photobiol. A, 1998, 112:255-259 doi: 10.1016/S1010-6030(97)00293-1
-
[12]
Gao W L, Jin R C, Chen M X, et al. Catal. Today, 2004, 90:331-336 doi: 10.1016/j.cattod.2004.04.043
-
[13]
Bems B, Jentoft F C, Schlogl R. Appl. Catal. B, 1999, 20:155-163 doi: 10.1016/S0926-3373(98)00105-2
-
[14]
Najah W, Mira J, Chantal G, et al. Appl. Catal. A, 2009, 368:1-8 doi: 10.1016/j.apcata.2009.07.038
-
[15]
Li L Y, Xu Z Y, Liu F L, et al. J. Photochem. Photobiol. A, 2010, 212:113-121 doi: 10.1016/j.jphotochem.2010.04.003
-
[16]
Anderson J A. Catal. Today, 2011, 175:316-3211 doi: 10.1016/j.cattod.2011.04.009
-
[17]
Hirayama J, Kondo H, Miura Y K, et al. Catal. Commun., 2012, 20:99-102 doi: 10.1016/j.catcom.2012.01.011
-
[18]
李越湘, 彭绍琴, 戴超.催化学报, 1999, 20:378-380 http://www.cnki.com.cn/Article/CJFDTotal-CHUA199903047.htmLI Yue-Xiang, PENG Shao-Qin, DAI Chao. Chin. J. Catal., 1999, 20:378-380 http://www.cnki.com.cn/Article/CJFDTotal-CHUA199903047.htm
-
[19]
Li Y X, Xiang Y, Peng S Q, et al. Electrochim. Acta, 2013, 87:794-800 doi: 10.1016/j.electacta.2012.09.023
-
[20]
Anderson J A. Catal. Today, 2012, 18:171-176 http://www.sciencedirect.com/science/article/pii/S0920586111004391
-
[21]
Doudrick K, Yang T, Hristovski K, et al. Appl. Catal. B, 2013, 136:40-47 http://www.sciencedirect.com/science/article/pii/S0926337313000623
-
[22]
Wang R, Yue M F, Cong R H, et al. J. Alloys Compd., 2015, 651:731-736 doi: 10.1016/j.jallcom.2015.08.182
-
[23]
Yan H J, Yang H X. J. Alloys Compd., 2011, 509:26-29 doi: 10.1016/j.jallcom.2010.09.201
-
[1]
-
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 2
- 文章访问数: 938
- HTML全文浏览量: 146




 下载:
下载:














 下载:
下载:

