 图 1
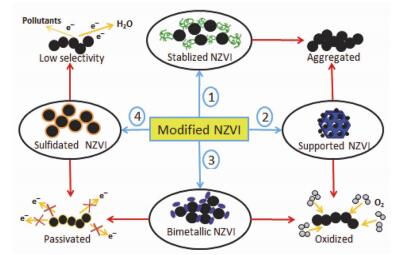
NZVI的改性策略(蓝色箭头)及其所改善的应用缺陷(红色箭头)关系图
Figure 1.
Diagram of modification strategies of NZVI (blue arrows) and its application drawbacks (red arrows) overcome by modified NZVI.
图 1
NZVI的改性策略(蓝色箭头)及其所改善的应用缺陷(红色箭头)关系图
Figure 1.
Diagram of modification strategies of NZVI (blue arrows) and its application drawbacks (red arrows) overcome by modified NZVI.

Citation: Tang Jing, Tang Lin, Feng Haopeng, Dong Haoran, Zhang Yi, Liu Sishi, Zeng Guangming. Research Progress of Aqueous Pollutants Removal by Sulfidated Nanoscale Zero-valent Iron[J]. Acta Chimica Sinica, 2017, 75(6): 575-582. doi: 10.6023/A17020045

硫化纳米零价铁去除水体污染物的研究进展
English
Research Progress of Aqueous Pollutants Removal by Sulfidated Nanoscale Zero-valent Iron
-
1 引言
自第二次工业革命以来, 由于工业的进一步发展, 水体污染日益严重.常见的污染物可分为重金属和有机物污染物.而传统的理化处理方法如化学、物理和生物法, 虽能处理这些污染物, 但同时也可能带来严重的二次污染, 因此研究人员致力于探索出既能有效降解目标污染物又能不对环境造成二次污染的处理方法.金属铁材料具有无毒、量丰富、成本低和易于制备等特点, 这使得铁系材料成为去除污染物的研究热点[1~6].零价铁化学活性强, 标准氧化还原电位E0(Fe2+/Fe0)大约等于-0.44 V, 因此还原能力强.随着纳米技术的出现, 由于纳米材料粒径达到纳米级, 表面原子占总原子的百分数急剧增加, 表面活性高, 反应速率迅速的特点为金属铁的应用开辟了新的研究方向, 因此纳米零价铁(NZVI)成为国内外研究的热点.
NZVI是指颗粒直径在1~100 nm范围内的零价铁颗粒, 它具有比表面积大、还原性强等特点.与宏观的零价铁材料相比, 它具有特殊性质, 如表面效应、体积效应和宏观量子隧道效应等[7].纳米零价铁颗粒相比于零价铁颗粒而言, 由于颗粒直径的减小, 表面原子占总原子的百分数显著增大, 由微米尺度时的1%~2%急剧增加到超过50%[8].随着纳米金属颗粒的表面积的增大而获得更高的表面能, 从而使纳米系列材料具有显著的反应活性.由于纳米零价铁的高反应活性, 使得其在水环境污染物的处理体系中具有优异的应用前景.
固然许多研究表明NZVI对有机物污染物具有很好的降解性能, 在环境污染治理方面也具有广阔的应用潜力, 但是由于其自身粒径小和活性高等特点导致在原位修复和储存等方面存在着局限[9, 10], 具体主要体现在如下三个方面: (1) 易团聚, NZVI跟普通的超微颗粒一样, 粒径小, 比表面积大, 由于表面效应使得颗粒相互间的结合力大于自身重量, 并且NZVI颗粒间存在磁性, 在水相中极易碰撞, 使得NZVI团聚为较大粒子或者呈链状, 导致其活性降低且难以迅速迁移到污染物附近; (2) 易氧化和钝化, NZVI化学活性高, 也就意味着其化学性质不稳定, 极易与周围介质(如氧气和水等)发生反应, 纯度较高的NZVI若直接暴露在空气中会自燃或冒火星, 缓慢接触空气中的氧气则容易在表面形成铁氧化物的壳层而降低活性[11, 12]; (3) 电子选择性差, 在与目标污染物作用时, 由NZVI产生的大部分电子无法有效地传递到反应基团, 而是传递到水相中的氢离子或溶解氧, 造成有效电子利用率降低[13, 14]; (4) 易流失, NZVI颗粒粒径小, 因此在原位修复过程中不容易回收, 而进入环境中的纳米级微粒对生态系统也存在潜在的威胁[15, 16].这四个方面主要限制了NZVI在实际中的应用, 因而, 针对NZVI易团聚、易被氧化、易钝化、电子选择性差等缺陷, 通过改性NZVI来优化提高其在实际水体中反应活性和分散性成为当今研究领域的新热点.目前, 改性策略大致可以分为四种(图 1): (1) 稳定型NZVI, 在液相还原法制备NZVI的过程中, 在合成反应液中加入适量的高分子稳定剂或表面活性剂(如淀粉和羧甲基纤维素等)来减弱NZVI间静电吸引力[17], 也就是能避免NZVI团聚为微米级颗粒, 通过维持其高比表面积从而提高其反应活性和迁移性.理论上讲, 高分子的添加能够增加空间位阻和颗粒间的静电排斥力, 使得NZVI颗粒在溶液中分布均匀, 极少团聚, 同时也能在一定程度上避免NZVI的高反应活性位点与周围介质的无效作用; (2) 负载型NZVI, 为了避免NZVI的团聚, 使NZVI生长于载体上, 使其在载体表面均匀地分布.负载型NZVI颗粒不仅提高了材料的比表面积, 进而提高了其与污染物的接触面积, 而且其载体本身具有的吸附性能能够加快污染物传递到活性位点, 因此有利于污染物降解反应[18~21].除此之外, 它还能减少NZVI颗粒进入环境的机率从而避免了其造成的环境风险; (3) 双金属型NZVI, 为了提高NZVI活性, 可以在其表面负载另外一种还原电位更高的金属单质如Cu[22], Ni[23, 24], Pd[25]等形成双金属纳米颗粒, 这不但可以使NZVI的活性吸附位点增多, 而且, 负载的单质贵重金属能催化氢解反应, 从而提高NZVI加氢反应能力, 也可降低NZVI被周围环境介质氧化而导致的损失; (4) 硫化型NZVI, 为了增加NZVI的活性, 尤其是碱性水体中的反应活性, 掺杂硫使得NZVI表面形成硫铁化物.疏水性较高的硫铁化物如四方硫铁矿和黄铁矿具有对污染物更高的亲和力[26, 27], 也就是说, 产生的电子倾向于传递到有机污染物分子而不是水分子, 这在一定程度上抑制了NZVI的析氢速率并提高了它的电子选择性.其中, 硫化型NZVI是近年来兴起的一项改性革命, 它将改性的研究重点从将提高NZVI反应活性转移到提高电子的选择性上.目前关于硫化型NZVI的综述类文章未见报道, 本文系统地梳理了近年来硫化型NZVI的合成及其在水环境修复领域中的反应机制, 并对硫化型NZVI的应用研究进行了较深刻的展望.
 图 1
NZVI的改性策略(蓝色箭头)及其所改善的应用缺陷(红色箭头)关系图
Figure 1.
Diagram of modification strategies of NZVI (blue arrows) and its application drawbacks (red arrows) overcome by modified NZVI.
图 1
NZVI的改性策略(蓝色箭头)及其所改善的应用缺陷(红色箭头)关系图
Figure 1.
Diagram of modification strategies of NZVI (blue arrows) and its application drawbacks (red arrows) overcome by modified NZVI.
2 硫化型NZVI的制备方法
总的来说, NZVI的硫化方法主要可以分为化学法和物理法.目前化学制备方法比较普遍, 相比较于NZVI而言, 硫化型NZVI已经在地下水和工业废水等领域展现了显著的优势, 它能更快速地降解有机物和去除重金属.尽管目前物理法制备的硫化型NZVI未有报道, 但是, 以零价铁和单质硫为原料, 通过球磨法合成微米级的硫化零价铁已有会议报道[28], 该微米级的硫化零价铁不仅能克服高成本的缺陷, 也能同时提高零价铁降解三氯乙烯的效率, 而本文主要介绍化学硫化法.
在化学合成方法中, 目前主要是在液相介质中硫化NZVI, 而不同的硫化试剂、硫化时间和硫负载量对硫化型NZVI的反应活性都有或多或少的影响.下面根据这些影响因素进行分类描述.
2.1 硫化试剂
目前使用的硫化试剂有连二亚硫酸钠、硫代硫酸盐和硫化物(如硫化钠), 然而不同的硫化试剂对这些硫化型NZVI的反应活性无明显影响[29].这是因为在本质上, 它们都能硫化NZVI, 使其表面形成硫铁化物.连二亚硫酸钠是一种在碱性pH中相当强的还原剂.在酸性溶液中, 能够水解为硫代硫酸盐和亚硫酸盐(Eq. 1))[26]; 而在碱性溶液中, 它能水解成亚硫酸盐和硫化物(Eq. 2)[30].硫代硫酸钠虽然不具有很强的还原能力, 但是它能发生岐化反应, 如Eq. 3[31], 生成亚硫酸盐和单质硫, 后者能够在单质铁的存在条件下被还原成硫铁化物(Eq. 4)[32, 33].而硫化钠, 硫化物的代表物, 是一种高度吸湿剂, 其在中性pH水相中则能分解出H2S或者HS ,它们是腐蚀性化学物质, 因此能够使单质铁表面形成一层硫铁化物的壳.
2.2 硫化时间
硫化时间以铁源被还原的时间节点分为前置硫化合成法和后置硫化合成法.前置硫化合成法最先是由Kim等[26]提出, 在溶液中的铁源被还原之前, 将连二亚硫酸钠加入到溶液中, 和硼氢化物一起作为还原剂与铁源反应形成硫化型NZVI; 后置硫化合成法是最近比较兴起的新方法, 具体的做法是合成的NZVI与溶液中的含硫物质反应形成硫化型NZVI[34, 35].研究表明, 这两种合成方法制备的硫化型NZVI在形貌上具有比较显著差异. 图 2为这两种硫化型NZVI代表性的透射电镜扫描(TEM)图[29].前置法制备的硫化型NZVI呈现出一些不均匀的与NZVI类似的球状粒子(图 2a白色箭头)和立方体形状(图 2a红色箭头)以及一些与硫化铁类似的扁平状结构(图 2a蓝色箭头).与之不同的是, 后置法合成的硫化型NZVI则呈现出均匀的球状颗粒, 并且团聚形成链状.研究还发现后置合成法制备的硫化型NZVI能很好地从水相中分离, 然而前置合成法制备的硫化型NZVI很难被0.2 μm的滤膜收集, 该现象的原因可能是因为前置合成的硫化型NZVI含有纤细和疏松的硫化铁颗粒, 这与TEM的研究结果一致.另外, XPS的研究发现, 后置合成法制备的硫化型NZVI的被氧化程度比前置法合成的高.尽管这两者在结构和组成上存在着一定差异, 但是它们都展现出相似的反应活性.在三氯乙烯的脱氯降解实验中, 前置法和后置法合成的硫化型NZVI的表观质量标准伪一级反应速率常数分别为(0.9±0.1)×10-3和(0.8±0.1)×10-3 L•g-1•min-1, 并且它们的中间产物组成也非常接近[29].
2.3 硫负载量
硫化制备的硫化型NZVI根据制备溶液中S与Fe元素的摩尔比不同可分为高S/Fe和低S/Fe的硫化型NZVI.有许多研究工作表明硫元素的负载量对该材料活性具有显著的影响[33, 34, 36].硫化型NZVI的反应活性随着硫负载量的增高呈现出先升高后降低的趋势.这是因为相对于未硫化的NZVI而言, 存在于NZVI表面的硫铁化物能够在同一平面上传导离域电子[37], 除此之外, 硫化型矿物比铁氧化物具有较低的亲水性, 因此Rajajayavel等[34]推断出硫铁化物的壳层能够增强三氯乙烯等疏水性有机物与材料的结合力并且能够更加有效地传导电子到该污染物而不是水分子, 从而避免了活性的无效损失.然而, 硫负载量的过度增加, 会导致过多的FeS2生成和零价铁还原活性的过度损失, 这使得硫化型NZVI的活性稍有降低; 较低的硫负载量会导致NZVI表面未能完全覆盖硫铁化物, 该材料的活性也就比合适硫负载量的硫化型NZVI的活性低[36].尽管目前针对硫负载量的研究很多, 但是所报道的确定的优化的硫负载量(即S/Fe比)不一致, 这可能是因为不同的研究组所采用的具体硫化方法有所不同, 并且S/Fe的计算方法也有或多或少的出入.为了规范硫化型NZVI的制备方法, 硫化方法和S/Fe比的规范需要进一步的优化和研究.
3 硫化型NZVI与水体有机污染物的反应机制
根据所降解污染物的种类(主要为重金属和有机污染物)和反应条件的不同, 硫化型NZVI与水体有机污染物与水体污染物的作用机制也有所不同, 只有深入了解其反应机制, 才能更好地为NZVI的硫化改性指明方向.总的来说, 目前的研究主要报道了三种反应机制:吸附作用、还原作用和氧化作用.
3.1 吸附作用
吸附机制被认为是一种在污染物去除体系中的普遍反应过程, 这是因为纳米材料表面一般存在丰富的含氧官能团[38], 其表面的含氧官能团能与污染物进行化学反应以共价键的形式或者通过分子间作用力即范德华力而结合.在硫化型NZVI去除重金属反应体系中, 吸附作用是一个很常见的反应机制.水体中常见的重金属或类金属, 如Ni, Co, Zn和Cd, 能被硫化型NZVI高效去除[38].以重金属Cd为例, 以连二亚硫酸钠为硫化剂, 采用前置硫化合成法制备的硫化型NZVI能够达到85 mg/g的去除能力, 该数值比纯NZVI超出100%以上[39].其中降解机理主要被认为是化学吸附作用, 即Cd2+与材料表面的FeS的离子交换作用(Eq. 5) 和Cd2+与反应位点≡FeSH+的络合作用(Eq. 6), 除此之外, FeSH+和Cd2+的共沉淀作用也可能发生(Eq. 7).硫化型NZVI之所以具有比纯NZVI更显著的重金属去除性能, 主要是因为硫离子的引入, 而大多数金属的硫化物溶度积比氧化物更小, 使得重金属更倾向于从水体中分离沉淀去除.而在水体有机污染物的去除过程中, 吸附作用往往与其他反应机制协同作用. Xu等[40]发现硫化型NZVI能高效吸附还原偶氮染料, 相对于纯NZVI, 降解效率的提高主要是由于材料表面的硫铁化物能加速电子传递和其较高的电子选择性.由此可以看出, 吸附作用在硫化型NZVI去除有机污染的过程中未起到决定性的作用, 并且相关研究报道不多.
3.2 还原作用
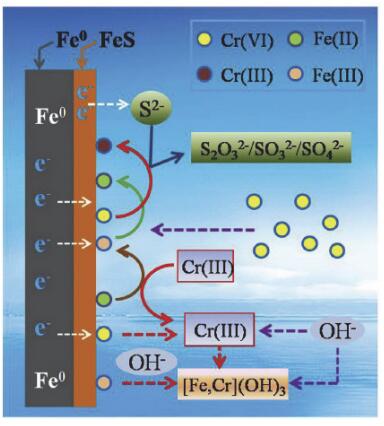
目前材料的电化学疏水性表征已经表明硫化型NZVI表面的铁硫化物比铁氧化物具有更优良的导电性和更强的疏水性[36, 41], 这意味着它比纯NZVI电子传递速率和电子选择性更高, 因此硫化型NZVI具有很强的还原能力.特别是在缺氧的水体中, 硫化型NZVI能高效地还原重金属和有机污染物.硫化型NZVI去除Cr(Ⅵ)的过程是一种典型的以还原为主的反应机制[42]. FeS@Fe0纳米颗粒去除Cr(Ⅵ)机理如图 3所示.固液界面的二价铁离子能被Cr(Ⅵ)氧化成三价铁离子, 这些表面的三价铁离子能够通过接受零价铁核产生的电子再次被还原成二价铁离子.即使较厚的铁氧化物壳能阻碍电子传递, 但是合适厚度的FeS由于其优异的导电性和较高的电负性能加速电子流.另一方面, 以FeS为导带的直接多电子传递能自发进行, 导致被吸附的Cr(Ⅵ)能得到电子被还原.然后, Cr(Ⅵ)被Fe(Ⅱ)和FeS原位还原, 同时也会产生铁氧化物如Fe3O4, Fe(OH)3和FeOOH以及各种硫化物.最后, 由于反应过程中溶液pH的上升, Cr(Ⅲ)与铁离子发生不可逆沉淀反应形成稳定的FexCr1-x(OH)3和Fe(OH)3-Cr(OH)3.除此之外, 放射性元素锝99 (99Tc)也能有效地被硫化型NZVI去除[35], 在再氧化固定实验中, 发现硫化后的NZVI能显著提高高锝酸盐被扣留的稳定性[43].
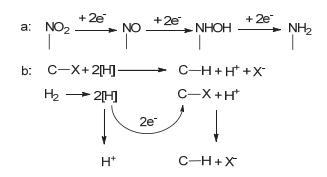
目前硫化型NZVI还原去除的有机物主要有硝基类和卤代有机污染物.虽然都是利用硫化型NZVI的还原性降解污染物, 然而这两类物质的作用机制有所不同, 其中硝基类物质被还原的具体作用机制为:硫化型NZVI作为还原剂, 被氧化失去电子传递到目标污染物, 从而使有毒物质转变为无毒或者毒性小的物质.最近研究表明, 对硝基酚能被NZVI或硫化型NZVI还原降解[36, 44, 45].在作用过程中, Fe0给出电子使得该类有机物上的硝基基团逐步还原成氨基基团, 如图 3a.由于氨基基团的毒性远小于硝基基团, 因此有机污染物的毒性大大降低, 使得污染水体得到一定程度的净化.而硫化型NZVI降解卤代有机物的过程往往涉及脱卤加氢(图 3b)这一关键步骤.硫化作用提高了NZVI的反应活性, 但NZVI和硫化型NZVI降解卤代有机物的过程大致类似[29, 46].首先, 硫化型NZVI腐蚀还原溶液氢离子产生氢气, 然后进一步将氢气分解成活性氢, 生成的活性氢能使碳卤键(C—X)断裂后形成碳氢键(C—H), 从而完成卤代有机物的降解过程[34].
3.3 氧化作用
在某些特殊的环境修复体系中, 与还原过程相反的是, 氧化过程也被认为是一种可能的反应机制.目前研究表明实验合成的NZVI一般以铁氧化物为壳, 零价铁为核的结构存在.另外, 某些研究通过调节壳核比例, 使得NZVI在氧化剂如氧气的存在下能反应生成数量可观的强氧化性物质, 从而能氧化重金属As(Ⅲ)[47]和降解有机物[48~50], 但是硫化型NZVI氧化去除有机物的研究不多, 并且关于重金属的氧化去除还没有相关报道.在溶解氧或者其他氧化剂的存在条件下, 硫化型NZVI与未硫化NZVI类似, 可以作为高级氧化降解有机污染物的异相芬顿试剂.以富氧水体为例, 有研究表明, NZVI能与分子氧反应产生能氧化甚至矿化有机物的活性氧物质[51, 52].未硫化的NZVI主要通过零价铁表面的亚铁氧化物活化分子氧, 而硫化型NZVI主要是通过材料表面的FeS活化分子氧, 由于FeS壳能加速电子流, 并且能在一定程度上抑制与水分子反应, 因此氧化能力也相应强一些[36].并且, 有研究表明硫化作用能抑制氧气与NZVI的直接反应, 使得反应更倾向于首先Fe—S键的断裂, 随后产生的Fe2+与S2-与氧气反应生成氧活性物质[53]. 图 5为硫化型NZVI在缺氧水体中还原降解对硝基酚在富氧水体中对硝基酚被硫化型NZVI产生的羟基自由基(•OH)氧化降解的示意图[36].另外, 溶液pH对活性氧物质的生成具有重大的影响[36].具体地讲, 在偏酸性溶液中, 通过双电子传递, 溶解氧能被硫化型NZVI还原成过氧化氢(H2O2) (Eq. 8), 生成的H2O2还可以被硫化型NZVI还原成水(Eq. 9), 紧接着, 在Fe2+的催化作用下, H2O2产生强氧化性的活性氧物质如•OH (Eq. 10);在中性溶液中, H2O2的生成可以通过氧化Fe2+与O2的初产物(Eqs. 11, 12), 然后, 活性氧物质通过Eq. 10产生; 然而, 在碱性条件下含水铁氧化物会生成, 同时少量的•OH也会产生, 如Eq. 13.显而易见, 在较低的溶液pH中, 富含氧的水体中倾向于生成更多的•OH.
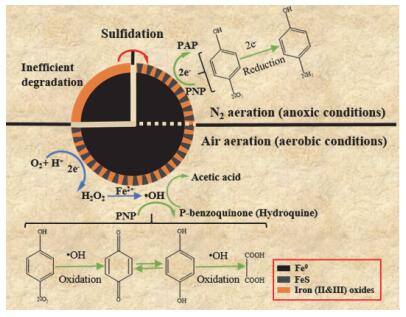 图 5
在富氧和缺氧体系中硫化型NZVI去除对硝基酚的主要降解机理图
Figure 5.
Main degradation mechanisms for p-nitrophenol (PNP) in sulfidated NZVI systems under aerobic or anoxic conditions[36]
图 5
在富氧和缺氧体系中硫化型NZVI去除对硝基酚的主要降解机理图
Figure 5.
Main degradation mechanisms for p-nitrophenol (PNP) in sulfidated NZVI systems under aerobic or anoxic conditions[36]
3.4 硫化型NZVI的性能与降解机制
研究硫化型NZVI的性能及其去除污染物的反应机制对其处理水体污染物的应用上具有重大意义. 表 1和表 2总结了硫化型NZVI的应用性能, 分别简要地说明其与重金属和有机物污染物的反应机制.近些年关于硫化型NZVI的研究越来越多, 同时硫化型NZVI在合成方法及其与污染物的去除机理等方面的研究也会有进一步的突破.因此, 表 1未来还有待于进一步地完善.
 表 1
硫化型NZVI的性能及其与重金属污染物的作用机制
Table 1.
The properties of sulfidated NZVI and its mechanisms with heavy metals
表 1
硫化型NZVI的性能及其与重金属污染物的作用机制
Table 1.
The properties of sulfidated NZVI and its mechanisms with heavy metals

 表 2
硫化型NZVI的性能及其与有机污染物的作用机制
Table 2.
The properties of sulfidated NZVI and its mechanisms with organic pollutants
表 2
硫化型NZVI的性能及其与有机污染物的作用机制
Table 2.
The properties of sulfidated NZVI and its mechanisms with organic pollutants

4 总结与展望
由于NZVI在实际水体中存在着易团聚、易被氧化、易钝化、电子选择性差等缺陷, NZVI的改性工作成为当今铁环境污染修复领域中的研究热点.尽管目前的改性方式百花齐放, 但是硫化型NZVI材料的研究更具有突破性, 目前关于硫化零价铁的一些方面的研究还不够成熟, 需要进一步探索.
(1) 合成稳定高性能的硫化型NZVI及其替代品.最新研究成果表明, 硫化型NZVI能够有效地抑制其与水之间的反应, 从而减少电子的无效损失.出现这一现象的主要原因是硫化能提高NZVI表面的疏水性从而降低了纳米铁对水的还原.因此, 未来关于NZVI的研究热点将会逐渐从提高NZVI的反应活性转移到提高NZVI的电子选择性. NZVI电子选择性的提高不仅可以通过提高其疏水性来使电子高效地传递到有机污染物的疏水官能团上, 也可以通过改性NZVI靶向特异性去除特定的有机污染物.目前关于硫化型NZVI材料性能稳定性报道还不够系统, 但是值得提出的是, 硫的溶出是不可避免的.然而, 与NZVI相比, 硫化作用使得NZVI的稳定性得到较显著的提高[41].目前仍需要深入研究影响该材料稳定性的主要因素, 也亟需开发出稳定性较高的硫化型NZVI或其他类似的掺杂型NZVI材料.
(2) 构筑以氧化反应为主导的硫化型NZVI氧化修复体系.硫化型NZVI往往利用零价态铁的强给电子性能还原降解有机物, 但是在这种以还原为主导的修复体系, 有机物一般只能脱卤或部分断键, 水体的修复程度低.而利用硫化型NZVI活化分子氧(或其他氧化剂)产生高活性氧化性物种, 如过氧化氢、氧负离子自由基、羟基自由基等, 构筑以氧化反应为主导的零价铁氧化修复体系, 可望达到深度氧化或彻底矿化有机污染物的目的.目前关于硫化型NZVI材料活化分子氧的氧化去除有机物的研究已初有报道, 但关于调控分子氧或其他氧化剂的活化途径及活性氧物质产量还需进一步研究.
(3) 研究水体常见生物与硫化型NZVI的互相作用机制.考虑到硫溶出的环境效应, 也为了进一步研究硫化型NZVI的实际应用潜力, 水体生物如浮游类植物和微生物对材料的活性以及该材料对水体生态系统的影响都需要被纳入考察范围之内.已有报道提到, 藻类的有机质能够降低某一硫化型NZVI的颗粒结合效率, 而高浓度的该纳米材料能导致该浮游植物的生长延缓[60].目前关于该方面的研究很少涉及, 需要更多的研究.
(4) 研究更大尺寸的硫化零价铁颗粒的应用潜能.硫化型NZVI仍存在一些实际应用的局限, 纳米颗粒制备成本高, 并且在运输和保存方法也存在安全隐患.目前关于微米级的零价铁处理实际废水的研究也逐渐成熟, 为了提高硫化型零价铁的实际应用能力, 研究微米级或更大尺寸的硫化型零价铁也许是未来研究的方向.
-
-
[1]
Zhang, Y.; Zeng, G.; Tang, L.; Huang, D.; Jiang, X.; Chen, Y. Biosens. Bioelectron. 2007, 22, 2121. doi: 10.1016/j.bios.2006.09.030
-
[2]
Tang, L.; Zeng, G.; Shen, G.; Li, Y.; Zhang, Y.; Huang, D. Environ. Sci. Technol. 2008, 42, 1207. doi: 10.1021/es7024593
-
[3]
Tang, L.; Fang, Y.; Pang, Y.; Zeng, G.; Wang, J.; Zhou, Y.; Deng, Y.; Yang, G.; Cai, Y.; Chen, J. Chem. Eng. J. 2014, 254, 302. doi: 10.1016/j.cej.2014.05.119
-
[4]
Tang, L.; Yang, G.; Zeng, G.; Ca, Y.; Li, S.; Zhou, Y.; Pang, Y.; Liu, Y.; Zhang, Y.; Luna, B. Chem. Eng. J. 2014, 239, 114. doi: 10.1016/j.cej.2013.10.104
-
[5]
李锦祥, 秦荷杰, 张雪莹, 关小红, 化学学报, 2017, DOI: 10.6023/A17010007.Li, J.; Qin, H.; Zhang, X.; Guan, X. Acta Chim. Sinica 2017, DOI: 10.6023/A17010007.
-
[6]
陈海军, 黄舒怡, 张志宾, 刘云海, 王祥科, 化学学报, 2017, DOI:10. 6023/A17010039.Chen, H.; Huang, S.; Zhang, Z.; Liu, Y.; Wang, X. Acta Chim. Sinica 2017, DOI: 10.6023/A17010039.
-
[7]
Zhou, Q.; Li, J.; Wang, M.; Zhao, D. Crit. Rev. Env. Sci. Tec. 2016, 46, 783. doi: 10.1080/10643389.2016.1160815
-
[8]
梁震, 王焰新, 环境保护, 2002, 4, 15. doi: 10.3969/j.issn.1004-6216.2002.02.006Liang, Z.; Wang, Y. Environ. Prot. 2002, 4, 15. doi: 10.3969/j.issn.1004-6216.2002.02.006
-
[9]
Jiemvarangkul, P.; Zhang, W.; Lien, H. L. Chem. Eng. J. 2011, 170, 482. doi: 10.1016/j.cej.2011.02.065
-
[10]
Phenrat, T.; Saleh, N.; Sirk, K.; Tilton, R. D.; Lowry, G. V. Environ. Sci. Technol. 2007, 41, 284. doi: 10.1021/es061349a
-
[11]
Shi, L.; Zhang, X.; Chen, Z. Water Res. 2011, 45, 886. doi: 10.1016/j.watres.2010.09.025
-
[12]
Greenlee, L. F.; Torrey, J. D.; Amaro, R. L.; Shaw, J. M. Environ. Sci. Technol. 2012, 46, 12913. doi: 10.1021/es303037k
-
[13]
Fan, D.; O'Brien Johnson, G.; Tratnyek, P. G.; Johnson, R. L. Environ. Sci. Technol. 2016, 50, 9558. doi: 10.1021/acs.est.6b02170
-
[14]
Fan, D.; O'Carroll, D. M.; Elliott, D. W.; Xiong, Z.; Tratnyek, P. G.; Johnson, R. L.; Garcia, A. N. Remediat. J. 2016, 26, 27.
-
[15]
Ma, X.; Gurung, A.; Deng, Y. Sci. Total Environ. 2013, 443, 844. doi: 10.1016/j.scitotenv.2012.11.073
-
[16]
El-Temsah, Y. S.; Joner, E. J. Chemosphere 2012, 89, 76. doi: 10.1016/j.chemosphere.2012.04.020
-
[17]
He, F.; Zhao, D.; Liu, J.; Roberts, C. B. Ind. Eng. Chem. Res. 2007, 46, 29. doi: 10.1021/ie0610896
-
[18]
Liu, Z.; Zhang, F.; Hoekman, S. K.; Liu, T.; Gai, C.; Peng, N. ACS Sustain. Chem. Eng. 2016, 4, 3261. doi: 10.1021/acssuschemeng.6b00306
-
[19]
Shi, L. N.; Zhang, X.; Chen, Z. L. Water Res. 2011, 45, 886. doi: 10.1016/j.watres.2010.09.025
-
[20]
Chen, Z.; Wang, T.; Jin, X.; Chen, Z.; Megharaj, M.; Naidu, R. J. Colloid Interface Sci. 2013, 398, 59. doi: 10.1016/j.jcis.2013.02.020
-
[21]
Wu, Y.; Yang, M.; Hu, S.; Wang, L.; Yao, H. Toxicol. Environ. Chem. 2014, 96, 227. doi: 10.1080/02772248.2014.931960
-
[22]
Krasae, N.; Wantala, K.; Tantriratna, P.; Grisdanurak, N. App. Env. Res. 2014, 36, 15.
-
[23]
Ryu, A.; Jeong, S. W.; Jang, A.; Choi, H. Appl. Catal. B-Environ. 2011, 105, 128. doi: 10.1016/j.apcatb.2011.04.002
-
[24]
Xie, Y.; Fang, Z.; Cheng, W.; Tsang, P. E.; Zhao, D. Sci. Total Environ. 2014, 485, 363. http://www.sciencedirect.com/science/article/pii/S0048969714003696
-
[25]
Shih, Y. H.; Chen, M. Y.; Su, Y. F. Appl. Catal. B-Environ. 2011 105, 24. doi: 10.1016/j.apcatb.2011.03.024
-
[26]
Kim, E. J.; Kim, J. H.; Azad, A. M.; Chang, Y. S. ACS Appl. Mater. Interfaces 2011, 3, 1457. doi: 10.1021/am200016v
-
[27]
Park, S. W.; Kim, S. K.; Kim, J. B.; Choi, S. W.; Inyang, H. I.; Tokunaga, S. Water Air Soil Pollut:Focus. 2006, 6, 97. doi: 10.1007/s11267-005-9016-z
-
[28]
何锋, 铁环境化学及污染控制技术研讨会, 上海, 2016, p. 41.He, F. In Iron Environmental Chemistry and Pollution Control Technology Seminar, Shanghai, 2016, p. 41.
-
[29]
Yanlai, H.; Weile, Y. Environ. Sci. Technol. 2016, 50, 12992. doi: 10.1021/acs.est.6b03997
-
[30]
Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements, 2nd ed., Elsevier Butterworth Heinemann, 1997.
-
[31]
Kappes, M.; Frankel, G. S.; Sridhar, N.; Carranza, R. M. J. Electrochem. Soc. 2012, 159, C195. doi: 10.1149/2.085204jes
-
[32]
Macdonald, D. D.; Roberts, B.; Hyne, J. B. Corros. Sci. 1978, 18, 411. doi: 10.1016/S0010-938X(78)80037-7
-
[33]
Schmitt, G. Corrosion 1991, 47, 285. doi: 10.5006/1.3585257
-
[34]
Rajajayavel, S. R. C.; Ghoshal, S. Water Res. 2015, 78, 144. doi: 10.1016/j.watres.2015.04.009
-
[35]
Fan, D.; Anitori, R. P.; Tebo, B. M.; Tratnyek, P. G. Environ. Sci. Technol. 2013, 47, 5302. doi: 10.1021/es304829z
-
[36]
Tang, J.; Tang, L.; Feng, H.; Zeng, G.; Dong, H.; Zhang, C.; Huang, B.; Deng Y.; Wang, J.; Zhou, Y. J. Hazard. Mater. 2016, 320, 581. doi: 10.1016/j.jhazmat.2016.07.042
-
[37]
Butler, E. C.; Hayes, K. F. Environ. Sci. Technol. 2001, 35, 3884. doi: 10.1021/es010620f
-
[38]
Zou, Y.; Wang, X.; Khan, A.; Wang, P.; Liu, Y.; Alsaedi, A.; Hayat, T.; Wang, X. Environ. Sci. Technol. 2016, 50, 7290. doi: 10.1021/acs.est.6b01897
-
[39]
Su, Y.; Adeleye, A. S.; Keller, A. A.; Huang, Y.; Dai, C.; Zhou, X.; Zhang, Y. Water Res. 2015, 74, 47. doi: 10.1016/j.watres.2015.02.004
-
[40]
Xu, C.; Zhang, B.; Wang, Y.; Shao, Q.; Zhou, W.; Fan, D.; Bandstra, J. Z.; Shi, Z.; Tratnyek, P. G. Environ. Sci. Technol. 2016, 50, 11879. doi: 10.1021/acs.est.6b03184
-
[41]
Li, D.; Mao, Z.; Zhong, Y.; Huang, W.; Wu, Y.; Peng, P. Water Res. 2016, 103, 1. doi: 10.1016/j.watres.2016.07.003
-
[42]
Du, J.; Bao, J.; Lu, C.; Werner, D. Water Res. 2016, 102, 73. doi: 10.1016/j.watres.2016.06.009
-
[43]
Fan, D.; Anitori, R. P.; Tebo, B. M.; Tratnyek, P. G. Environ. Sci. Technol. 2014, 48, 7409. doi: 10.1021/es501607s
-
[44]
Tang, L.; Tang, J.; Zeng, G.; Yang, G.; Xie, X.; Zhou, Y.; Pang, Y.; Fang, Y.; Wang, J.; Xiong, W. Appl. Surf. Sci. 2015, 333, 220. doi: 10.1016/j.apsusc.2015.02.025
-
[45]
Ling, X.; Li, J.; Zhu, W.; Zhu, Y.; Sun, X.; Shen, J.; Han, W.; Wang, L. Chemosphere 2012, 87, 655. doi: 10.1016/j.chemosphere.2012.02.002
-
[46]
Zhuang, Y.; Ahn, S.; Luthy, R. G. Environ. Sci. Technol. 2010, 44, 8236. doi: 10.1021/es101601s
-
[47]
Ramos, M. A.; Yan, W.; Li, X. Q.; Koel, B. E.; Zhang, W. X. J. Phys. Chem. C 2009, 113, 14591. doi: 10.1021/jp9051837
-
[48]
Ai, Z.; Gao, Z.; Zhang, L.; He, W.; Yin, J. J. Environ. Sci. Technol. 2013, 47, 5344. doi: 10.1021/es4005202
-
[49]
Wang, L.; Cao, M.; Ai, Z.; Zhang, L. Environ. Sci. Technol. 2014, 48, 3354. doi: 10.1021/es404741x
-
[50]
Liu, W.; Ai, Z.; Cao, M.; Zhang, L. Appl. Catal. B-Environ. 2014, 150~151, 1.
-
[51]
Xiong, Z.; Lai, B.; Yang, P.; Zhou, Y.; Wang, J.; Fang, S. J. Hazard. Mater. 2015, 297, 261. doi: 10.1016/j.jhazmat.2015.05.006
-
[52]
Keenan, C. R.; Sedlak, D. L. Environ. Sci. Technol. 2008, 42, 1262. doi: 10.1021/es7025664
-
[53]
Song, S.; Su, Y.; Adeyemi, S. A.; Zhang, Y. Appl. Catal. B-Environ. 2017, 201, 211. doi: 10.1016/j.apcatb.2016.07.055
-
[54]
Su, Y.; Adeleye, A. S.; Huang, Y.; Zhou, X.; Keller, A. A.; Zhang, Y. Sci. Rep. 2016, 6, 24358. doi: 10.1038/srep24358
-
[55]
Yang, X.; David, M. C. Environ. Sci. Technol. 2010, 44, 8649. doi: 10.1021/es102451t
-
[56]
Ariel, N. G.; Hardiljeet, K. B.; Denis, M. O. Environ. Sci. Technol. 2016, 50, 5243. doi: 10.1021/acs.est.6b00734
-
[57]
David, T.; Dimin, F.; Paul, G. T.; Eun-Ju, K.; Yoon-Seok, C. Environ. Sci. Technol. 2012, 46, 12484. doi: 10.1021/es303422w
-
[58]
Kim, E. J.; Murugesan, K.; Kim, J. H.; Tratnyek, P. G.; Chang, Y. S. Ind. Eng. Chem. Res. 2013, 52, 9343. doi: 10.1021/ie400165a
-
[59]
Eun-Ju, K.; Jae-Hwan, K.; Yoon-Seok, C.; David, T.; Paul, G. T. Environ. Sci. Technol. 2014, 48, 4002. doi: 10.1021/es405622d
-
[60]
Adeleye, A. S.; Stevenson, L. M.; Su, Y.; Nisbet, R. M.; Zhang, Y.; Keller, A. A. Environ. Sci. Technol. 2016, 50, 5597. doi: 10.1021/acs.est.5b06251
-
[1]
-
图 5 在富氧和缺氧体系中硫化型NZVI去除对硝基酚的主要降解机理图
Figure 5 Main degradation mechanisms for p-nitrophenol (PNP) in sulfidated NZVI systems under aerobic or anoxic conditions[36]
表 1 硫化型NZVI的性能及其与重金属污染物的作用机制
Table 1. The properties of sulfidated NZVI and its mechanisms with heavy metals

表 2 硫化型NZVI的性能及其与有机污染物的作用机制
Table 2. The properties of sulfidated NZVI and its mechanisms with organic pollutants

-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 105
- 文章访问数: 6381
- HTML全文浏览量: 1996



 下载:
下载:




 下载:
下载:

