 图1
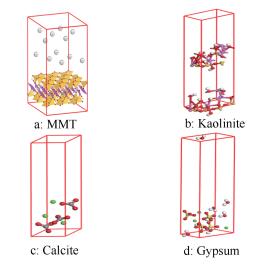
四种矿物质最低能量构型示意图
Figure1.
Minimal energy configurations of four mineral substances
图1
四种矿物质最低能量构型示意图
Figure1.
Minimal energy configurations of four mineral substances

Citation: WANG Qing, LI Chu-an, PAN Shuo, JIANG Jia-qi. A molecular simulation study on the adsorption of CH4 and CO2 on the mineral substances in oil shale[J]. Journal of Fuel Chemistry and Technology, 2017, 45(11): 1310-1316.

CH4和CO2在油页岩中矿物质结构内部吸附的分子模拟
English
A molecular simulation study on the adsorption of CH4 and CO2 on the mineral substances in oil shale
-
Key words:
- oil shale
- / mineral
- / molecular simulation
- / adsorption
- / CH4
- / CO2
-
众所周知,世界对能源的需求日益增加,石油储量日益枯竭,因此,寻求一种非常规的替代能源是未来能源需求的趋势,油页岩作为重要的补充和替代能源之一[1],储量十分巨大,据统计,其蕴藏资源量约有为1×1013 t,比煤资源储量多约40%[2]。油页岩是一种富含有机质、具有微细层理、可燃烧的细粒沉积岩[3]。随着现代油页岩工业的发展,对油页岩的利用已由单一的炼油向着产品多元化,产品深加工的方向前进。油页岩干馏炼油制气作为现代油页岩综合利用产业的前端,使得油页岩热解成为产业链中核心环节,而热解气的生成与释放对于油页岩干馏过程是尤为关键的,直接影响出油率、出焦率等重要的工业指标。因此,研究热解气中主要气态热解产物的输运和吸附规律将有助于理解油页岩热解过程及为热解气的生成与脱挥发分过程提供有力的理论依据和实践指导[4]。
长期以来,虽然学者们采用各种物理和化学方法对油页岩中矿物质的结构以及矿物质与有机质的相互作用进行了探索,但这些基本上仍然停留在叙述性、半经验和半定量的阶段,还不能完全与众多实验数据进行关联。计算机分子模拟相比于传统实验是一种可以在分子水平对复杂体系进行研究的有效手段。分子模拟技术深入探索油页岩中矿物质与其热解产物相关研究报道还较少,更多地是集中在生物质和煤等大分子结构特征与反应性之间的关系以及在热解过程中产物生成机理方面的研究工作。研究初期,吉利明等[5, 6]通过甲烷吸附实验,证明了蒙脱石黏土的吸附能力大于高岭石。孙仁远等[7]对页岩中黏土矿物进行了甲烷吸附的分子模拟,证明了伊利石的吸附能力最强。侯新娟等[8]对煤结构进行了量子化学计算并解释了煤分子结构的反应性,证明了煤催化加氢产物大部分是芳香族和环烷族烃。Yang等[9]应用分子动力学方法,研究了CO2在黏土孔隙中的扩散系数和吸附行为证明了受限二氧化碳的各向异性平移扩散较慢。
因此,本研究借助分子模拟技术,采用巨正则蒙特卡洛方法(Grand Canonical Monte Carlo, GCMC)和分子动力学方法(Molecular Dynamics, MD),研究在不同温度、不同压力下,CH4和CO2在蒙脱石、高岭石、方解石和生石膏中的输运和吸附机理。从分子水平研究黏土矿物(蒙脱石、高岭石)、脆性矿物方解石、可溶矿物石膏对甲烷和二氧化碳的吸附行为,系统地考察油页岩中各个矿物质对热解主要产物的影响,为油页岩干馏过程提供理论依据并加深对热解过程中的气体吸附机理的理解,已期实现提高油页岩热解转化率和油产率,同时对于油页岩热解过程中生油母质和矿物热解行为的研究具有重大意义,为今后油页岩中矿物与液态有机组合的相互作用起到理论指导意义,并以提高页岩油的品质。
1 模拟体系
1.1 分子模型的搭建
假设四种矿物质均为无水化理想模型,利用Materials Studio2017建立高岭石、方解石、生石膏和蒙脱石的矿物模型[10]。
高岭石是一种含水的铝硅酸盐,化学式为Al2Si2O5(OH)4,其基本结构特征为:a=0.51 nm,b=0.89 nm,c=0.74 nm,α=92°,β=105°,γ=90°,平均密度2.62 g/cm3。方解石是一种碳酸钙矿物,分子式为CaCO3,其基本结构特征为:a=0.5 nm,b=0.5 nm,c= 1.71nm,α=90°,β=90°,γ=120°,平均密度2.71 g/cm3。生石膏即天然二水石膏,化学式为CaSO4·2H2O,其基本结构特征为:a=0.57 nm,b=1.52 nm,c=0.65 nm,α=90°,β=118°,γ=90°,平均密度2.31 g/cm3。对矿物扫描电镜特征孔隙划分方案,分别将直径小于0.6 nm、0.6-2 nm、2-50 nm、50 nm-2 μm、2-50 μm、>50 μm的孔隙称之为超微孔、微孔、中孔、大孔、毛细孔和巨毛细孔。矿物质的比表面积直接决定了矿物质表面的反应能力以及吸附容量的大小。蒙脱石中多发育圆形、狭缝状的大孔与毛细孔,且总比表面积最大;高岭石中多发育不规则、狭缝状的中孔与大孔,比表面积小于蒙脱石;生石膏多发育微孔与中孔,比表面积小于高岭石;方解石多发育超微孔与微孔,且比表面积最小[11]。
蒙脱石的结构最为复杂,蒙脱石是一个铝氧八面体片夹在两个硅氧四面体片中间而组成的铝硅酸盐,根据蒙脱石(MMT)基本结构特征(2:1型层状叶蜡石结构;单斜晶体,空间群类型C2/m;晶胞参数a=0.52 nm,b=0.92 nm,c=1.013 nm,α=90°,β=90°,γ=90°,平均密度2.82 g/cm3)建立了模拟计算3×2×2的超晶胞,四面体与八面体共角顶相连,其中,白色为氢原子,红色为氧原子,灰色为钾原子,黄色四面体是四个氧原子和一个硅原子组成的硅氧四面体,紫色的是六个氧原子和一个铝原子组成的铝氧八面体。无论是四面体还是八面体,相邻的原子不能被同时取替,该模型中每32个硅原子有一个被铝取替,每八个铝有一个被镁取替。类质同象产生的层电荷为0.75,产生的层间负电荷可以由K+与Mg2+进行平衡,离子的位置可以由Sorption模块的location任务确定。蒙脱石晶胞的结构式为K0.75(Si7.75Al0.25)(Al3.5Mg0.5)O20(OH)4[12, 13]。
1.2 计算模型的优化
在吸附模拟之前,对矿物质模型进行结构优化,搜索势能最低点即能量最小化,得到的几何优化结构。优化过程采用分子动力学模块Forcite plus中的Geometry Optimization任务对所建立的结构模型进行优化,获得稳定的矿物模型。Geometry Optimization模块的设置参数为:形态优化方法选择smart;质量(Quality)设定为Fine;力场设定为COMPASS[14]; 电荷计算为Forcefield assigned;静电力加和方法为Ewald;范德华力加和方法为Atom based。蒙脱石、高岭石、方解石和生石膏优化后的模型结构见图 1。蒙脱石、高岭石、方解石和生石膏分子经优化后,采用周期性边界条件,模拟盒子的大小均不发生改变,能量均明显下降,其中,蒙脱石分子中钾原子脱离出来;高岭石分子中层间距离增大;方解石分子中碳氧组合数位置发生改变并相应减少;生石膏分子中水分子脱离出来。
1.3 计算方法
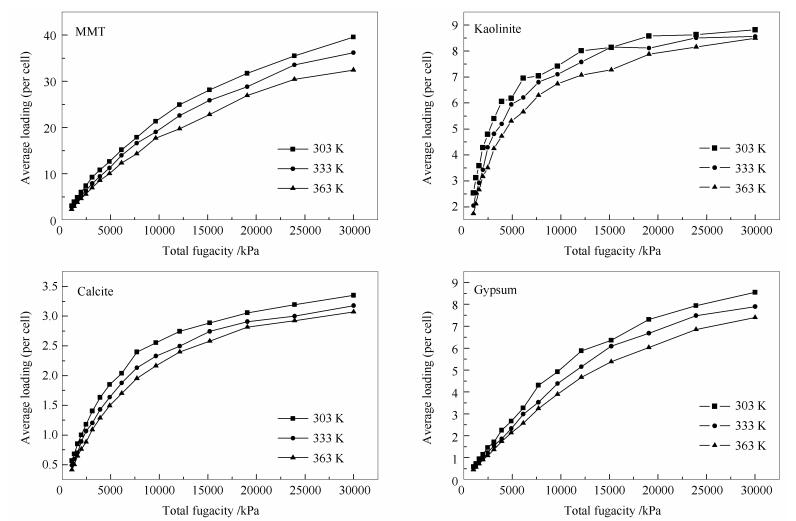
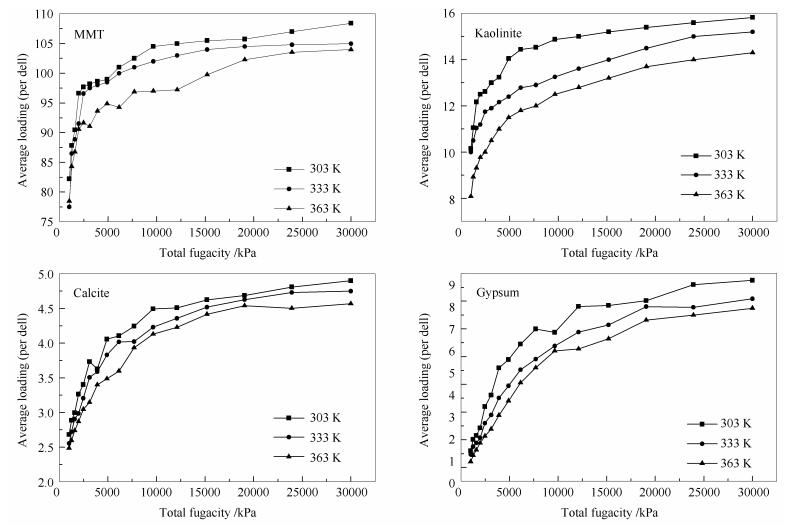
Astashov等[15]和Liu等[16]的研究表明,GCMC方法是分析多孔材料吸附机理和输运等微观机制的有力工具。本研究中等温吸附量与吸附热均采用巨正则蒙特卡洛模拟方法。模拟细节如下:采用Sorption模块中的Adsorption isothem任务对不同矿物分子吸附量进行计算。模拟体系采用周期性边界条件。Sorption模块参数设置:任务选择Adsorption isothem;平衡步数(Equilibration steps)为10 000;模拟加载最大步数(Production steps)为100 000;计算方法为Metropolis;Quality为Fine; 吸附质为CH4和CO2;压力为1 000 kPa-30 000 kPa;力场选择COMPASS; 电荷计算由力场分配;静电力加和方法为Ewald;范德华力加和方法为Atom based;温度的设定首先考虑到吉利明等[5]对泥页岩中黏土矿物甲烷的吸附实验以及孙仁远等[7]对页岩中黏土矿物吸附特性分子模拟的温度,其次油页岩的热解通常包括三个过程,首先是油页岩的加热过程,当温度达到105 ℃左右时,发生的主要变化是油页岩中水分的脱除,当热解温度达到(400-450 ℃)油页岩中矿物质才发生细微变化[17],故将温度分别设定为303、333和363 K。不同温度和压力条件下的CH4/CO2 单组分气体在蒙脱石、高岭石、方解石和生石膏中的等温吸附线见图 2、图 3。
吸附热模块参数设置:任务选择Fixed pressure,其他参数同上。
2 结果与讨论
2.1 等温吸附量
由图 2、图 3可知,蒙脱石、高岭石、方解石和生石膏四种模型对CH4/CO2单组分气体在不同压力下的等温线均符合Langmuir吸附的特征。Ji等[18]研究表明,矿物对CH4/CO2气体的最大吸附量主要受到比表面积的影响,与其比表面积成正比。在温度和压力相同条件下,蒙脱石对单组分气体CH4/CO2 的吸附量最大,其次是高岭石和生石膏,吸附量最小的是方解石,这一结果与Ross等[19]研究页岩甲烷吸附量与微孔隙体积实验和吉利明等[5, 6]分别在三个温度点(35、50和65 ℃)对蒙脱石、高岭石、伊利石等黏土矿物进行甲烷等温吸附实验结论是一致,证明了本研究所构建的四种矿物质分子模型的合理性。由图 2、图 3还可知,在同一温度,低压区阶段,四种矿物质分子对CH4/CO2单组分气体的吸附量随着压力的增大而快速变大,CO2的增速要更快,几乎成线性增加,随着压力的继续增大,吸附量缓慢增加直至最后接近恒定值。是由于随着温度的升高,导致矿物质分子动能增大使运动加剧,矿物质分子活性表面上的水分子数量将减少,矿物质分子表面活性增强,CH4和CO2与活性表面接触概率增加使其吸附量增大;当温度进一步升高后,矿物质分子获得更大的动能,布朗运动加剧,CH4和CO2受到层间引力作用减弱最后趋近于平衡。在同一压力下,随着温度的升高,四种矿物质对CH4和CO2分子的吸附量均减小,表明高温不利于CH4和CO2单组分气体的吸附[20]。这是因为温度的升高增加了CO2和CH4分子的动能,使它不易被矿物质表面吸附。相同温度和压力下CO2的吸附量要大于CH4的吸附量,说明了矿物质分子对单组分的吸附难易程度也是CO2大于CH4,这一结论与Krooss等[21]和Mastalerz等[22]的研究结果一致。
2.2 吸附热
吸附热是区分化学吸附和物理吸附的一个重要热力学参数,吸附热大于42 kJ/mol时为化学吸附,吸附热小于42 kJ/mol时为物理吸附[23], 同时吸附热的大小也是衡量吸附强弱的重要指标。
由表 1可知,四种矿物质分子对CH4的模拟等量吸附热为7.301-15.178 kJ/mol,属于物理吸附。同温度一下随着压力的不断增加等量吸附热大体呈增加趋势,这和矿物质分子对CH4吸附是吸热过程是一致的。由表 2可知,四种矿物质分子对CO2的模拟等量吸附热为30.034-41.249 kJ/mol,属于物理吸附,CO2的变化比较复杂,这可能是由于矿物质与CO2相互作用所导致的。CH4和CO2两者都是随着温度的升高,等量吸附热随之减小,表明温度与等量吸附热成负相关,即温度越高,等量吸附热也就越小,造成这一结论的原因是温度升高导致CH4和CO2分子的动能增加,使之更加容易逃脱矿物质分子模型表面的束缚,最终导致CH4和CO2分子的吸附热也随之降低。这一结论与前面等温吸附量时所得出的高温不利于矿物质分子对气体吸附的结论是一致的。
Pressure p/MPa MMT Qst/(kJ·mol-1) Kaolinite Qst/(kJ·mol-1) Calcite Qst/(kJ·mol-1) Gypsum Qst/(kJ·mol-1) 303 K 333 K 363 K 303 K 333 K 363 K 303 K 333 K 363 K 303 K 333 K 363 K 1 8.330 8.146 8.021 13.665 13.075 12.920 9.894 9.966 9.807 6.673 6.389 6.372 2 8.594 8.335 8.314 14.184 13.631 13.472 10.109 10.016 10.068 6.971 6.682 6.816 3 8.983 8.560 8.289 14.677 14.259 13.619 10.410 10.238 10.159 7.109 7.075 6.912 4 9.142 8.816 8.399 15.100 14.385 13.849 10.523 10.372 10.121 7.519 7.226 7.205 5 9.129 8.824 8.590 15.360 14.941 14.351 10.694 10.489 10.406 7.678 7.448 7.406 6 9.322 8.891 8.728 15.468 15.067 14.636 10.887 10.690 10.623 8.033 7.607 7.464 7 9.548 9.042 8.673 15.690 15.284 14.975 10.941 10.745 10.774 8.184 7.699 7.527 8 9.669 9.075 8.870 15.686 15.514 14.878 11.104 10.853 10.746 8.431 8.017 7.556 9 9.644 9.217 8.799 15.949 15.443 14.970 11.242 10.974 10.807 8.464 7.966 7.799 10 9.858 9.468 9.033 15.999 15.518 15.113 11.276 11.121 10.824 8.924 8.280 8.042 Average 9.222 8.837 8.572 15.178 14.712 14.278 10.708 10.546 10.434 7.799 7.439 7.301 Pressure p/MPa MMT Qst/(kJ·mol-1) Kaolinite Qst/(kJ·mol-1) Calcite Qst/(kJ·mol-1) Gypsum Qst/(kJ·mol-1) 303 K 333 K 363 K 303 K 333 K 363 K 303 K 333 K 363 K 303 K 333 K 363 K 1 39.456 39.13 38.569 36.807 30.003 29.911 35.706 35.016 34.189 29.305 28.702 27.606 2 39.596 39.396 38.974 36.84 33.459 31.643 36.175 35.147 34.286 29.956 29.018 28.059 3 39.998 39.859 39.156 37.105 35.74 31.974 36.526 35.974 34.982 30.128 29.296 28.569 4 40.256 41.569 39.561 37.946 34.141 32.869 37.115 36.185 35.458 30.569 29.996 29.194 5 40.569 40.296 39.912 38.526 35.987 35.968 37.256 37.859 35.832 31.458 31.586 29.569 6 41.256 41.103 41.296 38.782 35.968 35.948 37.809 36.984 36.095 32.146 30.856 30.128 7 41.968 41.597 41.203 38.859 36.434 36.102 38.258 37.284 36.859 33.589 31.149 30.596 8 42.698 42.302 42.105 39.108 36.894 36.258 38.478 37.963 36.596 32.869 31.596 31.182 9 43.102 42.919 42.221 39.547 37.548 37.154 39.502 38.589 36.785 33.105 32.569 32.859 10 43.596 43.008 42.968 40.568 38.483 38.559 39.984 38.986 37.156 33.558 33.294 32.586 Average 41.249 41.117 40.596 38.408 35.465 34.638 37.680 36.998 35.823 31.668 30.806 30.034 2.3 等量吸附热与吸附量的关系
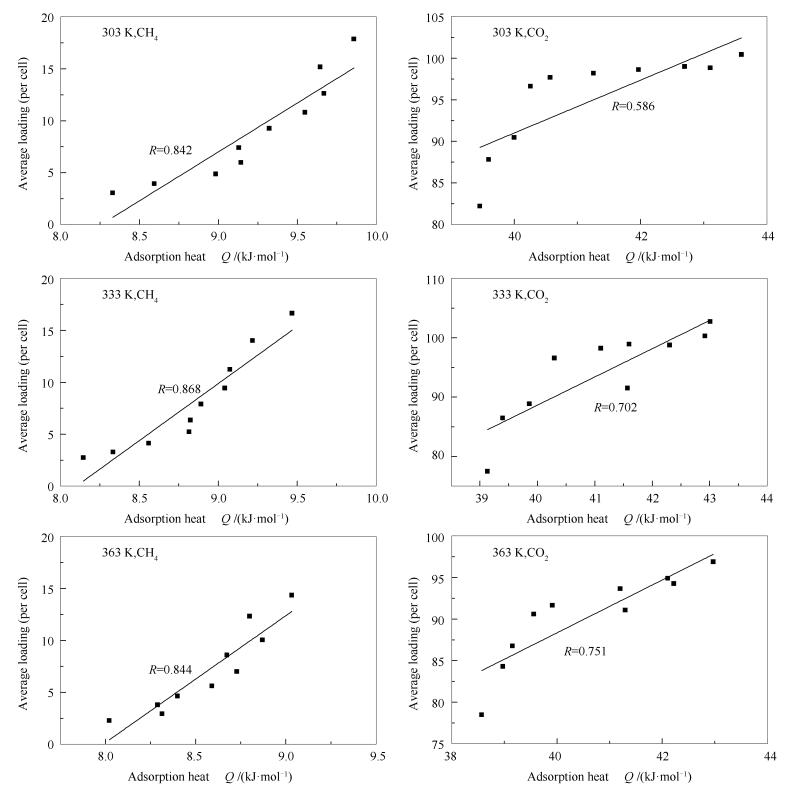
图 4为以蒙脱石为例分别对单组分CH4和CO2在不同温度下等量吸附热和等温吸附线的相关关系图。由图 4可知,CH4和CO2的等量吸附热和等温吸附量之间呈现良好的正相关关系,CH4比CO2的正相关关系更加显著,这与蒙脱石对单组分CH4和CO2的吸附作用机理的差异相关。
通常情况下,吸附作用一般从吸附活性位开始,吸附热相对也比较大,随着前期吸附活性位的占据,而后期吸附就会随之转移到不活泼的吸附位上,并且前期分子和后期吸附分子之间会产生排斥作用,使得吸附热变小。而蒙脱石对表面活性位前期吸附的CH4分子可以和后期H2O分子之间形成氢键,进而还可以作为后期吸附的活性位,因此, 随着蒙脱石对CH4分子的吸附量增加,吸附热也会增加。而蒙脱石对CO2的吸附虽然是以范德华为主,但要小于CH4分子的范德华力,因此, 吸附量和吸附热的变化仍是正相关,并且这种正相关关系较CH4的吸附显著性较差。
3 结论
在相同的温度和压力条件下,四种矿物质对CH4和CO2分子的吸附量从大到小为,蒙脱石>高岭石>生石膏>方解石。说明由于蒙脱石和高岭石层状结构自由体积大,空间位阻效应小,容易发生片层结构的交错,更有利于CH4和CO2的吸附。
随着压力的增大,四种矿物质对CH4和CO2分子的吸附量开始增加较快,压力到达一定值后趋于平缓;随着温度的升高,CH4和CO2分子吸附量和吸附热均减小,同时也表明了高温不利于吸附。
蒙脱石、高岭石、方解石和生石膏对CH4和CO2分子的等量吸附热均小于42 kJ/mol,说明四种矿物质对CH4和CO2的吸附均为物理吸附。
CH4和CO2的等量吸附热大体随温度的升高而减少,CH4和CO2的等量吸附热和吸附量之间呈良好的正相关,只是CO2的显著性要低一些。这是由于吸附机理的差异造成的,同时也表明了CH4和CO2的吸附能主要由范德华能构成。
-
-
[1]
DENG S, WANG Z, GU Q. Extracting hydrocarbons from Huadian oil shale by sub-critical water[J]. Fuel Process Technol, 2011, 92(5): 1062-1067. doi: 10.1016/j.fuproc.2011.01.001
-
[2]
姚宗惠, 张明山, 曾令邦. 鄂尔多斯盆地北部断裂分析[J]. 石油勘探与开发, 2003,30,(2): 20-23. YAO Zong-hui, ZHANG Ming-shan, ZENG Ling-bang. Analysis of the faults in the northern Ordos Basin[J]. Petrol Explor Dev, 2003, 30(2): 20-23.
-
[3]
钱家麟, 王剑秋, 李术元. 世界油页岩综述[J]. 中国能源, 2006,28,(8): 16-19. QIAN Jia-lin, WANG Jian-qiu, LI Shu-yuan. World oil shale[J]. Energy China, 2006, 28(8): 16-19.
-
[4]
邹永文. 桦甸油页岩及其半焦基础特性研究[D]. 吉林: 东北电力大学, 2010. doi: 10.3969/j.issn.1005-2992.2010.01.004ZOU Yong-wen. Study on the basic characteristics of the Huadian oil shales and their semi-cokes[D]. Jilin:Northeast Electric Power University, 2010. doi: 10.3969/j.issn.1005-2992.2010.01.004
-
[5]
吉利明, 邱军利, 张同伟. 泥页岩主要黏土矿物组分甲烷吸附实验[J]. 地球科学-中国地质大学学报, 2012,37,(5): 1043-1050. JI Li-ming, QIU Jun-li, ZHANG Tong-wei. Experiments on methane adsorption of common clay minerals in shale[J]. Earth Sci:J China Univ Geosci, 2012, 37(5): 1043-1050.
-
[6]
吉利明, 邱军利, 夏燕青. 常见黏土矿物电镜扫描微孔隙特征与甲烷吸附性[J]. 石油学报, 2012,33,(2): 249-256. doi: 10.7623/syxb201202009JI Li-ming, QIU Jun-li, XIA Yan-qing. Micro-pore characteristics and methane adsorption properties of common clay minerals by electron microscope scanning[J]. Acta Pet Sin, 2012, 33(2): 249-256. doi: 10.7623/syxb201202009
-
[7]
孙仁远, 张云飞, 范坤坤. 页岩中黏土矿物吸附特性分子模拟[J]. 化工学报, 2015,66,(6): 2118-2122. SUN Ren-yuan, ZHANG Yun-fei, FAN Kun-kun. Molecular simulations of adsorption characteristics of clay minerals in shale[J]. J Chem Ind Eng, 2015, 66(6): 2118-2122.
-
[8]
侯新娟, 杨建丽, 李永旺. 煤大分子结构的量子化学研究[J]. 燃料化学学报, 1999,27,(s1): 143-149. HOU Xin-juan, YANG Jian-li, LI Yong-wang. Quantum chemistry study on coal molecular structure[J]. J Fuel Chem Technol, 1999, 27(s1): 143-149.
-
[9]
YANG X, ZHANG C. Structure and diffusion behavior of dense carbon dioxide fluid in clay-like slit pores by molecular dynamics simulation[J]. Chem Phys Lett, 2005, 407(4): 427-432.
-
[10]
茹鑫. 油页岩热解过程分子模拟及实验研究[D]. 吉林: 吉林大学, 2013.RU-Xin. Study on the experiment and molecular simulation of oil shale pyrolysis[D]. Jilin:Jilin University, 2013.
-
[11]
王茂桢, 柳少波, 任拥军. 页岩气储层粘土矿物孔隙特征及其甲烷吸附作用[J]. 地质论评, 2015,61,(1): 207-216. WANG Mao-zhen, LIU Shao-bo, REN Yong-jun. Pore characteristics and methane adsorption of clay minerals in Shale gas reservoir[J]. Geol Rev, 2015, 61(1): 207-216.
-
[12]
JIN Z, FIROOZABADI A. Methane and carbon dioxide adsorption in clay-like slit pores by Monte Carlo simulations[J]. Fluid Phase Equilib, 2013, 360(1): 456-465.
-
[13]
SKIPPER N T. Monte Carlo simulation of interlayer molecular structure in swelling clay minerals. 1. methodology[J]. Clays Clay Miner, 1995, 43(3): 285-293. doi: 10.1346/CCMN
-
[14]
LEVY J H, DAY S J, KILLINGLEY J S. Methane capacities of Bowen Basin coals related to coal properties[J]. Fuel, 1997, 76(9): 813-819. doi: 10.1016/S0016-2361(97)00078-1
-
[15]
ASTASHOV A V, BELYI A A, BUNIN A V. Quasi-equilibrium swelling and structural parameters of coals[J]. Fuel, 2008, 87(15/16): 3455-3461.
-
[16]
LIU Y, WILCOX J. Effects of surface heterogeneity on the adsorption of CO2 in microporous carbons[J]. Environ Sci Technol, 2012, 46(3): 1940. doi: 10.1021/es204071g
-
[17]
王擎, 孙斌, 刘洪鹏. 油页岩热解过程矿物质行为分析[J]. 燃料化学学报, 2013,41,(2): 163-168. WANG Qin, SUN Bin, LIU Hong-peng. Analysis of mineral behavior during pyrolysis of oil shale[J]. J Fuel Chem Technol, 2013, 41(2): 163-168.
-
[18]
JI L, ZHANG T, MILLIKEN K L. Experimental investigation of main controls to methane adsorption in clay-rich rocks[J]. Appl Geochem, 2012, 27(12): 2533-2545. doi: 10.1016/j.apgeochem.2012.08.027
-
[19]
ROSS D J K, BUSTIN R M. The importance of shale composition and pore structure upon gas storage potential of shale gas reservoirs[J]. Mar Petrol Geol, 2009, 26(6): 916-927. doi: 10.1016/j.marpetgeo.2008.06.004
-
[20]
BUSTIN R M, CLARKSON C R. Geological controls on coalbed methane reservoir capacity and gas content[J]. Int J Coal Geol, 1998, 38(66): 3-26.
-
[21]
KROOSS B M, BERGEN F V, GENSTERBLUM Y. High-pressure methane and carbon dioxide adsorption on dry and moisture-equilibrated Pennsylvanian coals[J]. Int J Coal Geol, 2002, 51(2): 69-92. doi: 10.1016/S0166-5162(02)00078-2
-
[22]
MASTALERZ M, GLUSKOTER H, RUPP J. Carbon dioxide and methane sorption in high volatile bituminous coals from Indiana, USA[J]. Int J Coal Geol, 2004, 60(1): 43-55. doi: 10.1016/j.coal.2004.04.001
-
[23]
NODZEŃSKI A. Sorption and desorption of gases (CH4, CO2) on hard coal and active carbon at elevated pressures[J]. Fuel, 1998, 77(11): 1243-1246. doi: 10.1016/S0016-2361(98)00022-2
-
[1]
-
表 1 CH4的等量吸附热
Table 1. Adsorption heat of CH4 on the surface of four mineral substances
Pressure p/MPa MMT Qst/(kJ·mol-1) Kaolinite Qst/(kJ·mol-1) Calcite Qst/(kJ·mol-1) Gypsum Qst/(kJ·mol-1) 303 K 333 K 363 K 303 K 333 K 363 K 303 K 333 K 363 K 303 K 333 K 363 K 1 8.330 8.146 8.021 13.665 13.075 12.920 9.894 9.966 9.807 6.673 6.389 6.372 2 8.594 8.335 8.314 14.184 13.631 13.472 10.109 10.016 10.068 6.971 6.682 6.816 3 8.983 8.560 8.289 14.677 14.259 13.619 10.410 10.238 10.159 7.109 7.075 6.912 4 9.142 8.816 8.399 15.100 14.385 13.849 10.523 10.372 10.121 7.519 7.226 7.205 5 9.129 8.824 8.590 15.360 14.941 14.351 10.694 10.489 10.406 7.678 7.448 7.406 6 9.322 8.891 8.728 15.468 15.067 14.636 10.887 10.690 10.623 8.033 7.607 7.464 7 9.548 9.042 8.673 15.690 15.284 14.975 10.941 10.745 10.774 8.184 7.699 7.527 8 9.669 9.075 8.870 15.686 15.514 14.878 11.104 10.853 10.746 8.431 8.017 7.556 9 9.644 9.217 8.799 15.949 15.443 14.970 11.242 10.974 10.807 8.464 7.966 7.799 10 9.858 9.468 9.033 15.999 15.518 15.113 11.276 11.121 10.824 8.924 8.280 8.042 Average 9.222 8.837 8.572 15.178 14.712 14.278 10.708 10.546 10.434 7.799 7.439 7.301 表 2 CO2的等量吸附热
Table 2. Adsorption heat of CO2 on the surface of four mineral substances
Pressure p/MPa MMT Qst/(kJ·mol-1) Kaolinite Qst/(kJ·mol-1) Calcite Qst/(kJ·mol-1) Gypsum Qst/(kJ·mol-1) 303 K 333 K 363 K 303 K 333 K 363 K 303 K 333 K 363 K 303 K 333 K 363 K 1 39.456 39.13 38.569 36.807 30.003 29.911 35.706 35.016 34.189 29.305 28.702 27.606 2 39.596 39.396 38.974 36.84 33.459 31.643 36.175 35.147 34.286 29.956 29.018 28.059 3 39.998 39.859 39.156 37.105 35.74 31.974 36.526 35.974 34.982 30.128 29.296 28.569 4 40.256 41.569 39.561 37.946 34.141 32.869 37.115 36.185 35.458 30.569 29.996 29.194 5 40.569 40.296 39.912 38.526 35.987 35.968 37.256 37.859 35.832 31.458 31.586 29.569 6 41.256 41.103 41.296 38.782 35.968 35.948 37.809 36.984 36.095 32.146 30.856 30.128 7 41.968 41.597 41.203 38.859 36.434 36.102 38.258 37.284 36.859 33.589 31.149 30.596 8 42.698 42.302 42.105 39.108 36.894 36.258 38.478 37.963 36.596 32.869 31.596 31.182 9 43.102 42.919 42.221 39.547 37.548 37.154 39.502 38.589 36.785 33.105 32.569 32.859 10 43.596 43.008 42.968 40.568 38.483 38.559 39.984 38.986 37.156 33.558 33.294 32.586 Average 41.249 41.117 40.596 38.408 35.465 34.638 37.680 36.998 35.823 31.668 30.806 30.034 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 8
- 文章访问数: 1684
- HTML全文浏览量: 278


 下载:
下载:



 下载:
下载:

