 图式1
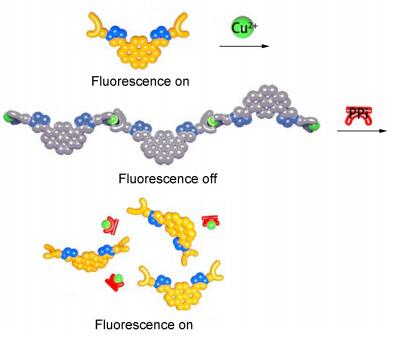
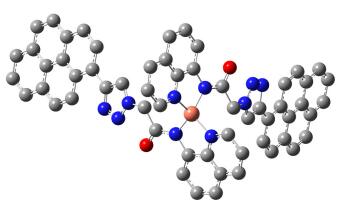
探针L接力识别Cu2+和PPi的原理
图式1.
Proposed sequential recognition mechanism of L with Cu2+ and PPi
图式1
探针L接力识别Cu2+和PPi的原理
图式1.
Proposed sequential recognition mechanism of L with Cu2+ and PPi

Citation: Zhong Keli, Guo Baofeng, Sun Xiaohan, Zhou Xue, Zhang Qiang, Tang Lijun, Zhang Xingrong. A Novel 1, 8-Disubstituted Pyrene-Based Fluorescent Probe for Subsequent Detection of Cu2+ and Pyrophosphate[J]. Chinese Journal of Organic Chemistry, 2017, 37(8): 2002-2007. doi: 10.6023/cjoc201702005

一种基于1, 8-双取代芘的荧光探针对Cu2+和焦磷酸根的接力识别
English
A Novel 1, 8-Disubstituted Pyrene-Based Fluorescent Probe for Subsequent Detection of Cu2+ and Pyrophosphate
-
Key words:
- disubstituted pyrene
- / fluorescence probe
- / Cu2+
- / PPi
- / recognition
-
铜是生物体所必需的第三大微量元素, 由于其具有氧化还原性质, 可参与多种酶如酪氨酸酶、超氧化物歧化酶的代谢[1], 在动植物体内起至关重要的作用.铜的毒性很小, 人体每日铜的摄入量在0.6~1.6 mg范围内为最佳[2].当铜的摄入量过高时, 会损害肝肾[3]; 当体内缺少铜时, 会造成贫血, 引起骨骼变脆, 心血管功能紊乱等疾病[4]; 若铜在体内的代谢出现异常, 则会引起阿尔茨海默氏症、威尔森氏症等[5].因此检测铜离子, 跟踪其在生命活动中的作用过程具有重要意义.
焦磷酸根(PPi)是活细胞中三磷酸腺苷水解的产物, 其稳定的代谢过程保证了生物体功能的正常运转[6, 7], 它是工业废水中较难处理的含磷污染源之一, 也是一类非常重要的生物目标阴离子, 与PPi相关的生物发光分析也已应用于肿瘤诊断, 可见, PPi的检测在生命科学、环境科学以及医学科学等领域都具有重要的科学意义[8~10].近几年来, 单独识别Cu2+或PPi的探针已被广泛报道[11], 利用Cu2+配合物识别PPi的文献也有很多[12~20], 但是利用同一分子接力识别Cu2+和PPi (即在一定条件下识别Cu2+, 利用原位生成的L-Cu2+配合物在同一条件下继续识别PPi)的报道仍然很少[21].接力识别型荧光探针能够使两种离子的识别操作在同一测试条件下连续进行, 操作简单, 并能降低探针合成的工作量, 有利于节能减排[22].目前, Guo等[23]合成了一种亲水性共聚物poly(HEMA-co-DCPDP), 可以作为一种薄膜探针荧光“开-关-开”接力识别Cu2+和PPi. Huang等[24]利用商品化的4-(5-氯-2-吡啶基偶氮)-1, 3-苯二胺在六次甲基四胺介质中(黄色溶液)与Cu2+结合后呈现红色, 形成的络合物继续滴加PPi变成蓝绿色, 通过裸眼即可接力识别Cu2+和PPi.我们[25]曾合成了一种喹啉衍生物在二甲基亚砜/水(V:V=1:1, HEPES, pH=7.4) 中与Cu2+结合后发生荧光猝灭, 向Cu2+络合物中滴加PPi后, 通过PPi对Cu2+置换引起荧光恢复, 从而接力识别Cu2+和PPi.本文设计了一种新颖的双取代芘化合物L (Eq. 1), 利用相同的识别原理(Scheme 1)在THF/H2O (V:V=1:1, HEPES 1×10-2mol/L, pH=7.4) 中高选择性快速识别Cu2+, 形成的1:1多元配合物又可选择性和高灵敏度的识别PPi, 具有响应快速, 检测限低等优点.
1 结果与讨论
1.1 化合物L的表征
以8-氨基喹啉为原料, 经过酰胺化、叠氮化后, 所得产物1与1, 8-二乙炔基芘(2)进行click反应, 得到探针L. 8-氨基喹啉是很好的螯合基团, 而芘是优良的荧光团, 将两者通过click反应连接在一起, 得到的1, 2, 3-三唑结构即可作为连接体, 又可作为荧光团延长共轭体系, 使发射波长红移.所合成的荧光探针L核磁氢谱图显示, δ 10.79归属于酰胺氮上的氢, δ 7.58~8.95范围内的峰归属于喹啉和芘上的氢, 5.82处为与酰胺相连亚甲基上的氢.另外, 针L的核磁碳谱图显示, δ 165.52归属于羰基碳的峰, δ 117.78~149.52范围内为芳香环上碳的峰, 53.34归属于亚甲基碳的峰.此外, 高分辨质谱和红外谱图也进一步证明成功得到了所设计的目标分子L.
1.2 受体L对Cu2+的识别性能研究
1.2.1 探针L对金属阳离子的选择性
将探针L用THF/H2O (V:V=1:1, HEPES 1× 10-2 mol/L, pH=7.4) 溶液稀释成1×10-5mol/L, 取2 mL溶液加入到试管中, 再加入2×10-5 mol·L-1各种金属离子溶液, 摇匀后静止放置5 min, 以λ=366 nm为激发波长测试荧光发射光谱, 结果如图 1所示.从图中可看出, 探针L显示出芘的特征发射峰, 最大发射波长分别在410和430 nm处.当向L溶液中分别加入各种金属离子时, 只有Cu2+引起显著的荧光猝灭, 强度降低了44倍, 蓝色荧光褪去(图 1内插图), 最大发射波长发生了轻微蓝移, 这些结果说明L对Cu2+有良好的选择性.受体L与Cu2+结合后荧光猝灭的原因可能是由于Cu2+的顺磁性以及配体向金属离子电荷转移(LMCT)导致的.
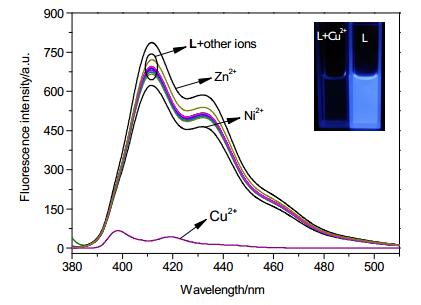 图 1
向探针L (1×10-5 mol/L)的THF/H2O (V:V=1:1, HEPES 1×10-2 mol/L, pH=7.4) 中, 加入Ni2+, Hg2+, Ba2+, Mg2+, Ag+, Fe2+, K+, Al3+, Pb2+, Na+, Mn2+, Sr2+, Cu2+, Co2+, Zn2+, Cd2+, Cr3+, Fe3+, Ca2+的荧光光谱变化谱图(λex=366 nm)
Figure 1.
Fluorescence spectra of L (1×10-5mol/L) in THF/ H2O (V:V=1:1, HEPES 1×10-2 mol/L, pH=7.4), respectively upon addition of metal ions including Ni2+, Hg2+, Ba2+, Mg2+, Ag+, Fe2+, K+, Al3+, Pb2+, Na+, Mn2+, Sr2+, Cu2+, Co2+, Zn2+, Cd2+, Cr3+, Fe3+, Ca2+(λex=366 nm)
图 1
向探针L (1×10-5 mol/L)的THF/H2O (V:V=1:1, HEPES 1×10-2 mol/L, pH=7.4) 中, 加入Ni2+, Hg2+, Ba2+, Mg2+, Ag+, Fe2+, K+, Al3+, Pb2+, Na+, Mn2+, Sr2+, Cu2+, Co2+, Zn2+, Cd2+, Cr3+, Fe3+, Ca2+的荧光光谱变化谱图(λex=366 nm)
Figure 1.
Fluorescence spectra of L (1×10-5mol/L) in THF/ H2O (V:V=1:1, HEPES 1×10-2 mol/L, pH=7.4), respectively upon addition of metal ions including Ni2+, Hg2+, Ba2+, Mg2+, Ag+, Fe2+, K+, Al3+, Pb2+, Na+, Mn2+, Sr2+, Cu2+, Co2+, Zn2+, Cd2+, Cr3+, Fe3+, Ca2+(λex=366 nm)
1.2.2 不同Cu2+浓度对探针L光谱的影响
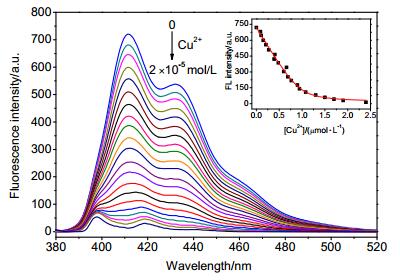
探针L的荧光强度受不同浓度Cu2+的影响如图 2所示, 当加入Cu2+为0~0.5×10-5mol/L时, L的荧光强度原位猝灭; 当加入Cu2+大于0.5×10-5mol/L时, 在398 nm处出现微弱发射峰, 410和430 nm处的发射峰继续降低, 直到加入2×10-5mol/L (L的2倍)的Cu2+时, 410和430 nm处的发射峰猝灭完全, 并蓝移至398和420 nm处.以410 nm处的荧光强度数据, 利用1:1的非线性拟合公式进行拟合[26], 可得到相关系数为R2=0.99247, 计算出L与Cu2+的结合常数Ka=2.48×106 mol·L-1 (图 2内插图).
1.2.3 探针L识别Cu2+的抗干扰性能及其他影响因素
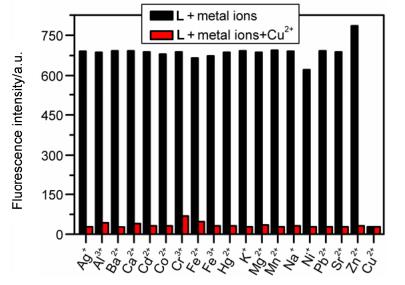
由于共存离子干扰是影响探针识别性能的一个重要因素, 因此我们完成了抗干扰实验, 结果如图 3所示.图中各种离子与L混合后荧光强度无明显变化, 只有Zn2+略有升高, Ni2+略有降低.但是随后加入Cu2+均发生显著淬灭, 这表明在其他金属离子存在下, 探针L对Cu2+荧光识别不受影响, 说明L识别Cu2+具有较好的抗干扰能力.此外, 利用荧光滴定数据, 以log[Cu2+]为横坐标, (Imax-I)/(Imax-Imin)为纵坐标, 利用Origin对数据进行线性拟合[27], 得到的检测限为1.82×10-6 mol/L, 说明该受体有较好的灵敏度. pH影响实验表明探针L识别Cu2+的pH最佳适用范围是6.0~13.0, 时间响应曲线说明探针L与Cu2+结合在10 s内即可完成, 可实现快速识别.
1.2.4 探针L与Cu2+的结合模式
为了确定探针L与Cu2+的结合模式, 我们进行了Job’s实验和高分辨质谱测试, 结果均显示L与Cu2+的计量比是1:1.然而, 利用B3LYP/LANL2DZ混合泛函和6-311G基函数对结合的稳定构型进行密度泛函理论计算[28], 发现不管如何调节结合位点, 分子中两个喹啉基团结合一个Cu2+都不能收敛.如果只有一个喹啉基团结合一个Cu2+, 剩余的喹啉基团在两倍的Cu2+溶液中显然是不稳定的, 因此猜测可能形成了多受体多阳离子的配合物.由于L分子较大, 为了计算方便, 我们简化分子进行了重新计算, 发现两个受体中8-氨基喹啉上的两个N结合一个Cu2+很稳定(图 4), 由此可推断L与Cu2+形成了多元配合物, 其结合模式如Scheme 1所示.受体L与Cu2+结合后荧光猝灭的原因可能是由于Cu2+的顺磁性以及配体向金属离子电荷转移(LMCT)导致[29].
1.3 配合物L-Cu2+对PPi的识别性能研究
1.3.1 配合物L-Cu2+对阴离子的选择性
为了确定L-Cu2+对PPi是否有识别作用, 我们将原位生成的含有1×10-5mol/L的L和2×10-5mol/L Cu2+的L-Cu2+溶液[V(THF)/V(H2O)=1/1, HEPES, 1×10-2 mol/L, pH=7.4]中分别加入4×10-5mol/L的F-, Cl-, Br-, I-, SCN-, CN-,
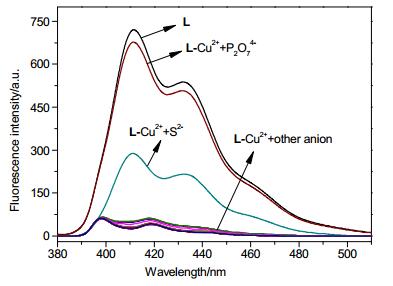
${{\text{H}}_{\text{2}}}\text{PO}_{\text{4}}^{\text{2-}}\text{,NO}_{\text{2}}^{\text{-}}\text{,NO}_{\text{3}}^{\text{-}}\text{,ClO}_{\text{4}}^{\text{-}}\text{,SO}_{\text{4}}^{\text{2-}}\text{,SiO}_{\text{3}}^{\text{2-}}\text{,}{{\text{S}}_{\text{2}}}\text{O}_{\text{3}}^{\text{2-}}\text{,}{{\text{P}}_{\text{2}}}\text{O}_{\text{7}}^{\text{4-}}\text{,HSO}_{\text{4}}^{\text{-}}\text{,CO}_{\text{3}}^{\text{2-}}\text{,HCO}_{\text{3}}^{\text{-}}$ , S2-等阴离子溶液, 摇匀后放置5 min测试荧光光谱.实验结果表明, S2-能引起荧光部分恢复, 而加入P2O74-后, L-Cu2+的荧光显著增强, 基本达到了L的荧光强度(图 5和6), 这说明$ {{\text{P}}_{2}}\text{O}_{7}^{4-}$ 可以夺取配合物中铜离子释放出L, 其他阴离子没有呈现此变化.由此可知, L-Cu2+可以选择性识别PPi.此外, 我们测试紫外-可见吸收光谱表明, 探针与铜形成络合物后在330~380 nm处吸收强度增加, 而加入PPi后吸收强度又基本恢复到探针L的吸收强度, 再次证明${{\text{P}}_{2}}\text{O}_{7}^{4-}$ 夺取配合物中铜离子而释放出L.另外, L-Cu2+紫外吸收在波长600~700 nm处有微弱吸收, 说明受体L与Cu2+存在多元络合作用[30].通过用激光照射三种溶液, 发现只有L-Cu2+溶液中存在丁达尔效应, 表明存在聚集体[31, 32], 说明L中加入Cu2+可能形成了多元配合物.1.3.2 L-Cu2+对PPi的滴定
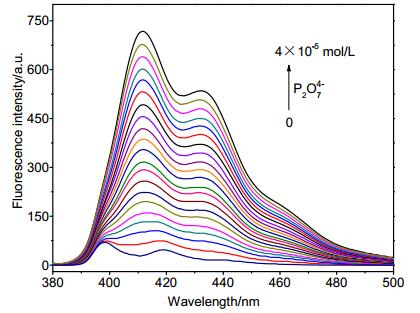
L-Cu2+对PPi的滴定实验结果如图 7所示, 随着PPi浓度的增加, 溶液的荧光强度也逐渐增大, 当L-Cu2+溶液中加入4倍的PPi时, 荧光不再发生明显变化, 荧光强度基本恢复到探针L的强度.利用1:1的非线性拟合公式进行拟合, 计算出L-Cu2+与PPi的结合常数为Ka=6.4×106 mol·L-1.此外, 时间响应曲线显示向L-Cu2+溶液中滴加PPi后在30 s内荧光即可恢复完全, 说明L-Cu2+可快速识别PPi.
1.3.3 L-Cu2+识别PPi的检测限及抗干扰能力
依据文献[33]中报道的方法, 以log[
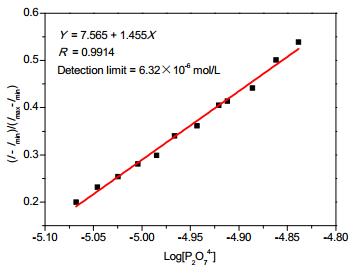
${{\text{P}}_{2}}\text{O}_{7}^{4-}$ ]为横坐标, (I-Imin)/(Imax-Imin)为纵坐标, 利用Origin对数据进行线性拟合, 得到线性相关系数为R=0.9914的一条直线(图 8), 经计算可得识别PPi的最低浓度为6.32×10-6mol/L, 达到了微摩尔级.此外抗干扰实验表明除S2-外, 其他共存的阴离子对PPi的识别过程无明显影响, 说明L-Cu2+对PPi的识别具有一定的抗干扰能力.1.3.4 pH对L-Cu2+识别PPi的影响
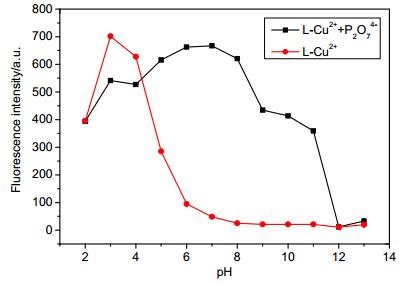
为了明确L-Cu2+识别PPi实际应用范围, 实验测定了不同pH对L-Cu2+和L-Cu2++PPi荧光强度的影响.如图 9所示, pH在2~5范围内, L-Cu2+具有一定的荧光强度, 在pH 6~13之间L-Cu2+显示出明显的荧光淬灭. L-Cu2+中加入PPi后, pH在5~8范围内具有较强的荧光信号, 这表明L-Cu2+可以在pH 5~8范围内对PPi进行检测, 可潜在应用于生物体系中实现对PPi的识别.
1.4 探针L的应用
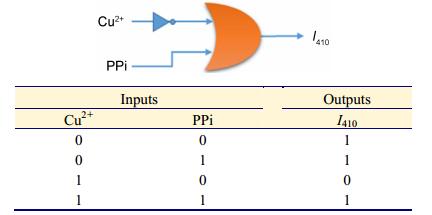
基于探针L对Cu2+和PPi的接力识别现象, 我们利用这种特性构建一个蕴函分子逻辑门(图 10).以410 nm处的荧光发射为输出信号, 受体L可以通过两个化学输入信号Cu2+和PPi来调控逻辑门的开关.当输入Cu2+而没有PPi输入时, 410 nm处的荧光猝灭, 表示以0的形式输出, 逻辑门处于“OFF”状态.相反, 当输入PPi而不管Cu2+是否存在, L仍然保持强荧光, 逻辑门会以1的形式输出, 处于“ON”状态.此外, Cu2+和PPi都不输入时, 探针L荧光强度没有变化, 以1的形式输出, 探针L作为蕴函逻辑门的详情被总结在图 10中.此外, 我们将裁减的试纸条浸泡于探针L母液中, 取出试纸分别滴加不同浓度的铜离子和PPi, 晾干后在365 nm手提式荧光灯照射下可看出, 当加入1倍和2倍铜离子时, 试纸上L的荧光颜色逐渐退去, 而继续滴加PPi离子又逐渐恢复.因此, 合成的探针L可以方便快速检测铜离子和PPi, 说明该探针具有潜在的应用价值.
2 结论
本文合成了一种新型的荧光探针L, 该探针在THF/H2O (V:V=1:1, HEPES 10×10-6 mol/L, pH=7.4) 中能快速识别Cu2+, 具有较好的选择性和抗干扰性能. Job’s实验和高分辨质谱证明L与Cu2+的计量比为1:1, 密度泛函理论计算表明L与Cu2+形成了多受体多阳离子配合物.利用L-Cu2+配合物可以接力识别PPi, 具有较好的选择性和灵敏度, 识别速度快, 检测限低, 并能在pH 5~8范围内对PPi进行检测.
3 实验部分
3.1 仪器与试剂
仪器:超声波清洗器(江苏昆山超声波仪器厂); TopPette弹道手动可调移液器(天津市泰斯特仪器有限公司); 970CRT荧光分光光度计(上海三科); pH计为PHS-25B(上海大普); SP-1900型双光束紫外分光光度计(上海光谱公司); 核磁共振光谱仪(400 MHz, Agilent公司, 美国); 液相色谱/质谱分析仪为Bruker micr OTOF-Q.
试剂: CH2Cl2、乙酸乙酯、四氢呋喃、二甲基亚砜等均为市售分析纯, 无需干燥.柱层析所用的硅胶(100~200目)是在青岛裕名源化工厂购得.
药品: 2-甲基-3-丁炔基-2-醇、8-氨基喹啉、抗坏血酸钠、醋酸钠、氯乙酰氯、NaN3、芘、碘粒、碘酸钾、浓硫酸、Na2S2O3、CuI、四(三苯基膦)钯、氢氧化钠、五水硫酸铜、氨水等原料均来自阿拉丁(上海, 中国), 无需纯化即可使用.
3.2 实验方法
3.2.1 荧光探针L的合成
称取化合物1 (680 mg, 3 mmol), 2 (250 mg, 1 mmol)溶于10 mL的V(THF):V(H2O)=4:1中, 加入五水硫酸铜(250 mg, 1 mmol)、抗坏血酸钠(400 mg, 2 mmol), 升温至66 ℃搅拌过夜.加氨水和CH2Cl2萃取, 用无水Na2SO4干燥, 常压下过滤, 浓缩获得的粗产物用柱色谱法分离纯化, 先用CH2Cl2为洗脱剂, 再V(用乙酸乙酯):V(二氯甲烷)=1:13洗脱, 得到155 mg黄色固体L, 产率22%. m.p. 156.4~158.4 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 10.79 (s, 2H), 8.95 (d, J=4.1 Hz, 2H), 8.90 (s, 2H), 8.87 (s, 2H), 8.60 (d, J=7.6 Hz, 2H), 8.41 (dd, J=7.1, 6.4 Hz, 6H), 8.26 (s, 2H), 7.70 (d, J=8.4 Hz, 2H), 7.64 (dd, J=8.4, 4.1 Hz, 2H), 7.58 (d, J=7.6 Hz, 2H), 5.82 (s, 4H); 13C NMR (100 MHz, DMSO) δ: 165.52, 149.52, 146.28, 138.73, 137.11, 134.47, 131.35, 128.2, 127.67, 127.38, 126.84, 126.19, 125.84, 124.91, 123.15, 122.73, 117.78, 53.34. HRMS (ESI+) calcd for C42H29N10O2 [M+H]+: 705.2475, found 705.2462.
3.2.2 荧光光谱测定方法
探针L以DMSO为溶剂配制成1.0×10-3mol/L的溶液, 然后用THF/H2O (V:V=1:1, HEPES 1.0×10-2mol/L, pH=7.4) 缓冲液(0.01mol/L)稀释成1.0×10-5mol/L溶液; 以二次蒸馏水为溶剂, 采用钠盐或钾盐配制5.0×10-3mol/L的各种阴离子(F-, Cl-, Br-, I-, SCN-, CN-,
$\text{PO}_{\text{4}}^{3-}, {{\text{H}}_{\text{2}}}\text{PO}_{\text{4}}^{-}, {{\text{H}}_{\text{2}}}\text{PO}_{\text{4}}^{\text{2}-}, \text{NO}_{\text{2}}^{-}, \text{NO}_{3}^{-}, \text{ClO}_{\text{4}}^{-}, \text{SO}_{\text{4}}^{2-}, \text{SiO}_{3}^{2-}, {{\text{S}}_{2}}\text{O}_{3}^{2-}, {{\text{P}}_{2}}\text{O}_{7}^{4-}, \text{HSO}_{\text{4}}^{-}, \text{CO}_{\text{3}}^{2-}, \text{HCO}_{\text{3}}^{-}$ ).荧光光谱测定均在室温下条件下进行.样品池为1 cm×1 cm×4 cm石英比色皿, 灵敏度2, EX缝宽2, EM缝宽10, 激发波长λex为366 nm.辅助材料(Supporting Information) L的1H NMR、13C NMR和HRMS谱图, L识别Cu2+及L-Cu2+识别PPi的光谱数据.这些材料可以免费从本刊网站(http://siocjournal.cn/)上下载.
-
-
[1]
Gadhari, N. S.; Sanghavi, B. J.; Srivastava, A. K. Anal. Chim. Acta 2011, 703, 31. doi: 10.1016/j.aca.2011.07.017
-
[2]
Tapiero, H.; Tew, K. D. Biomed. Pharmacother. 2003, 57, 399. doi: 10.1016/S0753-3322(03)00081-7
-
[3]
张应鹏, 尤彩霞, 杨云裳, 刘小育, 郭慧琛, 董玉莹, 有机化学, 2016, 36, 1401. http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract345443.shtmlZhang, Y.; You, C.; Yang, Y.; Liu, X.; Guo, H.; Dong, Y. Chin. J. Org. Chem. 2016, 36, 1401(in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract345443.shtml
-
[4]
Barnham, K. J.; Masters, C. L.; Bush, A. I. Nat. Rev. Drug Discovery 2004, 3, 205. doi: 10.1038/nrd1330
-
[5]
Swamy, K. M. K.; Ko, S.-K.; Kwon, S. K.; Lee, H. N.; Mao, C.; Kim, J.-M.; Lee, K.-H.; Kim, J.; Shin, I.; Yoon, J. Chem. Commun. 2008, 5915. http://www.ncbi.nlm.nih.gov/pubmed/19030537
-
[6]
Kumari, N.; Zelder, F. Chem. Commun. 2015, 51, 17170. doi: 10.1039/C5CC07413D
-
[7]
徐勤超, 金灿, 朱雪慧, 邢国文, 有机化学, 2014, 34, 647. http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract343722.shtmlXu, Q.; Jin, C.; Zhu, X.; Xing, G. Chin. J. Org. Chem. 2014, 34, 647(in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract343722.shtml
-
[8]
Kim, S. K.; Lee, D. H.; Hong, J.-I.; Yoon J. Acc. Chem. Res. 2009, 42, 23. doi: 10.1021/ar800003f
-
[9]
Xu, S.; He, M.; Yu, H.; Cai, X.; Tan, X.; Lu, B.; Shu, B. Anal. Biochem. 2001, 299, 188. doi: 10.1006/abio.2001.5418
-
[10]
王军, 初紅涛, 陈微微, 孙荣国, 有机化学, 2016, 36, 2545. http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract345640.shtmlWang, J.; Chu, H.; Chen, W.; Sun, R. Chin. J. Org. Chem. 2016, 36, 2545(in Chinese). http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract345640.shtml
-
[11]
Li, D.; Sun, X.; Huang, J.; Wang, Q.; Feng, Y.; Chen, M.; Meng, X.; Zhu, M.; Wang, X. Dye Pigm. 2016, 125, 185. doi: 10.1016/j.dyepig.2015.10.016
-
[12]
Kim, M. J.; Swamy, K. M.; Lee, K. M.; Jagdale, A. R.; Kim, Y.; Kim, S. J.; Yoo, K. H.; Yoon, J. Chem. Commun. 2009, 7215. http://www.ncbi.nlm.nih.gov/pubmed/19921034
-
[13]
Roy, B.; Rao, A. S.; Ahn, K. H. Org. Biomol. Chem. 2011, 9, 7774. doi: 10.1039/c1ob05999h
-
[14]
Huang, X.; Guo, Z.; Zhu, W.; Xie, Y.; Tian, H. Chem. Commun. 2008, 44, 5143. http://www.ncbi.nlm.nih.gov/pubmed/18956049
-
[15]
Yu, W.; Qiang, J.; Yin, J.; Kambam, S.; Wang, F.; Wang, Y.; Chen, X. Org. Lett. 2014, 16, 2220. doi: 10.1021/ol5007339
-
[16]
Zhu, W.; Huang, X.; Guo, Z.; Wu, X.; Yu, H.; Tian, H. Chem. Commun. 2012, 48, 1784. doi: 10.1039/c2cc16902a
-
[17]
Zhang, J. F.; Park, M.; Ren, W. X.; Kim, Y.; Kim, S. J.; Jung, J. H.; Kim, J. S. Chem. Commun. 2011, 47, 3568. doi: 10.1039/c1cc00021g
-
[18]
Watchasit, S.; Kaowliew, A.; Suksai, C.; Tuntulani, T.; Ngeontae, W.; Pakawatchai, C. Tetrahedron Lett. 2010, 51, 3398. doi: 10.1016/j.tetlet.2010.04.095
-
[19]
Chen, Z.-h.; Lu, Y.; He, Y.-b.; Huang, X.-H. Sens. Actuators, B 2010, 149, 407. doi: 10.1016/j.snb.2010.06.038
-
[20]
Kim, S. Y.; Hong, J.-I. Tetrahedron Lett. 2009, 50, 1951. doi: 10.1016/j.tetlet.2009.02.036
-
[21]
Guo, M.; Dong, P.; Feng, Y.; Xi, X.; Shao, R.; Tian, X.; Zhang, B.; Zhu, M.; Meng, X. Biosens. Bioelectron 2017, 90, 276. doi: 10.1016/j.bios.2016.11.069
-
[22]
Wang, M. Q.; Li, K.; Hou, J. T.; Wu, M. Y.; Huang, Z.; Yu X. Q. J. Org. Chem. 2012, 77, 8350. doi: 10.1021/jo301196m
-
[23]
Guo, Z.; Zhu, W.; Tian, H. Macromolecules 2010, 43, 739. doi: 10.1021/ma902466g
-
[24]
Zhao, X. J.; He, L.; Huang, C. Z. Talanta 2012, 101, 59. doi: 10.1016/j.talanta.2012.08.046
-
[25]
Tang, L.; Zhou, P.; Huang, Z.; Zhao, J.; Cai, M. Tetrahedron Lett. 2013, 54, 5948. doi: 10.1016/j.tetlet.2013.08.047
-
[26]
Yang, C.; Gong, D.; Wang, X.; Iqbal, A.; Deng, M.; Guo, Y.; Tang, X.; Liu, W.; Qin, W. Sens. Actuators, B 2015.
-
[27]
Tang, L.; Zhou, P.; Zhong, K.; Hou, S. Sens. Actuators, B 2013, 182, 439. doi: 10.1016/j.snb.2013.03.043
-
[28]
Rimola, A.; Rodriguez-Santiago, L.; Ugliengo, P.; Sodupe, M. J. Phys. Chem. B 2007, 111, 5740. doi: 10.1021/jp071071o
-
[29]
Zhong, K.; Zhou, X.; Hou R.; Zhou, P.; Hou, S.; Bian, Y.; Zhang, G.; Tang, L.; Shang, X. RSC Adv. 2014, 4, 16612. doi: 10.1039/c4ra00060a
-
[30]
Liu, Y.-L.; Wang, Z.-K.; Qin, W.; Hu, Q.-L.; Tang, B. Z. Chin. J. Polym. Sci. 2017, 35, 365. doi: 10.1007/s10118-017-1876-y
-
[31]
Yu, G.; Zhou, X.; Zhang, Z.; Han, C.; Mao, Z.; Gao, C.; Huang, F. J. Am. Chem. Soc. 2012, 134, 19489. doi: 10.1021/ja3099905
-
[32]
Wang, K.; Guo, D. S.; Zhao, M. Y.; Liu, Y. Chem.-Eur. J. 2016, 22, 1475. doi: 10.1002/chem.201303963
-
[33]
Yang, Y.; Gao, W.; Sheng, R.; Wang, W.; Liu, H.; Yang, W.; Zhang, T.; Zhang, X. Spectrochim. Acta, Part A 2011, 81, 14. doi: 10.1016/j.saa.2011.05.016
-
[34]
Ji, S.; Yang, J.; Yang, Q.; Liu, S.; Chen, M.; Zhao, J. J. Org. Chem. 2009, 74, 4855. doi: 10.1021/jo900588e
-
[1]
-
图 1 向探针L (1×10-5 mol/L)的THF/H2O (V:V=1:1, HEPES 1×10-2 mol/L, pH=7.4) 中, 加入Ni2+, Hg2+, Ba2+, Mg2+, Ag+, Fe2+, K+, Al3+, Pb2+, Na+, Mn2+, Sr2+, Cu2+, Co2+, Zn2+, Cd2+, Cr3+, Fe3+, Ca2+的荧光光谱变化谱图(λex=366 nm)
Figure 1 Fluorescence spectra of L (1×10-5mol/L) in THF/ H2O (V:V=1:1, HEPES 1×10-2 mol/L, pH=7.4), respectively upon addition of metal ions including Ni2+, Hg2+, Ba2+, Mg2+, Ag+, Fe2+, K+, Al3+, Pb2+, Na+, Mn2+, Sr2+, Cu2+, Co2+, Zn2+, Cd2+, Cr3+, Fe3+, Ca2+(λex=366 nm)
Inset: the fluorescence changes of probe L without and with Cu2+ under a portable UV lamp at 365 nm
图 3 L (1×10-5 mol/L)在THF/H2O (V:V=1:1, HEPES 1×10-2 mol/L, pH=7.4) 中加入各种金属阳离子后的荧光强度以及加入各种金属阳离子后又加入Cu2+后的荧光强度
Figure 3 Fluorescence intensities of L in THF/H2O (V:V=1:1, HEPES 1×10-2 mol/L, pH=7.4) in the presence of various metal ions and further addition of 2×10-5 mol/L Cu2+
Intensity was recorded at 410 nm, excitation at 366 nm
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 11
- 文章访问数: 1978
- HTML全文浏览量: 277



 下载:
下载:










 下载:
下载:

