
Citation: Tong Qing, Gao Qiang, Xu Bolian, Yu Lei, Fan Yining. Pt/WO3/ZrO2-Catalyzed Selective Hydrogenolysis of Glycerol to Produce 1, 3-Propanediol[J]. Chinese Journal of Organic Chemistry, 2017, 37(3): 753-758. doi: 10.6023/cjoc201610002

Pt/WO3/ZrO2催化甘油选择性氢解制备1, 3-丙二醇
English
Pt/WO3/ZrO2-Catalyzed Selective Hydrogenolysis of Glycerol to Produce 1, 3-Propanediol
-
Key words:
- glycerol
- / hydrogenolysis
- / catalysis
- / biomass
- / 1, 3-propanediol
-
甘油是生物柴油生产过程中的副产物, 每生产9 kg生物柴油就会伴生1 kg甘油[1].最近, 随着生物柴油产业的迅猛发展, 甘油产能过剩.因此, 将之转化为有用的下游产品, 可维持化工产业链中物料平衡, 有着重要实用价值.为了实现这一目的, 人们开始研究的各种甘油转化途径, 比如重整、脱水、氢解、氧化、羧化、醚化等[2-5].其中, 选择性氢解反应可生成1, 3-丙二醇.由于1, 3-丙二醇是合成市场需求量巨大的聚对苯二甲酸丙二醇酯 (PPT) 的重要有机中间体, 该反应为将甘油转化为有用的下游产品提供了一个重要途径.甘油氢解反应通常使用贵金属催化剂, 比如铂[3]、铑[4]、铱[5].其中, 铂系催化剂, 尤其是负载于WO3/ZrO2上的铂催化剂, 有着较好的化学和热稳定性, 被广泛应用于甘油氢解反应.早在2008年, Sasaki等[3a]用不同的载体 (TiO2、HY、Al2O3、ZrO2、AlMCM-41、SiO2-Al2O3)、不同贵金属催化剂 (Pt、Pd、Ru、Ir) 催化甘油氢解制备1, 3-丙二醇.其中Pt/WO3/ZrO2催化剂性能最优, 并且发现不同的浸渍顺序对催化剂的催化性能也有影响.他们用2 wt% Pt/WO3/ZrO2催化剂, 在170 ℃、氢气压力8 MPa、1, 3-二甲基-2-咪唑啉酮 (DMI) 为溶剂的反应条件下, 得到甘油转化率为78.4%、1, 3-丙二醇的选择性为28 %的最佳结果 (Table 1, Entry 1).接着, Ding等[3b]研究了Pt/WO3/ZrO2催化甘油氢解反应中的溶剂效应, 发现使用质子溶剂 (例如乙醇和水) 会使1, 3-丙二醇的选择性明显高于非质子溶剂.此外, 二元溶剂, 例如DMI-水、乙醇-水和DMI-乙醇, 可起到协同作用, 使得1, 3-丙二醇的收率大于使用任意一种单一溶剂的反应.其中, 以DMI-水组成的混合溶剂效果最优.在170 ℃、氢气压力5 MPa下, 经过12 h反应, 甘油转化率为31.6%, 1, 3-丙二醇选择性为34.9% (Table 1, Entry 2). Chen等[3c]也报道了不同反应温度、反应压力及甘油浓度对Pt/WO3/ZrO2催化性能的影响.最后得出在以3 wt% Pt/WO3/ZrO2为催化剂, 在130 ℃、氢气压力4 MPa的反应条件下进行水相固定床反应效果最佳, 其中甘油转化率为70.2%, 1, 3-丙二醇选择性为45.6% (Table 1, Entry 3).
 表 1
已有Pt/WO3/ZrO2催化甘油选择性氢解方法的对比
Table 1.
Comparison of the known Pt/WO3/ZrO2-catalyzed glycerolselective hydrogenolysis
表 1
已有Pt/WO3/ZrO2催化甘油选择性氢解方法的对比
Table 1.
Comparison of the known Pt/WO3/ZrO2-catalyzed glycerolselective hydrogenolysis
Entry Catalyst Pa/MPa Cb/% Sc/% Ref. 1 Pt/WO3/ZrO2 8 85.8 28 [3a] 2 Pt/WO3/ZrO2 5 31.6 34.9 [3b] 3 Pt/WO3/ZrO2 4 70.2 45.6 [3c] 4 Pt/WO3/ZrO2/SiO2 5 54.3 52.0 [3d] 5 Pt-Re/WO3/ZrO2 2.5 99.0 20.4 [3e] 6 Pt/WO3/ZrO2 2.5 87.3 32.7 This work aH2 pressure; bglycerol conversion; c1, 3-PDO selectivity. 表 1 已有Pt/WO3/ZrO2催化甘油选择性氢解方法的对比
Table 1. Comparison of the known Pt/WO3/ZrO2-catalyzed glycerolselective hydrogenolysis早期对Pt/WO3/ZrO2催化剂的研究主要是集中在反应条件的摸索以及溶剂的选择上. 2014年, Zhu等[3d]研究了SiO2掺杂的Pt/WO3/ZrO2催化剂催化甘油选择性加氢制备1, 3-丙二醇, 发现加入SiO2后, Pt的分散度和催化剂的酸性都有所提高.当Pt的负载量为5 wt%时, 1, 3-丙二醇的选择性提高到52.0%, 但甘油的转化率仍然较低, 仅为54.3% (Table 1, Entry 4).本课题组致力于有工业应用前景的均相[6]与非均相[7]催化技术的研究.最近, 我们在前人的研究基础上, 往Pt/WO3/ZrO2催化剂中添加Re助剂, 从而大大提高Pt的分散度以及催化剂的酸性, 大幅度提高甘油的转化率[3e].在175 ℃, 氢气压力减少到2.5 MPa时, 得到甘油转化率为99.0 %, 但是1, 3-丙二醇的选择性较低, 为20.4% (Table 1, Entry 5).
从已报道的工作中, 不难发现, WO3作为酸性氧化物, 催化甘油氢解过程的第一步反应——甘油脱水反应. WO3含量与甘油氢解催化剂的活性必然有着密切联系.因此, 我们研究了不同WO3负载量对甘油催化氢解反应以及产物分布的影响.发现在175 ℃、氢气压力2.5 MPa、WO3负载量6.0 wt%时, 甘油转化率最高, 为87.3%, 而1, 3-丙二醇的选择性也可达到32.7% (Table 1, Entry 6).本文将报道这一部分工作.
1 结果与讨论
我们首先考察了反应时间对Pt/WO3/ZrO2催化剂 (其中WO3含量为15 wt%) 催化甘油氢解性能的影响.实验采用固定床微型催化反应装置.将催化剂置于管式不锈钢反应器中, 经过H2预还原后, 将10 wt%浓度甘油水溶液通过平流泵以固定流速2.4 mL/h打入反应管, 同时以97 mL/min的速度通入H2.如表 2所示, 反应主要生成1, 3-丙二醇、1, 2-丙二醇、正丙醇、异丙醇、丙酮、丙酮醇和少量的丙酸 (Table 2, Entries 1~9).起初, 催化剂活性较高, 可完全转化甘油 (Entries 1~3), 但此时的主要产物并非1, 3-丙二醇 (1, 3-PDO), 而是正丙醇 (1-PO).随着使用时间的延长, 催化剂活性逐步降低, 从而导致甘油转化率下降.催化剂在使用14 h以后趋于稳定, 可以转化47%左右的甘油.但此时, 1, 3-丙二醇的选择性显著上升, 达到30%左右, 而正丙醇选择性由开始时的70%下降到50%左右 (Entries 4~9).
 表 2
反应时间对Pt/WO3/ZrO2(WO3含量为15 wt%) 催化剂催化甘油加氢的影响a
Table 2.
Influence of reaction time to Pt/WO3/ZrO2 (contain 15 wt% of WO3)-catalyzed glycerol hydrogenolysis
表 2
反应时间对Pt/WO3/ZrO2(WO3含量为15 wt%) 催化剂催化甘油加氢的影响a
Table 2.
Influence of reaction time to Pt/WO3/ZrO2 (contain 15 wt% of WO3)-catalyzed glycerol hydrogenolysis

Entry t/h Glyerol conversion/% Product selectivityb/% 1, 3-PDO Yield/% 1, 3-PDO 1, 2-PDO 1-PO 2-PO AT ATol PA 1 6 100 8.9 2.5 74.3 7.2 4.2 1.9 1.0 8.9 2 8 100 9.0 2.9 73.5 6.7 5.8 1.5 0.6 9.0 3 10 100 17.9 5.1 63.4 5.8 6.1 1.0 0.7 17.9 4 12 61.1 27.4 6.8 53.8 5.2 5.5 0.8 0.5 16.7 5 14 47.2 29.9 7.1 51.1 4.8 5.8 0.6 0.7 14.1 6 16 47.0 30.8 7.4 50.0 5.1 5.6 0.4 0.7 14.5 7 18 47.9 30.1 7.1 50.5 4.8 6.1 0.6 0.8 14.4 8 20 49.2 31.2 8.0 50.4 4.4 5.0 0.3 0.7 15.4 9 22 48.3 31.1 8.0 50.6 4.8 4.7 0.2 0.6 15.0 aReaction conditions: 175 ℃, 2.5 MPa, 2 g of catalyst was used; the aqueous glycerol (10 wt%) was fed at the speed of 2.4 mL/h; hydrogen flow rate was 97 mL/min. bAbbreviations: 1, 3-PDO=1, 3-propanediol, 1, 2-PDO=1, 2-propanediol, 1-PO=1-propanol, 2-PO=2-propanol, AT=acetone, ATol=acetol, PA=propionate acid. 表 2 反应时间对Pt/WO3/ZrO2(WO3含量为15 wt%) 催化剂催化甘油加氢的影响a
Table 2. Influence of reaction time to Pt/WO3/ZrO2 (contain 15 wt% of WO3)-catalyzed glycerol hydrogenolysis随后, 我们研究了不同WO3含量的Pt/WO3/ZrO2催化剂催化的甘油加氢反应 (Table 3).选取催化剂稳定时的数据做分析 (反应20 h时).研究表明, WO3是催化剂的必需成分, 而使用不含WO3的Pt/ZrO2催化剂, 甘油转化率很低, 仅9.1%, 此时产物中并没有1, 3-丙二醇生成 (Entry 1).添加1.7 wt% WO3, 可稍许提高甘油转化率, 但仍然无1, 3-丙二醇生成 (Entry 2).当催化剂中WO3含量达到3.4 wt%时, 产物中开始有1, 3-丙二醇生成, 其选择性为25.5% (Entry 3). WO3含量的增加可进一步提高甘油转化率与1, 3-丙二醇选择性 (Entries 4~5).但是, 过量的WO3会导致催化剂活性下降, 从而降低甘油转化率, 但此时1, 3-丙二醇选择性保持稳定 (Entries 6~7).使用Pt/WO3催化剂, 甘油转化率迅速降低到8.3%, 表明ZrO2同样也是催化剂的必需组分 (Entry 8)[8].
 表 3
不同WO3含量的Pt/WO3/ZrO2催化剂催化甘油加氢的研究a
Table 3.
Investigations on the glycerol hydrogenolysis catalyzed by Pt/WO3/ZrO2 catalysts with different WO3 content
表 3
不同WO3含量的Pt/WO3/ZrO2催化剂催化甘油加氢的研究a
Table 3.
Investigations on the glycerol hydrogenolysis catalyzed by Pt/WO3/ZrO2 catalysts with different WO3 content

Entry WO3/wt% Glyerol conversion/% Product Selectivityb/% 1, 3-PDO Yield/% 1, 3-PDO 1, 2-PDO 1-PO 2-PO AT ATol PA 1 0 (Pt/ZrO2) 9.1 0 75.7 4.7 0 0 1.0 0 0 2 1.7 11.7 0 79.5 5.2 0 0 1.3 0 0 3 3.4 22.3 25.5 46.2 17.8 6.4 0 0.5 0.3 5.7 4 4.7 61.6 33.6 14.2 43.0 6.0 2.5 0.2 0.5 20.7 5 6.0 87.3 32.7 10.1 50.1 5.7 1.4 0.1 0.2 28.5 6 10.0 62.2 31.7 7.2 49.1 6.3 5.0 0.2 0.5 19.7 7 15 49.2 31.2 8.0 50.4 4.4 5.0 0.3 0.7 15.4 8 Pt/WO3 8.3 35.0 8.7 40.3 5.0 7.9 2.9 0.2 2.9 aReaction conditions: 175 ℃, 2.5 MPa, 2 g of catalyst was used, the aqueous glycerol (10 wt%) was fed at the speed of 2.4 mL/h; hydrogen flow rate was 97 mL/min. bAbbreviations: 1, 3-PDO=1, 3-propanediol, 1, 2-PDO=1, 2-propanediol, 1-PO=1-propanol, 2-PO=2-propanol, AT=acetone, ATol=acetol, PA=propionate acid. 表 3 不同WO3含量的Pt/WO3/ZrO2催化剂催化甘油加氢的研究a
Table 3. Investigations on the glycerol hydrogenolysis catalyzed by Pt/WO3/ZrO2 catalysts with different WO3 content因此, 由上表可知, WO3含量为6.0 wt%时, 催化剂性能最佳, 可转化高达87.3%的甘油, 并且1, 3-丙二醇选择性较高 (32.7%).与前人的工作相比 (Table 1, Entries 1~4), 甘油的转化率得到了显著地提高, 从而可提高相关工业产能.并且, 本方法所使用的氢气压力更低, 从而降低了反应中对设备的需求以及能耗.与我们先前工作相比较 (Table 1, Entry 5), 使用适当WO3含量的催化剂, 可在无需额外添加剂的情况下, 显著提高1, 3-丙二醇选择性, 并且甘油转化率也可保持较高水平.
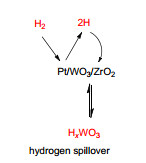
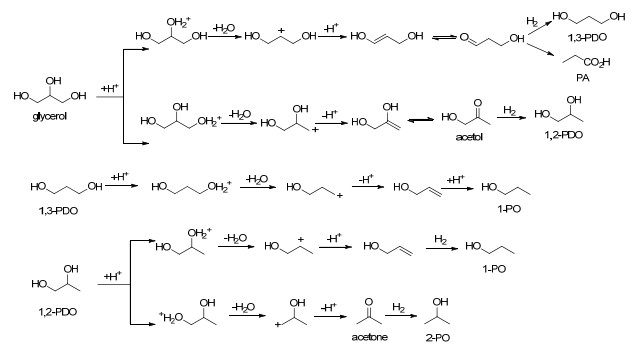
基于前述实验结果, 我们提出了可能的反应机理.首先, 在铂催化下, 氢分子被活化, 其中一部分发生了氢溢出反应, 被催化剂吸附, 形成了酸性的钨酸物种 (图 1)[9].在酸催化下, 甘油首选发生了脱水反应.随着脱水位置的不同, 产物亦不相同.其中, 中间羟基脱水, 可生成β-羟基丙醛中间体, 其进一步氢化, 可得产物1, 3-丙二醇 (1, 3-PDO), 而重排则得丙酸 (PA) (Scheme 1).甘油的末端羟基脱水, 则生成丙酮醇中间体 (acetol), 进一步氢化可得1, 2-丙二醇 (1, 2-PDO) (Scheme 1). 1, 3-丙二醇进一步脱水加氢, 得正丙醇 (Scheme 1).而1, 2-丙二醇不同位置的羟基脱水加氢, 可分别得正丙醇或异丙醇 (Scheme 1).结合机理, 表 3的结果表明, WO3含量的增加, 有利于提高催化剂酸性, 从而更加有利于中间羟基的脱水反应, 生成1, 3-丙二醇[3i, 3n, 10].而随着WO3含量的增加到6 wt%, 催化剂酸性达到最大稳定值.因此, 后续1, 3-丙二醇选择性保持稳定, 但由于增加WO3含量导致了铂分散度的下降, 使得催化剂活性下降, 从而降低了甘油转化率[3s].
2 结论
检验了WO3含量对Pt/WO3/ZrO2催化剂在甘油加氢反应中性能的影响.研究表明, 添加适量的WO3, 可提高催化剂酸性, 从而有利于1, 3-丙二醇的生成, 提高甘油转化率.我们发现, 当WO3含量为6.0 wt%时效果最佳, 甘油转化率可提高到87.3%, 超过前人报道的工作, 而1, 3-丙二醇选择性可保持30%以上, 从而大大改进了先前所报道的方法.
3 实验部分
3.1 仪器与试剂
气相色谱仪:产物定量分析所使用的仪器为GC-5890型气相色谱仪; 色谱条件为: FID检测器, PEG-20M毛细管柱 (膜厚0.5 µm, 内径0.32 mm, 柱长30 m); 使用纯度为99.99%的氮气作为载气, 纯度为99.96%的氢气作为燃气, 空气作为助燃气, 且三种气体的流速分别为30、30和350 mL/min; 柱温采用多段式程序升温:初温50 ℃保持2 min, 以10 ℃/min的升温速率至200 ℃保持10 min; 进样器温度为290 ℃, 检测器温度为290 ℃, 柱温50 ℃; 采用N2000色谱工作站处理数据.
Zr (NO3)4•5H2O (国药集团化学试剂有限公司, 分析纯), 钨酸铵H40N10O41W12•xH2O (国药集团化学试剂有限公司, 分析纯), 草酸H2C2O4•2H2O (国药集团化学试剂有限公司, 分析纯), 氯铂酸溶液H2PtCl6(国药集团化学试剂有限公司, 分析纯), 丙三醇C3H8O3(国药集团化学试剂有限公司, 分析纯).
3.2 实验方法
3.2.3 甘油加氢反应性能评价
在固定床微型催化反应装置中考察催化剂甘油加氢反应性能.将催化剂置于管式不锈钢反应器 (高45 cm, 外径22 mm, 内径11 mm) 中.催化剂经H2预还原后, 调节至反应所需压力和温度, 将10 wt%浓度甘油水溶液经过平流泵以固定流速2.4 mL/h打入反应管, 通入足量H2提供物料流动推动力.反应从开始向反应体系泵入液相反应物开始计时, 每2 h收集液相产物留待气相色谱分析.反应条件:催化剂2 g, 经250 ℃下H2还原3 h后, 反应温度调节为175 ℃, p(H2)=2.5 MPa, H2流速97 mL/min, 甘油水溶液浓度10 wt%, 流速2.4 mL/h.
辅助材料 (Supporting Information) Pt/WO3/ZrO2催化剂甘油加氢反应产物的GC色谱图和质谱图.这些材料可以免费从本刊网站 (http://sioc-journal.cn/) 上下载.
3.2.2 Pt/WO3/ZrO2催化剂的制备
将计量的钨酸铵H40N10O41W12•xH2O与草酸H2C2O4•2H2O按质量比为1:1溶解于一定量去离子水.溶液中W原子浓度为0.08 mol/L.
称取计量的ZrO2粉末浸入一定体积的上述钨酸铵溶液, 95 ℃水浴中搅拌蒸干, 110 ℃空气干燥5 h.样品研磨后置于管式炉中, 以3 ℃/min的速率升温至500 ℃, 恒温2 h, 冷至室温, 得WO3/ZrO2样品.随WO3含量增加, WO3/ZrO2粉末样品颜色从白色向黄色逐渐加深.
用移液管准确量取H2PtCl6溶液 (0.13 mol/L), 称取计量的WO3/ZrO2样品浸入其中, 95 ℃水浴中搅拌蒸干, 110 ℃空气干燥5 h.样品研磨置于管式炉中经450 ℃焙烧2 h, 并经过水蒸气脱氯处理得到Pt/WO3/ZrO2样品. Pt的负载量以m(Pt)/[m(WO3)+m(ZrO2)]×100%计, 恒定为2 wt%; WO3的负载量以m(WO3)/m(ZrO2)×100 %计, 从0~15 wt%变化.
3.2.1 m-ZrO2制备
本实验采用Zr (NO3)4为锆源, 氨水为沉淀剂制备单斜m-ZrO2.制备过程如下:将25 g Zr (NO3)4•5H2O溶于250 mL去离子水中, 逐滴加入浓氨水, 调节pH值9~10, 继续搅拌0.5 h后室温陈化4 h, 过滤洗涤至滤液pH值为7, 经110 ℃干燥5 h.研磨后的样品置于管式炉中, 以3 ℃/min的速率升温至500 ℃, 恒温2 h, 自然冷至室温, 得单斜晶相m-ZrO2.
-
-
[1]
(a) Suppes, G. J.; Dasari, M. A.; Doskocil, E. J.; Mankidy, P. J.; Goff, M. J. Appl. Catal., A 2004, 257, 213.
(b) Huber, G. W.; Iborra, S.; Corma, A. Chem. Rev. 2006, 106, 4044. -
[2]
(a) Behr, A.; Eilting, J.; Irawadi, K.; Leschinski, J.; Lindner, F. Green Chem. 2008, 10, 13.
(b) Alhanash, A.; Kozhevnikova, E. F.; Kozhevnikov, I. V. Appl. Catal., A 2010, 378, 11.
(c) King, D. L.; Zhang, L.; Xia, G.; Karim, A. M.; Heldebrant, D. J.; Wang, X.-Q.; Peterson, T.; Wang, Y. Appl. Catal., B 2010, 99, 206. -
[3]
(a) Kurosaka, T.; Maruyama, H.; Naribayashi, I.; Sasaki, Y. Catal. Commun. 2008, 9, 1360.
(b) Gong, L.-F.; LÜ , Y.; Ding, Y.-J.; Lin, R.-H.; Li, J.-W.; Dong, W.-D.; Wang, T.; Chen, W.-M. Chin. J. Catal. 2009, 30, 1189.
(c) Qin, L.-Z.; Song, M.-J.; Chen, C.-L. Green Chem. 2010, 12, 1466.
(d) Zhu, S.-H.; Gao, X.-Q.; Zhu, Y.-L.; Cui, J.-L.; Zheng, H.-Y.; Li, Y.-W. Appl. Catal., B 2014, 158, 391.
(e) Tong, Q.; Zong, A.-Y.; Gong, W.; Yu, L.; Fan, Y.-N. RSC Adv. 2016, 6, 86663.
(f) Gong, L.-F.; Lu, Y.; Ding, Y.-J.; Lin, R.-H.; Li, J.; Dong, W.-D.; Wang, T.; Chen, W.-M. Appl. Catal., A 2010, 390, 119.
(g) Daniel, O. M.; DeLaRiva, A.; Kunkes, E. L.; Datye, A. K.; Dumesic, J. A.; Davis, R. J. ChemCatChem2010, 2, 1107.
(h) Gandarias, I.; Arias, P.; Requies, J.; Güemez, M.; Fierro, J. Appl. Catal., B 2010, 97, 248.
(i) Liu, L.-J.; Zhang, Y.-H.; Wang, A.-Q.; Zhang, T. Chin. J. Catal. 2012, 33, 1257.
(j) Zhu, S.-H.; Zhu, Y.-L.; Hao, S.-L.; Chen, L.-G.; Zhang, B.; Li, Y.-W. Catal. Lett. 2012, 142, 267.
(k) Arundhathi, R.; Mizugaki, T.; Mitsudome, T.; Jitsukawa, K.; Kaneda, K. ChemSusChem2013, 6, 1345.
(l) Dam, J. ten; Djanashvili, K.; Kapteijn, F.; Hanefeld, U. ChemCatChem2013, 5, 497.
(m) Zhang, Y.-H.; Zhao, X.-C.; Wang, Y.; Zhou, L.-K.; Zhang, J.-Y.; Wang, J.; Wang, A.-Q.; Zhang, T. J. Mater. Chem. A2013, 1, 3724.
(n) Zhu, S.-H.; Gao, X.-Q.; Zhu, Y.-L.; Zhu, Y.-F.; Xiang, X.-M.; Hu, C.-X.; Li, Y.-W. Appl. Catal., B 2013, 140, 60.
(o) Zhu, S.-H.; Qiu, Y.-N.; Zhu, Y.-L.; Hao, S.-L.; Zheng, H.-Y.; Li, Y.-W. Catal. Today2013, 212, 120.
(p) Deng, C.-H.; Duan, X.-Z.; Zhou, J.-H.; Chen, D.; Zhou, X.-G.; Yuan, W.-K. Catal. Today2014, 234, 208.
(q) Priya, S. S.; Kumar, V. P.; Kantam, M. L.; Bhargava, S. K.; Chary, K. V. RSC Adv. 2014, 4, 51893.
(r) García-Fernández, S.; Gandarias, I.; Requies, J.; Güemez, M. B.; Bennici, S.; Auroux, A.; Arias, P. L. J. Catal. 2015, 323, 65.
(s) Zhu, S.-H.; Gao, X.-Q.; Zhu, Y.-L.; Li, Y.-W. J. Mol. Catal., A 2015, 398, 391. -
[4]
(a) Furikado, I.; Miyazawa, T.; Koso, S.; Shimao, A.; Kunimori, K.; Tomishige, K. Green Chem. 2007, 9, 582.
(b) Shimao, A.; Koso, S.; Ueda, N.; Shinmi, Y.; Furikado, I.; Tomishige, K. Chem. Lett. 2009, 38, 540.
(c) Guan, J.; Chen, X.-F.; Peng, G.-M.; Wang, X.-C.; Cao, Q.; Lan, Z.-G.; Mu, X.-D. Chin. J. Catal. 2013, 34, 1656. -
[5]
(a) Amada, Y.; Shinmi, Y.; Koso, S.; Kubota, T.; Nakagawa, Y.; Tomishige, K. Appl. Catal., B 2011, 105, 117.
(b) Auneau, F.; Noë l, S.; Aubert, G.; Besson, M.; Djakovitch, L.; Pinel, C. Catal. Commun. 2011, 16, 144.
(c) Nakagawa, Y.; Ning, X.; Amada, Y.; Tomishige, K. Appl. Catal., A 2012, 433, 128.
(d) Tamura, M.; Amada, Y.; Liu, S.-B.; Yuan, Z.-L.; Nakagawa, Y.; Tomishige, K. J. Mol. Catal., A 2014, 388, 177. -
[6]
(a) Yu, L. ; Chen, F. -L. ; Ding, Y. -H. ChemCatChem2016, 8, 1033.
(b) Yu, L. ; Bai, Z. -B. ; Zhang, X. ; Zhang, X. -H. ; Ding, Y. -H. ; Xu, Q. Catal. Sci. Technol. 2016, 6, 1804.
(c) Zhang, X. ; Sun, J. -J. ; Ding, Y. -H. ; Yu, L. Org. Lett. 2015, 17, 5840.
(d) Yu, L. ; Ye, J. -Q. ; Zhang, X. ; Ding, Y. -H. ; Xu, Q. Catal. Sci. Technol. 2015, 5, 4830.
(e) Zhang, X. ; Ye, J. -Q. ; Yu, L. ; Shi, X. -K. ; Zhang, M. ; Xu, Q. ; Lautens, M. Adv. Synth. Catal. 2015, 357, 955.
(f) Yu, L. ; Li, H. -Y. ; Zhang, X. ; Ye, J. -Q. ; Liu, J. -P. Xu, Q. ; Lautens, M. Org. Lett. 2014, 16, 1346.
(g) Yu, L. ; Wang, J. ; Cao, H. -E. ; Ding, K. -H. ; Xu, Q. Chin. J. Org. Chem. 2014, 34, 1986 (in Chinese).
(俞磊, 王俊, 曹洪恩, 丁克鸿, 徐清, 有机化学, 2014, 34, 1986. )
(h) Yu, L. ; Wang, J. ; Chen, T. ; Ding, K. -H. ; Pan, Y. Chin. J. Org. Chem. 2013, 33, 1096 (in Chinese).
(俞磊, 王俊, 陈天, 丁克鸿, 潘毅, 有机化学, 2013, 33, 1096. ) -
[7]
(a) Deng, S. -C. ; Meng, T. -T. ; Xu, B. -L. ; Gao, F. ; Ding, Y. -H. ; Yu, L. ; Fan, Y. -N. ACS Catal. 2016, 6, 5807.
(b) Wang, Y. -G. ; Yu, L. -H. ; Zhu, B. -C. ; Yu, L. J. Mater. Chem. A2016, 4, 10828.
(c) Xu, L. ; Wang, F. ; Huang, J. -J. ; Xu, Q. ; Yu, L. ; Fan, Y. -N. Chin. J. Org. Chem. 2016, 36, 2232 (in Chinese).
(徐林, 王芳, 黄杰军, 徐清, 俞磊, 范以宁, 有机化学, 2016, 36, 2232. )
(d) Deng, S. -C. ; Zhuang, K. ; Xu, B. -L. ; Ding, Y. -H. ; Yu, L. ; Fan, Y. -N. Catal. Sci. Technol. 2016, 6, 1772.
(e) Zhou, H. -L. ; Gong, J. -J. ; Xu, B. -L. ; Yu, L. ; Fan, Y. -N. Appl. Catal. , A 2016, 527, 30.
(f) Yu, L. ; Han, Z. Mater. Lett. 2016, 184, 312.
(g) Yu, L. ; Huang, Y. -P. ; Wei, Z. ; Ding, Y. -H. ; Su, C. -L. ; Xu, Q. J. Org. Chem. 2015, 80, 8677.
(h) Fan, L. ; Yi, R. ; Yu, L. ; Wu, Y. -L. ; Chen, T. ; Guo, R. Catal. Sci. Technol. 2012, 2, 1136. -
[8]
(a) Scheithauer, M.; Grasselli, R. K.; Knö zinger, H. Langmuir 1998, 14, 3019.
(b) Sohn, J. R.; Park, M. Y. Langmuir 1998, 14, 6140. -
[9]
(a) Schott, F. J. P.; Balle, P.; Adler, J.; Kureti, S. Appl. Catal., B 2009, 87, 18.
(b) Triwahyono, S.; Jalil, A. A.; Hattori, H. J. Nat. Gas Chem. 2007, 16, 252. -
[10]
Balaraju, M.; Rekha, V.; Prasad, P. S. S.; Devi, B. L. A. P.; Pra-sad, R. B. N.; Lingaiah, N. Appl. Catal., A 2009, 354, 82. doi: 10.1016/j.apcata.2008.11.010
-
[1]
-
表 1 已有Pt/WO3/ZrO2催化甘油选择性氢解方法的对比
Table 1. Comparison of the known Pt/WO3/ZrO2-catalyzed glycerolselective hydrogenolysis
表 2 反应时间对Pt/WO3/ZrO2(WO3含量为15 wt%) 催化剂催化甘油加氢的影响a
Table 2. Influence of reaction time to Pt/WO3/ZrO2 (contain 15 wt% of WO3)-catalyzed glycerol hydrogenolysis

Entry t/h Glyerol conversion/% Product selectivityb/% 1, 3-PDO Yield/% 1, 3-PDO 1, 2-PDO 1-PO 2-PO AT ATol PA 1 6 100 8.9 2.5 74.3 7.2 4.2 1.9 1.0 8.9 2 8 100 9.0 2.9 73.5 6.7 5.8 1.5 0.6 9.0 3 10 100 17.9 5.1 63.4 5.8 6.1 1.0 0.7 17.9 4 12 61.1 27.4 6.8 53.8 5.2 5.5 0.8 0.5 16.7 5 14 47.2 29.9 7.1 51.1 4.8 5.8 0.6 0.7 14.1 6 16 47.0 30.8 7.4 50.0 5.1 5.6 0.4 0.7 14.5 7 18 47.9 30.1 7.1 50.5 4.8 6.1 0.6 0.8 14.4 8 20 49.2 31.2 8.0 50.4 4.4 5.0 0.3 0.7 15.4 9 22 48.3 31.1 8.0 50.6 4.8 4.7 0.2 0.6 15.0 aReaction conditions: 175 ℃, 2.5 MPa, 2 g of catalyst was used; the aqueous glycerol (10 wt%) was fed at the speed of 2.4 mL/h; hydrogen flow rate was 97 mL/min. bAbbreviations: 1, 3-PDO=1, 3-propanediol, 1, 2-PDO=1, 2-propanediol, 1-PO=1-propanol, 2-PO=2-propanol, AT=acetone, ATol=acetol, PA=propionate acid. 表 3 不同WO3含量的Pt/WO3/ZrO2催化剂催化甘油加氢的研究a
Table 3. Investigations on the glycerol hydrogenolysis catalyzed by Pt/WO3/ZrO2 catalysts with different WO3 content

Entry WO3/wt% Glyerol conversion/% Product Selectivityb/% 1, 3-PDO Yield/% 1, 3-PDO 1, 2-PDO 1-PO 2-PO AT ATol PA 1 0 (Pt/ZrO2) 9.1 0 75.7 4.7 0 0 1.0 0 0 2 1.7 11.7 0 79.5 5.2 0 0 1.3 0 0 3 3.4 22.3 25.5 46.2 17.8 6.4 0 0.5 0.3 5.7 4 4.7 61.6 33.6 14.2 43.0 6.0 2.5 0.2 0.5 20.7 5 6.0 87.3 32.7 10.1 50.1 5.7 1.4 0.1 0.2 28.5 6 10.0 62.2 31.7 7.2 49.1 6.3 5.0 0.2 0.5 19.7 7 15 49.2 31.2 8.0 50.4 4.4 5.0 0.3 0.7 15.4 8 Pt/WO3 8.3 35.0 8.7 40.3 5.0 7.9 2.9 0.2 2.9 aReaction conditions: 175 ℃, 2.5 MPa, 2 g of catalyst was used, the aqueous glycerol (10 wt%) was fed at the speed of 2.4 mL/h; hydrogen flow rate was 97 mL/min. bAbbreviations: 1, 3-PDO=1, 3-propanediol, 1, 2-PDO=1, 2-propanediol, 1-PO=1-propanol, 2-PO=2-propanol, AT=acetone, ATol=acetol, PA=propionate acid. -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 8
- 文章访问数: 1899
- HTML全文浏览量: 223


 下载:
下载:

 下载:
下载:

