 图 4
四乙烯基四苯基及四乙烯基四氨基苯基异官能基笼型倍半硅氧烷 (TVTA-HFCSQ及TVTP-HFCSQ) 的结构式
Figure 4.
Chemical structures of TVTA-HFCSQ and TVTP-HFCSQ
图 4
四乙烯基四苯基及四乙烯基四氨基苯基异官能基笼型倍半硅氧烷 (TVTA-HFCSQ及TVTP-HFCSQ) 的结构式
Figure 4.
Chemical structures of TVTA-HFCSQ and TVTP-HFCSQ

Citation: Peng Jun, Xing Yuxiu, Xu Kai. A Study on Synthesis of Janus Heterofunctional Cubic Silsesquioxanes[J]. Chinese Journal of Organic Chemistry, 2017, 37(3): 636-645. doi: 10.6023/cjoc201608032

Janus异官能基笼型倍半硅氧烷的合成研究
-
关键词:
- 异官能基笼型倍半硅氧烷
- / Janus纳米粒子
- / 功能单体
English
A Study on Synthesis of Janus Heterofunctional Cubic Silsesquioxanes
-
近年来, 在纳米材料与技术领域, 利用“自上而下”构建纳米结构材料研究取得了重要的进展, 使得在纳米尺度构建杂化结构材料成为一种可能, 这为相关科技工作者提供了新的挑战与机遇[1].笼型倍半硅氧烷 (Cubic Silsesquioxane, CSQ), 作为一种日渐重要的纳米结构构筑单元, 由于其自身优异的机械及热稳定性能, 在多个领域内得到应用, 如杂化高分子[2]、光学材料[3]、生物医学材料[4]、多孔材料[5]等. CSQ分子通式为[RSiO1.5]n (n=6, 8, 10, 12), 是一类有机-无机分子内杂化笼型分子结构, 其内核为无机的Si—O—Si骨架, 顶角带有有机官能基团[6].目前, 研究最多的是高度对称结构的八官能基立方笼型倍半硅氧烷, 然而, 倍半硅氧烷笼子的衍生化反应受到顶角同官能基团的限制.
具有两种不同官能基团的笼型倍半硅氧烷异官能基笼型倍半硅氧烷 (Hetero-functional Cubic Silsesquioxane, HFCSQ) 越来越引起研究者的兴趣. HFCSQ能够拓宽笼型倍半硅氧烷的应用, 如制备主链中含CSQ聚合物、星型接枝聚合物及各向异性材料等等[7].合成制备具有准确结构的HFCSQ一直是本领域科研攻关的难题, 相关工作至今仍鲜有报道.目前, 主要有五种方法制备HFCSQ: (1) 不同硅氧烷或氯硅烷单体直接共水解缩合的方法[8]; (2) 亲核试剂诱导重排的方法[9]; (3) 两类半笼型倍半硅氧烷双盖帽的方法[10]; (4) 利用非完整笼型倍半硅氧烷的顶点盖帽的方法[11]; (5) 全同官能基CSQ部分官能化的方法[12].然而, 上述制备方法的实例中, 很多HFCSQ都是只有一个活性的官能基团, 另一官能基团大多数为烷基等惰性基团.惰性集团无法满足进一步官能衍生化的要求, 故此类HFCSQ不能称作真正意义上的HFCSQ.不仅如此, 上述方法中所得的目标产物结构不明确, 其中间产物也难以分离提纯.不同硅氧烷或氯硅烷单体共水解缩合的方法、重排法、部分官能化的方法具有共同的产物复杂、分离难度大, 难以实现可控合成的缺点, 因此, 我们在前期合成探索实验阶段积极探索了一种利用非完整笼型倍半硅氧烷的顶点盖帽以及两类半笼型倍半硅氧烷双盖帽的方法合成一类含有双键及苯基的HFCSQ的方法.非完整笼型倍半硅氧烷的顶点盖帽的方法需要七聚苯基开笼型倍半硅氧烷前驱体, 其合成途径一般有八苯基CSQ的开笼[13]或苯基三甲氧基硅烷的直接水解缩合[14].我们发现, 采用七聚苯基开笼型倍半硅氧烷前驱体, 通过乙烯基三氯硅烷“顶角盖帽”的方法能够得到乙烯基苯基CSQ, 但是该方法存在着七聚苯基开笼型倍半硅氧烷前驱体的结构不确定、得率受限且有一定分离难度, 导致HFCSQ的总体合成难度增大等缺点.半笼型倍半硅氧烷双盖帽的方法能够形成完整的笼型倍半硅氧烷结构, 但是存在结构难以调控的缺点.例如通过乙烯基半笼型倍半硅氧烷与苯基半笼型倍半硅氧烷双盖帽的方法制备目标乙烯基苯基HFCSQ, 结果表明其主要产物却为苯基CSQ.这主要是由于苯基CSQ的溶解性最差, 使得反应中的溶解平衡被打破, 从而生成更多的苯基CSQ[15].
上述两种方法有一个共同点, 即从纳米结构单元而非传统的分子单体出发构建目标HFCSQ.从分子设计角度看, 半笼型倍半硅氧烷作为一种纳米模板单元, 可成为有趣的合成完整笼型倍半硅氧烷的前体材料[16].基于此, 我们提出了一种基于半笼型倍半硅氧烷结构“自下而上”“生长”合成目标HFCSQ的新方法.本章中, 我们将合成两类HFCSQ, 即四乙烯基四氨基苯基HFCSQ (TVTA-HFCSQ) 和四乙烯基四苯基HFCSQ (TVTP-HFCSQ).以相应的氨基苯基半笼型硅醇钠盐及苯基半笼型硅醇钠盐为生长模板, 乙烯基三氯硅烷在四甲基氢氧化铵 (TMAH)/三乙胺 (Et3N) 催化下水解链接生长及成笼, 从而得到完整的具有双面结构的异官能基笼型倍半硅氧烷. TVTA-HFCSQ和TVTP-HFCSQ在四氢呋喃、氯仿、二甲基亚砜等溶剂中展现了良好的溶解性, 且产物通过傅里叶红外光谱、核磁共振氢谱、飞行时间质谱、硅谱、广角X射线衍射、热重分析等多种手段进行表征, 证明其具有明确的结构.
1 结果与讨论
1.1 前期研究探索
1.2 TVTA-HFCSQ及TVTP-HFCSQ的设计合成
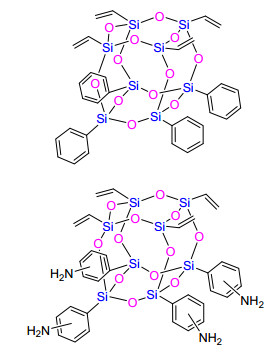
TVTA-HFCSQ及TVTP-HFCSQ的分子结构如图 4所示. TVTA-HFCSQ与TVTP-HFCSQ均具有无机Si—O—Si骨架结构, 顶角基团分别有氨基苯基、乙烯基及苯基、乙烯基, 是一类典型的Janus纳米粒子.
 图 4
四乙烯基四苯基及四乙烯基四氨基苯基异官能基笼型倍半硅氧烷 (TVTA-HFCSQ及TVTP-HFCSQ) 的结构式
Figure 4.
Chemical structures of TVTA-HFCSQ and TVTP-HFCSQ
图 4
四乙烯基四苯基及四乙烯基四氨基苯基异官能基笼型倍半硅氧烷 (TVTA-HFCSQ及TVTP-HFCSQ) 的结构式
Figure 4.
Chemical structures of TVTA-HFCSQ and TVTP-HFCSQ
1.1.1 七聚苯基开笼型三硅醇[Ph-T7-(OH)3]及七聚苯基开笼型三硅醇钠盐[Ph-T7-(ONa)3]的制备
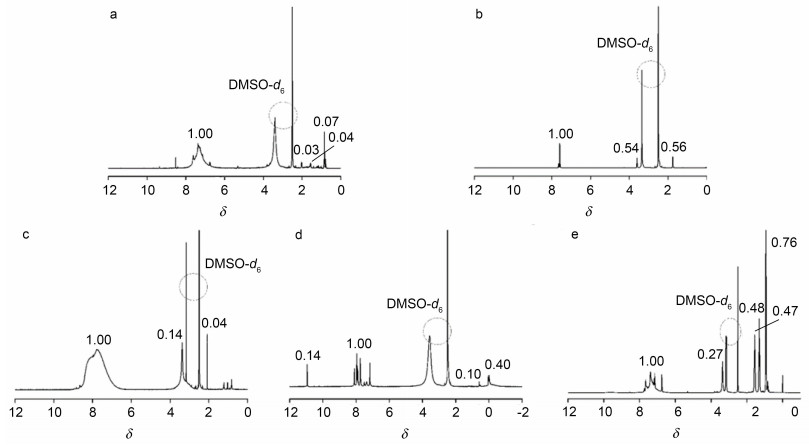
主要研究了利用非完整笼型倍半硅氧烷的顶点盖帽的方法.研究发现, 顶角盖帽的方法关键在于非完整笼型倍半硅氧烷的可控制备.为宏量制备Ph-T7-(OH)3, 采用了两种合成路线:一种是八苯基笼型倍半硅氧烷 (OPS) 的可控开笼, 另一种是苯基三甲氧基硅烷直接水解缩合的方法. 图 1为不同催化剂 (氢氧化钠、TMAH、Et3N、邻磺酰苯甲酰亚胺及TBAF) 催化下OPS开笼反应初产物的1H NMR数据.从图 1可以看出, 几类催化剂开笼产物主要的峰位移保持一致, 在δ 7~8处有明显的苯环质子氢的共振峰, 硅羟基的质子峰位移在δ 0~2间.从核磁氢谱积分面积看, 积分面积比与Ph-T7-(OH)3理论的苯环质子氢与硅羟基质子氢的个数比35:3不能符合, 表明其产物结构并不只有目标的Ph-T7-(OH)3, 为不同程度开笼产物的混合体系.虽然, 后续的薄层柱层析的分离方法可以实现Ph-T7-(OH)3的分离提纯, 但是操作复杂、周期长、得率较低这些问题将限制了进一步的盖帽.进而, 我们尝试了苯基三甲氧基硅烷直接水解缩合的方法制备Ph-T7-(ONa)3.从图 2可以看出, Ph-T7-(ONa)3初产物的核磁谱图中, 主要有较强的苯环质子氢共振峰以及疑似硅羟基的共振峰.可以看出, 除了目标的Ph-T7-(ONa)3之外还存在一些副产物, 进一步提纯可得到Ph-T7-(ONa)3.这两种方法都能得到七苯基非完整笼型产物, 为后续的顶角盖帽法提供前体材料, 缺点在于产物分离复杂且得率不高.
1.1.2 半笼倍半硅氧烷双盖帽的方法制备TVTP-HFCSQ探索实验
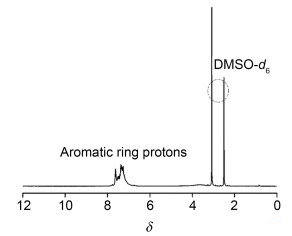
探究了四乙烯基环硅氧烷四硅醇 (TVS) 的合成与四苯基环硅氧烷四硅醇 (TPS) 双盖帽的方法制备具有两面官能基团各异的TVTP-HFCSQ.如图 3所示, 产物的核磁氢谱中, 只有δ 7.0~8.0处有明显的苯环质子氢共振峰, 乙烯基质子氢在δ 6.0附近并未观察到, 由此可见, 双盖帽的方法得到的产物可能为八苯基笼型倍半硅氧烷.可能是由于笼型产物的溶解性决定了其生成的速率及结果. OPS的溶解性较差, 因此双盖帽时, 更多的TPS自身缩合形成了OPS.双盖帽法作为一种潜在的制备双面结构HFCSQ的方法仍有一些问题亟待克服.
1.2.1 TVTA-HFCSQ及TVTP-HFCSQ的完整笼型结构及异官能基Janus结构特征
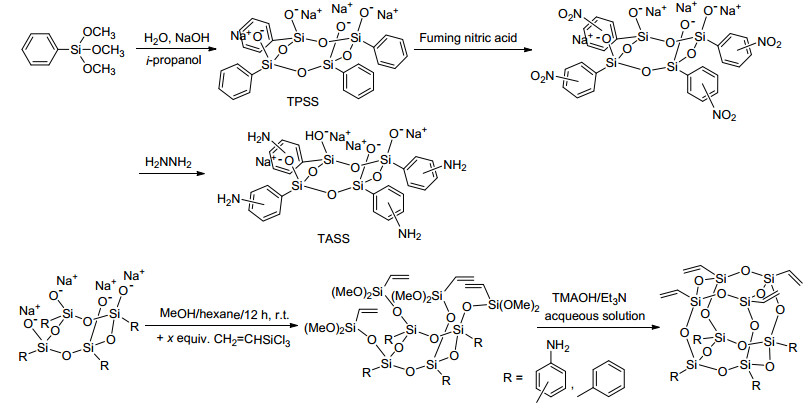
TVTA-HFCSQ及TVTP-HFCSQ的合成路线如Scheme 1所示.利用氢氧化钠催化苯基三甲氧基硅烷水解的方法, 成功地制备出四苯基环硅氧烷钠盐 (TPSS).其表征结果与文献报道符合[17]. FT-IR (KBr)v: 1583与1460 cm-1 (苯环的骨架震动), 1116 cm-1 (s, Si—O—Si); 1H NMR (DMSO-d6) δ: 6.0~7.8 (m, 1H), 核磁图谱除此峰和溶剂峰之外无其他共振峰. TPSS经过发烟硝酸硝化反应得到四硝基苯基环硅氧烷钠盐.进一步在水合肼还原为四氨基苯基环硅氧烷钠盐 (TASS). TASS的表征结果: FTIR (KBr) v: 1578与1448 cm-1(苯环的骨架震动峰), 3369, 3220 (w, N—H), 1119 cm-1 (s, Si—O—Si); 1H NMR (DMSO-d6)δ: 6.9~8.1 (d, 2.0H), 5.3~3.7 (d, 1.0H).下一步通过乙烯基三氯硅烷的模板生长法及缩合反应制备目标TVTA-HFCSQ和TVTP-HFCSQ. TMAH是一类很好的用于催化烷氧基硅烷单体水解的催化剂, 且Et3N催化条件下缩合反应更倾向于形成笼型结构[18].因此, 我们采取TMAH/Et3N复配催化体系进行第二步的二甲氧基衍生物闭笼. TVTA-HFCSQ和TVTP-HFCSQ的得率分别为37.4%及40.1%. TVTA-HFCSQ和TVTP-HFCSQ在常见有机溶剂如CHCl3、DMSQ中有较好的溶解度, 其结构通过FT-IR、1H NMR、29Si NMR、Maldi-tof MS手段进行了表征, 结晶性及热稳定性能分别由WAXD及TGA分析测得.
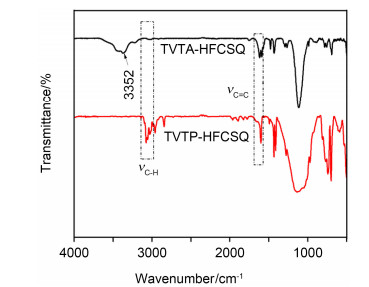
TVTA-HFCSQ和TVTP-HFCSQ的两种活性官能基团及内核的完整Si—O—Si骨架可以通过FT-IR光谱数据初步确定.从图 5可以看到, TVTA-HFCSQ和TVTP-HFCSQ两者的红外谱图中, 分别在1117, 1141 cm-1处有强的Si-O-Si伸缩振动吸收峰, 表明了内核Si-O-Si骨架的存在, 结合其在3600 cm-1附近没有Si-OH吸收峰, 可以初步判断其具有完整的笼型结构.两者谱图中同样存在3000 cm-1处附近的C-H伸缩振动峰、1432、1610 cm-1处明显的苯环骨架振动峰、1625 cm-1处附近C=C的特征振动吸收峰, 由此可见, TVTA-HFCSQ和TVTP-HFCSQ两者化学结构上都拥有苯环以及双键基团. TVTA-HFCSQ的红外谱图在3352 cm-1处有明显的N—H振动吸收峰, 硝基的特征峰消失, 表明硝基完全被还原.上述结果分析初步表明了TVTA-HFCSQ和TVTP-HFCSQ具有完整的笼型结构且分别含有氨基苯基与双键以及苯环与双键两种活性官能基团.
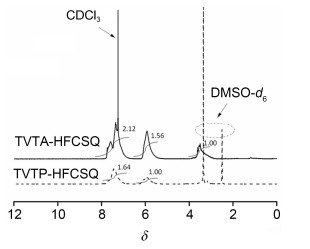
TVTA-HFCSQ和TVTP-HFCSQ两者的核磁共振氢谱数据进一步证实上述FT-IR分析的结果, 同时提供了两种活性官能基团比率的数据.如图 6所示, TVTA-HFCSQ的核磁共振氢谱图中, 可以看到, 在δ 7.28~7.81处有较强的苯环质子氢产生的多重共振峰, δ 5.76~6.12处为乙烯基氢原子产生的共振峰, δ 3.36~3.68处为氨基氢原子产生共振峰, 三者的峰积分面积之比为2.12:1.56:1, 接近理论值4:3:2, 说明TVTA-HFCSQ分子中氨基苯基与双键基团的个数相同, 为Janus纳米粒子. TVTP-HFCSQ的核磁共振氢谱中, δ 7.18~7.75为苯环质子氢的共振峰, δ 5.74~6.15为乙烯基氢原子共振峰, 两者的峰积分面积比为1.64:1, 接近理论值5:3, 表明TVTP-HFCSQ分子中苯环与双键个数相同, 结合制备方法的特点, 我们可推测其为具有双面结构的Janus纳米粒子.两者的核磁共振氢谱图中没有出现Si-OH及Si-OCH3氢原子的共振峰, 也进一步表明了闭笼过程的完全进行, 形成了目标Janus TVTA-HFCSQ和TVTP-HFCSQ结构.
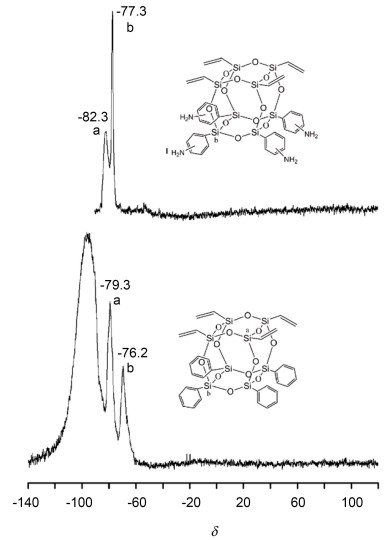
图 7为TVTA-HFCSQ及TVTP-HFCSQ的核磁共振硅谱图.首先, 可以看到两者的硅谱图中都存在两种不同环境硅原子的共振峰.在TVTA-HFCSQ及TVTP-HFCSQ硅谱图中, 分别在δ-82.3, -77.3处及δ-79.3, -76.2产生了两组共振峰. δ-82.3及-79.3处共振峰被归属为与乙烯基基团链接的硅原子, 其位移的较小变化与分子所处总体环境有关[19]; δ-77.3, 及-76.2处共振峰分别归属为与氨基苯基及苯基键接的硅原子[20].其结果表明TVTA-HFCSQ及TVTP-HFCSQ均具有两种硅原子环境, 可作为Janus结构的佐证.
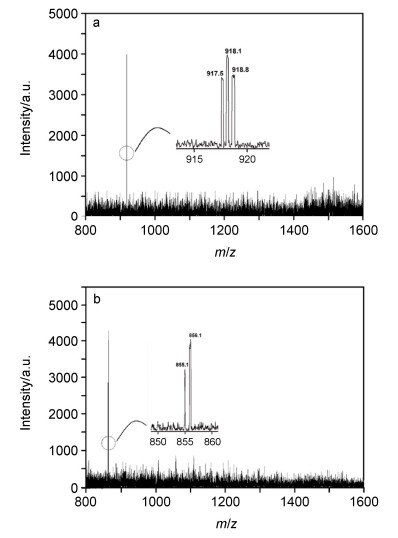
图 8是TVTA-HFCSQ及TVTP-HFCSQ的Maldi-tof质谱图. TVTA-HFCSQ及TVTP-HFCSQ的Maldi-tof质谱分别在m/z 918及856处有较强的分子缔合峰, 且没有其他的分子峰, 这说明产物具有较高的纯度.通过右上角局部放大的谱图可以看到, 主峰分别在m/z 918及856处.由于测试过程中会加入适量的钠盐辅助分子激发, 所以测试结果为真实分子量加上23, TVTA-HFCSQ及TVTP-HFCSQ理论分子量为892及832, 加上23为915及855, 与测试值918及856很吻合.综合FT-IR、1H NMR、29Si NMR及Maldi-tof质谱数据分析, 可知目标Janus TVTA-HFCSQ及TVTP-HFCSQ被成功制备, 其具有明确的化学结构及两面各异官能基团的特点.
1.2.2 TVTA-HFCSQ及TVTP-HFCSQ结晶性及热稳定性能
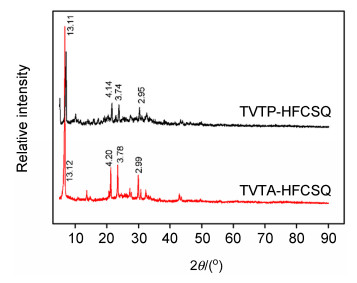
进一步利用WAXD (Wide Angle X Ray Diffraction) 对TVTA-HFCSQ及TVTP-HFCSQ可能存在的结晶结构与形态进行了表征.如图 9所示, 以TVTA-HFCSQ为例分析, 观察到在2θ=6.72°、21.10°、23.63°及29.82°, 对应的d为13. 12、4. 20、3.78及2.99 Å, 有明显的结晶衍射峰. 2θ=6.72°处最强的衍射峰被归属为由倍半硅氧烷笼型结构长程有序的排列引起的. 2θ=21.10°、23.63°及29.82°处是笼型倍半硅氧烷分子菱形结晶的衍射峰[21]. WAXD数据表明TVTA-HFCSQ及TVTP-HFCSQ存在一定的结晶性.我们进一步希望利用DSC (Differential Scanning Calorimetry) 测试其结晶熔融温度, 发现其无结晶熔融峰, 这可能是由于TVTA-HFCSQ TVTP-HFCSQ的结晶不完善, 不呈现结晶熔融峰.
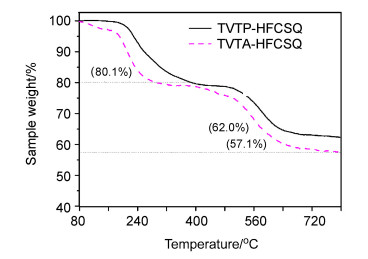
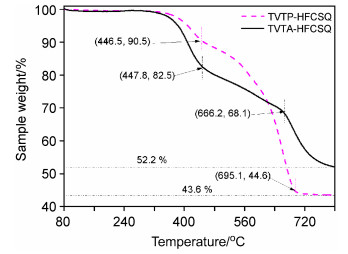
图 10为TVTA-HFCSQ及TVTP-HFCSQ氮气下的热失重曲线图.可以看到, 两者的热失重曲线比较相似, 都有两个热分解平台. TVTA-HFCSQ及TVTP-HFCSQ分子中存在几类主要的共价键: Si—O、Si—C、C—N及C=C, 其键能分别为460、347、305及611 kJ/mol.因此, 热降解应该先由共价键较弱的地方开始.氮气流下, 两者的热失重曲线在低于400 ℃时都有接近20%的失重, 这可以被归结为与乙烯基相关的Si—C键的断裂, 乙烯基基团的热分解.对于TVTA-HFCSQ及来讲, 第一个热分解平台前C—N键也会断裂, 氨基会热降解.进一步提高温度, 苯环开始热降解, 最终残余Si—O. TVTA-HFCSQ及TVTP-HFCSQ最终的Si—O残余率分别为57.1及62.0 wt%, 分别高于理论残余率46.6及55.2 wt%.这主要是因为笼型倍半硅氧烷分子在降解过程中残余下来的Si—O部分在外围形成类似陶瓷防护层, 有效保护内层快速降解, 并且有可能截留包含一部分苯基缩合形成的自由碳材料[22].结果表明TVTA-HFCSQ及TVTP-HFCSQ具有优异的耐热稳定性, 无机Si—O—Si的刚性内核为其应用于耐高温材料提供了可能.另外, 如图 11所示, 在空气中, TVTA-HFCSQ及TVTP-HFCSQ热分解行为与其在氮气中总体类似, 存在三个阶段.在空气气氛中, 热失重中间过程没有出现明显的平台期, 这与在空气中燃烧更加快速且彻底有关.并且, TVTP-HFCSQ及TVTA-HFCSQ最终残余率分别为52.2%及43.6%, 这更加接近于理论残余率55.2%及46.6%.
1.2.3 TVTA-HFCSQ及TVTP-HFCSQ电子携带及传输“超级共轭”效应
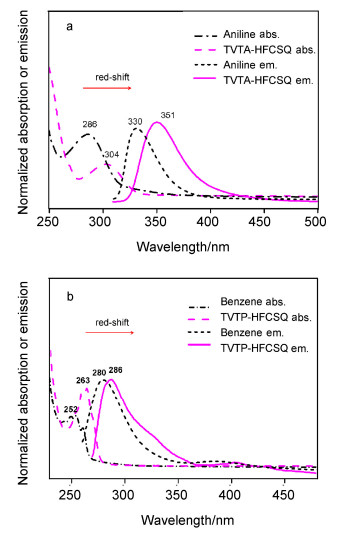
一直以来, 倍半硅氧烷笼子结构被认为是不导电的介质, 近来, 有文献报道发现其可能存在超级共轭效应[23].我们利用荧光发射及紫外吸收光谱来验证TVTA-HFCSQ及TVTP-HFCSQ内的大范围电子离域, 侧面也证实了合成的TVTA-HFCSQ及TVTP-HFCSQ具有完整的笼型结构.如图 12所示, 苯胺、苯、TVTA-HFCSQ及TVTP-HFCSQ的最大紫外吸收峰分别位于286、252、304及263 nm.比较苯胺与TVTA-HFCSQ以及苯与TVTP-HFCSQ的最大吸收峰波长, 后者紫外吸收峰都出现了红移.同样, 苯胺、苯、TVTA-HFCSQ及TVTP-HFCSQ的荧光发射光谱图也有类似的红移现象, 由苯胺的荧光发射波长为330 nm变为TVTA-HFCSQ的荧光发射波长为351 nm; 苯的荧光发射波长为280 nm变为TVTP-HFCSQ的荧光发射波长为286 nm.紫外可见光吸收及荧光发射光谱分析出现的红移可能是由于TVTA-HFCSQ及TVTP-HFCSQ的内部共轭作用引起的, 这也说明倍半硅氧烷笼子存在一定的延伸电子云共轭的作用, 对于TVTA-HFCSQ及TVTP-HFCSQ来讲, 电子云极有可能从一端经过笼子结构离域至另一端, 形成更大范围的超级共轭作用, 为TVTA-HFCSQ及TVTP-HFCSQ应用于光电材料或电子屏蔽材料提供了可能.
2 结论
成功探索出一种可宏量制备具有Janus结构的异官能基笼型倍半硅氧烷的新方法, 其包含两步反应:基于半笼型倍半硅氧烷模板进行生长以及缩合闭笼. TVTA-HFCSQ及TVTP-HFCSQ数据表征结果完整, 结构明确, 是一类新型的Janus功能纳米粒子.实验同时证实了倍半硅氧烷笼子结构的电子携带“超级共轭”效应的存在.另外, 利用其异官的特征, 可以制备出Janus各向异性的CSQ基聚合物材料, 方便得到更多种类和功能特性的CSQ聚合物. TVTA-HFCSQ及TVTP-HFCSQ有可能在主链含CSQ聚合物杂化材料、有机光电材料、太阳能电池以及各向异性材料领域有潜在的应用.其准确结构的表征数据完善, 为相关研究人员提供一定的参考.
3 实验部分
3.1 仪器与试剂
四甲基氢氧化铵五水化合物 (TMAH)、氢氧化钠、邻磺酰苯甲酰亚胺、四丁基氟化铵 (TBAF)、三乙胺、苄基三甲基氢氧化铵 (BzTMAH)、苯基三氯硅烷、苯基三甲氧基硅氧烷、乙烯基三氯硅烷、发烟硝酸、水合肼、三氯化铁、活性碳粉末, 上海阿拉丁试剂厂, 分析纯; 苯基笼型倍半硅氧烷 (OPS) 为实验室制备, 蒸馏水自制.除有特别说明, 其他材料和试剂使用前均未作处理.
红外光谱 (FT-IR) 采用美国Analect公司RFX-65A型傅里叶红外光谱仪, 固体样品采用溴化钾压片法, 液体样品溶解在丙酮中然后涂布在溴化钾片上, 红外烘干溶剂待测.核磁共振氢谱 (1H NMR)、碳谱 (13C NMR) 和硅谱 (29Si NMR) 采用德国-瑞士Bruker公司DRX 400型400 M超导核磁共振仪, 四甲基硅 (TMS) 为内标.基质辅助激光解吸时间飞行质谱仪 (MALDI-TOF) 使用AutoflexTM Ⅲ smartbean型, 辅助基质为α-氰基-4-羟基肉桂酸, 为了检测的需要适当加入了钠盐, 分别采用线性模式和反射模式.示差扫描量热 (DSC) 采用Perkin Elmer公司Diamond/Pyris Ⅰ型示差扫描量热仪, N2气氛, 升温速率20 ℃/min, 温度扫描范围为50至300 ℃, 以DSC曲线的最大峰值确定物质熔点.热重分析 (TGA) 采用Perkin-Elmer TGA-6型热重分析仪, 温度扫描范围为50至750 ℃, 检测合成产物热稳定性. UV光谱采用是UV-8000型紫外可见光分光光度计, 扫描范围为800至100 nm.荧光光谱采用的是Hitachi F-4600仪器, 样品溶解于四氢呋喃, TVTA-HFCSQ、TVTP-HFCSQ激发波长分别为300、250 nm; TVTN-HFCSQ由于硝基的强吸电子效应, 荧光淬灭.广角X射线衍射分析 (WAXD) 采用是日本Rigaku D/MAX-1200型X射线衍射仪, 以Cu Kα辐射 (λ=1. 54 Å) 为X光源, 经过Ni过滤器, 在室温下分析测试.
3.2 实验方法
3.2.6 闭笼反应制备TVTA-HFCSQ和TVTP-HFCSQ
TVTA-HFCSQ的合成: 50 mL三口烧瓶中, 1.0 g四氨基苯基四乙烯基二甲氧基衍生物溶于20 mL甲醇溶剂, 加入15 wt% TMAH/Et3N (m/m=1/1) 水溶液, 上述混合体系回流反应24 h, 直至生成淡黄色的固体产物析出.过滤后用甲醇溶剂洗涤至中性, 40 ℃真空干燥, 得到0.31 g产物, 产率37.4%. 1H NMR (400 MHz, CHCl3) δ: 8.06~6.75 (m, 2.1H), 6.61~4.96 (m, 1.6H), 3.36~3.68 (s, 1H); IR (KBr) ν: 1117, 1108, 1141, 1432, 1610, 1625, 3352; 29Si NMR (400 MHz, CHCl3) δ:-77.3, -82.3.
TVTP-HFCSQ的合成步骤如上, 得到的白色结晶状固体产物有0.34 g, 产率41.5%. 1H NMR (400 MHz, DMSO-d6) δ: 8.24~6.75 (m, 1.6H), 6.52~5.48 (m, 1H); IR (KBr) ν: 1116, 1108, 1142, 1432, 1612, 1625; 29Si NMR (400 MHz, DMSO-d6) δ:-69.5, -79.2.
辅助材料(Supporting Information) 关键中间产物及产物的核磁共振氢谱谱图和硅谱图谱.这些材料可以免费从本刊网站 (http://sioc-journal.cn/) 上下载
3.2.1 七聚苯基开笼型三硅醇 (Ph-T7-(OH)3) 及七聚苯基开笼型三硅醇钠盐 (Ph-T7-(ONa)3) 的制备
OPS可控开笼制备Ph-T7-(OH)3参照文献[13]报道的方法改进了实验.典型的投料比为n(OPS):n(水):n(催化剂)=1:1:2, OPS/异丙醇=1 mmol/10 mL.反应条件为:氮气保护下磁力搅拌回流反应24 h.采取不同的催化剂[四甲基氢氧化铵五水化合物 (TMAH)、氢氧化钠、邻磺酰苯甲酰亚胺、四丁基氟化铵 (TBAF)、三乙胺等]研究其开笼反应的结果.
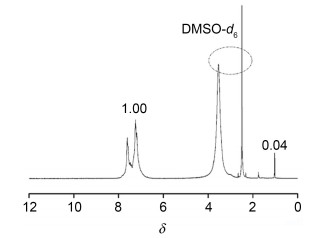
苯基三甲氧基硅烷直接水解缩合法制备Ph-T7-(ONa)3参照文献[14]的方法进行.典型的配比为: 4.5 g苯基三甲氧基硅烷、25 mL去离子水及0.4 g氢氧化钠投入到50 mL三口烧瓶中, 磁力搅拌下, 回流反应5 h, 冷却至室温后, 继续搅拌15 h, 停止反应后去除挥发性组分, 真空干燥箱干燥后得到白色固体产物.
3.2.3 四苯基环硅氧烷钠盐 (TPSS) 的制备
TPSS的合成制备参照文献[17]报道的路线合成.较优的实验典型配比为: 9.9 g (50 mmol) 苯基三甲氧基硅烷、50 mL异丙醇为溶剂、0.9 mL (50 mmol) H2O、2.0 g (50 mmol) 氢氧化钠, 室温反应12 h.随着反应的进行, 白色固体产物析出.反应结束后, 过滤, 用适量的异丙醇、甲醇分别洗涤2~3次, 再溶于适量乙醚中, 加入过量正己烷中, 析出白色固体产物, 经过真空干燥箱干燥, 得到4.8 g产物TPSS, 产率60.2%. 1H NMR (400 MHz, DMSO-d6) δ: 7.79~7.22 (m, 301H), 7.22~4.89 (m, 114H); IR (KBr) ν: 1578, 1448, 3369, 3220, 1119 cm-1; 29Si NMR (400 MHz, DMSO) δ:-69. 5.
3.2.2 两类半笼倍半硅氧烷双盖帽的方法
四乙烯基环硅氧烷四硅醇的合成 (TVS) 参照文献[17]. 4.48 g乙烯基三甲氧基硅烷、0.45 mL水、3 mL乙醇、21 mL正己烷、1.65 g氢氧化钾加入带有回流装置的50 mL三口烧瓶中, 20 ℃反应1.5 h, 析出固体产物, 过滤后干燥.
四苯基环硅氧烷四硅醇 (TPS) 的合成参照文献[17]. 9.9 g (50 mmol) 苯基三甲氧基硅烷、50 mL异丙醇为溶剂、0.9 mL (50 mmol) H2O、2.0 g (50 mmol) 氢氧化钠, 室温反应12 h.随着反应的进行, 白色固体产物析出.反应结束后, 过滤, 用适量的异丙醇、甲醇分别洗涤2~3次, 产品置于真空干燥箱干燥; 产品溶于四氢呋喃, 加入醋酸中和, 生成TPS.
TVS与TPS双盖帽反应参照文献[10]. TVS (2.5 mmol)、TPS (2.5 mmol)、苯 (10 mL) 及BzTMAH (0.28 mL, 40 wt%甲醇溶液) 加入反应瓶, 氮气保护下, 磁力搅拌室温反应12 h, 过滤固体产物, 利用苯、甲醇洗涤多次, 真空干燥, 得到产物.
3.2.4 四氨基苯基环硅氧烷钠盐 (TASS) 的制备
TASS的合成是通过TPSS硝化、还原反应制备的, 参照了苯基笼型倍半硅氧烷硝化反应制备硝基苯基笼型倍半硅氧烷的实验方法[24]. 5.0 g TPSS分批次缓慢加入30 mL发烟硝酸中 (冰水浴反应30 min), 再移至室温继续反应6 h, 反应结束后利用玻璃漏斗过滤去掉不溶物, 滴加入100 g碎冰中, 析出淡黄色固体, 通风橱中过夜, 过滤, 去离子水洗、乙醇洗至中性, 真空干燥得到5.5 g淡黄色固体四硝基苯基硅氧烷钠盐.参照硝基苯基笼型倍半硅氧烷经过还原后得到氨基苯基笼型倍半硅氧烷.将5.0 g四硝基苯基硅氧烷钠盐、50 mg三氯化铁、4 g活性炭混合加入150 mL三口烧瓶, 滴加入四氢呋喃作为溶剂; 反应体系在氮气保护下回流15 min, 然后用恒压漏斗滴加入16 mL 80%水合肼, 混合溶液继续反应6 h后, 在布氏漏斗中平铺2 cm硅藻土, 将反应溶液倾倒入过滤掉活性炭; 滤液与25 mL乙酸乙酯合并, 蒸馏水洗, 分层, 干燥, 过滤后浓缩, 浓缩液加入500 mL石油醚中, 析出灰白色固体粉末, 真空干燥; 产品重新溶解于6 mL四氢呋喃与10 mL乙酸乙酯的混合溶液, 滴加入500 mL石油醚中, 析出产物, 提纯后得到3.2 g TASS, 产率75.2%. 1H NMR (400 MHz, DMSO-d6) δ: 6.9~8.1 (m, 2.0H), 5.3~3.7 (d, 1.0H); IR (KBr) ν: 1119, 1578, 1448, 3220, 3369; 29Si NMR (400 MHz, DMSO-d6) δ:-79.1, -71.6(两处峰与其氨基在苯环上可能存在的间位及对位取代有关).
3.2.5 乙烯基三氯硅烷基于TASS及TPSS生长法制备相应的四乙烯基二甲氧基衍生物
以TASS、乙烯基三氯硅烷反应为例说明. 2.50 g (3.57 mmol) TASS分散于25 mL甲醇溶剂, 加入100 mL圆底烧瓶中; 2.34 g (14.52 mmol) 乙烯基三氯硅烷溶解于25 mL正己烷中, 通过滴液漏斗加入甲醇溶剂中, 控制滴加速度, 上述非均相反应体系在氮气保护下室温搅拌反应24 h.随着反应的进行, 不断有不溶的NaCl析出.停止反应后, 过滤, 滤液静置分层, 有机层中加入无水硫酸钠干燥, 去除溶剂后得到3.27 g淡黄色固体四氨基苯基四乙烯基二甲氧基衍生物, 产率85.1%, 1H NMR (400 MHz, DMSO-d6) δ: 7.1~7.9 (m, 18.6H), 6.1~5.8 (m, 14.7H), 5.5~5.2 (s, 10H), 3.2~3.0 (m, 25.6H); IR (KBr) ν: 1119, 1382, 1578, 1448, 3352.
TPSS与乙烯基三氯硅烷反应与上述实验步骤一致, 得到淡黄色的四苯基四乙烯基二甲氧基衍生物, 产率78.4%. 1H NMR (400 MHz, DMSO-d6) δ: 7.40 (d, J=29.0, 16.8H), 5.96 (dd, J=20.0, 11.2 Hz, 10H), 3. 51 (s, 19.8H); IR (KBr) ν: 1118, 1382, 1579, 1448 cm-1.
-
-
[1]
(a) Dickson, W.; Beckett, S.; McClatchey, C.; Murphy, A.; O'Connor, D.; Wurtz, G. A.; Pollard, R.; Zayats, A. V. Adv. Mater. 2015, 27, 5974.
(b) Wang, L.; Li, X.; Zheng, F.; Guo, Y.; Zhang, Z.; Chi, H.; Dong, Y.; Wang, C.; Lu, G. Acta Chim. Sinica 2016, 74, 259 (in Chinese).
(王雷, 李雪, 郑斐, 郭玉鑫, 张志强, 迟海军, 董岩, 王翠苹, 卢公昊, 化学学报, 2016, 74, 259.)
(c) Luo, M.; Ge, J.; Sun, W.; Zhai, H. Acta Chim. Sinica 2016, 74, 839 (in Chinese).
(罗曼琳, 葛峻羽, 孙文正, 翟慧芳, 化学学报, 2016, 74, 839.) -
[2]
Lee, A. S. S.; Lee, J. H.; Lee, J.-C.; Hong, S. M.; Hwang, S. S.; Koo, C. M. J. Mater. Chem. 2014, 2, 1277.
-
[3]
(a) Peng, J.; Xing, Y.; Xu, K.; Lin, W.; Wu, J.; Yu, Z.; Zhang, Y.; Chen, M. J. Mater. Chem. C 2015, 3, 2897.
(b) Peng, J.; Lin, W.; Xing, Y.; Xu, K.; Shuxi, G.; Yuanyuan, R.; Chen, M. Mater. Lett. 2015, 143, 1. -
[4]
Zhou, Z.; Lu, Z.-R. Nanomedicine 2014, 9, 2387. doi: 10.2217/nnm.14.133
-
[5]
Xing, Y.; Peng, J.; Xu, K.; Lin, W.; Gao, S.; Ren, Y.; Gui, X.; Liang, S.; Chen, M. Chem.-Eur. J. 2016, 22, 2114. doi: 10.1002/chem.201504473
-
[6]
(a) Cordes, D. B.; Lickiss, P. D.; Rataboul, F. Chem. Rev. 2010, 110, 2081.
(b) Wen, Y.; Liu, A. Chin. J. Org. Chem. 2005, 25, 470 (in Chinese).
(温永向, 刘安华, 有机化学, 2005, 25, 470.) http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract332646.shtml -
[7]
(a) Kuo, S.-W.; Chang, F.-C. Prog. Polym. Sci. 2011, 36, 1649.
(b) Li, D.; Niu, Y.; Yang, Y.; Wang, X.; Yang, F.; Shen, H.; Wu, D. Chem. Commun. 2015, 51, 8296. -
[8]
Kraus-Ophir, S.; Jerman, I.; Orel, B.; Mandler, D. Soft Matter 2011, 7, 8862.
-
[9]
Jung, J. H.; Laine, R. M. Macromolecules 2011, 44, 7263.
-
[10]
Tateyama, S.; Kakihana, Y.; Kawakami, Y. J. Organomet. Chem. 2010, 695, 898. doi: 10.1016/j.jorganchem.2010.01.013
-
[11]
Liu, H.; Puchberger, M.; Schubert, U. Chem.-Eur. J. 2011, 17, 5019.
-
[12]
Lin, H.; Wan, X.; Jiang, X.; Wang, Q.; Yin, J. J. Mater. Chem. 2012, 22, 2616.
-
[13]
Li, Z.; Kawakami, Y. Chem. Lett. 2008, 37, 804.
-
[14]
Wang, L.; Li, J.; Li, L.; Zheng, S. J. Polym. Sci., Part A:Polym Chem. 2013, 51, 2079. doi: 10.1002/pola.26597
-
[15]
Bassindale, A. R.; Liu, Z.; MacKinnon, I. A.; Taylor, P. G.; Yang, Y.; Light, M. E.; Horton, P. N.; Hursthouse, M. B. Dalton. Trans. 2003, 2945.
-
[16]
(a) Sulaiman, S.; Bhaskar, A.; Zhang, J.; Guda, R.; Goodson Iii, T.; Laine, R. M. Chem. Mater. 2008, 20, 5563.
(b) Wu, L.; Zang, X.; Yan, S.; Tang, S.; Li, Z. Chin. J. Org. Chem. 2014, 34, 596 (in Chinese).
(吴林, 臧雄, 阎四海, 唐松青, 李战雄, 有机化学, 2014, 34, 596.)
(c) Zhang, L.; Liu, A.; Zeng, X. Chin. J. Org. Chem. 2007, 27, 424 (in Chinese).
(张利利, 刘安华, 曾幸荣, 有机化学, 2007, 27, 424.) http://sioc-journal.cn/Jwk_yjhx/CN/abstract/abstract334794.shtml -
[17]
(a) Shchegolikhina, O.; Pozdniakova, Y.; Antipin, M.; Katsoulis, D.; Auner, N.; Herrschaft, B. Organometallics 2000, 19, 1077.
(b) Ito, R.; Kakihana, Y.; Kawakami, Y. Chem. Lett. 2009, 38, 364. -
[18]
Peng, J.; Xu, K.; Cai, H.; Wu, J.; Lin, W.; Yu, Z.; Chen, M. RSC Adv. 2014, 4, 7124. doi: 10.1021/om049928g
-
[19]
Bassindale, A. R.; Parker, D. J.; Pourny, M.; Taylor, P. G.; Horton, P. N.; Hursthouse, M. B. Organometallics 2004, 23, 4400. doi: 10.1021/om049928g
-
[20]
Huang, J.-c.; He, C.-b.; Xiao, Y.; Mya, K. Y.; Dai, J.; Siow, Y. P. Polymer 2003, 44, 4491. doi: 10.1016/S0032-3861(03)00434-8
-
[21]
Fina, A.; Tabuani, D.; Carniato, F.; Frache, A.; Boccaleri, E.; Camino, G. Thermochim. Acta 2006, 440, 36.
-
[22]
Wang, X.-T.; Yang, Y.-K.; Yang, Z.-F.; Zhou, X.-P.; Liao, Y.-G.; Lv, C.-C.; Chang, F.-C.; Xie, X.-L. J. Therm. Anal. Calorim. 2010, 102, 739. doi: 10.1007/s10973-010-0772-2
-
[23]
Xu, K.; Lin, W.; Wu, J.; Peng, J.; Xing, Y.; Gao, S.; Ren, Y.; Chen, M. New J. Chem. 2015, 39, 8405. doi: 10.1039/C5NJ01376C
-
[24]
(a) Zhang, J.; Xu, R. W.; Yu, D. S. J. Appl. Polym. Sci. 2007, 103, 1004.
(b) Tamaki, R.; Tanaka, Y.; Asuncion, M. Z.; Choi, J.; Laine, R. M. J. Am. Chem. Soc. 2001, 123, 12416.
-
[1]
-
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 8
- 文章访问数: 3335
- HTML全文浏览量: 492


 下载:
下载:












 下载:
下载:

