
Citation: Liu Mingli, Wu Qi, Shi Huifang, An Zhongfu, Huang Wei. Progress of Research on Organic/Organometallic Mechanoluminescent Materials[J]. Acta Chimica Sinica, 2018, 76(4): 246-258. doi: 10.6023/A17110504

有机/金属有机力致发光材料的研究进展
English
Progress of Research on Organic/Organometallic Mechanoluminescent Materials
-
1. 引言
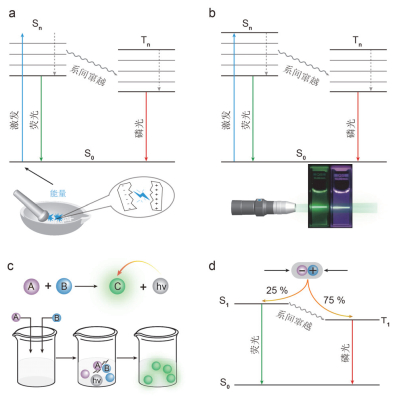
新材料是人类赖以生存的物质基础, 每种新材料的出现及应用都将伴随着现代科学技术的巨大飞跃.具有优异性能或者特定功能、应用前景广阔的新材料已成为发展信息、航天、能源、生物等高技术的重要基础材料.其中, 有机/金属有机配合物发光材料呈现出优异的光学特性, 被广泛应用于电致发光二极管[1~3]、物质检测[4, 5]、信息储器[6~10]、固体激光[11, 12]、生物/化学传感以及生物成像[13~16]等众多领域.根据材料的发光实现方式, 目前主要可以分为力致发光、光致发光、化学发光、电致发光等几种类型.力致发光(Mechanoluminescence, 简称ML)又称为摩擦发光(Triboluminescence, 简称TL), 是指当物质受到外界刺激(如研磨、摩擦、切割、粉碎或压缩等)后所呈现出的一种发光现象[17~21], 也是最早被报道的发光现象.最早发展的无机力致发光机理逐渐明确, 而有机/金属有机力致发光材料发光机理尚在探索中.近年来Fontenot, You, Nishida, Li和Chi等课题组, 对有机/金属有机力致发光材料的力致发光机理进行了深入研究, 他们认为当材料在受到外界应力作用时, 材料内部断裂, 在断裂表面形成正负电荷, 随后电荷复合形成激子, 再通过辐射跃迁衰减而发光(图 1a)[22~27].而Sijbesma课题组[28]对纯有机聚合物力致发光机理进行初探, 他们认为材料受到机械力作用后断裂, 处于激发态的结构跃迁回基态时发出光.光致发光主要包括荧光和磷光两种形式, 是指分子吸收外界激发光能量, 形成单线态激子, 以辐射跃迁衰减回到基态(S0)的发光过程称为荧光.当单线态激子通过系间窜跃转化为三线态激子, 衰减回到基态的发光过程称为磷光[29~34](图 1b).化学发光是指当A和B两种物质发生化学反应生成C物质的同时释放出化学能, 该化学能被分子C或反应中间态分子的电子吸收, 电子被激发到激发态, 并以发射光子的形式释放出光能回到基态(图 1c)[35].相比以上三种发光, 电致发光现象最晚被发现, 其原理是:在外加电场作用下, 电子和空穴分别从阴极和阳极向夹在电极之间的有机功能薄膜层注进, 注进的电子和空穴在发光层复合产生激子, 激子以辐射跃迁方式回到基态发出光的过程(图 1d)[36].相比较于其它类型发光材料, 力致发光材料因具有外力作用诱导产生发光的独特性质, 即可以将机械能转化为光能的特殊性质, 其对冲击力、张力或压力等应力作用具有敏感的光学响应, 因此这类材料在应力传感、显示、照明、成像等领域备受关注[17, 37~41].早在1605年, Bacon用刀刮方块糖时首次发现了ML现象[17, 39, 42]. 1888年Krafft发现十五烷基对甲苯基酮具有ML现象[43]. 20世纪60年代, Cotton和Goodgame等[44, 45]首次发现金属有机配合物也具备力致发光的性质.近年来, 有机/金属有机力致发光材料因其种类繁多、可修饰性强等优点而备受关注.人们通常认为有机/金属有机ML材料一般具有非中心对称结构和压电性质, 然而其发光机理尚不明确[22, 39, 46, 47], 从而导致该领域发展缓慢.根据力致发光材料的组成成份, 主要可分为无机材料、金属有机配合物材料与纯有机材料[48].无机力致发光材料虽然发光亮度强, 力致响应灵敏度高, 但其主要由贵金属元素构成, 不仅价格昂贵、毒性较大, 而且多数材料发光颜色局限于红光区域, 限制了它的发展.对于有机/金属有机力致发光材料, 由于其合成简单、成本低廉、毒性较小、发光范围宽等优点, 近年来引起了人们的高度关注.本文重点综述了自1980年以来的有机/金属有机力致发光材料进展, 最后对其未来发展予以展望.
图 1
 图 1 (a) 力致发光、(b)光致发光、(c)化学发光和(d)电致发光机理图Figure 1. (a) Mechanoluminescence, (b) photoluminescence, (c) chemiluminescence and (d) electroluminescence mechanism diagram
图 1 (a) 力致发光、(b)光致发光、(c)化学发光和(d)电致发光机理图Figure 1. (a) Mechanoluminescence, (b) photoluminescence, (c) chemiluminescence and (d) electroluminescence mechanism diagram2. 力致发光的表征
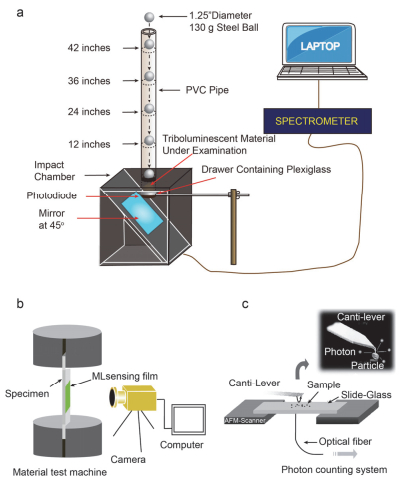
力致发光材料受到外力刺激后, 虽然有强光发出, 但是发光瞬间消失, 因此, 发光信号难以捕捉.于是, 人们根据ML的性质设计出了相应的测试设备, 主要包括落塔式、薄膜式和单个粒子式三种测试方式(图 2).如图 2a所示, 落塔式设备对ML信号表征方法如下:首先把0.1 g样品放在有机玻璃板上, 随后将130 g钢球从高1.1 m (42 inch)的桩上落下, 钢球与样品材料撞击发出光, 在距离样品2.25 cm处放置光电二极管探测器来检测ML信号, 并用线性放大器来增益ML信号振幅, 收集信号时间范围为500 ms, 收集到的信号在计算机后台进行模拟处理, 最后在显示器中显示出ML曲线, 使得ML材料性质得以表征[21, 49].薄膜式表征(图 2b)则是将ML薄膜装在试样机上, 以0.5 kN/s的速度单轴拉伸, 直到薄膜断裂, 材料试验机自动记录载荷和位移数据.同时, 利用高速相机记录ML行为, 通常实验在室温暗室中进行[50].单个粒子式表征ML行为相对简单, 如图 2c所示, 探针对样品进行力作用, 力致发光用光电倍增管来接收, 收集到的信号计算机后台处理, 最后采集记录ML的行为[51].根据材料的构成, 本文将从金属有机配合物力致发光材料与纯有机力致发光材料两个方面予以综述, 具体包括稀土金属(如Eu, Dy, Tb等)有机配合物、过渡金属(如Mn, Cu等)有机配合物及纯有机小分子和纯有机聚合物的设计与ML性质, 最后对该领域的发展进行了展望.
图 2
3. 金属有机配合物材料
3.1 稀土金属有机配合物
稀土元素因为具有特殊的电子层结构(如具有未充满并受到外界屏蔽的4f、5d电子组态)和丰富的能级数量(跃迁能级多达20余万个), 可产生丰富的辐射发光, 并且稀土离子发光具有发光谱带窄、色谱纯度高、色彩鲜艳、物理和化学性质稳定等优良的性能, 因此稀土材料在发光领域倍受追捧[52~54].因Eu3+, Dy3+和Tb3+等稀土配合物材料具有光吸收能力强、转换效率高和发光位于可见光区等特点, 所以这类稀土配合物在ML领域被广泛研究.
3.1.1 Eu3+配合物
铕离子(Eu3+)配合物具有优良的发光性能, 通常其发光光谱特征峰位于617 (5D0→7F2), 593 (5D0→7F1)和580 (5D0→7F0) nm.当Eu3+占据对称基质晶体的中心位置时, 配合物材料发光以5D0→7F1轨道跃迁为主导, 为橙色发光.若Eu3+未占据对称中心位置, 材料发光则以5D0→7F2轨道跃迁的红色发光为主导. ML材料通常为非中心对称结构, 所以人们多采用Eu3+未占据中心位置的非中心对称的分子设计, 因而ML的Eu3+配合物材料多呈现红光[55, 56]. Eu3+能形成五、六、八和九配位结构, 但ML材料多为八和九配位化合物.根据配位类型, 我们将ML的Eu3+配合物材料分为九配位的离子型和八配位的中性两类.
(1) 离子型Eu3+配合物
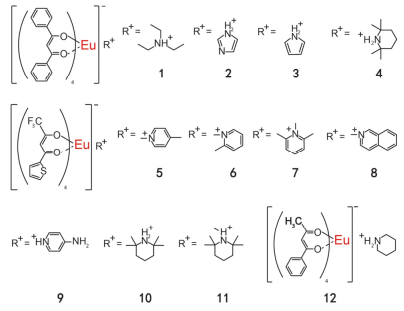
早在1966年, Hurt课题组[57]基于二苯甲酰甲烷Eu3+骨架结构, 率先报道了具有ML性质的离子型Eu3+配合物.他们通过比较不同离子配体(三乙胺、氮氮二甲基苄胺、二乙基甲胺、丙胺等)对ML性质的影响, 发现骨架结构同三乙胺形成的离子型配合物1具有最佳ML效果, 发光颜色为橙色.配合物1因具有高的ML量子产率[是常见无机物锰掺杂硫化锌(ZnS:Mn)发光材料的2倍多]和白天清晰可视的ML效果而备受关注.随后, Sweeting课题组[58]基于配合物1, 探索了不同溶剂体系制备晶体材料的ML性质, 发现仅在甲醇溶剂中长出的晶体具有ML特性, 通过对甲醇和二氯甲烷重结晶出的单晶数据分析, 发现二氯甲烷参与配合物1晶体生长, 形成的共晶结构猝灭了ML.随后他们继续探究了正己烷、乙醇和水中结晶出来的晶体, 发现都失去了ML性质.鉴于配合物1的高亮ML性质, Fontenot课题组[59]研究了有机分子、稀土金属元素以及聚合物等不同物质的掺杂对配合物1的ML性质影响.研究发现添加25 mmol%的97%胡椒碱分子对配合物1的ML性质有些许提高.当将甲基膦酸二甲酯(DMMP)掺杂到配合物1中后, 材料的ML变得非常敏感, 施加很小的作用力就会产生明亮红光, 并且掺杂后材料的ML产率比未掺杂体系约增加了55%.当掺杂摩尔比为0.95和1.25倍的磷酸二丁酯(DBP)时, ML效果分别提高了5倍和6倍.通过形貌分析发现, 掺杂DBP后, 配合物1由棒状转变成扁平块状[19].随后, 该课题组[60]将稀土Dy掺杂到配合物1中, 得到了明亮的红色发光, 当将1 mol% Dy掺杂到EuD4TEA中时, 其发光产率最高, ML强度比未掺杂的体系提高了80%.这主要是因为稀土离子与芳香衍生物发生协同作用, 增强了稀土发光激发态, 从而增加了量子效率.同年, 他们课题组[49]又掺杂了4 mol%乙酸铀酰, 其ML强度大约比未掺杂的提高了80%.此外, 该课题组[61]还研究了聚合物分子PMMA掺杂对ML性质的影响.并发现当加入体积比为3.4% PMMA时, 获得了最佳增强ML效果.若继续增加PMMA浓度, ML效果迅速减弱, 这主要是因为随着PMMA的增加, 形成的复合材料变硬, 不易于材料断裂, 从而影响ML效果.随后, You等[62]研究了二苯甲酰甲基骨架和不同芳烃离子配体(咪唑离子、吡咯离子)构成的离子型Eu3+配合物2和3的ML性质.研究发现, 虽然配合物2属于中心对称空间群, 不具有ML材料一般所应有的性质, 如非中心对称结构、压电性等, 但是配合物2属于离子型固体, 受到外力后, 可以电荷分离从而产生ML现象.从咪唑离子更换成吡咯离子后获得的Eu3+配合物3则属于非中心对称空间群, 具有压电性质, 从而产生红色的ML现象[63]. Law课题组[46]也合成了具有二苯甲酰甲基骨架的配合物4.研究发现, 配合物4中氢键可使Eu3+配合物与阳离子配体分开, 避免和阳离子配体接触, 使得该配合物的ML在白天受到外力作用下就能看到清晰的红光. You课题组[37, 64]还探索了一系列以噻吩甲酰三氟丙酮为骨架的离子型Eu3+配合物5~9的ML性质.其中, 配合物5的ML效果最佳, 白天清晰可视.结合单晶分析, 他们认为硫和氟原子的无规则排布为在裂缝的表面产生电荷分离从而形成ML现象提供了结构基础.之后Law课题组[46]又以噻吩甲酰三氟丙酮上合成出配合物10和11.经过分析, 他们认为骨架噻吩甲酰三氟丙酮结构中CF3基团比较大, 使得配体与Eu3+配合物分离较远, 阻碍氢键的形成.同时F离子旋转进入到空腔, 阻止阳离子进入, 留下一个水分子空间来协调Eu3+, 这种排布对ML的性质有影响, 当受到外力作用时H—O键振动增强, 荧光猝灭加速, 使得配合物10和11的ML效果减弱. 1989年, Rheingold课题组[27]发现苯甲酰丙酮为骨架的配合物12具有ML效果.他们课题组认为配合物12中的两个氧原子使相邻的苯基和三氟甲烷产生相互作用, 并且分子内的氢键也提供了一个压力诱导, 使得该配合物在受到外力作用时发出红色的光.
图 3
(2) 中性型Eu3+配合物
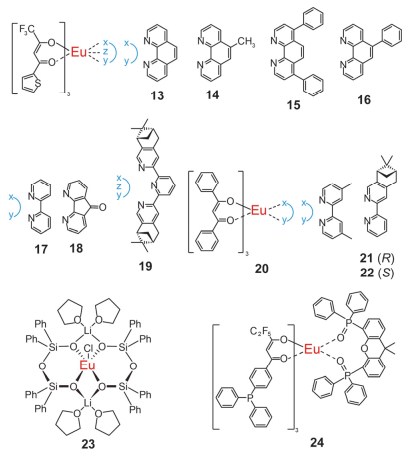
目前, ML的中性Eu3+配合物主要由第一配体的β-二酮单元与第二配体的氮杂或磷氧类芳基化合物共同组成. β-二酮结构能有效与镧系离子进行能量传递, 特别是与Eu3+离子之间. Takada课题组[65]以Eu(TTA)3配体为核, 即以噻吩甲酰三氟丙酮为骨架, 结合其它不同氮杂基团为辅助配体合成了多种配合物13~16, 并对材料的力致发光性质进行了深入研究.在1997年, 该课题组[66]发现合成的配合物13的ML光谱与Eu的PL光谱相似, 只在616 nm有些细微差异, 他们认为相似的光谱图是来源于Eu3+的发光, 不同之处是由不同的配体引起的.随后, 他们对配合物进行了不同晶轴方向的切割, 发现并不是所有切割方向都具有ML性质, 一个晶体能产生ML是因为在切割的时候, 断裂面产生压电电荷从而发出光, 所以在不同的方向切割晶体时, 当切割到具有压电电荷的地方才会有ML现象.同年, Takada课题组[67]又合成了本身具有ML效果的配合物14与不具有ML效果的配合物15和16, 然而当对配合物15和16进行10 wt% Eu3+配合物和90 wt%聚碳酸酯掺杂后, 该两种配合物又均表现出ML性质.从无到有的转变主要是因为当聚合物分散在配合物中, 两种物质受到外力后, 彼此摩擦使电子在碰撞界面产生了正负电荷, 因而激发Eu3+产生了ML现象.此外, You课题组[24]对Eu(TTA)3配体的ML材料也进行了大量研究.在1999年, 该课题组在配合物17, 18中发现了ML现象.配合物17在黑暗处能看到红色的ML, 而配合物18在白天就能清晰地看到红色的ML.如果配合物17从不同的溶剂中如甲醇、乙醇、乙腈或丙酮重结晶出来, 其ML强度会有所增强, 在白天就能发出红色光, 但配合物18重结晶后无明显变化.从晶体数据分析得知, 具有中心对称结构的配合物17能发出ML主要是因为无规则排布的噻吩环和三氟甲烷结构在受到外力作用后易使电荷分离, 从而得到ML现象. 2009年, 他们课题组[68]基于Eu(TTA)3配体合成了具有P21构型的配合物19, 这个配合物具有较小的偶极矩, 并且只有一个垂直双螺旋轴, 所以在外力作用下分子全部断裂从而发出光.随后, 该课题组[24]又以β-二苯丙酮(二苯甲酰甲基)为主体合成了新的配合物, 如配合物20, 在黑暗处能看到红色的ML, 其ML可能是因为水分子在晶体结构中形成了局部的不对称性, 促进电荷分离, 从而在受外力作用下产生力致发光现象.他们课题组[20]还引入手性分子形成非中心对称结构分子21和22, 因为引入手性分子使得配合物分子结构高度非中心对称, 更有利于产生压电作用, 合成的配合物在白天就能发出很强的红色ML现象. 2014年, Edelmann课题组[69]合成了配合物23, 发现其具有明显的红光ML现象.他们认为Eu3+离子配合物的ML源自Eu3+的5D0轨道和7F2轨道的辐射跃迁.最近, Reddy课题组[70]合成的配合物24在外力作用下发出明亮的红光, 同时在白天的情况下就能清楚地看到.该课题组认为产生ML是因为在摩擦后, 分子被激发, 引起材料断裂从而产生光发射.但是如果把配合物24与聚合物PMMA掺杂后, 配合物24的ML强度会略有下降, 可能由于掺杂后, 聚合物中分子排列间的距离变小, 导致其ML效果降低.
图 4
相比较于小分子材料, 聚合物材料具有更好的柔韧性和机械可加工性, 应用前景更为广泛.自2011年以来, Hasegawa课题组[71]对聚合物的ML材料与性质进行了深入研究. 2011年, 他们发现聚合物25在受到外力作用后, 在室温条件下白天就能观察到红色力致发光.因为它具有非对称的Cc结构, 这种结构适合压电摩擦发光, 并且低振动频率的结构抑制了非辐射跃迁失活, 从而导致有效的ML.随后, 他们[72]报道了基于刚性三角形构型的三苯基氧磷配体的Eu3+聚合物26, 该聚合物的ML寿命和效率分别为0.57 ms和49%.从图 5c中可以看出, 在紫外灯照射下自身发白光的聚合物26, 受到外力时发出红光, 从光谱图可以看出PL与ML具有不同的发射中心, ML的辐射跃迁(Kr)相比于PL小很多, 同时由于外力作用使聚合物的分子晶体破碎, 从而导致非辐射跃迁增强, 因此ML的非辐射跃迁(Knr)比PL大4倍, 所以PL的效率比ML的效率高很多. 2017年, 他们课题组[41]通过引入呋喃基团等极性桥连配体成功地制备了一系列具有高亮度的ML材料(聚合物27~29).其中27与28的ML强度在白天清晰可见, 而29在黑暗情况下才能看见(如图 5e下).通过对这三个聚合物晶体结构与ML活性之间的关系进行研究, 他们发现呋喃基桥联配体的偶极矩大于噻吩基桥联配体与二氧噻吩基桥联配体.偶极矩大有助于在聚合物中形成CF3面对面交替的分子间作用, 并且排列交叠面积大对ML活性也起到很重要作用(如图 5e右).此外, 他们还利用Tb3+与聚合物27进行掺杂, 发现当n(Tb)/n(Eu)=1时发出黄色的ML, 而当n(Tb)/n(Eu)=10时发出绿色的ML.通过图 5f中PL与ML光谱对比, 他们推论出当配体被激发, 其能量传递给Tb3+与Eu3+, 从而得到ML现象(如图 5f右).他们推论出掺杂后发出的光是稀土离子直接受激发为主, 当受到研磨后, 配体的能量转移并猝灭, 因而发光源自稀土离子发射.
图 5
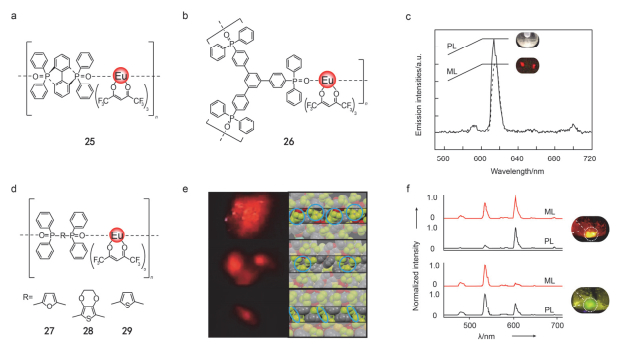 图 5 (a, b) 25, 26分子式、(c) 26的ML光谱图(虚线)和PL光谱图(实线)与各自发光现象、(d) 27~29分子式、(e) 27~29的ML现象(左)和27~29三个分子分子间CF3排列的空间填充模型(右)以及(f) n(Tb)/n(Eu)=1 (上)和n(Tb)/n(Eu)=10 (下)时的PL光谱图和ML光谱图(Eu:配合物27)Figure 5. (a, b) Chemical structures of 25, 26, (c) ML (dashed lines) and PL (solid lines) spectra (PL spectrum is obtained excited at 355 nm) of 26 (Insert: ML images), (d) chemical structures of 27~29 and (e) images of TL (left) and corresponding space filling models (right) on the intermolecular CF3 arrangement in 27, 28 and 29 and (f) PL and ML spectra of n(Tb)/n(Eu)=1 (top) and n(Tb)/n(Eu)=10 (bottom) (Eu: 27)
图 5 (a, b) 25, 26分子式、(c) 26的ML光谱图(虚线)和PL光谱图(实线)与各自发光现象、(d) 27~29分子式、(e) 27~29的ML现象(左)和27~29三个分子分子间CF3排列的空间填充模型(右)以及(f) n(Tb)/n(Eu)=1 (上)和n(Tb)/n(Eu)=10 (下)时的PL光谱图和ML光谱图(Eu:配合物27)Figure 5. (a, b) Chemical structures of 25, 26, (c) ML (dashed lines) and PL (solid lines) spectra (PL spectrum is obtained excited at 355 nm) of 26 (Insert: ML images), (d) chemical structures of 27~29 and (e) images of TL (left) and corresponding space filling models (right) on the intermolecular CF3 arrangement in 27, 28 and 29 and (f) PL and ML spectra of n(Tb)/n(Eu)=1 (top) and n(Tb)/n(Eu)=10 (bottom) (Eu: 27)3.1.2 Tb和Dy配合物
虽然稀土Eu3+, Dy3+和Tb3+类化合物材料具有光吸收能力强、转换效率高和发光位于可见光区等特殊性质, 但是具有ML现象的Dy3+和Tb3+类化合物材料却很少. 2013年Reddy课题组[73]用同一种配体分别与Tb3+和Dy3+合成了两种非中心对称结构并且具有压电性的配合物30和31, 在外力作用下白天即可观察到明亮的绿色ML(图 6a).作者归因于配体高的三线态能级和高的量子效率.化合物30和31的ML光谱和其PL光谱大体一致, 充分说明ML与PL具有相同的发色中心, 即稀土离子(图 6b). Pavlishchuk课题组[74]发现吡啶吡唑硼酸盐配体的三线态能级与镧系元素激发态之间的能级匹配, 配体能量可以有效地转移给金属离子, 并且该配体具有强的消光系数, 能加强稀土离子对光的吸收, 从而使其成为与稀土离子配位形成发光材料的优选. 2015年, 他们以吡啶吡唑硼酸盐为中心与不同的稀土离子进行配位, 得到具有红色ML的配合物32和绿色ML的配合物34.同时1 mol% Eu3+/Tb3+掺杂到配合物33中, 混合材料也能发出肉眼可见的ML.他们认为配合物32和34能产生的ML现象是因为化学键机械断裂使得断裂的电荷分布不对称, 从而产生光.然而配合物33在掺杂后能产生ML现象是由于机械能转化并转移到稀土离子, 并以光子能量形式表现出, 从而发出光.
图 6
3.2 过渡金属有机配合物
3.2.1 Mn配合物
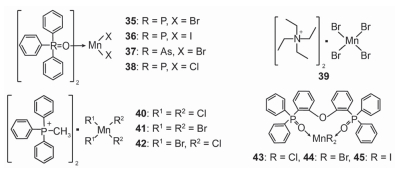
在过去的几十年中, 过渡金属Mn2+在发光领域一直很受关注[75].因为它是从4T1(G)→6A1发射, 并且不同的分子构型会产生不同的发射, 从而表现出不同的发光颜色.当Mn2+以四面体构型存在时发射出绿色荧光, 以八面体构型存在时会产生橙色到红色荧光[76]. Cotton和Chandra两个课题组发现了Mn2+奇特的发光现象, 把Mn2+应用于ML方面开展了大量研究工作.早在1961年, Cotton等[45]首次报道了过渡金属Mn2+配合物的力致发光现象.他们发现ML颜色为浅绿和浅黄色的配合物35与36在常温下就具有ML性质, 而ML颜色是浅黄绿色的配合物37在80 K下才会有ML.对于这三种物质不同的发光现象, 他们认为, 这三个物质受到外部刺激后表面结构断裂, 而断裂面处的高局部电位的放电, 激发四面体配位的Mn2+, 从而产生ML现象.随后, Cotton课题组[44]又发现了具有黄绿色力致发光现象的配合物38~40. Chandra课题组[77]发现配合物38具有ML现象, 但是没有光致发光现象.对配合物38的ML原理进行探索, 他们猜测配合物38的ML可能是由于晶体具有压电性质, 或是由于附近缺陷压电相的存在使其在外力作用下诱导发光. 1986年, 该课题组[78]用活塞对配合物35, 38, 39, 40进行挤压, 通过改变外部刺激的方法对ML性质进行研究, 他们发现对材料晶体研磨的速度和温度会影响ML发光强度.由于Mn2+的配合物合成方法简单、容易获得, 同时具有有趣的固态发光性质, Natarajan课题组[48]对该类配合物也做了大量研究.他们发现配合物41和42在白天室温条件下研磨就能清楚地观察到非常强的绿光发射.经过对光强的分析发现, 配合物41与42研磨后发出的光比ZnS/Mn发射的ML弱、比水杨酰水杨酸发射的ML强.与光致发光对比, ML和PL发光颜色一致, 所以他们猜测这两种配合物的ML发射激发态可能与PL是同一激发态.他们认为研磨导致有机单元和无机单元上的电荷产生, 当这些电荷有效再复合后产生ML.此外, 他们还发现将两个配合物暴露在质子性溶剂中(甲醇、乙醇、异戊醇、水等)会失去固体的ML性质, 当进一步利用非质子性溶剂(丙酮和甘醇)处理时, ML现象又恢复, 从而实现可逆的力致发光行为.他们认为以上的可逆变化是材料相变导致.而导致这种溶剂诱导相变的原因主要是通过中间磷原子和芳基单元之间二面角的变化以及弱C—H•••π和π•••π键之间的分子相互作用变化所致. 2015年, Zheng课题组[76]合成了一系列空气下稳定的中心对称非离子型力致发光Mn2+配合物43~45.在外力作用下有强的绿色ML, ML与其各自的PL光谱发光颜色相似, 说明这三种配合物的ML发光原理与PL相同, 都是由4T1(G)→6A1过渡态跃迁引起的发光.
图 7
3.2.2 Cu配合物
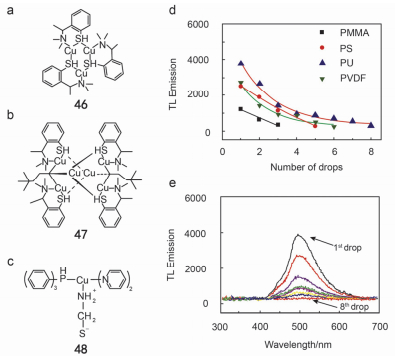
Cu配合物不仅分子结构多样性, 而且其发光光谱覆盖蓝光到红光整个可见光区, 此外, Cu+形成的配合物又有很好的光化学和光物理性质, 因此Cu配合物被广泛应用于发光领域[79, 80].同样, 该类材料在力致发光方面也有崭露头角. 1991年, Koten课题组[81]合成了配合物46并在白天观察到了明亮绿色的ML现象.随后, 基于手性配体, 合成了具有ML性质的手性配合物47.通过对该类化合物的光谱进行分析, 他们认为配合物46和47的发光源自配体到金属的电荷转移发光[82].近期, Demir课题组[83]合成出具有蓝绿色ML的配合物48.他们认为配合物48的ML性质主要是因为当外部机械力刺激后, Cu—N键断裂, 正负离子电荷分离产生电场, 因而导致ML发射.作者将配合物48跟高分子纤维材料聚甲基丙烯酸甲酯(PMMA)、聚苯乙烯(PS)、聚亚安酯(PU)和聚偏乙烯(PVDF)混合成复合物材料, 研究发现掺杂在高分子聚合物PU中的ML效果最好(图 8d).这是因为PU聚合物结构中含有苯环和羰基结构, 提高配合物与聚合物之间的范德华力, π•••π与偶极−偶极相互作用, 从而增强ML.如图 8e可以看出PU与配合物48混合材料, 在受到外界8次刺激后ML信号逐渐消失, 而ML发射的波长和轮廓在连续下降情况下保持不变, 只是强度降低.
图 8
3.2.3 Pt配合物
铂(Ⅱ)金属配合物因具有独特的方形平面分子结构, 高的磷光量子效率以及其发光在整个可见光区连续可调等特殊性质, 从而引起人们对其发光性质的研究, 并在力致发光领域展现出一定的应用潜力[84].
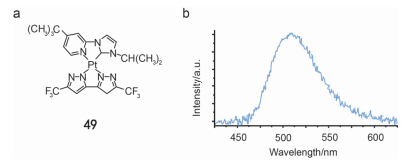
2016年Chi课题组[85]首次发现具有非中心对称的P3121空间群的配合物49具有ML性质.他们认为配合物49能够产生ML是由于材料受到外力后, Pt•••Pt键和π•••π作用力被削弱使得电荷分离, 分离松动的电荷分子重新复合衰减, 从而发出蓝绿色的力致发光.研究发现:在配合物49中的叔丁基和异丙基基团的引入为构建非中心对称分子结构实现ML性质起到了重要作用(图 9).
图 9
4. 纯有机化合物材料
4.1 纯有机小分子材料
4.1.1 咔唑类衍生物
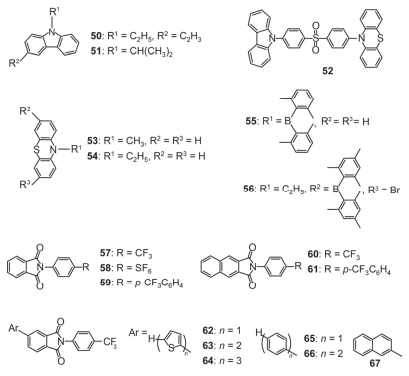
咔唑及其衍生物因具有高的三线态能级、发光量子效率和长的磷光寿命等优点, 在有机光电子学领域备受青睐.同样, 在力致发光领域也展现出很大潜力.早在1981年, Inoue等[86]发现咔唑衍生物50具有ML性质, 并把芘与该化合物进行掺杂, 通过对比掺杂前后材料的ML光物理性质来研究其发光形成原因.研究发现, 与芘掺杂材料的ML光谱特征峰主要是芘的荧光峰, 而咔唑衍生物50的ML峰消失.结果表明化合物50的ML属于单线态发射. 1983年Samoc等[87]对咔唑衍生物51的ML性质研究认为力致发光物质属于对称性热释电类材料, 其发光主要是因为晶体断裂产生新的表面, 并且引起晶体极化的改变, 使得断裂面上产生大量未补偿电荷, 电荷的能量以光的形式释放, 从而表现出强烈的绿色ML现象.最近, Chi课题组[25]发现:具有聚集诱导发光(AIE)和延迟荧光(DF)性质的非对称结构咔唑衍生物52, 在外力作用时有ML现象产生, 且在白天表现出强的绿色ML现象.经研究分析, 化合物52属于Pna21非中心对称空间群, 具有压电性, 当其受到外力作用时, 晶体断裂, 裂纹表面产生电荷, 电子放电诱导化合物产生激发态, 实现力致发光.
4.1.2 吩噻嗪衍生物
由于杂环化合物吩噻嗪是富电子材料, 并且具有扭曲的蝴蝶结构的空间构型, 引起许多课题组兴趣.不久前, Li课题组[88]以吩噻嗪结构为发光基团合成了化合物53和54, 实现了力致荧光与磷光的双发射.该两种化合物在外力作用下发出蓝色ML现象, 其中化合物53的ML现象比化合物54的ML现象弱, 在黑暗情况下才能看见.从单晶结构分析, 化合物54二聚体中C—H•••π、C—H•••N作用力比化合物53强, 从而导致两个化合物ML现象有所差别.并且该课题组认为化合物53与54产生ML原因同化合物81 ML发光原因相同.通过单晶X射线衍射分析及TD-DFT计算, 得出化合物二聚体存在分子间电荷转移态, 有利于产生磷光, 近一步研究该两种化合物, 发现力致荧光占主导地位, 即单分子激发态占主要地位, 其原因为:当对ML材料进行研磨时部分二聚体被破坏, 降低了系间窜跃从而产生弱的力致磷光和强的力致荧光.由于吩噻嗪结构特殊性, Thilagar课题组[40]也以其为中心发现了具有ML性质的化合物55, 并且在外力作用下, 白天就能看到黄绿色的光.从分子结构可以看出, 该化合物具有非常扭曲的非中心对称结构, 属于极性非对称R3C的压电空间群, 所以在外力作用下该化合物表现出力致发光现象.随后Ghosh课题组[89]做了与Thilagar课题组类似的工作, 发现了非中心对称吩噻嗪硼烷衍生物56也具有同样的ML性质.
图 10
4.1.3 N-苯基酰亚胺衍生物
众所周知, 力致发光性质与固体的压电性密切相关, 并且有压电性质的物质必须同时具有偶极结构和非中心对称的分子排列.基于此, Nishida课题组[47]把目光抛向了不对称N-苯基酰亚胺衍生物, 因为酰亚胺衍生物基团易于发生反应, 并且分子自身具有偶极矩, 当引入其它基团时很容易构建出新的具有偶极矩的化合物.他们在N-苯基酰亚胺衍生物上分别修饰CF3, SF5, p-CF3C6H4基团得到了N-苯基酰亚胺衍生物57~59.这三种化合物在常温黑暗情况下均表现出蓝色力致发光.而在白天液氮冻融状态下, 57~59固体样品仍然表现出ML特性, 与常温比较发光更明显. 57~59分子中具有强的吸电子基团CF3, SF5, 使得化合物的偶极矩增大.在外力作用下, 固体表面断裂, 裂开的表面电荷放电使化合物和周围的N2作用产生激发态, 从而发出光.进一步, 他们在N-苯基酰亚胺衍生物苯环一侧联接苯环, 扩展其共轭程度和增大分子平面, 得到了具有蓝色ML的N-苯基酰亚胺衍生物60和61, 其力致发光峰值分别位于436和460 nm.这两个材料分子偶极矩比较大, 分子结构呈现层状结构, 具有高介电性能和扭曲的构象交叉式堆积, 所以在受到外力作用时, 分子容易断裂产生电荷, 并实现力致发光现象.他们认为, 能产生ML的物质需要具有非中心对称的分子排列和扭曲的构型并且分子具有较大的偶极矩等特征.随后, 该课题组[22]发现了N-三氟甲基苯取代邻苯二甲酰亚胺衍生物具有独特的非中心对称结构, 并且能产生明亮的ML.因此, 他们将N-三氟甲基苯取代邻苯二甲酰亚胺衍生物为核心, 合成了六种新型化合物62~67.在室温暗室里, 可以清楚看到多彩的ML, 发光颜色分别为绿蓝、橙色、红橙色、蓝色、蓝绿色和浅蓝色.其中, 化合物66表现出的ML比其余五个化合物更强, 在白天即可观察到.这主要是因为分子66的偶极矩相对较高, 分子共轭程度相对较大, C—H•••π间相互作用和氢键作用使分子间刚性增强, 抑制非辐射失活, 提高荧光量子产率.也就是说, 合适的刚性芳基取代基有助于ML、PL效率的提高, 同时可以将其发光颜色调节至可见光区.若在低温下, 六种化合物的力致发光强度会大幅度提高.
4.1.4 四苯乙烯类衍生物
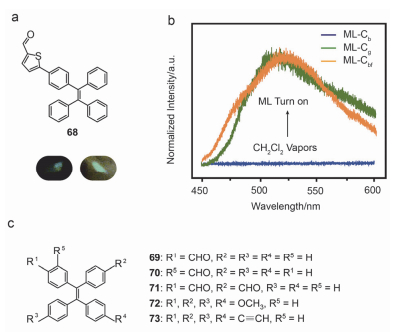
四苯乙烯(TPE)由于其特殊的分子结构和AIE性质, 在有机发光材料体系受到广泛关注.近年来, 以TPE分子为核的发光材料在ML领域也取得了快速发展.鉴于羰基的强吸电子性质, 其有利于形成大的分子偶极矩和强的分子间氢键等性质, Chi课题组以四苯乙烯为核心, 引入含有羰基结构的醛基, 获得了一系列ML材料. 2015年, Chi等[39]发现TPE衍生物68具有两种晶体构型, 其中具有Cg构型的材料在外力作用下可以发出绿光, 而Cb构型没有ML性质.通过晶体结构分析发现Cg构型中噻吩环与相连的苯环呈现扭转结构, Cb结构中两个芳香环近似共平面, 所以他们认为不同分子构型表现出不同的发光现象.分子结构扭曲的Cg构型具有强的压电性质和非中心对称结构, 所以当晶体被破坏时发出耀眼的绿光(图 11a).当Cb构型材料通过二氯甲烷的熏蒸转变成Cg构型后, 在外力作用下也能观察到绿色ML现象(图 11b).随后, 他们[38]合成了一系列TPE衍生物69~71研究了不同醛基取代位点对ML性质的影响.在外力刺激下化合物69和71晶体在白天环境下便可观察到蓝色的力致发光现象.然而, TPE衍生物70仅能在黑暗下可观察到蓝色ML. 2016年, Li课题组[17]报道了具有P21(c)和C2两种空间群的TPE衍生物72, 研究发现只有P21(c)空间群的材料具有ML现象.从晶体数据分析, 以垂直排列的Cp构型具有紧密的分子堆积, 并且分子间的C—H•••O, C—H•••π键长都比Cc构型的键长短, 由此可看出Cp1构型的分子内作用力比Cc大, 其共轭效应也比Cc好.对于化合物72的Cp构型, 具有刚性的分子堆积和较强的分子间作用力, 使得分子轻微滑移较小并且减少非辐射跃迁, 当受到外力刺激时随着晶体断裂转变成较小的晶体辐射跃迁通道慢慢打开, 发出深蓝色的ML.近期, Li课题组[90]首次报道了具有非极性中心对称结构的纯碳氢ML材料73.虽然TPE衍生物73是非压电性质材料, 但是强的分子间作用力使其具有ML性质.即具有sp杂化类型的碳碳叁键(C≡C)与其它分子形成C—H•••π作用, 使得分子间形成强的静电相互作用, 从而当受到外力刺激时晶体断裂, 并被激发从而产生绿色ML现象.
图 11
4.1.5 其它类化合物
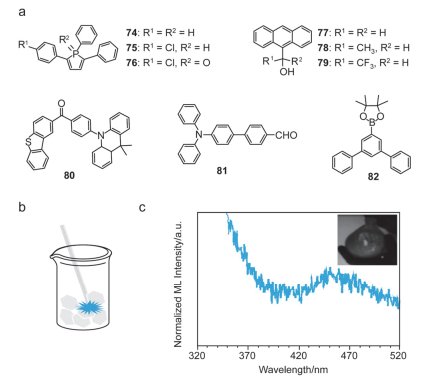
除了上述四类力致发光材料体系外, 人们还研究了一系列苯基、蒽等衍生物材料的力致发光现象.早在1981年, Zink课题组[91]提出晶体的极性会影响ML性质, 压电性对ML有一定作用, 并且ML的材料通常为C2和P21cn空间群.在1989年, 他们[19]以苯环为主体合成的三个苯环衍生物74~76, 在外力作用下均呈现出黄绿色的ML, 这主要归因于材料不对称的分子晶体结构.此外, 这三个分子的ML还可能依赖于结晶溶剂, 即通过痕量掺杂诱导局部缺陷产生电荷, 使其发光. 1988年, Rheingold等[92]基于苯环衍生物蒽得到了三个具有ML性质的化合物77~79.他们认为这三个物质具有ML性质可能是因为在外力作用后结构变形, 局部电荷断裂, 在裂纹的相对面上或在单个表面上分离电荷, 最后电荷跨过间隙或沿着断裂表面放电. Tang课题组[93]一直是材料界领军人物, 并在TADF材料方面有深入研究, 今年该课题组报道了具有非对称D-A-D’(D:给体, A:受体)结构的TADF(热激活延迟荧光)材料(化合物80)具有ML性质.当受到外力作用时, 化合物80在室温条件下可以观察到明亮的蓝绿光.经研究发现, 该材料属于正交晶系的Pca21空间群.因其特殊的偶极矩和高度扭曲的分子结构使得其具有ML性质. Li课题组[26]对ML材料一直颇有研究, 并且该课题组以苯环为核心, 合成出了许多ML材料.在今年, 该课题组发现了非AIE基团的ML材料, 即苯环衍生物三苯胺为核心的分子81.对其单晶结构进行分析, 发现化合物81属于Pca21非中心对称的正交晶系构型, 由于其有效的分子间相互作用使得分子具有刚性结构, 当受到外力作用时减少分子滑移, 并且自由电子产生导致光子发射从而产生绿色ML现象.最近几年他们首次合成出了具有力致荧光、磷光双发射的磷光材料, 如在2016年, 首次报道了荧光和磷光双发射且具有AIE特性的ML材料(化合物82).如图 12c所示, 材料的力致荧光发射峰位于350 nm, 磷光发射450 nm处.通过单晶结构分析, 他们得出化合物82上氧原子的孤对电子与相邻的苯环有强的相互作用, 即C—H•••O作用, 增强了n-π*的跃迁, 提高了系间窜越.降低非辐射衰减, 从而产生力致磷光.进一步从晶体结构和理论计算分析, 得出有效的分子间和分子内的相互作用导致力致荧光、磷光双发射, 并有利于系间窜越和低温有机磷光的产生[94].
图 12
4.2 纯有机聚合物材料
机械应力转化为化学信号已经被广泛研究, 并且机械力化学传导过程可以实现多种的重要功能, 如听力、细胞粘附和离子通道门控.目前, 人们已经开发出将机械刺激转化为光响应的方法.然而, 分子水平传导力转化为光仍然是一个挑战. Sijbesma课题组[28]最近报道了有关将机械能转化为光的分子水平拉致发光的研究, 其研究都是围绕1, 2-二氧环丁烷展开.主要是因为1, 2-二氧环丁烷不稳定, 受热易分解, 形成两个酮式结构, 分别位于基态和激发态, 当激发态的酮式结构跃迁回基态时, 蓝色荧光随之产生. 2012年, 他们将1, 2-二氧环丁烷引入到聚合物里, 并且作为聚合物的主链, 当83受到外力拉伸时1, 2-二氧环丁烷聚合物断裂, 发出微弱的蓝光.因为发射的蓝光大部分不能被肉眼捕获, 所以他们向聚合物中加入荧光量子效率高的小分子受体如9, 10-二苯基蒽、苝等, 发光强度得到很大提高, 并且颜色也得到调控(如图 13a).随后, 该课题组[95]以聚二甲基硅烷作为交联剂, 蒽作为接受能量受体, 掺杂乙烯基硅烷和酮聚合物, 在Pt作催化剂情况下合成聚合物84, 在外力拉伸下聚合物的共价键断裂, 从而可发出光, 随着断裂的数目增加发出的光越来越强, 当断裂数目达到最大时发出的光最强.这种化学发光优点在于不需要激发光, 只需外力拉断即可发光, 操作简易.热塑性弹性体是一类重要的工程弹性体.由于有良好的机械强度、撕裂、耐磨、高弹性和可熔融加工性质, 这类材料已经被广泛应用在商业和工业领域, 然而热塑性弹性体的ML材料却鲜有报道.值得指出的是, 通过缩聚反应制备的一系列热塑性弹性体, 特别是含1, 2-二氧环丁烷的聚胺酯, 由于氢键的物理交联作用和微相分离作用, 呈现出很好的机械强度和发光性能. 2014年, 第一例具有ML性质的热塑性弹性体聚酰胺和聚酯85~87被报道.其中聚酰胺85~87在受到拉伸时随着氢键密度的增加发光强度明显增加, 但是没有氢键的聚酯85被拉伸时依然可以观察到微弱的发光.结果表明, 氢键作为物理交联点能够有效提高链缠结作用, 但并不是必须的[96].
图 13
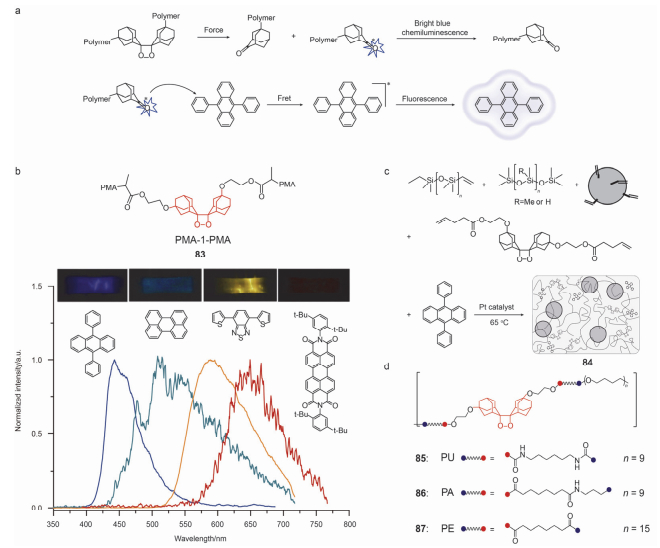 图 13 (a) 机械诱导化学发光(机械作用于1, 2-二氧环丁烷, 断裂形成激发态的1, 2-二氧环丁烷将能量转移给荧光体9, 10-二苯并蒽, 且发射峰在420 nm)、(b)掺杂不同荧光受体的聚合物薄膜拉伸过程中的荧光光谱[插图:薄膜的光学图像变形和相应的受体的化学结构式(从左到右: 9, 10-二苯并蒽, 苝, 4, 7-二噻吩苯并[1, 2, 5]噻重氮和N, N'-二(2, 5-二叔丁基苯基)-3, 4, 9, 10-二甲酰亚胺]、(c) 84的合成路线和(d) 85~87的结构式Figure 13. (a) The mechano-induced chemoluminescence. 9, 10-diphenylanthracene accepts excitated energy from the mechanically formed excited state adamantanones via fret, then releases energy as fluorescence at 420 nm (Reprinted with permission from ref [95]. Copyright 2016 WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim), (b) luminescence spectra obtained during stretching of films of 81 that with different acceptors [Inserts show the corresponding optical images of the films during deformation and the chemical structures of the acceptors (from left to right: 9, 10-diphenylanthracene, perylene, 4, 7-di(thiophen-2-yl)-benzo[c][1, 2, 5]-thiadiazole and N, N'-bis(2, 5-di-tert-but-ylphenyl)-3, 4, 9, 10-perylene dicarboximide). Reprinted with permission from ref [28]. Copyright 2017 Nature Chemistry], (c) synthetic route of 84 and (d) chemical structures of 85
图 13 (a) 机械诱导化学发光(机械作用于1, 2-二氧环丁烷, 断裂形成激发态的1, 2-二氧环丁烷将能量转移给荧光体9, 10-二苯并蒽, 且发射峰在420 nm)、(b)掺杂不同荧光受体的聚合物薄膜拉伸过程中的荧光光谱[插图:薄膜的光学图像变形和相应的受体的化学结构式(从左到右: 9, 10-二苯并蒽, 苝, 4, 7-二噻吩苯并[1, 2, 5]噻重氮和N, N'-二(2, 5-二叔丁基苯基)-3, 4, 9, 10-二甲酰亚胺]、(c) 84的合成路线和(d) 85~87的结构式Figure 13. (a) The mechano-induced chemoluminescence. 9, 10-diphenylanthracene accepts excitated energy from the mechanically formed excited state adamantanones via fret, then releases energy as fluorescence at 420 nm (Reprinted with permission from ref [95]. Copyright 2016 WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim), (b) luminescence spectra obtained during stretching of films of 81 that with different acceptors [Inserts show the corresponding optical images of the films during deformation and the chemical structures of the acceptors (from left to right: 9, 10-diphenylanthracene, perylene, 4, 7-di(thiophen-2-yl)-benzo[c][1, 2, 5]-thiadiazole and N, N'-bis(2, 5-di-tert-but-ylphenyl)-3, 4, 9, 10-perylene dicarboximide). Reprinted with permission from ref [28]. Copyright 2017 Nature Chemistry], (c) synthetic route of 84 and (d) chemical structures of 855. 总结与展望
主要针对有机/金属有机力致发光现象, 归纳总结了有机/金属有机力致发光材料、机理与性能的发展现状.在材料方面, 具体包括稀土金属有机配合物材料、过渡金属有机配合物材料、纯有机小分子材料和纯有机聚合物材料.近年来, 有机/金属有机力致发光材料取得了飞速发展, 但是目前的材料体系主要局限在少数小分子材料体系, 设计制备新型的材料体系依旧是有机/金属有机力致发光的核心.随着柔性电子的发展, 聚合物的力致发光材料孕育着巨大潜力.相比较于材料的设计与制备, 力致发光机理的进展相对滞后, 有机/金属有机力致发光机理争论相对较大.目前, 普遍公认有机/金属有机力致发光材料的ML机理为:具有非中心对称结构与压电性质的材料易于产生力致发光现象, 因为扭曲的非对称结构的有机/金属有机材料在受到外界刺激时, 结构被破坏使得分子内部断裂并在断裂表面产生电荷, 随后电荷复合并发光.该机理主要衍生于无机力致发光的机理, 对于有机/金属有机力致发光材料的机理有待进一步实验与理论推理验证.而对于纯有机聚合物力致发光机理进行初探, Sijbesma课题组认为当材料受到机械力拉伸时, 处于激发态的结构跃迁回基态时发出光.此外, 对于无机力致发光材料的应用已经取得了一定发展, 被广泛应用于冲击力、应力、张力或压力敏感的传感器领域, 同时在显示、照明、成像等方面也有着广泛的应用.然而, 对于有机/金属有机力致发光材料的应用探索目前却寥寥无几, 拓展材料的应用, 将进一步推动有机/金属有机力致发光材料的发展.
-
-
[1]
Liang, X.; Wang, Z.; Wang, L.; Hanif, M.; Hu, D.; Su, S.; Xie, Z.; Gao, Y.; Yang, B.; Ma, Y. Chin. J. Chem. 2017, 35, 1559. doi: 10.1002/cjoc.v35.10
-
[2]
潘凌翔, 罗文文, 陈明, 刘峻恺, 徐露, 胡蓉蓉, 赵祖金, 秦安军, 唐本忠, 有机化学, 2016, 36, 1316. Pan, L.; Luo, W.; Chen, M.; Liu, J.; Xu, L.; Hu, R.; Zhao, Z.; Qin, A.; Tang, B. Chin. J. Org. Chem. 2016, 36, 1316.
-
[3]
张振宇, 李婉君, 叶开其, 张红雨, 化学学报, 2016, 74, 179. doi: 10.6023/A15090603Zhang, Z.; Li, W.; Ye, K.; Zhang, H. Acta Chim. Sinica 2016, 74, 179. doi: 10.6023/A15090603
-
[4]
Tang, Y.; Huang, H.; Peng, Y.; Ruan, Q.; Wang, K.; Yi, P.; Liu, D.; Zhong, C. Chin. J. Chem. 2017, 35, 1091. doi: 10.1002/cjoc.v35.7
-
[5]
管伟江, 周文娟, 吕超, 化学学报, 2016, 74, 929. doi: 10.6023/A16080427Guan, W.; Zhou, W.; Lü, C. Acta Chim. Sinica 2016, 74, 929. doi: 10.6023/A16080427
-
[6]
An, Z.; Zheng, C.; Tao, Y.; Chen, R.; Shi, H.; Chen, T.; Wang, Z.; Li, H.; Deng, R.; Liu, X.; Huang, W. Nat. Mater. 2015, 14, 685. doi: 10.1038/nmat4259
-
[7]
Li, L.; Cao, X.; Huang, R. Chin. J. Chem. 2016, 34, 143. doi: 10.1002/cjoc.v34.2
-
[8]
Wei, J.; Liang, B.; Duan, R.; Cheng, Z.; Li, C.; Zhou, T.; Yi, Y.; Wang, Y. Angew. Chem., Int. Ed. 2016, 55, 15589. doi: 10.1002/anie.201607653
-
[9]
Zhao, W.; He, Z.; Lam, J.; Peng, Q.; Ma, H.; Shuai, Z.; Bai, G.; Hao, J.; Tang, B. Chem 2016, 1, 592. doi: 10.1016/j.chempr.2016.08.010
-
[10]
Cao, Y.; Wang, R.; Wu, G.; Fang, Q.; Qiu, S. Chin. J. Chem. 2016, 34, 196. doi: 10.1002/cjoc.v34.2
-
[11]
李文强, 彭谦, 谢育俊, 张天, 帅志刚, 化学学报, 2016, 74, 902. Li, W.; Peng, Q.; Xie, Y.; Zhang, T.; Shuai, Z. Acta Chim. Sinica 2016, 74, 902.
-
[12]
Xu, H.; Chen, R.; Sun, Q.; Lai, W.; Su, Q.; Huang, W.; Liu, X. Chem. Soc. Rev. 2014, 43, 3259. doi: 10.1039/C3CS60449G
-
[13]
Shi, H.; Ma, X.; Zhao, Q.; Liu, B.; Qu, Q.; An, Z.; Zhao, Y.; Huang, W. Adv. Funct. Mater. 2014, 24, 4823. doi: 10.1002/adfm.v24.30
-
[14]
黄玉章, 雷洛奇, 郑超, 危博, 赵祖金, 秦安军, 胡蓉蓉, 唐本忠, 化学学报, 2016, 74, 885. Huang, Y.; Lei, L.; Zheng, C.; Wei, B.; Zhao, Z.; Qin, A.; Hu, R.; Tang, B. Acta Chim. Sinica 2016, 74, 885.
-
[15]
Peng, Z.; Wang, Z.; Tong, B.; Ji, Y.; Shi, J.; Zhi, J.; Dong, Y. Chin. J. Chem. 2016, 34, 1071. doi: 10.1002/cjoc.v34.11
-
[16]
钱鑫, 苏萌, 李风煜, 化学学报, 2016, 74, 565. doi: 10.3866/PKU.WHXB201511301Qian, X.; Su, M.; Li, F. Acta Chim. Sinica 2016, 74, 565. doi: 10.3866/PKU.WHXB201511301
-
[17]
Wang, C.; Xu, B.; Li, M.; Chi, Z.; Xie, Y.; Li, Q.; Li, Z. Mater. Horiz. 2016, 3, 220. doi: 10.1039/C6MH00025H
-
[18]
Chandra, B. P.; Zink, J. I. J. Chem. Phys. 1980, 73, 5933. doi: 10.1063/1.440151
-
[19]
Hocking, M. B.; Preston, D. M.; Zink, J. I. J. Lumin. 1989, 43, 309. doi: 10.1016/0022-2313(89)90101-4
-
[20]
Li, X.; Zheng, Y.; Zuo, J.; Song, Y.; You, X. Polyhedron 2007, 26, 5257. doi: 10.1016/j.poly.2007.07.047
-
[21]
Fontenot, R. S.; Bhat, K. N.; Hollerman, W. A.; Aggarwal, M. D.; Nguyen, K. M. CrystEngComm. 2012, 14, 1382. doi: 10.1039/C2CE06277A
-
[22]
Nishida, J. I.; Ohura, H.; Kita, Y.; Hasegawa, H.; Kawase, T.; Takada, N.; Sato, H.; Sei, Y.; Yamashita, Y. J. Org. Chem. 2016, 81, 433. doi: 10.1021/acs.joc.5b02191
-
[23]
Fontenot, R. S.; Bhat, K. N.; Owens, C. A.; Hollerman, W. A.; Aggarwal, M. D. J. Lumin. 2015, 158, 428. doi: 10.1016/j.jlumin.2014.10.026
-
[24]
Chen, X.; Zhu, X.; Xu, Y.; Raj, S. S. S.; Öztürk, S.; Fun, H.; Ma, J.; You, X. J. Mater. Chem. 1999, 9, 2919. doi: 10.1039/a904411f
-
[25]
Xu, S.; Liu, T.; Mu, Y.; Wang, Y.; Chi, Z.; Lo, C.; Liu, S.; Zhang, Y.; Lien, A.; Xu, J. Angew. Chem., Int. Ed. 2015, 54, 874. doi: 10.1002/anie.201409767
-
[26]
Fang, M.; Yang, J.; Liao, Q.; Gong, Y.; Xie, Z.; Chi, Z.; Peng, Q.; Li, Q.; Li, Z. J. Mater. Chem. C 2017, 5, 9879. doi: 10.1039/C7TC03641H
-
[27]
Rheingold, A. L.; King, W. Inorg. Chem. 1989, 28, 1715. doi: 10.1021/ic00308a025
-
[28]
Chen, Y.; Spiering, A. J. H.; Karthikeyan, S.; Peters, G. W. M.; Meijer, E. W.; Sijbesma, R. P. Nat. Chem. 2012, 4, 559. doi: 10.1038/nchem.1358
-
[29]
Wang, M.; Guo, G.; Chen, W.; Xu, G.; Zhou, W.; Wu, K.; Huang, J. Angew. Chem., Int. Ed. 2007, 46, 3909. doi: 10.1002/(ISSN)1521-3773
-
[30]
Wang, G.; Xu, G.; Wang, M.; Cai, L.; Li, W.; Guo, G. Chem. Sci. 2015, 6, 7222. doi: 10.1039/C5SC02501J
-
[31]
Wang, M.; Guo, G. Chem. Commun. 2016, 52, 13194. doi: 10.1039/C6CC03184F
-
[32]
Zhang, N.; Sun, C.; Jiang, X.; Xing, X.; Yan, Y.; Cai, L.; Wang, M.; Guo, G. C. Chem. Commun. 2017, 53, 9269. doi: 10.1039/C7CC05446G
-
[33]
Wang, M.; Guo, S.; Li, Y.; Cai, L.; Zou, J.; Xu, G.; Zhou, W.; Zheng, F.; Guo, G. J. Am. Chem. Soc. 2009, 131, 13572. doi: 10.1021/ja903947b
-
[34]
杨贺玮, 张宇哲, 李艳杰, 王京翔, 李小萌, 宋健, 张宝, 冯亚青, 有机化学, 2017, 37, 1991. Yang, H.; Zhang, Y.; Li, Y.; Wang, J.; Li, X.; Song, J.; Zhang, B.; Feng, Y. Chin. J. Org. Chem. 2017, 37, 1991.
-
[35]
Mukherjee, S.; Thilagar, P. Chem. Commun. 2015, 51, 10988. doi: 10.1039/C5CC03114A
-
[36]
Tao, Y.; Yuan, K.; Chen, T.; Xu, P.; Li, H.; Chen, R.; Zheng, C.; Zhang, L.; Huang, W. Adv. Mater. 2014, 26, 7931. doi: 10.1002/adma.v26.47
-
[37]
Chen, X.; Duan, C.; Zhu, X.; You, X.; Raj, S. S. S.; Fun, H.; Wu, J. Mater. Chem. Phys. 2001, 72, 11. doi: 10.1016/S0254-0584(01)00299-1
-
[38]
Xu, B.; Li, W.; He, J.; Wu, S.; Zhu, Q.; Yang, Z.; Wu, Y.; Zhang, Y.; Jin, C.; Lu, P.; Chi, Z.; Liu, S.; Xu, J.; Bryce, M. R. Chem. Sci. 2016, 7, 5307. doi: 10.1039/C6SC01325B
-
[39]
Xu, B.; He, J.; Mu, Y.; Zhu, Q.; Wu, S.; Wang, Y.; Zhang, Y.; Jin, C.; Lo, C.; Chi, Z.; Lien, A.; Liu, S.; Xu, J. Chem. Sci. 2015, 6, 3236. doi: 10.1039/C5SC00466G
-
[40]
Neena, K. K.; Sudhakar, P.; Dipak, K.; Thilagar, P. Chem. Commun. 2017, 53, 3641. doi: 10.1039/C6CC09717K
-
[41]
Hirai, Y.; Nakanishi, T.; Kitagawa, Y.; Fushimi, K.; Seki, T.; Ito, H.; Hasegawa, Y. Angew. Chem., Int. Ed. 2017, 56, 7171. doi: 10.1002/anie.201703638
-
[42]
Eddingsaas, N. C.; Suslick, K. S. J. Am. Chem. Soc. 2007, 129, 6718. doi: 10.1021/ja0716498
-
[43]
Walton, A. J. Adv. Phys. 1977, 26, 887. doi: 10.1080/00018737700101483
-
[44]
Cotton, F. A.; Goodgame, D. M. L.; Goodgame, M. J. Am. Chem. Soc. 1962, 84, 167. doi: 10.1021/ja00861a008
-
[45]
Goodgame, D. M. L.; Cotton, F. A. J. Chem. Soc. 1961, 3735. doi: 10.1039/jr9610003735
-
[46]
Wong, H. Y.; Lo, W. S.; Chan, W. T. K.; Law, G. L. Inorg. Chem. 2017, 56, 5135. doi: 10.1021/acs.inorgchem.7b00273
-
[47]
Nakayama, H.; Nishida, J.; Takada, N.; Sato, H.; Yamashita, Y. Chem. Mater. 2012, 24, 671. doi: 10.1021/cm202650u
-
[48]
Balsamy, S.; Natarajan, P.; Vedalakshmi, R.; Muralidharan, S. Inorg. Chem. 2014, 53, 6054. doi: 10.1021/ic500400y
-
[49]
Fontenot, R. S.; Hollerman, W. A.; Bhat, K. N.; Aggarwal, M. D. J. Lumin. 2013, 134, 477. doi: 10.1016/j.jlumin.2012.07.042
-
[50]
Li, C.; Xu, C. N.; Imai, Y.; Bu, N. Strain 2011, 47, 483. doi: 10.1111/str.2011.47.issue-6
-
[51]
Sakai, K.; Koga, T.; Imai, Y.; Maehara, S.; Xu, C. Phys. Chem. Chem. Phys. 2006, 8, 2819. doi: 10.1039/b604656h
-
[52]
Cheng, Z.; Lin, J. Macromol. Rapid Commun. 2015, 36, 790. doi: 10.1002/marc.201400588
-
[53]
许晓玉, 王蒙, 林琳, 赵斌, 何丹农, 材料导报, 2015, 29, 61. doi: 10.11896/j.issn.1005-023X.2015.01.010Xu, X.; Wang, M.; Lin, L.; Zhao, B.; He, D. Mater. Rev. 2015, 29, 61. doi: 10.11896/j.issn.1005-023X.2015.01.010
-
[54]
Liu, Z.; Lai, B.; Wen, H.; Robbins, J.; Nei, H. Chin. J. Chem. 2016, 34, 1304. doi: 10.1002/cjoc.v34.12
-
[55]
杨智, 林建华, 苏勉曾, 陶冶, 王渭, 化学学报, 2001, 59, 736. doi: 10.3321/j.issn:0567-7351.2001.05.020Yang, Z.; Lin, J.; Su, M.; Tao, Z.; Wang, W. Acta Chim. Sinica 2001, 59, 736. doi: 10.3321/j.issn:0567-7351.2001.05.020
-
[56]
Huang, J.; Hou, B.; Ling, H.; Liu, J.; Yu, X. Inorg. Chem. 2014, 53, 9541. doi: 10.1021/ic500748c
-
[57]
Hurt, C. R.; Mcavoy, N.; Bjorklund, S.; Filipescu, N. N. Nature 1966, 212, 179.
-
[58]
Sweeting, L. M.; Rheingold, A. L. J. Am. Chem. Soc. 2002, 109, 2652. doi: 10.1021/ja00243a017
-
[59]
Fontenot, R. S.; Hollerman, W. A.; Bhat, K. N.; Aggarwal, M. D. J. Lumin. 2012, 132, 1812. doi: 10.1016/j.jlumin.2012.02.027
-
[60]
Fontenot, R. S.; Bhat, K. N.; Hollerman, W. A.; Alapati, T. R.; Aggarwal, M. D. ECS J. Solid State Sci. Technol. 2013, 2, 384. doi: 10.1149/2.030309jss
-
[61]
Fontenot, R. S.; Hollerman, W. A.; Bhat, K. N.; Aggarwal, M. D.; Penn, B. G. Polym. J. 2013, 46, 111.
-
[62]
Chen, X.; Liu, S.; Yu, Z.; Cheung, K.; Ma, J.; Min, N.; You, X. J. Coord. Chem. 1999, 47, 349. doi: 10.1080/00958979908023067
-
[63]
Xiong, R.; You, X. Inorg. Chem. 2002, 5, 677. doi: 10.1016/S1387-7003(02)00519-1
-
[64]
Chen, X.; Liu, S.; Duan, C.; Xu, Y.; You, X. Polyhedron 1998, 17, 1883. doi: 10.1016/S0277-5387(97)00519-6
-
[65]
Takada, N.; Sugiyama, J.; Minami, N.; Hieda, S. Mol. Cryst. Liq. Cryst. 1997, 295, 71. doi: 10.1080/10587259708042799
-
[66]
Takada, N.; Hieda, S.; Sugiyama, J.; Katoh, R.; Minami, N. Synth. Met. 2000, 111, 587.
-
[67]
Takada, N.; Sugiyama, J.; Katoh, R.; Minami, N.; Hieda, S. Synth. Met. 1997, 91, 351. doi: 10.1016/S0379-6779(98)80058-1
-
[68]
Li, D.; Li, C.; Wang, J.; Kang, L.; Wu, T.; Li, Y.; You, X. Eur. J. Inorg. Chem. 2009, 2009, 4844. doi: 10.1002/ejic.v2009:32
-
[69]
Rausch, J.; Lorenz, V.; Hrib, C. G.; Frettloh, V.; Adlung, M.; Wickleder, C.; Hilfert, L.; Jones, P. G.; Edelmann, F. T. Inorg. Chem. 2014, 53, 11662. doi: 10.1021/ic501837x
-
[70]
George, T. M.; Sajan, M. J.; Gopakumar, N.; Reddy, M. L. P. J. Photochem. Photobiol., A 2016, 317, 88. doi: 10.1016/j.jphotochem.2015.11.016
-
[71]
Hasegawa, Y.; Hieda, R.; Miyata, K.; Nakagawa, T.; Kawai, T. Eur. J. Inorg. Chem. 2011, 2011, 4978. doi: 10.1002/ejic.201100688
-
[72]
Hasegawa, Y.; Tateno, S.; Yamamoto, M.; Nakanishi, T.; Kita-gawa, Y.; Seki, T.; Ito, H.; Fushimi, K. Chem.-Eur. J. 2017, 23, 2666. doi: 10.1002/chem.201605054
-
[73]
Biju, S.; Gopakumar, N.; Bunzli, J. C. G.; Scopelliti, R.; Kim, H. K.; Reddy, M. L. P. Inorg. Chem. 2013, 52, 8750. doi: 10.1021/ic400913f
-
[74]
Mikhalyova, E. A.; Yakovenko, A. V.; Zeller, M.; Kiskin, M. A.; Kolomzarov, Y. V.; Eremenko, I. L.; Addison, A. W.; Pavlishchuk, V. V. Inorg. Chem. 2015, 54, 3125. doi: 10.1021/ic502120g
-
[75]
Wu, Z.; Huang, X. Chin. J. Chem. 2016, 34, 703 doi: 10.1002/cjoc.v34.7
-
[76]
Chen, J.; Zhang, Q.; Zheng, F.; Liu, Z.; Wang, S.; Wu, A.; Guo, G. Dalton Trans. 2015, 44, 3289. doi: 10.1039/C4DT03694H
-
[77]
Chandra, B. P.; Jaiswal, A. K.; Cwandraker, T. R.; Kaza, B. R. J. Lumin. 1982, 27, 101. doi: 10.1016/0022-2313(82)90032-1
-
[78]
Chandra, B. P.; Deshmukh, N. G.; Sahu, R. B.; Verma, A. K. Cryst. Res. Technol. 1986, 21, 1559. doi: 10.1002/(ISSN)1521-4079
-
[79]
Kobayashi, A.; Hasegawa, T.; Yoshida, M.; Kato, M. Inorg. Chem. 2016, 55, 1978. doi: 10.1021/acs.inorgchem.5b02160
-
[80]
SchÖnweiz, S.; Sorsche, D.; Schwarz, B.; Rau, S.; Streb, C. Dalton Trans. 2017, 46, 9760. doi: 10.1039/C7DT02316B
-
[81]
Knotter, D. M.; Van Maanen, H. L.; Grove, D. M.; Spek, A. L.; Van Koten, G. Inorg. Chem. 1991, 30, 3309. doi: 10.1021/ic00017a017
-
[82]
Knotter, D. M.; Blasse, G.; Vliet, J. P. M. V.; Koten, G. V. Inorg. Chem. 1992, 31, 2196. doi: 10.1021/ic00037a038
-
[83]
İncel, A.; Varlikli, C.; McMillen, C. D.; Demir, M. M. J. Phys. Chem. C 2017, 121, 11709. doi: 10.1021/acs.jpcc.7b02875
-
[84]
Tseng, C.; Fox, M. A.; Liao, J.; Ku, C.; Sie, Z.; Chang, C.; Wang, J.; Chen, Z.; Lee, G.; Chi, Y. J. Mater. Chem. C 2017, 5, 1420. doi: 10.1039/C6TC05154E
-
[85]
Hsu, C. W.; Ly, K. T.; Lee, W. K.; Wu, C. C.; Wu, L. C.; Lee, J. J.; Lin, T. C.; Liu, S. H.; Chou, P. T.; Lee, G. H.; Chi, Y. ACS Appl. Mater. Interfaces 2016, 8, 33888. doi: 10.1021/acsami.6b12707
-
[86]
Inoue, T.; Tazuke, S. Chem. Lett. 1981, 5, 589.
-
[87]
Nowak, R.; Krajewska, A.; Samoć, M. Chem. Phys. Lett. 1983, 94, 270. doi: 10.1016/0009-2614(83)87085-7
-
[88]
Yang, J.; Gao, X.; Xie, Z.; Gong, Y.; Fang, M.; Peng, Q.; Chi, Z.; Li, Z. Angew. Chem., Int. Ed. 2017, 56, 15299. doi: 10.1002/anie.201708119
-
[89]
Arivazhagan, C.; Maity, A.; Bakthavachalam, K.; Jana, A.; Panigrahi, S. K.; Suresh, E.; Das, A.; Ghosh, S. Chem.-Eur. J. 2017, 23, 7046. doi: 10.1002/chem.201700187
-
[90]
Xie, Y.; Tu, J.; Zhang, T.; Wang, J.; Xie, Z.; Chi, Z.; Peng, Q.; Li, Z. Chem. Commun. 2017, 53, 11330. doi: 10.1039/C7CC04663D
-
[91]
Hardy, G. E.; Kaska, W. C.; Chandra, B. P.; Zink, J. I. J. Am. Chem. Soc. 1981, 103, 1074. doi: 10.1021/ja00395a014
-
[92]
Sweeting, L. M.; Rheingold, A. L. J. Phys. Chem. 1988, 92, 5648. doi: 10.1021/j100331a022
-
[93]
Guo, J.; Li, X.; Nie, H.; Luo, W.; Gan, S.; Hu, S.; Hu, R.; Qin, A.; Zhao, Z.; Su, S.; Tang, B. Adv. Funct. Mater. 2017, 27, 1606458. doi: 10.1002/adfm.v27.13
-
[94]
Yang, J.; Ren, Z.; Xie, Z.; Liu, Y.; Wang, C.; Xie, Y.; Peng, Q.; Xu, B.; Tian, W.; Zhang, F.; Chi, Z.; Li, Q.; Li, Z. Angew. Chem., Int. Ed. 2017, 56, 880. doi: 10.1002/anie.201610453
-
[95]
Clough, J. M.; Creton, C.; Craig, S. L.; Sijbesma, R. P. Adv. Funct. Mater. 2016, 26, 9063. doi: 10.1002/adfm.v26.48
-
[96]
Chen, Y.; Sijbesma, R. P. Macromolecules 2014, 47, 3797. doi: 10.1021/ma500598t
-
[1]
-
图 5 (a, b) 25, 26分子式、(c) 26的ML光谱图(虚线)和PL光谱图(实线)与各自发光现象、(d) 27~29分子式、(e) 27~29的ML现象(左)和27~29三个分子分子间CF3排列的空间填充模型(右)以及(f) n(Tb)/n(Eu)=1 (上)和n(Tb)/n(Eu)=10 (下)时的PL光谱图和ML光谱图(Eu:配合物27)
Figure 5 (a, b) Chemical structures of 25, 26, (c) ML (dashed lines) and PL (solid lines) spectra (PL spectrum is obtained excited at 355 nm) of 26 (Insert: ML images), (d) chemical structures of 27~29 and (e) images of TL (left) and corresponding space filling models (right) on the intermolecular CF3 arrangement in 27, 28 and 29 and (f) PL and ML spectra of n(Tb)/n(Eu)=1 (top) and n(Tb)/n(Eu)=10 (bottom) (Eu: 27)
Reprinted with permission from ref. [41]. Copyright 2017 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim
图 8 (a~c) 46~48配合物的分子式、(d) PMMA、PS、PVDF和PU复合材料的ML发射量与滴数的关系和(e) PU复合材料的ML响应
Figure 8 (a~c) Chemical structures of 46, 47 and 48 complexes, (d) TL emission of the composites prepared by PMMA, PS, PVDF, and PU as a function of the number of drops and (e) TL response of the PU composite
Reprinted with permission from ref. [83]. Copyright 2017 American Chemical Society
图 12 (a) 化合物74~82分子式、(b)化合物82的力致发光产生过程示意图和(c)化合物82力致发光光谱图(插图:在白天用刮刀研磨样品82的发光现象)
Figure 12 (a) Chemical structures of 74~82, (b) the ML production diagram of compound 82 and (c) ML spectra of 82 (Inset: ML image of as-prepared 82 sample upon grinding with a spatula in daylight)
Reprinted with permission from ref. [94]. Copyright 2017 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim
图 13 (a) 机械诱导化学发光(机械作用于1, 2-二氧环丁烷, 断裂形成激发态的1, 2-二氧环丁烷将能量转移给荧光体9, 10-二苯并蒽, 且发射峰在420 nm)、(b)掺杂不同荧光受体的聚合物薄膜拉伸过程中的荧光光谱[插图:薄膜的光学图像变形和相应的受体的化学结构式(从左到右: 9, 10-二苯并蒽, 苝, 4, 7-二噻吩苯并[1, 2, 5]噻重氮和N, N'-二(2, 5-二叔丁基苯基)-3, 4, 9, 10-二甲酰亚胺]、(c) 84的合成路线和(d) 85~87的结构式
Figure 13 (a) The mechano-induced chemoluminescence. 9, 10-diphenylanthracene accepts excitated energy from the mechanically formed excited state adamantanones via fret, then releases energy as fluorescence at 420 nm (Reprinted with permission from ref [95]. Copyright 2016 WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim), (b) luminescence spectra obtained during stretching of films of 81 that with different acceptors [Inserts show the corresponding optical images of the films during deformation and the chemical structures of the acceptors (from left to right: 9, 10-diphenylanthracene, perylene, 4, 7-di(thiophen-2-yl)-benzo[c][1, 2, 5]-thiadiazole and N, N'-bis(2, 5-di-tert-but-ylphenyl)-3, 4, 9, 10-perylene dicarboximide). Reprinted with permission from ref [28]. Copyright 2017 Nature Chemistry], (c) synthetic route of 84 and (d) chemical structures of 85
-

计量
- PDF下载量: 207
- 文章访问数: 7439
- HTML全文浏览量: 2414

 下载:
下载:

 下载:
下载:
 下载:
下载:

