 图 图式1
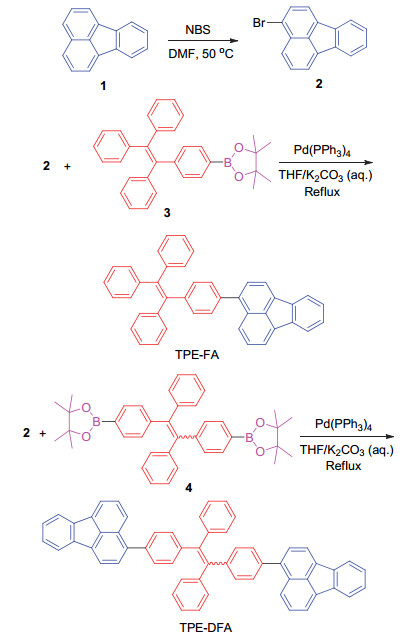
TPE-FA与TPE-DFA的合成路线
Figure 图式1.
Synthetic routes to TPE-FA and TPE-DFA
图 图式1
TPE-FA与TPE-DFA的合成路线
Figure 图式1.
Synthetic routes to TPE-FA and TPE-DFA

Citation: Bai Wei, Shi Yang, Song Chen, He Jie, Qin Anjun, Sun Jing Zhi, Tang Ben Zhong. Fluoranthene-Modified Tetraphenylethene Derivatives: Synthesis, Aggregation-Enhanced Emission Characteristic and Their Highly Sensitive Detection of Picric Acid[J]. Acta Chimica Sinica, 2016, 74(11): 893-901. doi: 10.6023/A16080410

荧蒽修饰的四苯基乙烯衍生物:分子合成、聚集增强荧光特性及其对苦味酸的高灵敏度检测
-
关键词:
- 四苯基乙烯
- / 荧蒽
- / 聚集诱导发光(AIE)
- / 聚集增强荧光(AEE)
- / 苦味酸
English
Fluoranthene-Modified Tetraphenylethene Derivatives: Synthesis, Aggregation-Enhanced Emission Characteristic and Their Highly Sensitive Detection of Picric Acid
-
1 引言
得益于出色的发光效率和丰富的发光颜色等优点, 有机发光功能材料已经被广泛用于化学检测、生物传感与成像、光电转换器件等领域的研究, 展现出巨大的应用前景[1].然而, 在研究和应用中, 目前常用的荧光材料面临不可回避的难题.由于其具有的刚性大π共轭体系, 传统的荧光材料分子在聚集状态下通常会在强的π-π相互作用下形成猝灭荧光的激基缔合物或激基复合物, 显著降低其荧光发光效率[2].这一聚集荧光猝灭(Aggregation-caused quenching, ACQ)现象使这些荧光分子的应用受到了限制.
幸运的是, ACQ并非所有荧光分子的固有性质, 与之截然相反的光物理现象在若干分子体系中被发现, 这一现象被命名为聚集诱导发光(Aggregation-induced emission, AIE)[3].具有AIE性质的分子在稀溶液中不发荧光或者荧光很微弱, 而在聚集时或固态下发射强烈荧光, 其固态荧光量子产率较之溶液有数量级的提高.如果分子在稀溶液中有一定发光, 但聚集时荧光大幅增强, 则被称为聚集增强荧光(Aggregation-enhanced emission, AEE)分子, AEE可看作AIE的特例.AIE现象突破了传统荧光分子在固态使用时面临的困境, 可提高材料的发光性能与检测灵敏度, 故而受到科学界和工业界的极大重视, 成为化学与材料科学研究的热点领域之一.越来越多的化学-生物传感和光电转换器件等领域的研究基于AIE展开[4].研究者提出了多种机理来解释这种光物理行为, 其中分子内运动受限(Restriction of intramolecular motions, RIM)机理得到众多实验事实的支持被广泛采纳[3c, 5].自2001年唐本忠等[3a]首次报道一种多苯环修饰的硅杂环戊二烯(噻咯)衍生物的AIE行为后, 这一领域的研究不断取得新的成果.多个AIE核心分子体系被发现和应用起来, 其中最著名的有四苯基乙烯(TPE)[6]、二苯基乙烯基蒽[7]、四苯基吡嗪[8]、多苯基苯[9]等.由于AIE现象光明的应用前景, 不断地开发和拓展新的AIE体系对于推进AIE领域的发展始终具有极其重大的意义.
基于对RIM机理的理解与认识, 新型AIE分子可被设计出来.增强分子内运动的限制, 核心在于增加分子所处空间的拥挤程度.在这样的思路指导下, 即便共轭体系成线形结构, 如1, 4-对二吡啶基乙炔基苯, 通过成盐反应将两个这样的分子合环, 巨大的空间拥挤程度赋予其分子内运动的阻碍, 也能使其成为AIE分子[10].李振课题组通过在典型的ACQ生色团芘的分子两侧化学键接大位阻的方向取代基(间三联苯、二苯基芴、TPE等), 使分子体积增大, 克服了聚集时芘分子间的π-π相互作用; 而取代基与芘间合适的扭转角和共轭又使其具有AIE特性, 因而构建了以芘为核心的新AIE分子[11].
除此之外, 通过已有的AIE基元改造ACQ分子, 也是构筑新的AIE分子的有效手段.在之前的研究中, 将不同的ACQ生色团与AIE基元共轭键接, 研究者们实现对分子的共轭长度与给受体作用程度的调节, 进而制备得到覆盖全可见光到红外区的不同AIE分子, 它们的荧光量子产率与荧光寿命等性质也各具特色, 在不同领域有各自的优势与潜在价值[12].朱为宏课题组[13]发现一种新AIE生色团喹啉腈(Quinoline-malononitrile, QM), 通过π桥调控QM的D-π-A结构, 修饰给电子性不同的基团, 可实现红光到近红外的荧光发射; 增加π桥结构的柔性, 还可控制聚集体从棒状向球状的转变, 使分子在小鼠体内拥有更好的肿瘤细胞靶向性.
荧蒽(Fluoranthene, FA)是芘的同分异构体, 其可看作蒽与苯通过五元环相连而得到的平板状大π共轭结构.作为一种典型且常见的多环芳香碳氢化合物(Polycyclic aromatic hydrocarbons, PAHs), 荧蒽具有高蓝光发光效率和电子传输性能, 且热稳定性好, 因此荧蒽及其衍生物多被用于有机光电材料与荧光传感材料的研究中[14].其中, 裴坚课题组通过对含酰亚胺结构的荧蒽衍生物进行官能团修饰与结构优化, 得到一系列不同带隙的荧蒽分子, 这些分子在有机本体异质结太阳能电池中可充当受体, 替代富勒烯, 这样的器件也能实现高的能量转换效率和高的开路电压[14b, c].而在化学传感领域, 荧蒽及其衍生物常用于对缺电子分子(如多硝基苯类的爆炸物)的微量或痕量检测.Kaner等[15]对荧蒽进行三价铁催化下的环聚和, 得到含五个荧蒽的大环状化合物, 这样的分子对2, 4, 6-三硝基苯酚的响应猝灭常数可达104 L/mol量级.而基于单荧蒽基元的小分子荧光探针对爆炸物也具有较好的检测效果[16].总之, 荧蒽及其衍生物由于出色的性能引起了广泛的关注.
将典型具有ACQ性质的荧蒽与AIE生色团共轭键接, 可望得到荧蒽修饰的AIE分子, 使荧蒽的富电子性与AIE分子的高聚集体发光强强联合.Patil等[17]已经成功通过Diels-Alder反应得到了四个二苯基荧蒽修饰的TPE衍生物TFPE, 这个分子在四氢呋喃(THF)与水的混合溶剂体系中体现出聚集荧光增强蓝移性能, 荧光量子产率达39.4%, 将其用于溶液中爆炸物的检测, 效果良好.然而, TFPE的制备须在210 ℃的高温下进行, 反应条件苛刻.这里, 我们报道通过条件更加温和的Suzuki-Miyaura偶联反应合成的荧蒽修饰的TPE衍生物, 分别为单荧蒽修饰的TPE衍生物(TPE-FA)与双荧蒽修饰的TPE衍生物(TPE-DFA), 这两个分子具有典型的AIE特性, 而且研究发现这两个分子在THF与水的混合溶剂体系中对强缺电子的爆炸物模型分子苦味酸(Picric acid, PA)具有良好的响应性, 检测限达1 μg·g-1.
2 结果与讨论
2.1 TPE-FA与TPE-DFA的制备
TPE-FA与TPE-DFA的合成路线见Scheme 1.荧蒽与N-溴代丁二酰亚胺(NBS)直接溴化得到3-溴代荧蒽(分子2), 此分子2分别与单硼酸酯和双硼酸酯修饰的TPE衍生物在Pd (PPh3)4与K2CO3的催化下通过简单的Suzuki-Miyaura偶联反应, 成功制备得到TPE-FA与TPE-DFA.TPE-FA为淡黄色粉末, TPE-DFA为黄色粉末.它们的分子结构均通过核磁共振波谱与高分辨质谱测试的确认.
值得注意的是, 对于稠环芳烃类化合物, 其芳环上的氢在核磁共振氢谱上均集中在低场区域, 因此3-溴代荧蒽的分子结构难以精确认定.而NBS溴化的位点选择性并不突出, 得到的产物纯度较为有限, 为我们判定溴的取代位点带来了困难.因此在研究中, 我们通过进一步对分子2进行Sonogashira偶联反应, 接上三甲基硅基炔基, 得到分子5.对其二维核磁COSY、HMQC、HMBC, 以及单晶结构(CCDC 1499072)进行分析, 最终确定取代位点为3-位, 进而确定分子2为3-溴代荧蒽.相关合成步骤与表征数据见辅助信息.
2.2 TPE-FA与TPE-DFA的光物理性能
通过对两个目标分子的结构表征并确认得到预期产物后, 我们对其光物理性能进行了研究.首先考察它们在THF稀溶液中的紫外-可见吸收光谱, 如图 1A所示.为进行数据的比较, 我们对数据进行了归一化处理.TPE-FA与TPE-DFA分别在370 nm与372 nm出现一个明显的吸收峰, 代表分子的π-π*跃迁的吸收.虽然两个分子的荧蒽取代数目不同, 但是取代数目带来的共轭长度变化, 并没有给它们的吸收光谱带来巨大变化, 共轭的增长只引起了2 nm的光谱红移.接下来的荧光性能研究中, 我们采用370 nm作为激发波长进行测试.
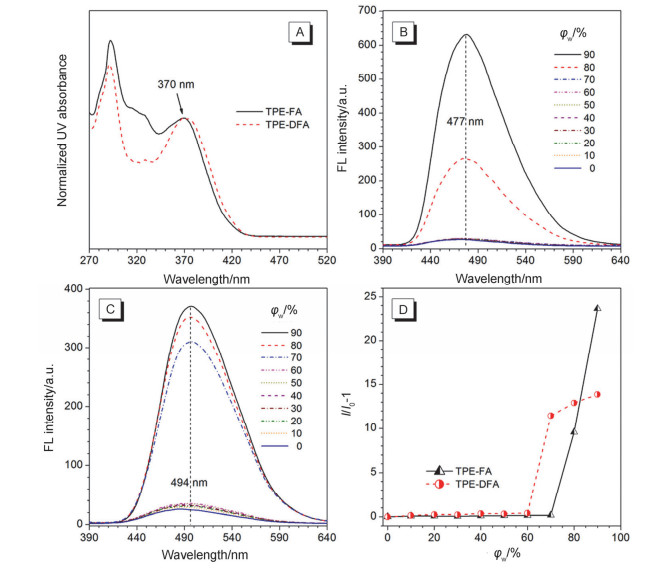 图 1
A)归一化后的TPE-FA与TPE-DFA的THF溶液的紫外-可见吸收光谱. (B)和(C)分别为TPE-FA和TPE-DFA在不同水含量的THF/水混合溶剂中的荧光发射光谱. (D) TPE-FA与TPE-DFA的荧光增强程度随水含量变化的曲线. [TPE-FA]=[TPE-DFA]=10-5 mol/L, 两个分子的荧光测试中λex=370 nm
Figure 1.
(A) Normalized UV-vis absorption spectra of TPE-FA and TPE-DFA in THF solution. (B) and (C) Fluorescence (FL) emission spectra of TPE-FA and TPE-DFA in THF/water mixtures with different water fractions, respectively. (D) Plots of the emission enhancements of TPE-FA and TPE-DFA in accordance with various water fractions in the THF/water mixtures. [TPE-FA]=[TPE-DFA]=10-5 mol/L. λex=370 nm for all the measurements
图 1
A)归一化后的TPE-FA与TPE-DFA的THF溶液的紫外-可见吸收光谱. (B)和(C)分别为TPE-FA和TPE-DFA在不同水含量的THF/水混合溶剂中的荧光发射光谱. (D) TPE-FA与TPE-DFA的荧光增强程度随水含量变化的曲线. [TPE-FA]=[TPE-DFA]=10-5 mol/L, 两个分子的荧光测试中λex=370 nm
Figure 1.
(A) Normalized UV-vis absorption spectra of TPE-FA and TPE-DFA in THF solution. (B) and (C) Fluorescence (FL) emission spectra of TPE-FA and TPE-DFA in THF/water mixtures with different water fractions, respectively. (D) Plots of the emission enhancements of TPE-FA and TPE-DFA in accordance with various water fractions in the THF/water mixtures. [TPE-FA]=[TPE-DFA]=10-5 mol/L. λex=370 nm for all the measurements
为验证TPE-FA和TPE-DFA是否具有AIE特性, 我们测试了这两个分子在THF与水的混合溶剂体系中的荧光发射光谱, 待测物浓度为10 μmol/L, 所得的TPE-FA与TPE-DFA的荧光发射光谱测试结果见图 1B和1C.在THF与水的混合溶剂体系中, 在不良溶剂水的体积含量(φw)低于70%的条件下, TPE-FA的荧光发光谱线大体上平坦, 只在477 nm附近有一个小峰, 且此峰的强度不随水含量增加而变化; 然而, 当水含量提升到80%后, 荧光强度出现突变, 477 nm处的荧光强度明显增加, 水含量进一步上升到90%, 荧光强度与THF溶液中相比增强23倍(图 1D).TPE-FA的荧光强度在水的体积含量达到80%时急剧提高, 此时体系中的TPE-FA在不良溶剂的诱导下形成聚集体, 发出强烈的荧光, 这种现象为典型的聚集诱导发光现象.考虑到在THF溶液中TPE-FA就有弱的荧光, 分子聚集带来荧光的大幅度增强, 故而TPE-FA为具有聚集增强荧光(AEE)性质的分子.TPE-DFA的荧光发光行为与TPE-FA类似, 体现出AEE特性, 最大发射波长为494 nm, 当水体积含量为90%时, 荧光强度比在THF溶液中增强14倍.与TPE-FA略有不同的是, 当水含量达到70%, 体系即出现荧光增强, 这是因为TPE-DFA的溶解性较之TPE-FA略低.水含量高于70%后, TPE-DFA体系荧光上升趋缓, 则是由于部分荧光分子沉淀出来, 分子的吸收有所下降(图S13).
由于两个分子均不具有明显的给受体性质, 所以分子偶极矩受溶剂极性的影响微弱, 因此强极性的水的体积含量变化对体系荧光的光谱移动没有影响, 两个分子的体系发光在不同水含量的条件下不出现红移或蓝移, 具有良好的环境稳定性.相较于紫外-可见吸收光谱, 荧光发射光谱对于分子的共轭长度等因素响应更加敏感, TPE-DFA的荧光发射波长比TPE-FA的红移17 nm, 这是共轭体系增大引起的.
除了荧光发射光谱外, TPE-FA与TPE-DFA在THF和水混合溶剂中的荧光量子产率(Quantum yield, QY)测试结果也清晰地体现出它们的聚集诱导发光增强行为.TPE-FA与TPE-DFA的荧光量子产率随水体积含量变化的曲线见图 2, 其趋势均与荧光强度曲线相似.TPE-FA的THF溶液与聚集体(φw=90%)的荧光量子产率分别为1.9%与12.5%;TPE-DFA在相同的两个条件下的荧光量子产率则分别为1.5%与24.0%.聚集体的QY均比溶液提高了一个数量级, 与荧光测试结果一致.
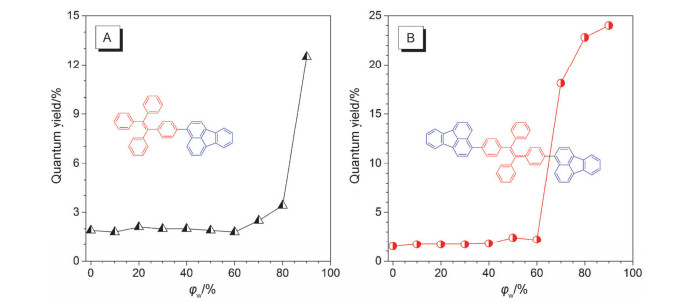 图 2
(A) TPE-FA的荧光量子产率随混合溶剂中水含量变化的曲线. (B) TPE-DFA的荧光量子产率随混合溶剂中水含量变化的曲线.溶质浓度: [TPE-FA]=[TPE-DFA]=10-5 mol/L, 激发波长: λex=370 nm
Figure 2.
(A) Plot of QY of TPE-FA in accordance with various water fractions in the THF/water mixtures. (B) Plot of QY of TPE-DFA in accordance with various water fractions in the THF/water mixtures. Concentration: [TPE-FA]=[TPE-DFA]=10-5 mol/L. λex=370 nm
图 2
(A) TPE-FA的荧光量子产率随混合溶剂中水含量变化的曲线. (B) TPE-DFA的荧光量子产率随混合溶剂中水含量变化的曲线.溶质浓度: [TPE-FA]=[TPE-DFA]=10-5 mol/L, 激发波长: λex=370 nm
Figure 2.
(A) Plot of QY of TPE-FA in accordance with various water fractions in the THF/water mixtures. (B) Plot of QY of TPE-DFA in accordance with various water fractions in the THF/water mixtures. Concentration: [TPE-FA]=[TPE-DFA]=10-5 mol/L. λex=370 nm
为进一步分析两个分子的光物理行为, 我们通过测试瞬态发射光谱研究了两个分子的荧光寿命.TPE-FA与TPE-DFA在THF溶液与THF/水混合溶剂中的荧光寿命见表 1(荧光寿命曲线见图S14).可以发现两个分子在溶液中的荧光寿命都非常短, 分别为0.87 ns与0.61 ns; 而在分子聚集时, TPE-FA和TPE-DFA两个分子的荧光寿命都有所增长, 荧光寿命分别为5.94 ns与2.09 ns, 这与它们由溶液中分散到聚集的荧光量子效率增大的变化趋势是一致的.除了两分子化学结构上的荧蒽取代数目的差异外, 分子聚集体的聚集形态和组织结构也可能存在很大区别, 另外双荧蒽取代造成分子可旋转组分增加, 这些因素综合作用, 使得尽管TPE-FA的荧光寿命较TPE-DFA长, 但荧光量子产率却低些.
Compound τ1/ns τ2/ns < τ > /ns χ2 TPE-FA Solutionb 0.31 (84%) 3.91 (15%) 0.87 1.24 Aggregate 3.89 (31%) 6.84 (69%) 5.94 1.19 TPE-DFA Solution 0.21 (91%) 4.65 (9%) 0.61 0.99 Aggregate 1.33 (61%) 3.27 (39%) 2.09 1.01 a The fluorescence lifetime results are recorded by an Edinburgh Instrument FLS920 Transient/Steady State Photoluminescence Spectrometer. The samples are excited by a 405-nm picosecond laser; b Results of solutions are measured in THF, and those of aggregates are measured in THF/water mixtures (THF/water=10/90 by volume). 表 1 TPE-FA与TPE-DFA的荧光寿命a
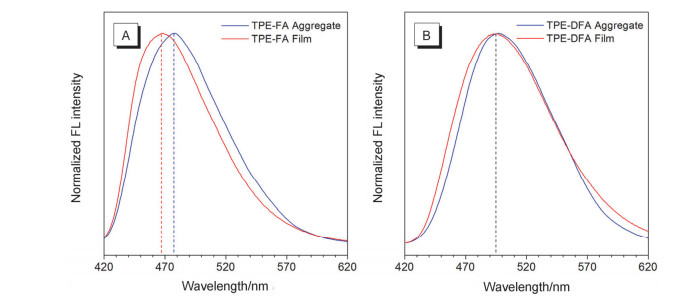
Table 1. Lifetime results of TPE-FA and TPE-DFAa在此基础上, 我们对两个分子的混合溶剂中的聚集体与固体薄膜的发光行为进行了对比研究.固体薄膜是通过旋涂法制备的, 配制浓度为10-3 mol/L的THF母液, 在干净的石英片上滴三滴母液, 在常温常压下进行低速旋涂(200 r/min, 10 s; 1000 r/min, 15 s), 溶剂挥发得到固体薄膜.根据归一化的荧光发射光谱(见图 3), 我们可发现TPE-FA的聚集体发射波长位于477 nm, 而固体薄膜的发射波长较之蓝移10 nm, 位于467 nm; TPE-DFA的聚集体与固体薄膜的发射波长则均位于494 nm.造成这种光谱差异的原因可能来源于两种分子在两个条件下聚集形态的差异.我们猜测, TPE-FA的固体薄膜可能形成分子更扭曲的聚集结构, 发射光谱蓝移.而TPE-DFA分子量较大且存在顺反异构体, 在旋涂成膜过程中结晶程度可能较低, 固体薄膜与混合溶剂的聚集体的聚集形态差异性小, 发光光谱的差异性也较小.结合荧光量子产率测试(如表 2所示), TPE-FA的聚集体量子产率最高测得12.5%, 而固体薄膜的量子产率则高达74.1%;相较而言, TPE-DFA的聚集体量子产率最高测得24.0%, 固体薄膜的量子产率并未大幅度提高, 为40.4%.这些结果说明, 对于AIE/AEE分子体系而言, 除了必要的分子内运动限制, 优化的分子堆积与排列, 有利于更大程度地提高分子的荧光量子产率.
Compound λem, aga/nm Φagb/% λem, fm/nm Φfm/% TPE-FA 477 12.5 467 74.1 TPE-DFA 494 24.0 494 40.4 a ag represents the aggregates (THF/water=10/90 by volume), fm represents the film; b The fluorescence quantum yields are measured by a Hamamatsu Absolute Quantum Yield Spectrometer. 表 2 两种分子在不同状态下的发射波长与荧光量子产率
Table 2. Emission wavelength and QY of the two compounds2.3 TPE-FA与TPE-DFA电子结构的理论模拟
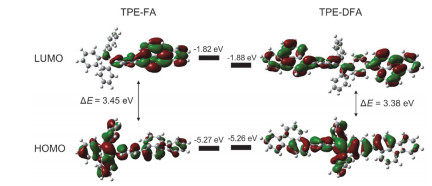
为更好地理解两个分子结构对其光物理行为的影响, 我们借助Gaussian软件的理论计算对分子构型进行优化, 并对其基态与激发态电子云分布和能级情况进行分析, 所用计算方法为基态下的DFT/B3LYP/6-31G (d).TPE-DFA存在顺式与反式结构, 经过理论模拟, 我们发现两种构型的最高占有轨道(HOMO)与最低未占有轨道(LUMO)能级与电子云分布差异均不大, 下面的讨论中反式的情况为代表, 顺式的理论模拟结果见辅助信息(图S15).
分析能量最低条件下得到的分子构型可见, 在两个分子中, 荧蒽与键接的TPE的苯环的二面角均在48.5°左右, 差异不大, 这说明两个分子中荧蒽与键接的苯环的共平面性较弱.同时, 荧蒽对TPE中心的乙烯基连接的苯环间的二面角影响也不大, 均在49°左右, 这说明荧蒽的取代也对TPE核的分子内运动扰动不大.因而在这两个分子中, TPE上的苯环与荧蒽均可被看作转子, 在溶液中分子内运动容易, 而聚集时由于分子间相互靠近, 空间拥挤, 构象变化受到限制, 处于激发态的能量通过振动耗散的途径就受到抑制, 体现聚集荧光增强的效应.
在最优构型的基础上计算两个分子的HOMO与LUMO能级(见图 4), TPE-FA的HOMO能级电子云分布于TPE与荧蒽上, 相对集中于TPE, 而其LUMO能级电子云则集中分布于荧蒽及与其键接的苯环上, TPE的其余部分电子云分布少.反式的TPE-DFA的HOMO与LUMO电子云分布情况与TPE-FA基本一致.两个分子的HOMO与LUMO都没有明显的电子云分离的情况, 这一结果是对TPE-FA与TPE-DFA分子的荧光发射光谱不具有溶剂极性响应的证明.另外, 计算得到, TPE-FA的HOMO与LUMO的能级差为3.45 eV, 反式的TPE-DFA的能级差为3.38 eV, TPE-FA的能级差略大, 在紫外-可见吸收光谱上体现为吸收峰的微弱蓝移.
2.4 TPE-FA与TPE-DFA对PA的检测
两个分子均为富电子体系, 且荧光量子产率较高, 可期望用于与缺电子分子相互作用, 通过激发态的光致电荷转移引起的荧光猝灭来实现对缺电子分子的荧光检测.含有多硝基的芳烃分子具有高度爆炸性, 如2, 4, 6-三硝基甲苯俗称TNT, 为威力巨大的爆炸物, 同时这类爆炸物具有强缺电子性, 因此TPE-FA与TPE-DFA可望用于这类分子的检测.这里, 我们以相似结构的苦味酸(PA)模型检测目标分子, 在THF与水的混合体系中对其进行荧光检测, TPE-FA与TPE-DFA的PA检测结果见图 5.
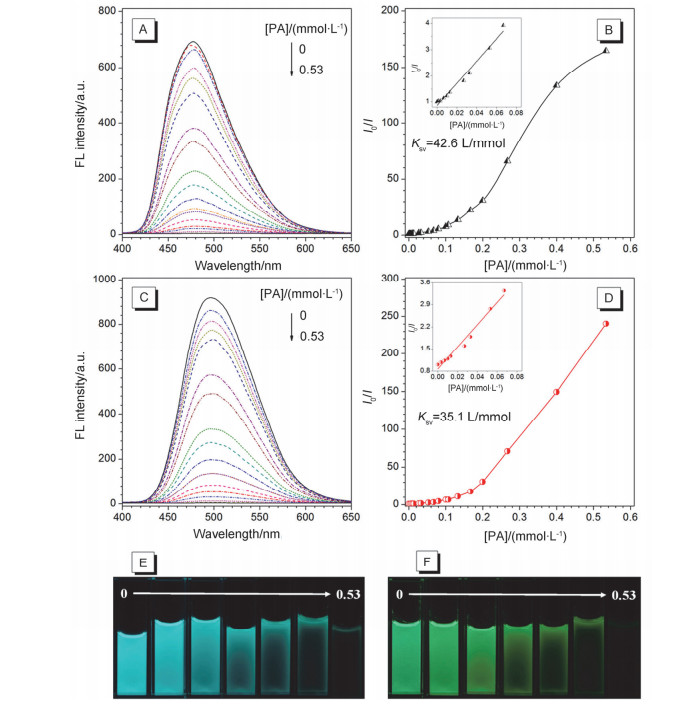 图 5
(A) TPE-FA在含不同浓度PA的THF/水混合溶液(水体积含量90%)中的荧光发射光谱. (B) TPE-FA在含不同浓度PA的混合溶液中的荧光猝灭曲线(发射波长477 nm). (C) TPE-DFA在含不同浓度PA的THF/水混合溶液(水体积含量90%)中的荧光发射光谱. (D) TPE-DFA在含不同浓度PA的混合溶液中的荧光猝灭曲线(发射波长494 nm). (E)与(F) TPE-FA与TPE-DFA的荧光猝灭的照片. [TPE-DFA]=10-5 mol/L.光谱测试λex=370 nm.荧光照片λex=365 nm
Figure 5.
(A) FL emission spectra of TPE-FA in THF/water mixtures (φw=90%) with different [PA]. (B) Plots of fluorescence quenching at 477 nm of TPE-FA in accordance with [PA] in THF/water mixtures. (C) FL emission spectra of TPE-DFA in THF/water mixtures (φw=90%) with different [PA]. (D) Plots of fluorescence quenching at 494 nm of TPE-DFA in accordance with [PA] in THF/water mixtures. (E) and (F) Digital images of fluorescence quenching of TPE-FA and TPE-DFA with different [PA] in THF/water mixtures. [TPE-DFA]=10-5 mol/L. λex=370 nm for FL spectroscopy. λex=365 nm for photos taken
图 5
(A) TPE-FA在含不同浓度PA的THF/水混合溶液(水体积含量90%)中的荧光发射光谱. (B) TPE-FA在含不同浓度PA的混合溶液中的荧光猝灭曲线(发射波长477 nm). (C) TPE-DFA在含不同浓度PA的THF/水混合溶液(水体积含量90%)中的荧光发射光谱. (D) TPE-DFA在含不同浓度PA的混合溶液中的荧光猝灭曲线(发射波长494 nm). (E)与(F) TPE-FA与TPE-DFA的荧光猝灭的照片. [TPE-DFA]=10-5 mol/L.光谱测试λex=370 nm.荧光照片λex=365 nm
Figure 5.
(A) FL emission spectra of TPE-FA in THF/water mixtures (φw=90%) with different [PA]. (B) Plots of fluorescence quenching at 477 nm of TPE-FA in accordance with [PA] in THF/water mixtures. (C) FL emission spectra of TPE-DFA in THF/water mixtures (φw=90%) with different [PA]. (D) Plots of fluorescence quenching at 494 nm of TPE-DFA in accordance with [PA] in THF/water mixtures. (E) and (F) Digital images of fluorescence quenching of TPE-FA and TPE-DFA with different [PA] in THF/water mixtures. [TPE-DFA]=10-5 mol/L. λex=370 nm for FL spectroscopy. λex=365 nm for photos taken
图 1中的荧光发射光谱测试结果显示, 在水体积含量为90%的混合溶剂中, 两个分子的发光强度均为最强, 且在这样的测试条件下, 有机溶剂比例小, 对于检测水中的微量PA具有较强的现实意义, 故我们选定以下测试条件:两个荧蒽修饰的TPE衍生物的测试浓度均为10 μmol/L, THF/水的体积比例为10/90, 调节不同的PA浓度, 测试370 nm激发波长下的荧光发射光谱.由于PA与TPE衍生物产生相互作用, 会猝灭TPE衍生物的聚集体的荧光, 因而提高PA的浓度, 体系荧光下降应越显著.图 5中实验结果显示, 两个体系对于PA均有响应.基于TPE-FA的检测体系的荧光强度对于PA有浓度依赖性, 在测试浓度范围(0~530 μmol/L)内, PA浓度增大, 体系荧光减弱.以PA浓度为横坐标, 以荧光猝灭比例(I0/I)为纵坐标作图, 其中I0为不加PA的体系荧光强度, I为加PA的体系荧光强度.我们可观察到, 当PA浓度低于80 μmol/L时, I0/I与PA浓度呈线性关系, 浓度继续增大, 则偏离线性, 曲线切线斜率增大, 这部分区域体现出荧光猝灭检测的放大效应, 是由于PA浓度过高, PA与荧光分子间相互作用不满足稀溶液的条件所致.在荧光猝灭的线性区间内, PA对荧光分子的猝灭效率可以根据Stern-Volmer方程来评价, 方程的表达式为I0/I=KSV[PA]+1, 其中KSV为Stern-Volmer常数, 即荧光猝灭常数.通过计算, 我们可得出TPE-FA在测试条件下的荧光猝灭常数为4.26×104 L·mol-1.同样地, 基于TPE-DFA的检测体系的荧光猝灭比例在PA浓度80 μmol/L以下亦满足Stern-Volmer方程, 得到猝灭常数为3.51×104 L·mol-1.两个分子对于PA的猝灭常数差异不大, 与Patil课题组用TFPE检测得到的猝灭常数在同一数量级, 在PA浓度较低时体现出对PA优良的检测灵敏度.由图 5E和F可见, 检测结果可以直观而清晰地通过荧光照片展示出来.
在检测限方面, 为满足荧光强度测试信号为噪音三倍以上的要求, TPE-FA可检出的最低PA浓度为1.3 μmol/L, TPE-DFA可检出的最低PA浓度为3.3 μmol/L, 折算成质量分数, TPE-FA与TPE-DFA的检测限分别低至0.3 μg·g-1与0.8 μg·g-1.综上, 我们制备的两个TPE衍生物TPE-FA与TPE-DFA均对PA有良好的荧光检测效果, 在PA浓度低于80 μmol/L的条件下, 荧光猝灭常数KSV分别可达4.26×104 L·mol-1与3.51×104 L·mol-1, 且最低PA检出浓度分别低至0.3与0.8 μg·g-1.
如前所述, 我们推测用TPE-FA和TPE-DFA检测PA的原理是荧光分子与苦味酸分子之间的光致电子转移.通常情况下, 两者之间存在能量转移与电荷转移.比较PA的紫外-可见吸收光谱与两个探针分子的荧光发光光谱(图S16)可发现TPE-FA或TPE-DFA的发射光谱与PA的吸收光谱的交叠区域均较小, 交叉的交点并未达到各自谱图的半峰宽的波长处, 这意味着PA与探
针间的能量转移效率很低, 不是荧光猝灭的主因.两个TPE衍生物的荧光猝灭常数相差无几, 且不受谱图中交叠面积差异的影响.在猝灭原理上, 一般认为此时发生了富电子与缺电子的分子间的电子转移, 从而实现荧光猝灭[17, 18].加入PA测试两个分子的荧光寿命的实验结果(表S6)表明, PA对TPE-FA与TPE-DFA的荧光猝灭更加符合静态猝灭模型, 但猝灭过程依然应认为是静态猝灭与动态猝灭共同作用的结果.
3 结论
我们通过条件较为温和的Suzuki-Miyaura偶联反应制备得到了单荧蒽修饰的TPE衍生物TPE-FA与双荧蒽修饰的TPE衍生物TPE-DFA, 成功用TPE这一AIE生色团改造了荧蒽这种典型的ACQ生色团.TPE-FA和TPE-DFA皆具有典型的AEE特性, 聚集体的发光波长分别位于477与494 nm, 荧光量子产率分别为12.5%和24.0%, 而其薄膜量子产率更高达74.1%和40.4%.通过量子化学计算给出的能级结构为其光物理行为的分析提供了有力的理论依据.TPE-FA与TPE-DFA可有效用于PA溶液的荧光检测, 猝灭常数达到4×104 L·mol-1以上, 检出限则均低于1 μg·g-1.该研究拓展了AIE分子体系, 所得产物有望用于实际爆炸物和其它缺电子分子体系的荧光检测.
4 实验部分
3-溴代荧蒽(分子2)的合成见辅助信息, 单硼酸酯与双硼酸酯修饰的TPE衍生物的合成见参考文献.分子表征与其它补充数据见参考文献.
1-(4-(3-荧蒽基)苯基)-1, 2, 2-三苯乙烯(TPE-FA)的合成.在100 mL双口瓶中加入分子2(281 mg, 1 mmol)、分子3(458 mg, 1 mmol)、Pd (PPh3)4(46 mg, 0.04 mmol), 抽真空换氮气三次, 用注射器加入除水除氧的THF (10 mL), 然后用注射器加入K2CO3水溶液(2 mol/L, 5 mL).随后在氮气保护下回流搅拌24 h.反应完成后, 停止加热, 待体系回到室温, 加入稀盐酸(10 mL)终止反应, 用二氯甲烷萃取三次, 收集有机相, 将有机相旋干, 所得粗产物经硅胶柱色谱分离, 淋洗剂为V(PE):V(DCM)=30:1, 得到的产物在PE与THF中重结晶, 最终得到淡黄色粉末状固体, 产率为18.8%.1H NMR (400 MHz, CDCl3)δ: 7.97~7.87(m, 4H), 7.85(d, J=8.4 Hz, 1H), 7.64~7.53(m, 2H), 7.40~7.35(m, 2H), 7.33(d, J=8.2 Hz, 2H), 7.20~7.02(m, 17H); 13C NMR (100 MHz, CDCl3)δ: 143.79, 143.75, 143.70, 142.90, 141.41, 140.64, 140.08, 139.56, 139.14, 137.74, 137.08, 136.19, 132.75, 131.49, 131.48, 131.41, 131.38, 129.62, 128.53, 128.37, 128.01, 127.80, 127.72, 127.60, 127.46, 126.61, 126.59, 126.53, 125.70, 121.51, 121.44, 120.05, 120.01.HRMS (MALDI-TOF, m/z) calcd for C42H28 [M+] 532.2186, found 532.2152.
1, 2-二(4-(3-荧蒽基)苯基)-1, 2-二苯乙烯(TPE-DFA)的合成.合成的操作步骤与TPE-FA的完全一样, 只需将分子3换为分子4, 并进行相应的化学计量比的调整即可.柱色谱分离的淋洗剂为V(PE):V(DCM)=10:1.得到的产物在PE与THF中重结晶, 最终得到黄色粉末状固体, 产率为31.7%.1H NMR (400 MHz, CDCl3)δ: 7.97~7.85(m, 10H), 7.66~7.43(m, 5H), 7.43~7.31(m, 6H), 7.31~7.10(m, 15H); 13C NMR (100 MHz, CDCl3)δ: 143.75, 143.55, 143.04, 142.89, 141.15, 141.06, 140.05, 139.56, 139.14, 137.92, 137.82, 137.09, 136.24, 132.76, 132.04, 131.62, 131.52, 131.44, 129.72, 129.66, 128.56, 128.38, 128.11, 128.03, 127.92, 127.86, 127.61, 127.48, 126.71, 126.39, 125.62, 121.53, 121.46, 120.07, 120.04.HRMS (MALDI-TOF, m/z) calcd for C58H36 [M+] 732.2812, found 732.2840.
-
-
[1]
Basabe-Desmonts, L.; Reinhoudt, D. N.; Crego-Calama, M. Chem. Soc. Rev. 2007, 36, 993; (b) Bao, Y.; Wang, T.; Li, Q.; Du, F.; Bai, R.; Smet, M.; Dehaen, W. Polym. Chem. 2014, 5, 792; (c) Yuan, L.; Lin, W.; Zheng, K.; He, L.; Huang, W. Chem. Soc. Rev. 2013, 42, 622; (d) Dias, F. B.; Bourdakos, K. N.; Jankus, V.; Moss, K. C.; Kamtekar, K. T.; Bhalla, V.; Santos, J.; Bryce, M. R.; Monkman, A. P. Adv. Mater. 2013, 25, 3707; (e) Li, W.; Pan, Y.; Xiao, R.; Peng, Q.; Zhang, S.; Ma, D.; Li, F.; Shen, F.; Wang, Y.; Yang, B.; Ma, Y. Adv. Funct. Mater. 2014, 24, 1609; (f) Zhang, Q.; Tsang, D.; Kuwabara, H.; Hatae, Y.; Li, B.; Takahashi, T.; Lee, S. Y.; Yasuda, T.; Adachi, C. Adv. Mater. 2015, 27, 2096.
-
[2]
Birks, J. B. Photophysics of Aromatic Molecules, Wiley, London, 1970. http://www.mendeley.com/research/photophysics-aromatic-moleculesa-postscript-5/
-
[3]
Luo, J.; Xie, Z.; Lam, J. W. Y.; Cheng, L.; Chen, H.; Qiu, C.; Kwok, H. S.; Zhan, X.; Liu, Y.; Zhu, D.; Tang, B. Z. Chem. Commun. 2001, 37, 1740; (b) Mei, J.; Hong, Y.; Lam, J. W. Y.; Qin, A.; Tang, Y.; Tang, B. Z. Adv. Mater. 2014, 26, 5429; (c) Mei, J.; Leung, N. L. C.; Kwok, R. T. K.; Lam, J. W. Y.; Tang, B. Z. Chem. Rev. 2015, 115, 11718; (d) Wang, H.; Zhao, E.; Lam, J. W. Y.; Tang, B. Z. Mater. Today 2015, 18, 365.
-
[4]
Wang, M.; Zhang, G.; Zhang, D.; Zhu, D.; Tang, B. Z. J. Mater. Chem. 2010, 20, 1858; (b) Liang, J.; Tang, B. Z.; Liu, B. Chem. Soc. Rev. 2015, 44, 2798; (c) Zhang, X.; Wang, K.; Liu, M.; Zhang, X.; Tao, L.; Chen, Y.; Wei, Y. Nanoscale 2015, 7, 11486; (d) Dong, Y. Q.; Lam, J. W. Y.; Tang, B. Z. J. Phys. Chem. Lett. 2015, 6, 3429; (e) Yang, J.; Huang, J.; Li, Q.; Li, Z. J. Mater. Chem. C 2016, 4, 2663.
-
[5]
Tseng, N.-W.; Liu, J.; Ng, J. C. Y.; Lam, J. W. Y.; Sung, H. H. Y.; Williams, I. D.; Tang, B. Z. Chem. Sci. 2012, 3, 493; (b) Liang, G.; Lam, J. W. Y.; Qin, W.; Li, J.; Xie, N.; Tang, B. Z. Chem. Commun. 2014, 50, 1725; (c) Parrot, E. P. J.; Tan, N. Y.; Hu, R.; Zeitler, J. A.; Tang, B. Z.; Pickwell-MacPherson, E. Mater. Horiz. 2014, 1, 251; (d) Yuan, H.; Wang, K.; Yang, K.; Liu, B.; Zou, B. J. Phys. Chem. Lett. 2014, 5, 2968; (e) Sun, G.; Zhao, Y.; Liang, W. J. Chem. Theory Comput. 2015, 11, 2257.
-
[6]
Zhao, Z.; Lam, J. W. Y.; Tang, B. Z. J. Mater. Chem. 2012, 22, 23726; (b) Wang, J.; Mei, J.; Hu, R.; Sun, J. Z.; Qin, A.; Tang, B. Z. J. Am. Chem. Soc. 2012, 134, 9956; (c) Bai, W.; Wang, Z.; Tong, J.; Mei, J.; Qin, A.; Sun, J. Z.; Tang, B. Z. Chem. Commun. 2015, 51, 1089; (d) Chen, S.; Hong, Y.; Zeng, Y.; Sun, Q.; Liu, Y.; Zhao, E.; Bai, G.; Qu, J.; Hao, J.; Tang, B. Z. Chem. Eur. J. 2015, 21, 4315; (e) Wang, C.; Xu, B.; Li, M.; Chi, Z.; Xie, Y.; Li, Q.; Li, Z. Mater. Horiz. 2016, 3, 220.
-
[7]
He, J.; Xu, B.; Chen, F.; Xia, H.; Li, K.; Ye, L.; Tian, W. J. Phys. Chem. C 2009, 113, 9892; (b) Lu, H.; Xu, B.; Dong, Y.; Chen, F.; Li, Y.; Li, Z.; He, J.; Li, H.; Tian, W. Langmuir 2010, 26, 6838; (c) Chen, J. L.; Ma, S. Q.; Xu, B.; Zhang, J. B.; Dong, Y. J.; Tian, W. J. Chin. Sci. Bull. 2013, 58, 2747.
-
[8]
Chen, M.; Li, L.; Nie, H.; Tong, J.; Yan, L.; Xu, B.; Sun, J. Z.; Tian, W.; Zhao, Z.; Qin, A.; Tang, B. Z. Chem. Sci. 2015, 6, 1932; (b) Chen, M.; Li, L.; Nie, H.; Shi, Y.; Mei, J.; Wang, J.; Sun, J. Z.; Qin, A.; Tang, B. Z. Chem. Commun. 2015, 51, 10710; (c) Pan, L. X.; Luo, W. W.; Chen, M.; Liu, J. K.; Xu, L.; Hu, R. R.; Zhao, Z. J.; Qin, A. J.; Tang, B. Z. Chin. J. Org. Chem. 2016, 36, 1316(in Chinese). (潘凌翔, 罗文文, 陈明, 刘峻恺, 徐露, 胡蓉蓉, 赵祖金, 秦安军, 唐本忠, 有机化学, 2016, 36, 1316.)
-
[9]
Hu, R.; Lam, J. W. Y.; Liu, Y.; Zhang, X.; Tang, B. Z. Chem. Eur. J. 2013, 19, 5617; (b) Li, L.; Chen, M.; Zhang, H.; Nie, H.; Sun, J. Z.; Qin, A.; Tang, B. Z. Chem. Commun. 2015, 51, 4830; (c) Xun, Z. Q.; Tang, H. Y.; Zeng, Y.; Chen, J. P.; Yu, T. J.; Zhang, X. H.; Li, Y. Acta Chim. Sinica 2015, 73, 819(in Chinese). (寻知庆, 唐海云, 曾毅, 陈金平, 于天君, 张小辉, 李嫕, 化学学报, 2015, 73, 819.)
-
[10]
Wang, Z.; Bai, W.; Tong, J.; Wang, Y. J.; Qin, A.; Sun, J. Z.; Tang, B. Z. Chem. Commun. 2016, 52, 10365. doi: 10.1039/C6CC02851A
-
[11]
Yang, J.; Li, L.; Yu, Y.; Ren, Z.; Peng, Q.; Ye, S.; Li, Q.; Li, Z. Mater. Chem. Front. 2017, DOI: 10.1039/c6qm00014b.
-
[12]
Song, Z.; Zhang, W.; Jiang, M.; Sung, H. H. Y.; Kwok, R. T. K.; Nie, H.; Williams, I. D.; Liu, B.; Tang, B. Z. Adv. Funct. Mater. 2016, 26, 824; (b) Zhao, Z.; Chen, S.; Chan, C. Y. K.; Lam, J. W. Y.; Jim, C. K. W.; Lu, P.; Chang, Z.; Kwok, H. S.; Qiu, H.; Tang, B. Z. Chem. Asian J. 2012, 7, 484; (c) Tong, J.; Wang, Y.; Mei, J.; Wang, J.; Qin, A.; Sun, J. Z.; Tang, B. Z. Chem. Eur. J. 2014, 20, 4661; (d) Wang, Y. J.; Shi, Y.; Wang, Z.; Zhu, Z.; Zhao, X.; Nie, H.; Qian, J.; Qin, A.; Sun, J. Z.; Tang, B. Z. Chem. Eur. J. 2016, 22, 9784.
-
[13]
Shao, A.; Xie, Y.; Zhu S.; Guo, Z.; Zhu, S.; Guo, J.; Shi, P.; James, T. D.; Tian, H.; Zhu, W.-H. Angew. Chem., Int. Ed. 2015, 54, 7275; (b) Guo, Z.; Shao, A.; Zhu, W.-H. J. Mater. Chem. C 2016, 4, 2640; (c) Xia, Z. Q.; Shao, A. D.; Li, Q.; Zhu, S. Q.; Zhu, W. H. Acta Chim. Sinica 2016, 74, 351(in Chinese). (夏志清, 邵安东, 李强, 朱世琴, 朱为宏, 化学学报, 2016, 74, 351.)
-
[14]
Ding, L.; Ying, H.-Z.; Zhou, Y.; Lei, T.; Pei, J. Org. Lett. 2010, 12, 5522; (b) Zhou, Y.; Ding, L.; Shi, K.; Dai, Y.-Z.; Ai, N.; Wang, J.; Pei, J. Adv. Mater. 2012, 24, 957; (c) Zheng, Y.-Q.; Dai, Y.-Z.; Zhou, Y.; Wang, J.-Y.; Pei, J. Chem. Commun. 2014, 50, 1591; (d) Saranya, G.; Kolandaivel, P.; Senthilkumar, K. J. Phys. Chem. A 2011, 115, 14647; (e) Goel, A.; Kumar, V.; Chaurasia, S.; Rawat, M.; Prasad, R.; Anand, R. S. J. Org. Chem. 2010, 75, 3656; (f) Goel, A.; Sharma, A.; Kathuria, M.; Bhattacharjee, A.; Verma, A.; Mishra, P. R.; Nazir, A.; Mitra, K. Org. Lett. 2014, 16, 756; (g) Han, L.; Zhang, Y.; Chen, W.; Cheng, X.; Ye, K.; Zhang, J.; Wang, Y. Chem. Commun. 2015, 51, 4477.
-
[15]
Li, X.-G.; Liao, Y.; Huang, M.-R.; Strong, V.; Kaner, R. B. Chem. Sci. 2013, 4, 1970. doi: 10.1039/c3sc22107e
-
[16]
Venkatramaiah, N.; Kumar, S.; Patil, S. Chem. Eur. J. 2012, 18, 14745; (b) Kumar, S.; Venkatramaiah, N.; Patil, S. J. Phys. Chem. C 2013, 117, 7236.
-
[17]
Chandrasekaran, Y.; Venkatramaiah, N.; Patil, S. Chem. Eur. J. 2016, 22, 5288. doi: 10.1002/chem.201504485
-
[18]
Feng, H.-T.; Zheng, Y.-S. Chem. Eur. J. 2014, 20, 195; (b) Wang, X.; Bian, J.; Xu, L.; Wang, H.; Feng, S. Phys. Chem. Chem. Phys. 2015, 17, 32472.
-
[1]
-
图 1 A)归一化后的TPE-FA与TPE-DFA的THF溶液的紫外-可见吸收光谱. (B)和(C)分别为TPE-FA和TPE-DFA在不同水含量的THF/水混合溶剂中的荧光发射光谱. (D) TPE-FA与TPE-DFA的荧光增强程度随水含量变化的曲线. [TPE-FA]=[TPE-DFA]=10-5 mol/L, 两个分子的荧光测试中λex=370 nm
Figure 1 (A) Normalized UV-vis absorption spectra of TPE-FA and TPE-DFA in THF solution. (B) and (C) Fluorescence (FL) emission spectra of TPE-FA and TPE-DFA in THF/water mixtures with different water fractions, respectively. (D) Plots of the emission enhancements of TPE-FA and TPE-DFA in accordance with various water fractions in the THF/water mixtures. [TPE-FA]=[TPE-DFA]=10-5 mol/L. λex=370 nm for all the measurements
图 2 (A) TPE-FA的荧光量子产率随混合溶剂中水含量变化的曲线. (B) TPE-DFA的荧光量子产率随混合溶剂中水含量变化的曲线.溶质浓度: [TPE-FA]=[TPE-DFA]=10-5 mol/L, 激发波长: λex=370 nm
Figure 2 (A) Plot of QY of TPE-FA in accordance with various water fractions in the THF/water mixtures. (B) Plot of QY of TPE-DFA in accordance with various water fractions in the THF/water mixtures. Concentration: [TPE-FA]=[TPE-DFA]=10-5 mol/L. λex=370 nm
图 5 (A) TPE-FA在含不同浓度PA的THF/水混合溶液(水体积含量90%)中的荧光发射光谱. (B) TPE-FA在含不同浓度PA的混合溶液中的荧光猝灭曲线(发射波长477 nm). (C) TPE-DFA在含不同浓度PA的THF/水混合溶液(水体积含量90%)中的荧光发射光谱. (D) TPE-DFA在含不同浓度PA的混合溶液中的荧光猝灭曲线(发射波长494 nm). (E)与(F) TPE-FA与TPE-DFA的荧光猝灭的照片. [TPE-DFA]=10-5 mol/L.光谱测试λex=370 nm.荧光照片λex=365 nm
Figure 5 (A) FL emission spectra of TPE-FA in THF/water mixtures (φw=90%) with different [PA]. (B) Plots of fluorescence quenching at 477 nm of TPE-FA in accordance with [PA] in THF/water mixtures. (C) FL emission spectra of TPE-DFA in THF/water mixtures (φw=90%) with different [PA]. (D) Plots of fluorescence quenching at 494 nm of TPE-DFA in accordance with [PA] in THF/water mixtures. (E) and (F) Digital images of fluorescence quenching of TPE-FA and TPE-DFA with different [PA] in THF/water mixtures. [TPE-DFA]=10-5 mol/L. λex=370 nm for FL spectroscopy. λex=365 nm for photos taken
表 1 TPE-FA与TPE-DFA的荧光寿命a
Table 1. Lifetime results of TPE-FA and TPE-DFAa
Compound τ1/ns τ2/ns < τ > /ns χ2 TPE-FA Solutionb 0.31 (84%) 3.91 (15%) 0.87 1.24 Aggregate 3.89 (31%) 6.84 (69%) 5.94 1.19 TPE-DFA Solution 0.21 (91%) 4.65 (9%) 0.61 0.99 Aggregate 1.33 (61%) 3.27 (39%) 2.09 1.01 a The fluorescence lifetime results are recorded by an Edinburgh Instrument FLS920 Transient/Steady State Photoluminescence Spectrometer. The samples are excited by a 405-nm picosecond laser; b Results of solutions are measured in THF, and those of aggregates are measured in THF/water mixtures (THF/water=10/90 by volume). 表 2 两种分子在不同状态下的发射波长与荧光量子产率
Table 2. Emission wavelength and QY of the two compounds
Compound λem, aga/nm Φagb/% λem, fm/nm Φfm/% TPE-FA 477 12.5 467 74.1 TPE-DFA 494 24.0 494 40.4 a ag represents the aggregates (THF/water=10/90 by volume), fm represents the film; b The fluorescence quantum yields are measured by a Hamamatsu Absolute Quantum Yield Spectrometer. -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 902
- HTML全文浏览量: 129


 下载:
下载:





 下载:
下载:

