 图1
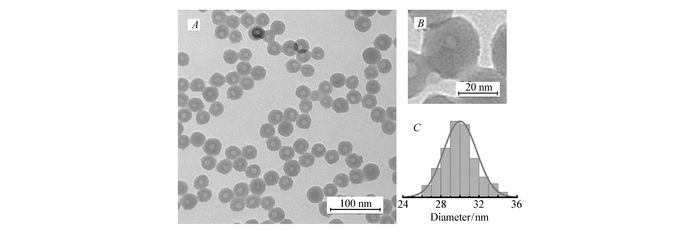
二氧化硅稳定金纳米颗粒的电子显微镜(A)、高分辨电子显微镜(B)及二氧化硅尺寸分布(C)
Figure1.
TEM(A) and HRTEM(B) images of the Au-SiO2, and size distribution histogram of silica(C)
图1
二氧化硅稳定金纳米颗粒的电子显微镜(A)、高分辨电子显微镜(B)及二氧化硅尺寸分布(C)
Figure1.
TEM(A) and HRTEM(B) images of the Au-SiO2, and size distribution histogram of silica(C)

Citation: WANG Cui, ZHANG Feiyun, LYU Rongwen, ZHANG Shufen. Gold Nanopaticle Surface Energy Transfer and Its Application for Thiols Detection[J]. Chinese Journal of Applied Chemistry, 2018, 35(1): 60-67. doi: 10.11944/j.issn.1000-0518.2018.01.170048

金纳米颗粒表面能量转移及巯基化合物的检测
English
Gold Nanopaticle Surface Energy Transfer and Its Application for Thiols Detection
-
Key words:
- surface energy transfer
- / gold nanoparticles
- / silica
- / Rhodamine B
- / thiols
-
表面能量转移通常是指荧光染料作为能量给体在激发态将能量转移至能量受体纳米颗粒表面,其本质与荧光共振能量转移相同,均是基于能量给体与受体之间偶极-偶极作用下的非辐射能量跃迁[1-2]。由于受体是拥有较大比表面积的纳米颗粒,其在几何学上的偶极向量分布具有各向同性,使得表面能量转移作用具有较高的能量转移效率以及作用范围,从而成为能量转移研究中的重要组成部分[3-4]。金纳米颗粒由于其特殊的电子结构和化学物理性质[5],常被作为表面能量转移受体,成为免疫分析检测、生物化学分析以及环境中重金属检测等研究常用的探针之一[6-11]。
巯基化合物是一类重要物质,它不仅广泛应用于化学研究中,而且在生物体的体液、组织、细胞中承担着多种至关重要的生理功能[12-13]。因此,巯基化合物的检测逐渐成为分析化学中的研究热点。目前,检测巯基化合物的常见方法有电化学分析法[14]、荧光分析法[15]、化学发光分析法[16]等,但是普遍存在探针合成耗时较长,作用较慢的问题。本文基于金纳米颗粒的表面能量转移作用,建立一种简单快速测定巯基化合物的荧光检测方法。金纳米颗粒作为能量受体,通过表面能量转移猝灭吸附于其表面的荧光染料的荧光;加入巯基化合物后,由于其与金纳米颗粒之间的强相互作用,使得荧光染料离开金纳米颗粒表面,进而染料荧光恢复,从而达到检测巯基化合物的目的。但是金属纳米颗粒在应用过程中常出现颗粒聚集或流失,因此需选择载体将其稳定以解决这一问题[17-18]。二氧化硅化学惰性,可以保留金属颗粒的原始性质[19-20];同时,二氧化硅还具有光学透明特性[21],以及多孔结构所带来的吸附特性[22-23]。因此,本文选择二氧化硅作为载体,采用微乳液法制备出均匀分散的二氧化硅稳定的金纳米颗粒(Au-SiO2);考察该金纳米颗粒与罗丹明B之间的能量转移过程,并基于巯基化合物对罗丹明B的荧光恢复,实现对巯基化合物的检测。由于二氧化硅对金纳米颗粒的稳定作用,可以在实验过程中对金纳米颗粒进行回收,从而使金纳米颗粒可重复使用。
1 实验部分
1.1 仪器和试剂
Tecnai F30型透射电子显微镜(美国FEI公司),Eacalab 250Xi型X射线光电子能谱仪(美国Thermo Fisher公司),F-7000型荧光光谱仪(日本Hitachi公司),Optima 2000DV型等离子原子发射光谱仪(美国Perkin Elmer公司)。聚氧乙烯醚(C20)购自美国Acros Organic试剂公司,环己烷、氯金酸(四水)、硼氢化钠、氨水、正硅酸四乙酯、异丙醇、罗丹明B、巯基乙醇、巯基丙醇、α-巯基甘油、乙醇、乙二醇、乙胺、乙二胺、乙醇胺、乙酸、草酸,均购自国药集团化学试剂有限公司。实验用水均为去离子水,试剂均为分析纯。
1.2 二氧化硅稳定的金纳米颗粒(Au-SiO2)的合成
参考文献[24]合成Au-SiO2,在100 mL圆底烧瓶中加入15 mL环己烷和3.37 g聚氧乙烯醚(C20),53 ℃下磁力搅拌直至体系澄清透明形成稳定的微乳液体系;将0.2 mL氯金酸水溶液(0.1 mol/L)滴加至体系当中,持续搅拌(500 r/min);5 min后逐滴加入硼氢化钠水溶液(0.14 mol/L, 0.7 mL),反应30 min;加入0.5 mL氨水和1.0 mL正硅酸四乙酯制备二氧化硅载体。产物离心/洗涤3次后,在100 ℃下干燥10 h,再经过空气焙烧(500 ℃,2 h)得到最终产品Au-SiO2。
1.3 罗丹明B-金纳米颗粒能量转移过程及其对巯基化合物的响应
罗丹明B-Au-SiO2能量转移过程检测:F-7000荧光光谱仪激发波长500 nm,狭缝宽度分别为2.5 nm和5 nm。取3 mL浓度为0.3 μmol/L罗丹明B水溶液,将研磨后的Au-SiO2纳米复合材料逐次加入,记录加入量,充分超声振荡后静置,测试直至荧光强度不再降低。重复实验5次并计算标准偏差。
SiO2载体对罗丹明B荧光强度的影响检测:取3 mL浓度为0.3 μmol/L罗丹明B水溶液,将研磨后的纯SiO2纳米材料分次加入,记录加入量,充分超声振荡后静置,测试直至荧光强度不再降低。重复实验5次并计算标准偏差。
罗丹明B-Au-SiO2混合体系对巯基化合物的响应:取3 mL浓度为0.3 μmol/L罗丹明B水溶液,加入30 mg Au-SiO2后溶液荧光猝灭;在荧光猝灭的罗丹明B-Au-SiO2混合体系中,逐次加入巯基化合物,记录巯基化合物的加入量,充分超声振荡后静置,直至荧光强度不再增加,测试终止。重复实验5次并计算标准偏差。
Au-SiO2的回收:将混合溶液过滤,得到的固体用去离子水洗涤3次,烘干后,空气焙烧(500 ℃,2 h)。
2 结果与讨论
2.1 Au-SiO2结构表征
在本研究组前期研究[24]的基础上,本文利用反相微乳液体系制备出二氧化硅稳定的金纳米颗粒,并对其结构进行透射电子显微镜与高分辨透射电子显微镜表征,结构如图 1所示。该纳米复合材料为球形结构,通过高分辨透射电子显微镜图可以看到球体上分散有黑色斑点,这些黑色斑点即是金纳米颗粒,球体是载体二氧化硅。通过Image J软件测量200个以上球形Au-SiO2的尺寸,统计结果如图 1C所示,其尺寸为(30.0±1.7) nm;金纳米颗粒在电镜图中只能看到黑色斑点,尺寸无法测量。等离子原子发射光谱仪测得复合材料中金质量分数为1.35%。
 图1
二氧化硅稳定金纳米颗粒的电子显微镜(A)、高分辨电子显微镜(B)及二氧化硅尺寸分布(C)
Figure1.
TEM(A) and HRTEM(B) images of the Au-SiO2, and size distribution histogram of silica(C)
图1
二氧化硅稳定金纳米颗粒的电子显微镜(A)、高分辨电子显微镜(B)及二氧化硅尺寸分布(C)
Figure1.
TEM(A) and HRTEM(B) images of the Au-SiO2, and size distribution histogram of silica(C)
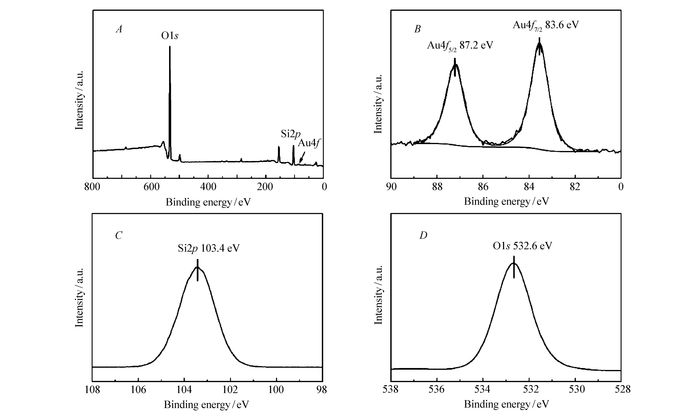
为进一步确定纳米复合材料的组成,采用X射线光电子能谱(XPS)分析材料所含元素以及价态,结果如图 2所示。在宽光谱扫描中可以看到Au、Si和O元素的存在,将校正后的Au4f、Si2p和O1s的窄光谱扫描进行分析,分别列于图 2B~2D中。Au窄光谱扫描的两个峰87.2和83.6 eV分别归属于Au0中的Au4f5/2和Au4f7/2;Si2p在103.4 eV处的谱峰正是SiO2中Si的结合能位置;O的谱峰532.6 eV与SiO2中O1s相对应。证明了复合材料是由Au和SiO2组成。
2.2 罗丹明B-Au-SiO2能量转移
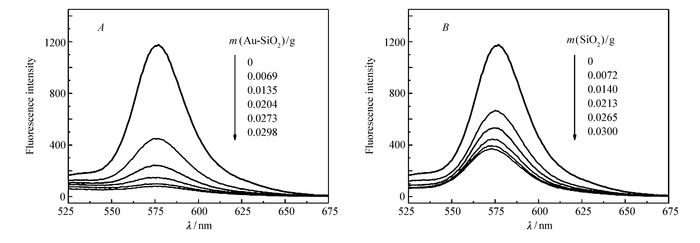
罗丹明B是常见的荧光染料,在水溶液中具有强烈荧光。本文在3 mL罗丹明B水溶液(0.3 μmol/L)中不断加入Au-SiO2(或SiO2),检测罗丹明B荧光强度变化,结果如图 3A所示,罗丹明B荧光强度随着Au-SiO2加入量的增加逐渐减弱,直至完全猝灭。这一现象表明罗丹明B与Au-SiO2之间发生了相互作用,使罗丹明B荧光猝灭。但由于Au-SiO2是复合材料,为确定该复合材料中Au和SiO2各自的作用,以形貌相同的纯SiO2纳米颗粒代替Au-SiO2进行对比实验。在实验条件相同的情况下,纯SiO2纳米颗粒加入量与Au-SiO2保持相同,结果如图 3B所示,罗丹明B的荧光强度随着纯SiO2纳米颗粒的加入同样有所下降,但不能使罗丹明B的荧光完全猝灭。这一结果说明纯SiO2纳米颗粒对罗丹明B具有吸附作用,可以使罗丹明B荧光强度有所下降,但在该实验条件下仅能使其荧光强度下降到67.7%,而Au-SiO2可以将罗丹明B的荧光完全猝灭,说明纳米复合材料中金纳米颗粒对罗丹明B的荧光猝灭发挥了重要作用。
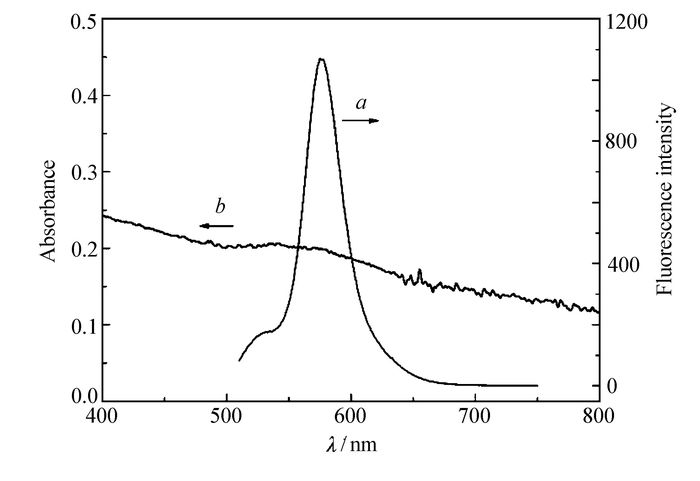
二氧化硅作为吸附材料已多见报道[22-23],此处不做讨论,金纳米颗粒对罗丹明B荧光猝灭可被归因于表面能量转移过程[9, 25],这一过程的发生要求能量供体的发射光谱与能量受体的吸收光谱必须重叠[6]。在罗丹明B-Au-SiO2混合体系中,罗丹明B由于具有强烈荧光,通常作为能量给体。如图 4谱线a所示,罗丹明B水溶液在575 nm处具有较强的荧光发射光谱。Au-SiO2作为能量受体,在500~650 nm波长范围有明显的金纳米颗粒表面等离子共振吸收峰,UV-Vis吸收光谱如图 4谱线b所示。因此,罗丹明B荧光发射光谱与金纳米颗粒表面等离子共振吸收光谱明显重叠,表明罗丹明B作为能量给体与能量受体Au纳米颗粒之间能够发生能量转移过程。
金纳米颗粒对罗丹明B荧光猝灭能力可通过Stern-Volmer猝灭常数来衡量[25-26]:
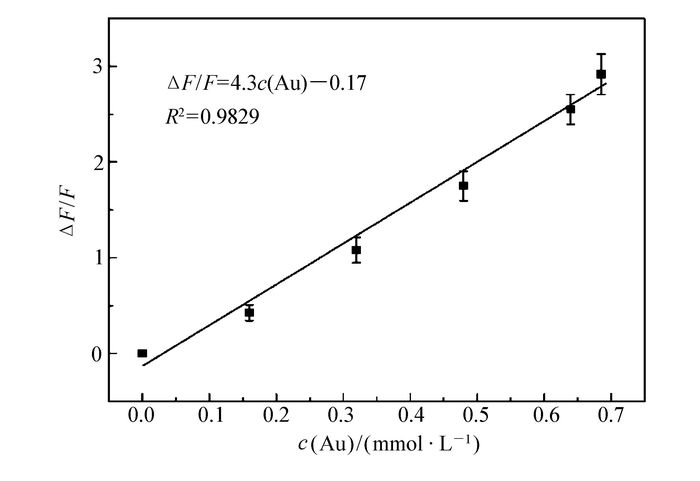
式中,Φ0和F0分别表示未加入猝灭剂时的量子产率和发射强度,Φ和F表示加入猝灭剂后的量子产率和发射强度;kq、kc和kd分别表示猝灭、发射以及钝化的比率;KSV和c(Q)分别为Stern-Volmer猝灭常数和猝灭剂的浓度。计算金纳米颗粒对罗丹明B的猝灭常数KSV,可对图 3所得数据(见辅助材料表S1和表S2)进行计算,扣除SiO2对罗丹明B荧光强度的影响,再依据关系式(1)进行处理,得到罗丹明B荧光强度差ΔF/F与猝灭剂金纳米颗粒浓度c(Au)之间的关系式,结果见图 5。图 5的斜率即对应Stern-Volmer关系式(1)中猝灭常数KSV,因此金纳米颗粒在该实验条件下对罗丹明B的猝灭常数为4.3×103 L/mol。这一结果说明二氧化硅稳定的金纳米颗粒对罗丹明B具有较好的猝灭能力。金纳米颗粒与罗丹明B之间发生能量转移,使罗丹明B荧光猝灭的原因主要归因于:1)罗丹明B的荧光发射光谱与金纳米颗粒表面等离子共振吸收光谱重叠;2)缺电子的金纳米颗粒对荧光染料具有较强的亲和力[1, 27];3)二氧化硅作为载体对罗丹明B的吸附发挥了辅助作用,因为表面能量转移过程要求给体-受体之间距离小于20 nm[3],二氧化硅的吸附作用有利于拉近金纳米颗粒与罗丹明B的距离,从而有效地发生能量转移过程。
2.3 罗丹明B-Au-SiO2体系对巯基化合物的响应
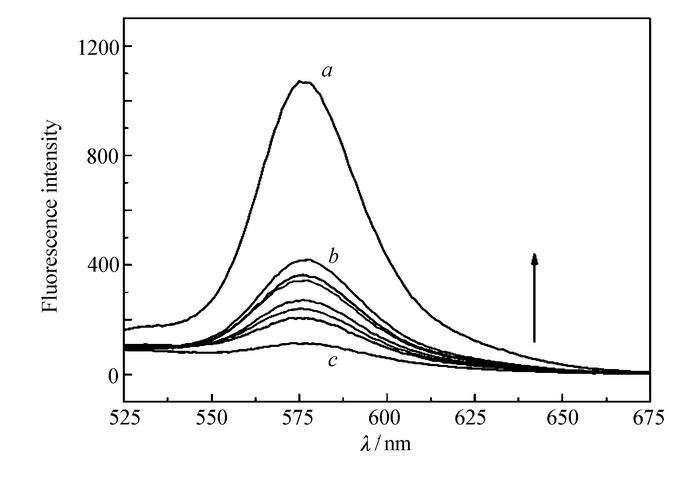
巯基取代基与贵金属之间具有非常好的配位能力[28-29]。基于这一特点,在荧光猝灭的罗丹明B-Au-SiO2体系中加入巯基化合物,将会引起巯基化合物与罗丹明B对金纳米颗粒相互作用的竞争。加入巯基乙醇后罗丹明B-Au-SiO2体系的荧光光谱变化如图 6所示,其中图 6谱线a表示0.3 mmol/L罗丹明B水溶液的荧光光谱,图 6谱线c表示3 mL罗丹明B水溶液(0.3 mmol/L)中加入30 mg Au-SiO2的荧光光谱(荧光猝灭),而后,向荧光猝灭的罗丹明B-Au-SiO2体系不断加入巯基乙醇,混合体系的荧光强度不断增强,并最终停留在图 6谱线b处不再变化(此时巯基乙醇加入量为70 μL)。图 6曲线b和c之间荧光强度差,与图 3所述金纳米颗粒对罗丹明B荧光强度影响相一致。而将巯基乙醇加入到罗丹明B-SiO2体系中,荧光强度基本不发生变化,说明罗丹明B-Au-SiO2体系荧光的恢复要归因于金的存在,即在罗丹明B-Au-SiO2体系中与巯基化合物发生作用并使罗丹明B荧光恢复的是金纳米颗粒。与此同时,增强的荧光光谱与初始罗丹明B光谱形状一致,发射峰始终保持在575 nm且没有新的发射峰出现,这说明荧光的增强并非来自于新发射荧光团的生成,而是来自于罗丹明B。这一结果表明,巯基化合物与金纳米颗粒之间强相互作用阻断了罗丹明B-金纳米颗粒表面能量转移,罗丹明B荧光恢复;同时这一结果也进一步证明罗丹明B荧光猝灭不是因为自身结构被破坏,而是罗丹明B-金纳米颗粒之间的能量转移。
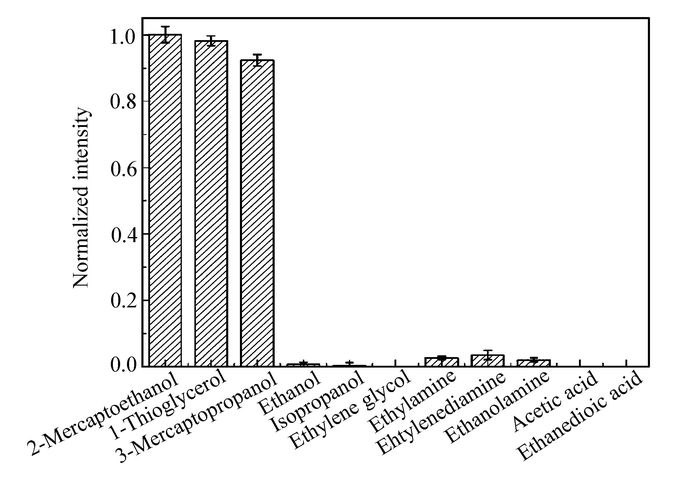
为深入研究巯基化合物对罗丹明B-Au-SiO2能量转移体系的作用,实验中对比考察了多种含有不同取代基的化合物对罗丹明B-Au-SiO2体系的响应,每组实验平行测定3次。结果如图 7所示,含有巯基取代基的化合物(巯基乙醇、巯基丙醇和α-巯基甘油)对混合体系荧光信号具有明显的增强作用,而含有其它基团(—OH、—NH2以及—COOH)化合物对混合体系的荧光信号不具有增强作用。这一现象表明罗丹明B-Au-SiO2能量转移体系对巯基化合物具有较好的识别作用。这是因为金纳米颗粒对罗丹明B的荧光猝灭来源于吸附在金纳米颗粒表面的罗丹明B与金纳米颗粒之间的非辐射能量跃迁,而巯基化合物与金纳米颗粒之间发生化学配位作用[6],因此巯基化合物的加入可以阻断罗丹明B-金纳米颗粒之间的能量转移作用,使罗丹明B荧光恢复。而其它化合物中的羟基、氨基以及羧基并不足以阻断罗丹明B-金纳米颗粒之间的能量转移作用,因此罗丹明B的荧光无法恢复。
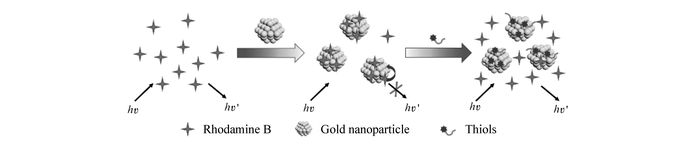
金纳米颗粒表面能量转移法识别巯基化合物的原理如图 8所示,水溶液中罗丹明B受到光激发后会产生荧光;加入Au-SiO2后,由于罗丹明B与金纳米颗粒发生相互作用,给体(罗丹明B)-受体(金纳米颗粒)之间发生能量转移,罗丹明B荧光猝灭;当荧光猝灭的罗丹明B-Au-SiO2体系加入巯基化合物后,由于金纳米颗粒与巯基之间相互作用更强,阻断罗丹明B-金纳米颗粒之间的能量转移,罗丹明B荧光得到恢复。
2.4 罗丹明B-Au-SiO2体系检测巯基乙醇的线性范围及灵敏度
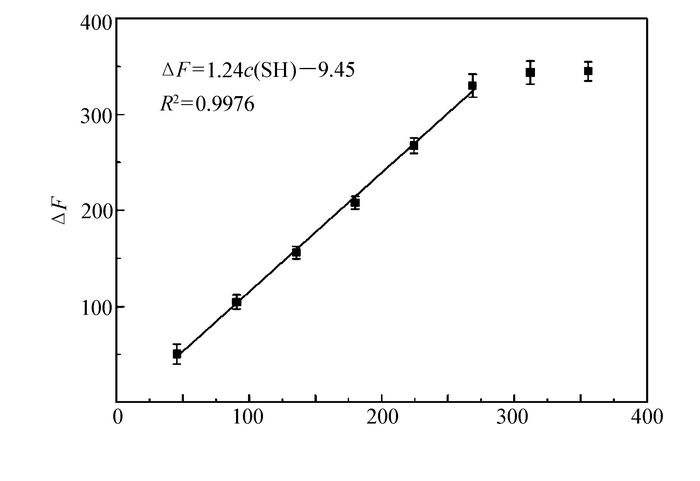
为考察罗丹明B-Au-SiO2体系对巯基化合物的识别能力,以巯基乙醇为例,研究罗丹明B-Au-SiO2体系对巯基乙醇响应的线性范围及灵敏度。如图 9所示,随着巯基乙醇滴加至罗丹明B-Au-SiO2体系中,混合体系的荧光强度不断增加,并且在巯基乙醇浓度45~268 mmol/L范围内,荧光强度的增加值与巯基乙醇的浓度呈现较好的线性关系。线性回归方程为ΔF=1.24c(SH)-9.45(其中ΔF表示体系荧光强度增加值,c(SH)表示巯基乙醇的浓度单位mmol/L,误差线表示5次平行实验的标准偏差),R2=0.9976,检出限(3σ)为7.5 mmol/L(σ表示10个空白样品的标准偏差)。基于这一结果,有望建立一种简单快速检测巯基化合物的方法。
2.5 二氧化硅稳定金纳米颗粒的重复利用
虽然目前检测巯基化合物的方法很多,但是鲜有探针能够做到重复使用[6, 13, 16]。本文合成的金纳米颗粒以二氧化硅作为载体,并将金纳米颗粒分散在其多孔结构中,利用物理限域效应实现金纳米颗粒的稳定性。这一稳定作用可以简化金纳米颗粒的分离与纯化,使金纳米颗粒的重复利用成为可能。
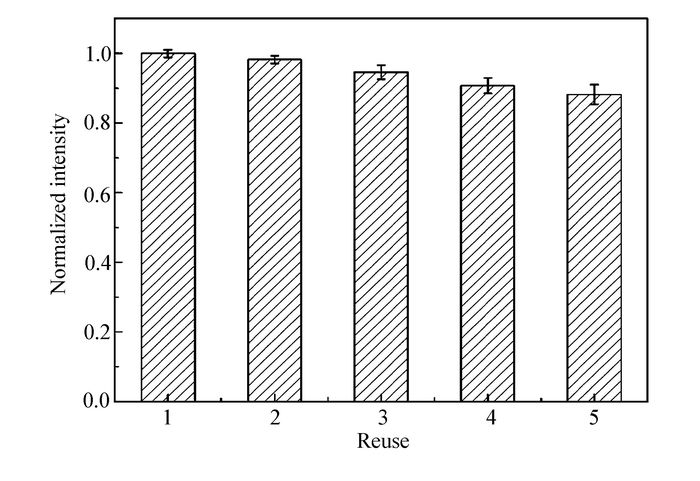
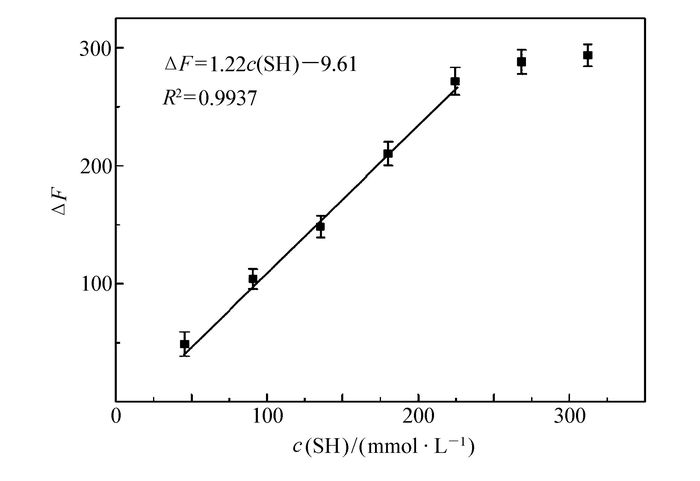
为了证明该二氧化硅稳定的金纳米颗粒检测巯基乙醇的重复利用性,将该检测过程循环5次进行对比。在循环实验过程中,0.3 μmol/L的罗丹明B用量始终保持3 mL,Au-SiO2重复回收利用,观察混合体系对巯基乙醇的响应情况,以罗丹明B-Au-SiO2体系的荧光强度增加值ΔF作为考察对象。结果发现,随着使用次数的增加,荧光强度的最大增加值ΔFmax随着使用次数的增加略有所降低(图 10),在第5次使用之后,ΔFmax变为初始荧光强度增加值的88%左右。这可能是由于金纳米颗粒与巯基乙醇之间的强相互作用使表面金原子发生部分流失,金含量随着重复次数增加而逐渐减少,因而使罗丹明B荧光恢复能力略有所减小。但是在检测过程中,荧光强度的增加值ΔF与巯基乙醇浓度c(SH)之间仍然具有较好的线性关系,如图 11所示,对第5次检测数据进行处理发现,荧光强度的增加值ΔF与巯基乙醇浓度c(SH)之间线性回归方程为ΔF=1.22c(SH)-9.61,这与之前结果基本一致。因此,二氧化硅稳定的金纳米颗粒检测巯基乙醇具有很好的重复使用性。
3 结论
基于金纳米颗粒表面能量转移,二氧化硅稳定的金纳米颗粒对罗丹明B具有较好的猝灭作用,计算金纳米颗粒对罗丹明B的Stern-Volmer猝灭常数为4.3×103 L/mol。当荧光猝灭的罗丹明B-Au-SiO2体系加入巯基化合物后,巯基化合物-金纳米颗粒之间的强相互作用阻断罗丹明B与金纳米颗粒之间的能量转移,罗丹明B荧光恢复。应用该方法检测巯基乙醇的线性范围为45~268 mmol/L,检出限(3σ)为7.5 mmol/L。二氧化硅稳定的金纳米颗粒可以有效循环利用,5次使用之后,最大荧光强度增加值保持原来的88%左右,荧光强度增加值与巯基乙醇浓度的线性回归方程基本保持不变。
辅助材料(Supporting Information)[平行实验数据]可以免费从本刊网站(http://yyhx.ciac.jl.cn/)下载。
-
-
[1]
Darbha G K, Ray A, Ray P C. Gold Nanoparticle-Based Miniaturized Nanomaterial Surface Energy Transfer Probe for Rapid and Ultrasensitive Detection of Mercury in Soil, Water, and Fish[J]. ACS Nano, 2007, 1(3): 208-214. doi: 10.1021/nn7001954
-
[2]
Prigogine I. Molecular Fluorescence and Energy Transfer near Interfaces[M]. Hoboken NJ:John Wiley & Sons Inc, 2007.
-
[3]
Yun C S, Javier A, Jennings T. Nanometal Surface Energy Transfer in Optical Rulers, Breaking the FRET Barrier[J]. J Am Chem Soc, 2005, 127(9): 3115-3119. doi: 10.1021/ja043940i
-
[4]
Jennings T L, Singh M P, Strouse G F. Fluorescent Lifetime Quenching near D=1.5 nM Gold Nanoparticles:Probing NSET Validity[J]. J Am Chem Soc, 2006, 128(16): 5462-5467. doi: 10.1021/ja0583665
-
[5]
Yamazoe S, Koyasu K, Tsukuda T. Nonscalable Oxidation Catalysis of Gold Clusters[J]. Acc Chem Res, 2014, 47(3): 816-824. doi: 10.1021/ar400209a
-
[6]
Gao F, Ye Q, Cui P. Selective "Turn-on" Fluorescent Sensing for Biothiols Based on Fluorescence Resonance Energy Transfer Between Acridine Orange and Gold Nanoparticles[J]. Anal Methods, 2011, 3(5): 1180-1185. doi: 10.1039/c1ay05073g
-
[7]
Huang C C, Chang H T. Selective Gold-Nanoparticle-Based "Turn-on" Fluorescent Sensors for Detection of Mercury(Ⅱ) in Aqueous Solution[J]. Anal Chem, 2006, 78(24): 8332-8338. doi: 10.1021/ac061487i
-
[8]
Shang L, Qin C, Wang T. Fluorescent Conjugated Polymer-Stabilized Gold Nanoparticles for Sensitive and Selective Detection of Cysteine[J]. J Phys Chem C, 2007, 111(36): 13414-13417. doi: 10.1021/jp073913p
-
[9]
He X, Liu H, Li Y. Gold Nanoparticle-Based Fluorometric and Colorimetric Sensing of Copper(Ⅱ) Ions[J]. Adv Mater, 2005, 17(23): 2811-2815. doi: 10.1002/(ISSN)1521-4095
-
[10]
Bu D, Zhuang H, Yang G. An Immunosensor Designed for Polybrominated Biphenyl Detection Based on Fluorescence Resonance Energy Transfer(FRET) Between Carbon Dots and Gold Nanoparticles[J]. Sens Actuators B, 2014, 195: 540-548. doi: 10.1016/j.snb.2014.01.079
-
[11]
刘春, 黄承志. 金纳米粒子表面能量转移法测定水中的铅离子[J]. 分析化学, 2014(8): 1196-1199. LIU Chun, HUANG Chengzhi. Detection of Lead Ions in Water Based on Surface Energy Transfer Between Gold Nanoparticles and Fluorescenct Dyes[J]. Chinese J Anal Chem, 2014, (8): 1196-1199.
-
[12]
Isokawa M, Kanamori T, Funatsu T. Analytical Methods Involving Separation Techniques for Determination of Low-Molecular-Weight Biothiols in Human Plasma and Blood[J]. J Chromatogr B Anal Technol Biomed Life Sci, 2014, 964: 103-115. doi: 10.1016/j.jchromb.2013.12.041
-
[13]
Dominy J E, Stipanuk M H. New Roles for Cysteine and Transsulfuration Enzymes:Production of H2S, a Neuromodulator and Smooth Muscle Relaxant[J]. Nutr Rev, 2004, 62(9): 348-353.
-
[14]
Wang W, Li L, Liu S. Determination of Physiological Thiols by Electrochemical Detection with Piazselenole and Its Application in Rat Breast Cancer Cells 4T-1[J]. J Am Chem Soc, 2008, 130(33): 10846-10847. doi: 10.1021/ja802273p
-
[15]
Manibalan K, Chen S M, Mani V. A Sensitive Ratiometric Long-Wavelength Fluorescent Probe for Selective Determination of Cysteine/Homocysteine[J]. J Fluoresc, 2016, 26(4): 1489-1495. doi: 10.1007/s10895-016-1844-x
-
[16]
Uzu T, Sasaki S. A New Copper(Ⅱ) Complex as an Efficient Catalyst of Luminol Chemiluminescence[J]. Org Lett, 2007, 9(21): 4383-4386. doi: 10.1021/ol702002e
-
[17]
White R J, Luque R, Budarin V L. Supported Metal Nanoparticles on Porous Materials. Methods and Applications[J]. Chem Soc Rev, 2009, 38(2): 481-494. doi: 10.1039/B802654H
-
[18]
Newton M A. Dynamic Adsorbate/Reaction Induced Structural Change of Supported Metal Nanoparticles:Heterogeneous Catalysis and Beyond[J]. Chem Soc Rev, 2008, 37(12): 2644-2657. doi: 10.1039/b707746g
-
[19]
Turner M, Golovko V B, Vaughan O P. Selective Oxidation with Dioxygen by Gold Nanoparticle Catalysts Derived from 55-Atom Clusters[J]. Nature, 2008, 454(7207): 981-983. doi: 10.1038/nature07194
-
[20]
Li W, Wang A, Yang X. Au/SiO2 as a Highly Active Catalyst for the Selective Oxidation of Silanes to Silanols[J]. Chem Commun, 2012, 48(73): 9183-9185. doi: 10.1039/c2cc33949h
-
[21]
Caltagirone C, Bettoschi A, Garau A. Silica-Based Nanoparticles:A Versatile Tool for the Development of Efficient Imaging Agents[J]. Chem Soc Rev, 2015, 44(14): 4645-4671. doi: 10.1039/C4CS00270A
-
[22]
Coasne B, Galarneau A, Pellenq R J. Adsorption, Intrusion and Freezing in Porous Silica:The View from the Nanoscale[J]. Chem Soc Rev, 2013, 42(9): 4141-4171. doi: 10.1039/c2cs35384a
-
[23]
Rimola A, Costa D, Sodupe M. Silica Surface Features and Their Role in the Adsorption of Biomolecules:Computational Modeling and Experiments[J]. Chem Rev, 2013, 113(6): 4216-4313. doi: 10.1021/cr3003054
-
[24]
Wang C, Lin X, Ge Y. Silica-Supported Ultra Small Gold Nanoparticles as Nanoreactors for the Etherification of Silanes[J]. RSC Adv, 2016, 6(104): 102102-102108. doi: 10.1039/C6RA22359A
-
[25]
Griffin J, Singh A K, Senapati D. Size-and Distance-Dependent Nanoparticle Surface-Energy Transfer(NSET) Method for Selective Sensing of Hepatitis C Virus RNA[J]. Chem-Eur J, 2009, 15(2): 342-351. doi: 10.1002/chem.200801812
-
[26]
刘春, 吴同, 黄承志. 金纳米微粒表面能量转移及半胱氨酸的高灵敏度高选择性分析法[J]. 中国科学:化学, 2010,40,531-537. LIU Chun, WU Tong, HUANG Chengzhi. Gold Nanoparticles Surface Energy Transfer and Its Application to Highly Selective and Sensitive Detection of Cysteine[J]. Sci Sin Chim, 2010, 40: 531-537.
-
[27]
Kamiya I, Tsunoyama H, Tsukuda T. Lewis Acid Character of Zero-Valent Gold Nanoclusters Under Aerobic Conditions:Intramolecular Hydroalkoxylation of Alkenes[J]. Chem Lett, 2007, 36(5): 646-647. doi: 10.1246/cl.2007.646
-
[28]
Wu Z L, Jiang D E, Mann A K P. Thiolate Ligands as a Double-Edged Sword for Co Oxidation on CeO2 Supported Au25(SCH2CH2ph)18 Nanoclusters[J]. J Am Chem Soc, 2014, 136(16): 6111-6122. doi: 10.1021/ja5018706
-
[29]
Jose D, Matthiesen J E, Parsons C. Size Focusing of Nanoparticles by Thermodynamic Control Through Ligand Interactions. Molecular Clusters Compared with Nanoparticles of Metals[J]. J Phys Chem Lett, 2012, 3(7): 885-890. doi: 10.1021/jz201640e
-
[1]
-
图 6 巯基乙醇对罗丹明B的荧光恢复
Figure 6 Fluorescence recovery of Rhodamine B by 2-mercaptoethanol
a.the fluorescence spectra of 0.3 μmol/L Rhodamine B; b.the fluorescence restore of curve c with the addition of 70 μL of 2-mercaptoethanol, c.the fluorescence quenching of curve a with the addition of 30 mg of Au-SiO2
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 5
- 文章访问数: 3612
- HTML全文浏览量: 1276


 下载:
下载:










 下载:
下载:

