 图1
不同Tm3+掺杂量Bi2WO6样品的XRD图
Figure1.
X-ray diffraction patterns of the Bi2WO6 samples doped with different amount of Tm3+
图1
不同Tm3+掺杂量Bi2WO6样品的XRD图
Figure1.
X-ray diffraction patterns of the Bi2WO6 samples doped with different amount of Tm3+

Citation: ZHAO Wei-Di, HE Jin-Yun, WANG Yan-Wu, LONG Fei, PENG Dai-Jiang, ZOU Zheng-Guang. Visible-Light Catalytic Performance of Rare Earth Ions Tm3+ Doped Bi2WO6[J]. Chinese Journal of Inorganic Chemistry, 2018, 34(2): 359-366. doi: 10.11862/CJIC.2018.062

稀土离子Tm3+掺杂Bi2WO6的可见光催化性能
English
Visible-Light Catalytic Performance of Rare Earth Ions Tm3+ Doped Bi2WO6
-
随着工业的发展,水污染日趋严重,已经成为不可忽视的环境难题,危害着人类健康和社会的可持续发展。因而,能够经济有效地将废水中的污染物降解的半导体光催化技术是环境治理研究领域的热点[1-3]。在各类半导体光催化剂中,TiO2由于其优异的光催化性能,光化学稳定性和无毒性,被认为是废水处理最有前景的光催化剂[4-6]。然而,TiO2的带隙较宽(3.2 eV),只能被紫外线激发,使其在实际应用中受到了很大的制约[7]。为了更高效的利用太阳光,近年来研究发现了多种可以被可见光激发的光催化材料。Bi2WO6由于其特殊的层状结构、合适的能带结构和良好的光稳定性,成为可见光催化材料研究的热点[8-10]。但由于Bi2WO6光生载流子的复合率较高,提高其光催化性能仍然是一大难题[11-12]。为了克服这一缺点,对Bi2WO6进行离子掺杂改性是一个非常好的解决方法[13-14]。将阴离子或阳离子引入Bi2WO6的主晶格中,可有效调节半导体光催化剂的带隙,所掺杂的离子还可以提高界面处的光生电子迁移效率,有效促进电子-空穴对的分离,从而提高其催化性能[15-16]。至今为止,已有较多离子掺杂Bi2WO6的研究报导。例如,Zhang等[17]通过水热法合成了非金属离子Br-掺杂的Bi2WO6,光照40 min后可降解96.73%的罗丹明B。Zhu[18]等通过回流-煅烧法制备了F-掺杂的Bi2WO6,不仅增强了光生载流子的迁移率,其价带还具有更好的氧化能力,其降解亚甲基蓝的效果为未掺杂的2倍。Wang等[19]通过金属离子Fe3+掺杂合成三维分级纳米Bi2WO6,因其新颖的纳米结构,能有效的提高Bi2WO6的光催化性能。Zhang等[20]通过Bi2WO6的铋自掺杂,在可见光下可有效降解五氯酚钠。近年来,稀土离子掺杂已被证明是提高光催化剂性能的有效方法[21-22]。这是因为稀土元素的原子轨道可以与各种路易斯碱形成配合物,从而将污染物沉积到催化剂表面[23-25]。与未掺杂的材料相比,掺杂稀土离子可有效增强Bi2WO6的光催化活性[26-29],但Tm3+掺杂Bi2WO6的研究尚未见报导。
本文采用水热法合成了Tm3+掺杂的Bi2WO6。通过XRD、SEM、TEM和UV-Vis DRS等多种测试方法对其进行了组成和结构表征,以研究掺杂Tm3+稀土离子后,Bi2WO6的理化性能;分别以有机染料罗丹明B和污水主要成分之一的焦糖色素为目标污染物,在模拟可见光条件下进行光催化实验,比较了不同Tm3+掺杂浓度对Bi2WO6光催化性能的影响,以获得具有优异可见光催化性能的Bi2WO6样品。
1 实验部分
1.1 合成
本研究所使用的试剂全部为分析纯,均购买自国药集团化学试剂有限公司。合成Tm3+掺杂Bi2WO6的具体方法如下:在室温下将Na2WO4·2H2O(2.5 mmol)溶解在10 mL去离子水中。同时在80 ℃下将Bi(NO3)3·5H2O(5 mmol)溶解在20 mL的硝酸溶液(1 mol·L-1)中。将2种溶液混合,并将一定质量的Tm(NO3)3·5H2O(nTm3+:nBi2WO6=0,2%,4%,6%,8%)加入到混合物中,搅拌2 h。然后用2 mol·L-1氢氧化钠溶液调节前驱体悬浮液的pH值至约4,再加入0.05 g聚乙烯吡咯烷酮(PVP),并在室温下搅拌均匀。将得到的前驱体溶液转移至100 mL不锈钢高压釜中,填充量为80%,并在烘箱中于160 ℃下保温12 h,待自然冷却至室温后取出。得到的淡黄色物质分别用水和无水乙醇离心洗涤3次,在60 ℃干燥12 h,最后得到淡黄色的Tm3+掺杂Bi2WO6样品。随着Tm(NO3)3·5H2O掺杂量的增加样品分别记为BWO-x(x=1,2,3,4),未掺杂的Bi2WO6样品记为BWO-0。
1.2 表征
采用X射线粉末衍射仪(XRD,Panalytical,X′pert PRO型,Cu Kα=0.154 06 nm,扫描电压40 kV,电流为40 mA,扫描范围为20°~80°)以10°·min-1的扫描速率对样品的组成进行分析;使用场发射扫描电子显微镜(FESEM,Hitachi,S-4800型,低真空模式的分辨率为5.0 nm,高真空模式的分辨率为3.0 nm,加速电压为0.5~30 kV,低真空度为1~270 Pa)和X射线能谱仪(EDS,Oxford,INCA IE350型)对样品的微观形貌和元素组成及元素含量进行分析;采用透射电子显微镜(TEM,JEOL,JEM-2100F,加速电压为120~200 kV)对样品的显微结构进行表征;使用UV-Vis分光光度计(Shimadzu,UV-3600型),以高纯BaSO4为参比,在200~800 nm波长范围内测试样品的光吸收性能;使用氮气吸附比表面积仪(Quantachrome,NOVA 1200e,吸附气体为N2)和激光拉曼光谱仪(Thermo Fisher Scientific,DXR型,激光波长为532 nm,激光功率为1 mW)分别测试样品的比表面积和拉曼光谱。
1.3 光催化性能测试
光催化反应在上海Bilang,BL-GHX-Ⅴ型光化学反应仪中进行。光源为500 W的氙灯(氙灯与反应器之间加入滤波片,λ>420 nm)。配制50 mL初始浓度为10 mg·L-1的罗丹明B溶液或100 mg·L-1焦糖色素溶液于石英试管中,加入50 mg催化剂。在光催化反应前,将含有催化剂的待降解悬浊液置于光化学反应器内避光磁力搅拌相应时间,使催化剂达到吸附脱附平衡。然后打开光源,边照射边搅拌,每隔一段时间取出约5 mL悬浊液,进行高速离心(11 000 r·min-1),以除去悬浊液中的催化剂颗粒,得到上层清液。采用UV-Vis光谱仪(Shimadzu UV-3600型)测试上层清液的吸光度。待降解物的降解率R按照下式计算:
式中:C0为暗反应后待降解物的初始浓度(mg·L-1);Ct为光催化反应不同时间后待降解物的浓度(mg·L-1)。
2 结果与讨论
2.1 物相分析
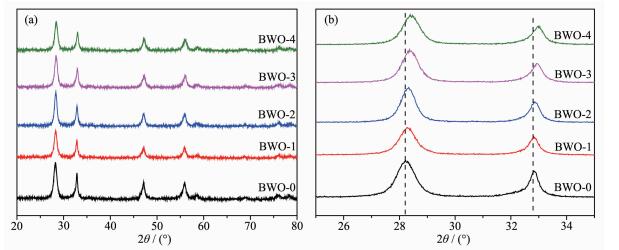
图 1为不同Tm3+掺杂量的Bi2WO6样品的XRD图。从图中可以看出,未掺杂Bi2WO6样品的所有衍射峰与正交晶系Bi2WO6(PDF No.39-0256)的衍射峰一致,且最强的衍射峰为(131)晶面(图 1a)。所有样品的XRD图中均未发现与Tm元素相关的衍射峰,说明所得到样品都是纯相Bi2WO6。掺杂Tm3+后,样品的衍射峰强度略有降低,说明离子掺杂抑制了Bi2WO6的晶粒生长。将样品的XRD衍射图在25°~35°范围内放大(图 1b),发现掺杂Tm3+后,样品的衍射峰全部向高角度方向偏移,并且偏移角度随着掺杂量增加而增加,这是因为Bi3+的离子半径为0.103 nm,比Tm3+的离子半径0.087 nm大,而W6+的离子半径只有0.062 nm。根据布拉格方程,样品的衍射峰向高角度偏移,是因为Tm3+取代Bi3+后,晶格间距减小。因而掺杂Tm3+后成功取代了Bi3+,这些结果表明Tm3+成功掺入了Bi2WO6。
 图1
不同Tm3+掺杂量Bi2WO6样品的XRD图
Figure1.
X-ray diffraction patterns of the Bi2WO6 samples doped with different amount of Tm3+
图1
不同Tm3+掺杂量Bi2WO6样品的XRD图
Figure1.
X-ray diffraction patterns of the Bi2WO6 samples doped with different amount of Tm3+
2.2 形貌分析
图 2为不同Tm3+掺杂量Bi2WO6样品的FESEM图及Tm3+掺杂量为6%样品的EDS图谱。观察图 2(a~e)发现所有样品均为一些纳米片组装而成的不规则颗粒。未掺杂Bi2WO6颗粒的纳米片较大,边角规整。而随着Tm3+掺杂量的增加,所得到样品颗粒的纳米片堆积更加松散,边缘遭到破坏呈现出不规则形状,且厚度明显变薄,样品的比表面积得到提高;因此,掺杂Tm3+后,样品的形貌变化有利于提高其光催化活性。图 2f为Tm3+掺杂量为6%时的X射线能谱分析(EDS),从2f中可以看出,EDS分别含有Bi、W、O和Tm元素的主峰,并且没有检测到其它杂质元素的峰,说明所得样品中有Tm元素的存在。
图 3为BWO-3样品的TEM和HRTEM图像。由图 3a可观察到样品中某些颗粒的大小为3~4 μm,颗粒边缘可见许多纳米片。由图 3b可知,样品中的纳米薄片由结晶度较好的纳米片堆叠而成,这些纳米片的粒径为40~80 nm。样品的HRTEM图像(图 3c)可见清晰的晶格条纹,晶面间距分别为0.273和0.315 nm,分别对应于Bi2WO6的(002)和(131)晶面。表 1是Tm3+不同掺量的能谱数据表,从表 1可以看出样品中含有微量的Tm元素,并且随着理论掺杂量的增加,样品中的Tm3+的含量也随之增加。掺杂后样品中的Bi3+与未掺杂的含量相比均有所降低,说明Tm3+已经成功掺入到Bi2WO6中。
Sample nBi/n / % nW/n /% nO/n /% nTm/n /% BWO-O 18.O4 8.84 73.12 O BWO-1 17.56 9.1O 71.15 O.19 BWO-2 17.33 9.27 73.O5 O.35 BWO-3 17.O3 8.92 73.46 O.59 BWO-4 16.63 8.93 73.69 O.75 2.3 拉曼光谱分析
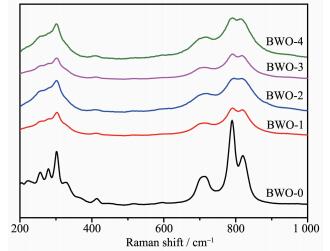
拉曼光谱是研究半导体材料晶格应变的有效方法。图 4为不同Tm3+掺杂量Bi2WO6样品的拉曼光谱图。从图中可以看出,所有样品的拉曼峰主要分布在200~450 cm-1和600~1 000 cm-1范围,其中820和791 cm-1处的峰分别为O-W-O键的对称伸缩振动模和反对称伸缩振动模的拉曼峰,301 cm-1处的峰对应于Bi3+和WO66-的谐振模式,279 cm-1处的峰则对应于Bi-O键的弯曲振动模式,这些结果与文献相一致[30]。与Bi2WO6纯样相比,Tm3+掺杂Bi2WO6样品的拉曼峰位置没有发生明显的偏移,说明掺杂Tm3+后没有改变Bi2WO6的晶型结构。但掺杂Tm3+后样品的拉曼峰强度有所降低,这是由于掺杂Tm3+后样品的结晶性降低,且掺入Tm3+后引起了晶格的应力改变[31],这与XRD的结果是一致的。
2.4 比表面积分析
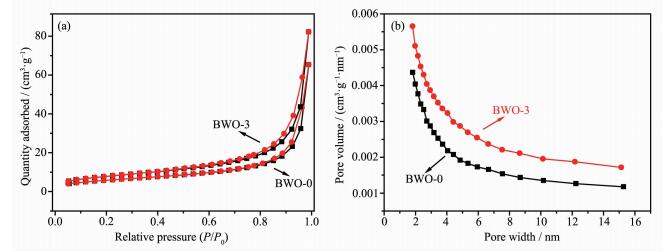
光催化材料的比表面积越大,其表面活性位点越多,可以吸附活性物质和污染物分子,从而使光催化反应更有效。图 5为BWO-0和BWO-3样品的氮气吸附-脱附等温线(图 5a)和孔径分布曲线(图 5b)。其中未掺杂Bi2WO6和不同Tm3+掺杂量样品的比表面积依次为21、26、28、29、23 m2·g-1,说明掺杂Tm3+后,Bi2WO6的晶体生长得到抑制,从而增加了比表面积。BWO-3具有最大的比表面积,因而在光催化方面表现出最优异的性能。从图 5a可知BWO-0和BWO-3样品都为具有滞后环的Ⅳ型吸附-脱附等温线,说明合成产物中存在着介孔结构,图 5b中未掺杂Bi2WO6和Tm3+掺杂样品分别在1.17和1.72 nm的区域中呈现出它们最大的孔径分布。
2.5 紫外-可见漫反射光谱分析
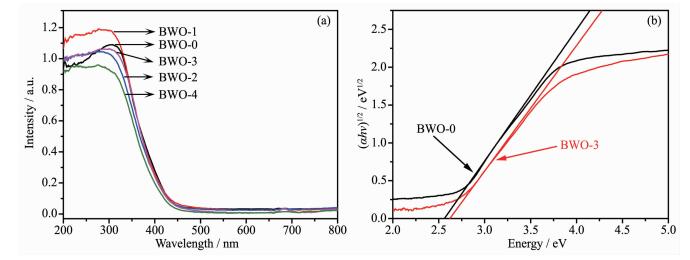
采用紫外-可见吸收光谱测试样品的光吸收性能。图 6a为不同Tm3+掺杂量Bi2WO6样品的紫外-可见吸收光谱。从图中可以看出,所有样品在可见光区域(λ>420 nm)均有明显吸收。掺入Tm3+后,样品在可见光区域均发生了蓝移,BWO-x(x=1,2,3,4)对于可见光的吸收并没有提高。由光子吸收系数(αhν)1/2和光子能量(hν)的关系曲线可估算样品的带隙。如图 6b所示,BWO-0和BWO-3样品的带隙分别为2.55和2.63 eV,掺杂Tm3+后,样品的带隙略有增大。说明带隙不是影响Tm3+提高样品光催化的原因。此结果与文献一致[32-33]。
2.6 荧光光谱分析
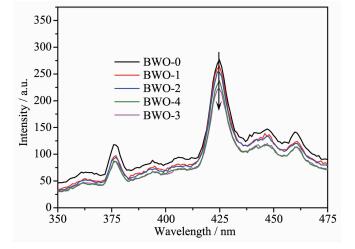
荧光光谱可以研究半导体的电子结构和光学特性,同时反映光生空穴-电子对的复合几率。一般荧光强度越高,复合几率越大。图 7所示为所有样品的荧光光谱。从图 7中可以看出,掺杂后的样品与纯样Bi2WO6相比,发光特征峰位置几乎没有变化,但是强度均有降低,说明掺杂后改善了电子-空穴的分离效率,并且使电子-空穴的复合率得到有效降低,促进了其光催化活性。
2.7 光催化性能
图 8a为不同Tm3+掺杂量Bi2WO6样品对罗丹明B的可见光催化降解效率图。不加催化剂,只加罗丹明B的空白对比实验中,光照射75 min后,罗丹明B几乎不发生降解,说明罗丹明B在具有很好的光稳定性。以Bi2WO6纯相为催化剂时,光照30 min时,罗丹明B的降解率为63.49%。掺杂Tm3+后,Bi2WO6的光催化降解罗丹明B的性能明显优于Bi2WO6纯相;当以BWO-3样品为催化剂时,光照30 min后罗丹明B的降解效率达91.27%,比Bi2WO6纯相提高了27.78%。以BWO-3样品为催化剂,罗丹明B的吸光度变化曲线如图 8b所示,首先进行的是羟基化,主峰消失以后,主要发生脱乙基作用。罗丹明B的最大光吸收特征峰位于553 nm,随着光照时间的增加,罗丹明B的特征峰强度逐渐降低、偏移,最后消失。30 min后溶液的颜色由玫瑰红逐渐变为黄绿色,45 min后溶液已经变成无色澄清溶液,说明罗丹明B被完全降解。图 8c为各样品为催化剂时,焦糖色素的可见光催化降解效率图。光照5 h后,无催化剂时,焦糖色素的降解率较小,说明焦糖色素的光稳定性较好。以Bi2WO6纯相为催化剂时,其降解效率仅为10.03%。但当以Tm3+掺杂Bi2WO6为催化剂时,焦糖色素的降解率得到了明显提高,其中BWO-3样品的降解率达45.25%,是Bi2WO6纯相的4倍。图 8d为以BWO-3样品为催化剂时,焦糖色素的吸光度变化曲线。焦糖色素的光吸收特征峰位于274 nm,随着光照时间的增加,焦糖色素的特征峰强度逐渐降低,说明BWO-3样品可有效催化降解焦糖色素。图 8e表明经过4次光催化循环实验之后,催化剂的光催化活性为初始催化能力的94.23%。因此光催化剂显示了极好的稳定性。
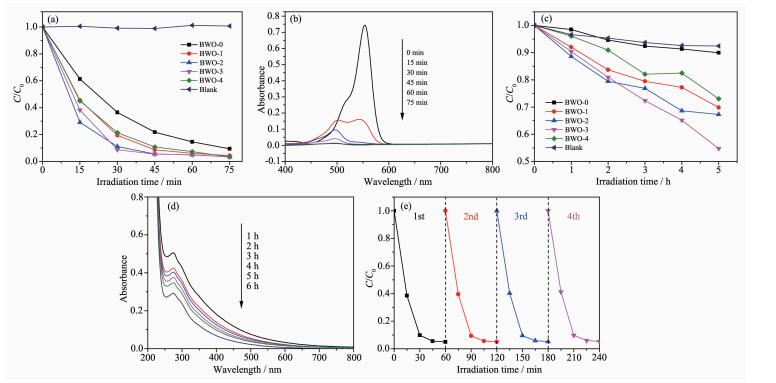 图8
不同Tm3+掺杂量Bi2WO6样品对罗丹明B(a)和焦糖色素(c)的可见光催化降解效率图; 以BWO-3样品为催化剂时, 罗丹明B(b)和焦糖色素(d)吸光度的变化曲线; BWO-3样品在可见光下降解罗丹明B的循环实验(e)
Figure8.
Degradation rates of RhB (a) and caramel (c) under visible-light illumination using Bi2WO6 catalysts doped with different amount of Tm3+ ions; Temporal evolution of the spectra for RhB (b) and caramel (d) mediated by BWO-3 catalyst under visible light illumination (b, d); Recycling degradation curves of BWO-3 sample for RhB (e)
图8
不同Tm3+掺杂量Bi2WO6样品对罗丹明B(a)和焦糖色素(c)的可见光催化降解效率图; 以BWO-3样品为催化剂时, 罗丹明B(b)和焦糖色素(d)吸光度的变化曲线; BWO-3样品在可见光下降解罗丹明B的循环实验(e)
Figure8.
Degradation rates of RhB (a) and caramel (c) under visible-light illumination using Bi2WO6 catalysts doped with different amount of Tm3+ ions; Temporal evolution of the spectra for RhB (b) and caramel (d) mediated by BWO-3 catalyst under visible light illumination (b, d); Recycling degradation curves of BWO-3 sample for RhB (e)
掺杂Tm3+后,Bi2WO6可见光催化性能得到提高的原因是:由XRD,SEM等结果可知,一定量的Tm3+取代Bi2WO6中的Bi3+后,形成了晶格缺陷,降低了光生电子-空穴的复合率;此外,掺杂Tm3+后,样品的比表面积增大,增大了污染物与样品的接触面积,减小了光生载流子迁移到催化剂颗粒表面的距离,加快了光生载流子迁移到颗粒表面的速率,降低了光生电子-空穴对的复合率,从而样品的光催化性能得到了有效提升[34]。并且当掺杂量为6%时,样品因具有最佳的比表面积以及光生电子-空穴复合率,从而具有最好的光催化活性。
3 结论
采用一步水热法合成了纳米片组装而成的Tm3+掺杂Bi2WO6微粒。掺杂Tm3+后,Bi2WO6的可见光催化性能得到了明显提高,当Tm(NO3)3·5H2O的添加量为6%时,样品的催化性能最佳,可见光照射30 min后对罗丹明B的降解率达91.27%。比Bi2WO6纯相提高了27.78%。可见光照射5 h后对焦糖色素的降解率达45.25%,与未掺杂Bi2WO6相比,提高了35.22%。掺杂适量的Tm3+可提高Bi2WO6样品的比表面积,降低样品的光生-电子复合率,从而提高样品的可见光催化性能。
-
-
[1]
Kudo A, Miseki Y. Chem. Soc. Rev., 2009, 38(1):253-27 doi: 10.1039/B800489G
-
[2]
Dong H J, Chen G, Sun J X, et al. Appl. Catal., B, 2013, 134(5):46-54
-
[3]
Yu X L, Shavel A, An X Q, et al. J. Am. Chem. Soc., 2014, 136(26):9236-9239 doi: 10.1021/ja502076b
-
[4]
Kang Y S, Park M K, Kwon Y T, et al. Chem. Mater., 2001, 13(7):2349-2355 doi: 10.1021/cm000858n
-
[5]
Chen X B, Liu L, Huang F Q. Chem. Soc. Rev., 2015, 44(7):2019-2019 doi: 10.1039/C5CS90019K
-
[6]
Leshuk T, Parviz R, Everett P, et al. ACS Appl. Mater. Interfaces, 2013, 5(6):1892-1895 doi: 10.1021/am302903n
-
[7]
Verbruggen S, Keulemans M, Filippousi M, et al. Appl. Catal., B, 2014, 156-157(3):116-121
-
[8]
Li C M, Chen G, Sun J X, et al. Appl. Catal., B, 2014, 160-161(1):383-389
-
[9]
Zhang L S, Prof W W, Zhou L, et al. Small, 2010, 3(9):1618-1625
-
[10]
Zhang N, Ciriminna R, Pagliaro M, et al. Chem. Soc. Rev., 2015, 43(15):5276-5287
-
[11]
Zhang L S, Wang H L, Chen Z G, et al. Appl. Catal., B, 2011, 106(1):1-13
-
[12]
Zhang L W, Man Y, Zhu Y F. ACS Catal., 2011, 1(8):841-848 doi: 10.1021/cs200155z
-
[13]
Fu Y, Chang C, Chen P, et al. J. Hazard. Mater., 2013, 254-255(1):185-192
-
[14]
Shi R, Huang G L, Lin J, et al. J. Phys. Chem. C, 2009, 113(45):19633-19638 doi: 10.1021/jp906680e
-
[15]
Yang Y F, Li Y G, Zhu L P, et al. Nanoscale, 2013, 5(21):10461-10471 doi: 10.1039/c3nr03160h
-
[16]
Tonda S, Kumar S, Kandula S, et al. J. Mater. Chem. A, 2014, 2(19):6772-6780 doi: 10.1039/c3ta15358d
-
[17]
张田, 邹正光, 何金云, 等.无机化学学报, 2017, 33(6):954-962 doi: 10.11862/CJIC.2017.093ZHANG Tian, ZOU Zheng-Guang, HE Jin -Yun, et al. Chinese J. Inorg. Chem., 2017, 33(6):954-962 doi: 10.11862/CJIC.2017.093
-
[18]
Fu H B, Zhang S C, Xu T G, et al. Environ. Sci. Technol., 2008, 42(6):2085-2091 doi: 10.1021/es702495w
-
[19]
王丹军, 岳林林, 郭莉, 等.无机化学学报, 2014, 30(4):961-968 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20140434&flag=1WANG Dan-Jun, YUE Lin-Lin, GUO Li, et al. Chinese J. Inorg. Chem., 2014, 30(4):961-968 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20140434&flag=1
-
[20]
Ding X, Zhao K, Zhang L Z. Environ. Sci. Technol., 2014, 48(10):5823-5831 doi: 10.1021/es405714q
-
[21]
李慧泉, 崔玉民, 吴兴才, 等.无机化学学报, 2012, 28(12):2597-2604 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20121215&flag=1LI Hui-Quan, CUI Yu-Min, WU Xing-Cai, et al. Chinese J. Inorg. Chem., 2012, 28(12):2597-2604 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20121215&flag=1
-
[22]
许青青, 吕亮, 叶冬菊, 等.无机化学学报, 2017, 33(7):1205-1216 doi: 10.11862/CJIC.2017.134Xu Qing-Qing, LÜ Liang, YE Dong-Ju, et al. Chinese J. Inorg. Chem., 2017, 33(7):1205-1216 doi: 10.11862/CJIC.2017.134
-
[23]
Wang W, Ding M Y, Lu C H, et al. Appl. Catal., B, 2014, 144(1):379-385
-
[24]
Wang M, Che Y S, Niu C, et al. J. Rare Earths, 2013, 31(9):878-884 doi: 10.1016/S1002-0721(12)60373-1
-
[25]
Peng S Q, Huang Y H, Li Y X. Mater. Sci. Semicond. Process., 2013, 16(1):62-69 doi: 10.1016/j.mssp.2012.06.019
-
[26]
Huang H W, Liu K, Chen K, et al. J. Phys. Chem. C, 2014, 118(26):14379-14387 doi: 10.1021/jp503025b
-
[27]
Tian N, Zhang Y H, Huang H W, et al. J. Phys. Chem. C, 2014, 118(29):15640-15648 doi: 10.1021/jp500645p
-
[28]
Zhang W H, Yu N, Zhang L S, et al. Mater. Lett., 2016, 163:16-19 doi: 10.1016/j.matlet.2015.09.113
-
[29]
Cao R R, Tian N, Guo Y X, et al. Mater. Charact., 2015, 101(19):166-172
-
[30]
Zhang L W, Wang Y J, Cheng H Y, et al. Adv. Mater., 2009, 40(23):1286-1290
-
[31]
Li C M, Chen G, Sun J X, et al. Appl. Catal., B, 2016, 188:39-47 doi: 10.1016/j.apcatb.2016.01.054
-
[32]
Huang H W, Qi H J, He Y, et al. J. Mater. Res., 2013, 28(21):2977-2984 doi: 10.1557/jmr.2013.296
-
[33]
Wang M, Qiao Z Y, Fang M H, et al. RSC Adv., 2015, 5(115):94887-94894 doi: 10.1039/C5RA19164E
-
[34]
Ni M, Leung M K H, Leung D Y C. Int. J. Hydrogen Energy, 2007, 32(13):2305-2313 doi: 10.1016/j.ijhydene.2007.03.001
-
[1]
-
图 8 不同Tm3+掺杂量Bi2WO6样品对罗丹明B(a)和焦糖色素(c)的可见光催化降解效率图; 以BWO-3样品为催化剂时, 罗丹明B(b)和焦糖色素(d)吸光度的变化曲线; BWO-3样品在可见光下降解罗丹明B的循环实验(e)
Figure 8 Degradation rates of RhB (a) and caramel (c) under visible-light illumination using Bi2WO6 catalysts doped with different amount of Tm3+ ions; Temporal evolution of the spectra for RhB (b) and caramel (d) mediated by BWO-3 catalyst under visible light illumination (b, d); Recycling degradation curves of BWO-3 sample for RhB (e)
表 1 BWO-x (x=0, 1, 2, 3, 4)样品的元素组成
Table 1. Elements composition of BWO-x (x=0, 1, 2, 3, 4)
Sample nBi/n / % nW/n /% nO/n /% nTm/n /% BWO-O 18.O4 8.84 73.12 O BWO-1 17.56 9.1O 71.15 O.19 BWO-2 17.33 9.27 73.O5 O.35 BWO-3 17.O3 8.92 73.46 O.59 BWO-4 16.63 8.93 73.69 O.75 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 2
- 文章访问数: 3394
- HTML全文浏览量: 392




 下载:
下载:







 下载:
下载:

