 图1
不同比例的乙二醇与乙醇混合溶剂中制得的粉体的XRD图
Figure1.
XRD patterns of powders synthesized with different volume ratio of EG and EtOH
图1
不同比例的乙二醇与乙醇混合溶剂中制得的粉体的XRD图
Figure1.
XRD patterns of powders synthesized with different volume ratio of EG and EtOH

Citation: PENG Xiang, CHEN Yu-Jie, LIU Jia-Xiang. Solvothermal Synthesis and Electrical Performance of Cubic ITO Powders[J]. Chinese Journal of Inorganic Chemistry, 2017, 33(10): 1769-1774. doi: 10.11862/CJIC.2017.224

溶剂热法制备立方状ITO粉体及其电性能
English
Solvothermal Synthesis and Electrical Performance of Cubic ITO Powders
-
Key words:
- solvothermal method
- / cubic shape
- / ITO powder
- / electric conductivity
-
0 引言
透明导电氧化物(TCO)因其宽能带隙而有着优异的光电性能[1]。铟锡氧化物(ITO)被认为是性能最好的TCO。ITO薄膜有极高的非线性光学性能,有望成为在光子学应用等领域引起新一轮变革的材料[2]。ITO薄膜作为透明显示电极被广泛应用在平板显示器(FPD)上[3]。ITO薄膜主要通过磁控溅射法制备。磁控溅射法制备ITO薄膜使用的阴极材料是ITO靶材。ITO靶材的密度、纯度和电性能很大程度影响ITO薄膜的质量[4]。而ITO粉体的形貌和粒径极大的影响了ITO靶材性能。立方状粉体由于其粉体粒子之间接触面积大,具有较小的电阻率,而小粒径的纳米颗粒具有较高的致密化驱动力,很多学者致力于这方面的研究。溶剂热法制备纳米粉体具有粒径小、团聚程度低、结晶度高等优点,并可以实现一步制备氧化物粉体的目的,制备工艺简单,产品性能优异[5]。Sasaki等[6]以乙二醇为溶剂通过改变NaOH浓度实现了立方状ITO纳米粉体粒径在15.1~43.5 nm的可控制备,并研究了Sn与In物质的量之比对粉体电阻率的影响。更小粒径的ITO纳米粉体及其导电性研究却鲜有报道[7-8]。本文采用了溶剂热法实现了ITO纳米粉体较小粒径的制备,研究了溶剂比例(体积比,下同)、NaOH浓度对粉体的XRD衍射峰强度比I400/I222和导电性的影响,并阐述了其影响机理。
1 实验方法
1.1 实验步骤
溶剂总体积为80 mL,分别添加不同比例的优级纯乙二醇(EG)与乙醇(EtOH),分为5组:(a) EG,(b) VEG:VEtOH=4:1,(c) VEG:VEtOH=1:1,(d) VEG:VEtOH=1:4,(e) EtOH。分别加入3.818 g(10 mmol)纯度大于99.99%的In(NO3)3·4.5H2O,1.909 g(5.4 mmol)纯度大于99.99%的SnCl4·5H2O至完全溶解,在65 ℃条件下分别加入适量优级纯NaOH,使溶液中NaOH浓度分别为0.275,0.550,0.825 mol·L-1,搅拌至完全溶解得到澄清混合溶液,置于100 mL水热反应釜中,在250 ℃下分别反应不同时间得到深蓝色ITO粉体沉淀。将制得的粉体用电阻大于15 MΩ的去离子水洗涤至无杂质离子,于真空干燥箱中干燥24 h制得ITO纳米粉体颗粒。
1.2 测试与表征
采用D8 AdvanceX射线衍射仪对ITO粉体的物相进行表征(Cu Kα,λ=0.154 056 nm,管电压40 kV,管电流40 mA,扫描角度范围2θ为10°~90°),FEIT-20型透射电镜对ITO粉体形貌进行表征(200 kV)。通过测量100个ITO纳米粉体粒径计算其平均粒径。将ITO粉体压成直径为15 mm的薄圆片,采用型号为SX1934四探针电阻仪测量ITO粉体样品的电阻率,根据电阻率计算电导率。
2 结果与讨论
2.1 溶剂不同比例对ITO粉体物相、形貌的影响
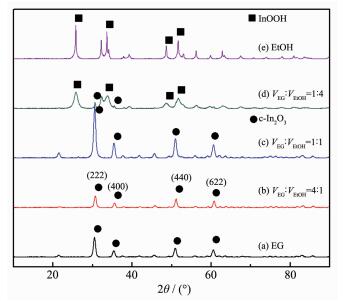
图 1为在不同比例的乙二醇与乙醇混合溶剂中250 ℃下反应12h,且NaOH浓度为0.550 mol· L-1时制得的粉体的XRD图。由图 1可知当溶剂全部为乙二醇以及VEG:VEtOH为4:1,1:1时,产物全部为立方相ITO(PDF No.06-0416),当溶剂比例为1:4时,产物中六方相ITO前驱体InOOH占主要成分,掺杂部分立方相ITO;当溶剂全部为乙醇时,产物全部为InOOH相。
 图1
不同比例的乙二醇与乙醇混合溶剂中制得的粉体的XRD图
Figure1.
XRD patterns of powders synthesized with different volume ratio of EG and EtOH
图1
不同比例的乙二醇与乙醇混合溶剂中制得的粉体的XRD图
Figure1.
XRD patterns of powders synthesized with different volume ratio of EG and EtOH
图 2为不同溶剂比例制得的粉体的TEM照片。由图 2可知,乙二醇与乙醇的比例对粉体的形貌和粒径有较大的影响,纯乙二醇作溶剂制得平均粒径14.7 nm的立方状ITO纳米颗粒,当VEG:VEtOH=4:1时,产物形貌为分散性良好、立方状ITO纳米颗粒,平均粒径为10.7 nm,与Scherrer公式计算出的粒径基本符合,说明加入适量的乙醇可以降低立方状ITO粉体的粒径。当溶剂比例为1:1时,出现部分球形颗粒,且平均粒径为18.3 nm,粒径随球形颗粒的出现变大。随乙醇掺杂比例的升高,产物由立方相氧化物转变为六方相氢氧化物。当VEG:VEtOH=1:4时,粉体主要为分散性较好的不规则球形颗粒,夹杂部分棒状颗粒和立方状颗粒,平均粒径为10.2 nm。可见,溶剂全部为乙醇时,前驱体粉体出现团聚,主要为不规则球形颗粒,夹杂有棒状颗粒,没有立方状颗粒,粉体平均粒径为9.8 nm。随混合溶剂中乙醇掺杂比例的升高,平均粒径先减小后增大,颗粒基本为立方状,粒径的变化与溶剂的粘度有关。当乙醇的掺杂比例继续升高时,颗粒形貌由立方状逐渐向不规则球状转变,并有棒状颗粒生成。
2.2 不同溶剂热反应时间对ITO粉体颗粒形貌的影响
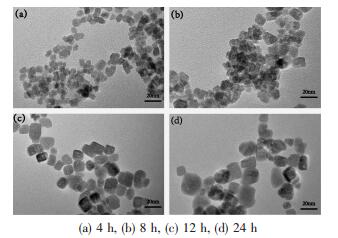
图 3为VEG:VEtOH=4:1时,NaOH浓度为0.550 mol·L-1,不同反应时间制得的ITO纳米粉体的TEM照片。由图 3可知,反应时间为4 h时,制得的ITO纳米颗粒平均粒径为8.4 nm,形貌近似立方状。当反应时间增加到8 h,制得的ITO纳米颗粒出现团聚,平均粒径为9.2 nm,形貌近似为立方状。当反应时间增加至12 h,产物为分散性良好,平均粒径为10.7 nm的立方状ITO纳米颗粒。当反应时间为24 h时,产物为平均粒径14.6 nm,分散性良好的立方状ITO纳米颗粒。邓小玲等[9]发现在乙二醇为溶剂的反应条件下,随溶剂热反应时间的增加ITO纳米颗粒不会长大,而乙二醇与乙醇作溶剂时纳米颗粒长大较明显,说明乙醇的添加改变了溶剂的性质。
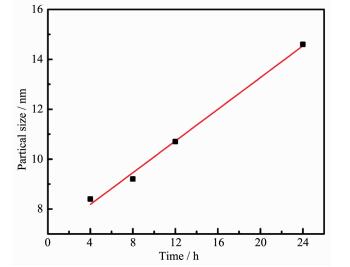
图 4为溶剂热反应时间与粒径的关系图。由图 4可知,反应时间与粉体粒径呈线性关系,关系式为式1(R2=0.992 3):
其中:D为粉体的平均粒径,nm;t为溶剂热反应时间,h。
2.3 不同NaOH浓度对ITO纳米粉体的物相及形貌影响
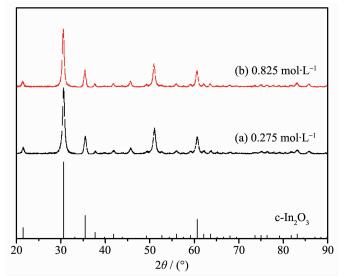
图 5为当VEG:VEtOH=4:1时,添加不同浓度的NaOH对ITO纳米粉体物相的影响。由图 5可知,不同NaOH浓度下制得的ITO纳米粉体均为In2O3晶体结构,与标准XRD卡片(PDF No.06-0416)一致,说明在0.275~0.825 mol·L-1范围内,NaOH浓度对ITO纳米粉体物相组成没有影响。
图 6为VEG:VEtOH=4:1时,添加不同浓度NaOH制得的ITO纳米粉体颗粒的TEM照片。由图 6可知,当NaOH浓度为0.275 mol·L-1时,ITO纳米粉体颗粒形貌为立方状,平均粒径为16.2 nm。当NaOH浓度为0.825 mol·L-1时,得到的粉体颗粒形貌为不规则球形,平均粒径为9.4 nm。根据溶解-再沉淀机理[10],添加少量的NaOH时,晶体成核速率较低,晶粒增长速率较块,最终生长为立方状晶粒,且其粒径较大。随着NaOH浓度的增加,晶体的成核速率就会变大,晶粒增长速率相对较小,最终粒径变小,形貌变为不规则球形。说明NaOH浓度对粉体的粒径和形貌均有较大影响。
2.4 溶剂热法制备的ITO纳米粉体电导性
采用溶剂热法得到的ITO纳米粉体是深蓝色的,对混合溶剂(VEG:VEtOH=4:1)制得的粉体进行XPS测试,通过XPS全谱(限于篇幅本文略)显示有In、O、Sn三种元素组成,并没有其他的杂质,这与XRD结果相一致;由O1s的XPS谱图显示氧元素有3个结合能峰位,分别是:529.9、531.1和531.7 eV,3个结合能峰位分别对应In-O键中的氧、Sn-O键中的氧以及存在缺陷时In-O键中的氧[11],其中氧空位的含量为32.526%。张怡青等[12]通过共沉淀法制备了黄绿色ITO纳米粉体,XPS分析结果显示黄绿色立方相ITO纳米粉体的氧空位含量为27.282%。研究也表明蓝色ITO粉体由于存在更多的氧空位,有着更高的载流子浓度,导电性也越高[13-14]。文献[15-16]指出X射线衍射峰强度较大的粉体具有较高的霍尔迁移率和较低的电阻。粒径也是影响电导率的关键因素,Ali等[17]发现薄膜电阻率与粉体晶粒大小成指数关系。XRD衍射峰强度比也可反映产物的电导率信息,Kamei等[18-19]发现沿(111)面生长的ITO薄膜具有不均匀的氧空位分布,容纳更多的间隙氧原子,间隙氧原子可以与ITO晶格中的替代Sn原子结合降低载流子浓度,因此(111)ITO薄膜总是比(100)薄膜导电性差,要想得到高密度自由电子的ITO纳米粉体必须要抑制(111)面的取向增长, 而相对自由电子密度可以用XRD衍射峰强度比I400/I222来表征。
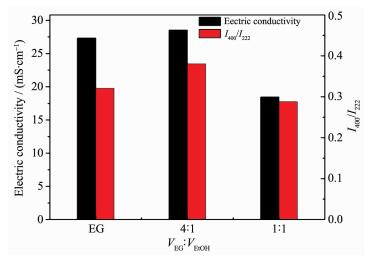
图 7为不同比例的乙二醇与乙醇混合溶剂中对应的粉体电导率与XRD衍射峰强度比I400/I222比值。由图 7可知,粉体电导率数值基本与I400/I222数值变化趋势相对应,当溶剂为乙二醇时,粉体的电导率较高,这是由于粉体的粒径较大,比表面积较低,电子在粉体表面散射程度较小,且形貌为立方状,XRD衍射峰强度较高,因此电导率较高。当溶剂比例VEG:VEtOH=4:1时,I400/I222最高为0.380,电导率最高。
Lee等[20]研究发现随溶剂粘度的增加,I400/I222逐渐增加。同时添加NaOH、In(NO3)3·4.5H2O和SnCl4·5H2O时,不同乙二醇与乙醇体积比的溶液粘度在表 1列出。该实验结果基本和虞大红[21]的拟二元溶质聚集模型相一致。即添加一定量的乙醇在某种程度上可增加溶剂的粘度。当溶剂比例VEG:VEtOH=4:1时,溶剂粘度增加,即部分乙醇的添加使分子间作用力变大,压缩了晶粒生长的空间,使其粒径变小。当溶剂比例VEG:VEtOH=1:1时,I400/I222降低了,这是由于溶剂粘度降低,分子间作用力变小,并出现部分球形颗粒,球形颗粒与其他颗粒间为点接触,使接触面积变小,电子散射增大,电导率下降。
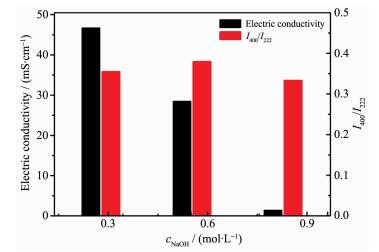
VEG:VEtOH Viscosity/(Pa·s) Ethylene glycol 0.011 4:1 0.033 1:1 0.013 图 8为不同浓度NaOH制备的ITO纳米粉体电导率和I400/I222比值曲线。韩兰英等[22]发现,随无机盐添加量的增加,烷基醚硫酸盐(AES)水溶液粘度先变大后变小。由图 8可知,添加少量NaOH时I400/I222较小,这是由于NaOH添加量较少,溶液中In3+和Sn4+浓度较高,溶液粘度较低,但其形貌为立方状,粒径小,XRD衍射峰强度高,导电率最高为46.75 mS·cm-1。继续增加NaOH浓度导致In3+和Sn4+减少,溶剂粘度增加,I400/I222也增加,粒径变小。添加过量NaOH导致溶液Na+电解质浓度增大,溶液粘度变小,且碱性变强,晶粒成核速率变强大,形貌为不规则球形,不利于I400/I222增大,导电性变差。
3 结论
使用乙二醇与乙醇作溶剂,且其比例VEG:VEtOH=4:1时制备出粒径为10.7 nm、分散性良好的立方状ITO纳米粉体;通过改变不同溶剂热反应时间,得出溶剂热反应时间与粉体粒径成线性关系,关系式为D=0.317 8+6.910 7t;改变NaOH的添加浓度,制得不同粒径和形貌的ITO纳米粉体颗粒。
乙二醇与乙醇作溶剂且其比例VEG:VEtOH=4:1,NaOH浓度为0.550 mol·L-1时,制得粉体I400/I222最高值为0.380;乙二醇与乙醇作溶剂且其比例为4:1,NaOH浓度为0.275 mol·L-1时, 粉体电导率最高为46.75 mS·cm-1。
-
-
[1]
钟志有, 陆轴.化工新型材料, 2016, 44(8):62-64ZHONG Zhi-You, LU Zhou. New Chemical Materials, 2016, 44(8):62-64
-
[2]
Alam M Z, De Leon I, Boyd R W. Science, 2016, 353(6287):795-797
-
[3]
Sunde T O L, Einarsrud M-A, Grande T. J. Eur. Ceram. Soc., 2013, 33(3):565-574 doi: 10.1016/j.jeurceramsoc.2012.09.023
-
[4]
段雨露, 叶锐, 闫星辰, 等.粉末冶金材料科学与工程, 2014, 19(13):413-419DUAN Yu-Lu, YE Rui, YAN Xing-Chen, et al. Materials Science and Engineering of Powder Metallurgy, 2014, 19(13):413-419
-
[5]
古映莹, 冯圣生, 张丽娟, 等.稀有金属, 2006, 30(4):466-468GU Ying-Ying, FENG Sheng-Sheng, ZHANG Li-Juan, et al. Chinese Journal of Rare Metal, 2006, 30(4):466-468
-
[6]
Sasaki T, Endo Y, Nakaya M, et al. J. Mater. Chem., 2010, 20:8153-8157 doi: 10.1039/c0jm01338b
-
[7]
Senthilkumar V, Senthil K, Vickraman P. Mater. Res. Bull., 2012, 47(4):1051-1056 doi: 10.1016/j.materresbull.2011.12.040
-
[8]
Huaman J L C, Tanoue K, Miyamura H, et al. New J. Chem., 2014, 38(8):3421-3428 doi: 10.1039/C4NJ00061G
-
[9]
邓小玲, 陈清清, 孟建新.无机化学学报, 2009, 25(6):991-994 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20090608&flag=1DENG Xiao-Ling, CHEN Qing-Qing, MENG Jian-Xin. Chinese J. Inorg. Chem., 2009, 25(6):991-994 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20090608&flag=1
-
[10]
Hirano M, Kato E. J. Am. Ceram. Soc., 1999, 82(3):786-788
-
[11]
Choi C H, Han S Y, Su Y W, et al. J. Mater. Chem. C, 2015, 3:854-860 doi: 10.1039/C4TC01568A
-
[12]
张怡青, 刘家祥.无机化学学报, 2017, 33(2):249-254 doi: 10.11862/CJIC.2017.041ZHANG Yi-Qing, LIU Jia-Xiang. Chinese J. Inorg. Chem., 2017, 33(2):249-254 doi: 10.11862/CJIC.2017.041
-
[13]
Ba J H, Fattakhova-Rohlfing D, Feldhoff A, et al. Chem. Mater., 2006, 18(12):2848-2854 doi: 10.1021/cm060548q
-
[14]
Shimada S, Mackenzie K J D. J. Cryst. Growth, 1981, 55:453-456 doi: 10.1016/0022-0248(81)90101-9
-
[15]
Kim D, Han Y, Cho J S, et al. Thin Solid Films, 2000, 377(388):81-86
-
[16]
Thilakan P, Kumar J. Vacuum, 1997, 48(5):463-466 doi: 10.1016/S0042-207X(96)00309-0
-
[17]
Ali D, Butt M Z, Muneer I, et al. Optik, 2017, 128:235-246 doi: 10.1016/j.ijleo.2016.10.028
-
[18]
Kamei M, Shigesato Y, Takaki S. Thin Solid Films, 1995, 259:38-45 doi: 10.1016/0040-6090(94)06390-7
-
[19]
Kamei M, Enomoto H, Yasui I. Thin Solid Films, 2001, 392:265-268 doi: 10.1016/S0040-6090(01)01041-0
-
[20]
Lee J S, Choi S C. J. Eur. Ceram. Soc., 2005, 25(14):3307-3314 doi: 10.1016/j.jeurceramsoc.2004.08.022
-
[21]
虞大红, 刘洪来, 胡英.华东化工学院学报, 1991(2):159-164YU Da-Hong, LIU Hong-Lai, HU Ying. Journal of East China Institute of Chemical Technology, 1991(2):159-164
-
[22]
韩兰英, 陈光定.上饶师专学报, 1997, 17(6):53-56HAN Lan-Ying, CHEN Guang-Ding. Journal of Shangrao Teachers College, 1997, 17(6):53-56
-
[1]
-
表 1 不同乙二醇与乙醇体积比溶液的粘度
Table 1. Viscosity of the solution with different volume ratios of EG to EtOH
VEG:VEtOH Viscosity/(Pa·s) Ethylene glycol 0.011 4:1 0.033 1:1 0.013 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 4
- 文章访问数: 3505
- HTML全文浏览量: 257




 下载:
下载:







 下载:
下载:

