
Citation: FENG Yong-Lan, KUANG Dai-Zhi, ZHANG Fu-Xing, YU Jiang-Xi, JIANG Wu-Jiu, ZHU Xiao-Ming. Two Di-n-butyltin Carboxylates with a Sn4O4 Ladder-like Framework: Microwave Solvothermal Syntheses, Structures and in Vitro Antitumor Activities[J]. Chinese Journal of Inorganic Chemistry, 2017, 33(5): 830-836. doi: 10.11862/CJIC.2017.107

两个具有Sn4O4梯状结构二丁基锡羧酸酯的微波溶剂热合成、结构和体外抗癌活性
English
Two Di-n-butyltin Carboxylates with a Sn4O4 Ladder-like Framework: Microwave Solvothermal Syntheses, Structures and in Vitro Antitumor Activities
-
0 引言
有机锡卤化物或氧化物前体与含氧 (氮、硫) 配体反应产生的有机锡化合物,具有结构多变和良好的生物活性等特点而备受人们关注[1-2]。在与有机锡反应的配体中,有机酸作为含氧多齿桥联配基,既可与锡形成简单的R′C (O) O-SnRx(A型)[3-4]、也可形成含配键[C=O→Sn](B型) 的有机锡羧酯[5],在B型结构中,通过羧基 (Sn-O-C=O→Sn) 桥联作用还可形成链状、环状,以及μ2-O,μ3-O桥联多锡结构的有机锡化合物[6-8]。近年来,在含O、N配基中,R2SnCl2或R3SnCl脱烃基水解[9-11]、R2SnO与有机酸反应[12-13],合成由 (μ3-O) Sn3构筑、中心结构具有[SnO]n的有机锡氧簇合物,引起合成化学工作者广泛兴趣。我们对苄基氯化锡的水解、丁基氧化锡与有机羧酸反应,也进行了初步实验探索[14-16],并利用微波辐射合成有机锡羧酸酯取得良好效果[16-18],微波辐射比传统的合成方法有着高效、简便等优点[19],本文报道微波甲醇溶剂热中,二丁基氧化锡 (n-Bu2Sn=O) 与有机芳香酸 (4-甲基苯甲酸、4-二甲氨基苯甲酸) 的反应,合成了2个中心具有四元环梯状结构的二丁基锡羧酸酯化合物。初步测试了化合物对5种人体外抗肿瘤生物活性。
1 实验部分
1.1 仪器与试剂
合成反应在微波有机合成系统 (Micro SYNT Labstation for Microwave assisted意大利) 完成。化合物的C、H和N组成用PE-2400(Ⅱ) 元素分析仪;红外光谱用Prestige-21(岛津, 400~4 000 cm-1) 光谱仪;1H NMR、13C NMR谱用Bruker INOVA-400 NMR测定,四甲基硅烷 (TMS) 内标,119Sn NMR用Bruker INOVA-500 NMR光谱仪测定,四甲基锡 (Me4Sn) 内标;晶体分子结构测定用Bruker Smart Apex Ⅱ CCD单晶衍射仪;热稳定性分析用德国NETZSCH TG 209 F3热重分析仪;化合物的熔点用北京泰克XT-4双目体视显微熔点仪测定 (温度计未经校正)。试剂购自上海太阳化学科技有限公司和上海晶纯试剂有限公司。
1.2 化合物的合成
取1 mmol二 (正丁基) 氧化锡、1 mmol芳香酸 (4-甲基苯甲酸、4-二甲氨基苯甲酸)、30 mL甲醇,置于聚氟乙烯反应瓶中,设置微波有机合成系统120 ℃微波辐射反应2 h,冷却至室温,过滤,减压蒸发溶剂,固体重结晶得产物,在适当溶剂中培养晶体,用于晶体结构测定。
无色晶体1,产率:75.6%(基于n-Bu2SnO),m.p. 158~160 ℃。1H NMR (CDCl3,400 MHz):δ 0.90(t,24H,J=6.4 Hz, -CH3, Butyl-H), 1.38~1.69(m, 48H, SnCH2CH2 CH2,Butyl-H), 2.40(s, 6H,Ar-CH3),3.49(s,6H,-OCH3),7.19(s, 4H, Ar-H), 7.88(s, 4H, Ar-H);13C NMR (CDCl3,100 MHz):δ 13.63~27.87(n-Bu-C),21.47(Ar-CH3),50.86,51.06(-OCH3),128.62,129.75,131.70,141.53(Ar-C),172.74(-COO); 119Sn NMR (CDCl3,186 MHz):δ-212.96, -213.95。IR (KBr,cm-1):1 623 νas(COO-),1 405νs(COO-),619 ν(Sn-O-Sn),551 ν(Sn-C),420 ν(Sn-O)。元素分析按C50H92O8Sn4计算值 (%):C 46.33,H 7.15;实测值 (%):C 46.61,H 7.30。
无色晶体2,产率:61.3%(基于n-Bu2SnO),m.p. 224~226 ℃。1H NMR (CDCl3,400 MHz):δ 0.90(t,24H,J=7.2 Hz,-CH3,Butyl-H);1.38~1.69 (m,48H,Sn CH2CH2CH2,Butyl-H),2.89(d,12H,-N (CH3)2),3.49(s,6H,-OCH3),6.66(s,4H,Ar-H),7.88(s,4H,Ar-H);13C NMR (CDCl3,100 MHz):δ 13.67~27.95(n-Bu-C),40.21(-N (CH3)2), 50.83, 51.22(-OCH3), 110.73, 121.63, 131.30, 152.59(Ar-C);172.58(-COO);119Sn NMR (CDCl3,186 MHz):δ-174.41,-215.25。IR (KBr,cm-1):1 606νas(COO-),1 349 νs(COO-),602 ν(Sn-O-Sn),551 ν(Sn-C),419 ν(Sn-O)。元素分析按C52H98N2O8Sn4计算值 (%):C 46.12,H 7.29,N 2.07;实测值 (%):C 46.31,H 7.34,N 2.09。
1.3 X射线晶体衍射
选取大小分别为0.20 mm×0.19 mm×0.17 mm (1) 和0.20 mm×0.20 mm×0.20 mm (2) 的晶体,在Bruker Smart Apex Ⅱ CCD单晶衍射仪上,采用经石墨单色化的Mo Kα射线 (λ=0.071 073 nm),在室温下以φ~ω扫描方式收集衍射数据。1在1.72°~27.00°范围内收集衍射点;2在1.69°~27.00°范围内收集点。衍射强度数据经多重扫描吸收校正,晶体结构中大部分非氢原子由直接法解出,其余部分非氢原子在随后的差值傅立叶合成中陆续确定,对所有非氢原子坐标及其温度因子采用全矩阵最小二乘法精修。由理论加氢法给出氢原子在晶胞中的位置坐标,对氢原子和非氢原子分别采用各向同性和各向异性热参数精修,全部结构分析工作在WINGX上调用SHELX-97程序[20]完成。化合物的主要晶体学数据列于表 1。
Compound 1 2 Empirical formula C50H92O8Sn4 C52H98N2O8Sn4 Formula weight 1 296.00 1 354.08 Crystal system Monoclinic Monoclinic Space group P21/n P21/n a / nm 1.359 54(6) 1.347 88(8) b/ nm 1.391 80(5) 1.391 05(9) c / nm 1.644 11(6) 1.745 35(11) β/(°) 106.775(2) 107.310(3) V/ nm3 2.978 6(2) 3.124 3(3) Z 2 2 Dc/(Mg·m-3) 1.445 1.439 Absorption coefficient / mm-1 1.701 1.626 F(000) 1312 1376 Limiting indices (h, k, l, ) -8~16, -13-16, -19-19 -16-17, -18-14, -22-22 Reflections collected 16 591 20 755 Unique reflections (Rint) 5 245 (0.039 3) 7 070 (0.023 7) Data with I>2σ(I) 2 978 5 140 Data, restraints, parameters 5 245, 138, 281 7 070, 20, 298 Goodness of fit on F2 1.276 1.062 Completeness 0.998 0.99 R1, wR2 [I>2σ(I)] 0.067 9, 0.201 5 0.038 1, 0.099 7 R1, wR2(all data) 0.118 4, 0.230 9 0.058 9, 0.118 1 (△ρ)max,(△ρ) min/ (e·nm-3) 763, -641 580, -542 表 1 化合物的晶体学数据
Table 1. Crystallographic data of the compoundsCCDC:892010,1;839191,2。
1.4 抗肿瘤活性测定
HT-29,HEPG2,MCF-7,KB和A549细胞取自美国组织培养库,用含10%牛胎血清的RPMI1640培养液,在含5%CO2(V/V) 的培养箱内于37 ℃下培养,用MTT法检测细胞增殖与生长抑制情况,调整实验细胞数量使在570 nm获得1.3到2.2的吸光度,将化合物测试药液 (0.1 nmol·L-1~10 μmol·L-1) 设置6个浓度,每个浓度至少3个平行和3次重复实验。应用GraphPad Prism 5.0软件统计分析确定IC50值。
2 结果与讨论
2.1 晶体结构
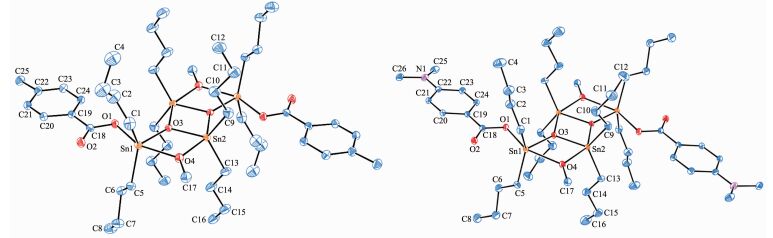
化合物的晶体分子结构见图 1,晶体属单斜晶系,P21/n空间群,主要键长和键角见表 2。晶体分子结构分析表明,化合物由2个芳香酸、4个二丁基锡和2个甲醇组成,其中甲醇氧以μ2-O桥联Sn1和Sn2,另一个氧以μ3-O桥联Sn1和Sn2之外,还桥联对称结构的Sn2A原子,形成Sn4O4架构的三梯状化合物。虽梯中四元环的Sn-O键长、键角∠Sn-O-Sn、∠O-Sn-O各不相等,但整个梯以中间四元环的中心为对称中心,且四元环内4个原子构成的二面角∠Sn-O-Sn-O和∠O-Sn-O-Sn、梯形与羧基构成的二面角均在0°~0.65°,因此,中心结构原子具有良好的共平面性。O1和O4、O3A和O4分别占据着Sn1和Sn2为中心的轴向位置, ∠O1-Sn1-O4为152.65(15)°, ∠O3A-Sn2-O4为146.45(14)°, O3、C1、C5和O3、C9、C13分别占据赤道位置,且O3、C9、C13和Sn2几乎共平面,其4个原子的二面角分别为0.43° (1),1.01° (2),但受Sn1…O2的影响,O3、C1、C5和Sn1原子偏离平面较多,它们的二面角分别为15.31°(1) 和16.31° (2)。4个Sn原子连同8个丁基分别位于平面两边形成对称。梯端的羧基和甲醇分子沿梯环平面向外延展,如MMTA[10]、吡啶-4-甲酸[16]、3,4-二甲氧基苯甲酸和N-(对甲苄基) 羟胺[15]等,因此,配基对中心骨架结构和Sn-O键长的影响不明显,但平面上基团的空间效应影响梯形结构,如以苄基替代丁基的类似化合物中,由于苄基比丁基的基团位阻大,锡 (Sn1和Sn2) 与苄基碳形成的Sn-CH2Ph键长比与丁基碳 (C1、C4、C9和C13) 形成的键更长,丁基碳与氧 (O3、O3A和O4) 形成的所有键角均不相等,羧基与梯端Sn1形成Sn1-O1共价键,羧基另一氧原子与Sn1形成分子内的弱作用,Sn1与O2距离分别为0.283 4 nm (1) 和0.284 4 nm (2),远低于范德华半径之和 (0.368 nm)[21],因此,Sn1与配基原子形成比Sn2与配基原子形成的三角双锥六面体畸变程度更高。
1 2 1 2 Sn1-C1 0.209 7(11) 0.211 6(6) Sn2-O3 0.203 5(4) 0.203 3(3) Sn1-C5 0.199 6(10) 0.210 8(6) Sn2-O4 0.212 8(5) 0.213 0(3) Sn2-C9 0.207 6(10) 0.210 9(6) Sn2-O3A 0.213 1(4) 0.212 9(3) Sn2-C13 0.203 3(9) 0.211 9(6) Sn2A-O3 0.213 1(4) 0.212 9(3) Sn1-O1 0.213 4(5) 0.213 2(3) C18-O1 0.125 5(10) 0.131 5(5) Sn1-O3 0.200 9(4) 0.202 7(3) C18-O2 0.121 3(10) 0.122 2(6) Sn1-O4 0.224 1(5) 0.226 9(3) C17-O4 0.145 6(10) 0.142 6(6) O3-Sn1-C1 112.8(4) 110.8(2) C13-Sn2-C9 116.0(4) 120.8(3) O3-Sn1-O1 81.87(19) 81.31(12) O3-Sn2-O4 72.64(18) 73.48(12) C1-Sn1-O1 102.2(3) 102.2(2) C13-Sn2-O4 98.9(4) 97.8(2) O3-Sn1-C5 118.1(4) 112.3(2) C9-Sn2-O4 98.7(3) 97.8(2) C1-Sn1-C5 125.3(5) 132.8(3) O3-Sn2-O3A 73.96(19) 73.39(12) O1-Sn1-C5 103.4(4) 102.4(2) C13-Sn2-O3A 99.4(3) 98.4(2) O3-Sn1-O4 70.71(18) 70.65(11) C9-Sn2-O3A 98.0(3) 98.4(2) C1-Sn1-O4 87.8(4) 87.98(19) O4-Sn2-O3A 146.59(19) 146.87(12) O1-Sn1-O4 152.6(2) 151.96(12) Sn1-O3-Sn2 114.46(19) 114.27(13) C5-Sn1-O4 90.9(4) 88.8(2) Sn1-O3-Sn2A 139.5(2) 139.12(14) O3-Sn2-C13 122.0(3) 118.9(2) Sn2-O3-Sn2A 106.05(19) 106.61(12) O3-Sn2-C9 121.9(3) 120.4(2) Symmetry codes: A:-x+1, -y+2, -z for 1; A:-x, -y+2, -z+2 for 2 表 2 化合物的部分键长和键角
Table 2. Selected bond lengths (nm) and angles (°) for 1 and 22.2 构象理论分析
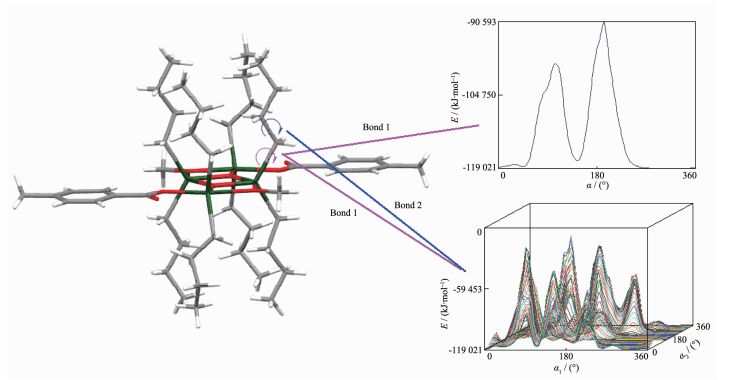
理论上,四元环梯形骨架平面结构的形成要求基团之间要有适度的空间。因此,羧基与二丁基氧化锡反应,应优先形成空间效应较小的 (A) 型丁基锡羧酸酯化合物[22]。标题化合物的合成存在,引起我们对结构的思考。晶体结构分析表明,位于平面上、下排列的丁基,通过Sn2-C键向梯外偏离10°~30°,∠O3-Sn2-C在100°~120°之间,以形成“稳定”结构,尽管产生梯状骨架结构的原因需进一步研究,但基团的空间位阻可能是重要因素。为了探索这种梯状骨架平面上基团取向对分子体系能的影响,我们以化合物1的晶体结构为例,考察了化合物1晶胞中丁基Sn2-C9键旋转360°产生的各个构象和对应的Lennard-Jones作用能之间的关系。理论计算表明,Sn2-C9键旋转所构成的E-α图如图 2(右上图),可见Sn2-C9单键旋转过程与基团间的作用有2个主要能垒,其中最大能垒E为28 340 kJ·mol-1,说明空间位阻较大,Sn2-C9单键不能自由旋转。还存在多个低能Eα构象:E0°=-119 021 kJ·mol-1,E44°=-118 675 kJ·mol-1,E144°=-117 512 kJ·mol-1,E289°=-119 016 kJ·mol-1,E339°=-119 021 kJ·mol-1,晶体结构正处于最低能构象 (α=0°),使化合物稳定。基于此,我们进一步考察了晶胞中Sn2-C9(Bond 1) 和C9-C10(Bond 2) 键同时旋转产生的构象和作用能,结果形成如图 2(右下图) 的E-α1, α2曲面图,出现有多个较大能垒Eα1, α2,阻碍丁基的位移。也形成27个低能构象,其中最低能构象正是晶体结构E0°, 0°时的构象,这可能是化合物梯形骨架平面结构能稳定存在的重要原因,也为苯基、环已基锡化合物空间位阻太大不能形成类似结构提供了理论参考。
2.3 谱学性质
有机锡羧酸酯的红外光谱特征峰νas(COO) 与νs(COO) 之差Δν为218 cm-1 (1)、257 cm-1 (2), 均大于200 cm-1,表明羧基>C=O的氧与锡未形成C=O→Sn配键,羧基的C=O双键和C-O单键有明显的差异,羧基氧与锡形成单齿 (A型) 化合物[23-24]。551cm-1 ν(Sn-C)[25],420(1)、419(2) cm-1 ν(Sn-O) 和619(1)、602(2) cm-1 ν(Sn-O-Sn) 特征峰佐证了化合物的结构[26]。化合物1和2中丁基、甲氧基的1H NMR,以及丁基、甲氧基和羧基的13C NMR谱的化学位移相似。化合物1和2分别受甲基和二甲氨基的影响,苯环的13C NMR化学位移有所不同。在119Sn NMR上4个Sn原子只出现2种锡119Sn的谱线。以上表征均支持化合物的结构与X射线晶体衍射实验结果一致。
2.4 化合物1的热稳定性
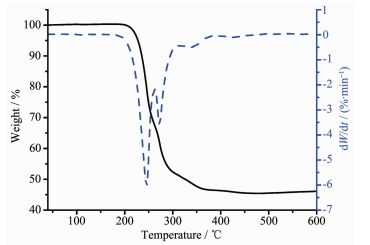
为了研究化合物的热稳定性,在空气氛下,以20 ℃·min-1的加热速度和20 mL·min-1气体流速,在40~600 ℃范围内,对化合物1进行热重测试,研究其热稳定性,结果如图 3。可见随温度的升高,化合物1在40~220 ℃范围几乎未发现失重,但在大于220 ℃时化合物明显失重,410 ℃后残余物恒重在46.1%,在220~410℃范围失重53.9%,若以化合物分解失去有机基团,残余物为SnO2计算,理论值为46.52%,与实验结果相吻合,因此,化合物1在低于220 ℃可稳定存在。
2.5 抗肿瘤活性
表 3列出化合物1、2及顺铂对体外肿瘤细胞 (人结肠癌 (HT-29)、肝癌细胞 (HepG2)、乳腺癌 (MCF-7)、鼻咽癌 (KB) 和肺癌细胞 (A549)) 的生长抑制活性,可见化合物1、2对5种肿瘤细胞都有明显的抑制作用,且都大大优于顺铂[27-29]。尤其对HT-29抑制作用效果更好。
3 结论
在微波甲醇溶剂热条件下,合成了2个Sn4O4梯形结构二丁基锡羧酸酯,化合物对人结肠癌 (HT-29)、肝癌细胞 (HepG2)、乳腺癌 (MCF-7)、鼻咽癌 (KB) 和肺癌细胞 (A549) 均显示出比临床使用的顺铂还强的体外抗癌活性, 可望作为广谱抗癌的候选化合物。
-
-
[1]
Fish R H. J. Organomet. Chem., 2015, 782:3-16 doi: 10.1016/j.jorganchem.2014.10.034
-
[2]
Hadjikakou S K, Hadjiliadis N. Coord. Chem. Rev., 2009, 253:235-249 doi: 10.1016/j.ccr.2007.12.026
-
[3]
Chandrasekhar V, Thirumoorthi R. Eur. J. Inorg. Chem., 2008:4578-4585
-
[4]
Ma C, Sun J, Zhang R. J. Organomet. Chem., 2006, 691:5873-5886 doi: 10.1016/j.jorganchem.2006.09.054
-
[5]
Zhang J H, Zhang R F, Ma C L, et al. Polyhedron, 2011, 30:624-631 doi: 10.1016/j.poly.2010.11.035
-
[6]
Ma C, Li Q, Guo M, et al. J. Organomet. Chem., 2009, 694:4230-4240 doi: 10.1016/j.jorganchem.2009.09.001
-
[7]
Airapetyan D V, Petrosyan V S, Gruener S V, et al. J. Organomet. Chem., 2013, 747:241-248 doi: 10.1016/j.jorganchem.2013.07.005
-
[8]
Iqbala M, Ali S, Muhammad N, et al. J. Organomet. Chem., 2013, 723:214-223 doi: 10.1016/j.jorganchem.2012.10.006
-
[9]
Zheng G L, Ma J F, Yang J, et al. Chem. Eur. J., 2004, 10:3761-3768 doi: 10.1002/(ISSN)1521-3765
-
[10]
Yu H X, Ma J F, Xu G H, et al. J. Organomet. Chem., 2006, 691:3531-3539 doi: 10.1016/j.jorganchem.2006.05.002
-
[11]
Wang Q F, Ma C L, He G F, et al. Heteroat. Chem., 2012, 23(6):531-538 doi: 10.1002/hc.2012.23.issue-6
-
[12]
Xiao X, Du D F, Tian M, et al. J. Organomet. Chem., 2012, 715:54-63 doi: 10.1016/j.jorganchem.2012.05.038
-
[13]
Sougoule A S, Mei Z M, Xiao X, et al. J. Organomet. Chem., 2014, 758:19-24 doi: 10.1016/j.jorganchem.2014.01.034
-
[14]
庾江喜, 冯泳兰, 彭雁.无机化学学报, 2014, 30(5):1135-1142 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20140524&flag=1YU Jiang-Xi, FENG Yong-Lan, PENG Yan, et al. Chinese J. Inorg. Chem., 2014, 30(5):1135-1142 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20140524&flag=1
-
[15]
张复兴, 王剑秋, 邝代治.应用化学, 2009, 26(6):662-666ZHANG Fu-Xing, WANG Jian-Qiu, KUANG Dai-Zhi, et al. Chinese J. Appl. Chem., 2009, 26(6):662-666
-
[16]
邝代治, 冯泳兰, 张复兴.无机化学学报, 2010, 26(12):2160-2164 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20101206&flag=1KUANG Dai-Zhi, FENG Yong-Lan, ZHANG Fu-Xing, et al. Chinese J. Inorg. Chem., 2010, 26(12):2160-2164 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20101206&flag=1
-
[17]
张复兴, 王剑秋, 邝代治.无机化学学报, 2011, 27(6):1111-1115 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20110617&flag=1ZHANG Fu-Xing, WANG Jian-Qiu, KUANG Dai-Zhi, et al. Chinese J. Inorg. Chem., 2011, 27(6):1111-1115 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?file_no=20110617&flag=1
-
[18]
张复兴, 王剑秋, 邝代治.应用化学, 2012, 29(5):520-525ZHANG Fu-Xing, WANG Jian-Qiu, KUANG Dai-Zhi, et al. Chinese J. Appl. Chem., 2012, 29(5):520-525
-
[19]
Baghurst D R, Chippindale A M, Mingos D M P. Nature, 1988, 332:311
-
[20]
Sheldrick G M. SHELX-97, Program for the Solution and the Refinement of Crystal Structures, University of Göttingen, Germany, 1997.
-
[21]
Bondi A. J. Phys. Chem., 1964, 68:441-451 doi: 10.1021/j100785a001
-
[22]
Ma C L, Han Y F, Zhang R F. J. Organomet. Chem., 2004, 689:1675-1683 doi: 10.1016/j.jorganchem.2004.02.024
-
[23]
Chandrasekhar V, Singh P. Organometallics, 2008, 27:4083-4087 doi: 10.1021/om800359b
-
[24]
Ma C, Sun J, Zhang R, et al. Inorg. Chim. Acta, 2006, 359:4179-4190 doi: 10.1016/j.ica.2006.07.001
-
[25]
Chandrasekhar V, Thirumoorthi R, Metre R K, et al. J. Organomet. Chem., 2011, 696:600-606 doi: 10.1016/j.jorganchem.2010.09.032
-
[26]
Zhu C, Yang L, Li D, et al. Inorg. Chim. Acta, 2011, 375:150-157 doi: 10.1016/j.ica.2011.04.049
-
[27]
Shang X, Ding N, Xiang G. Eur. J. Med. Chem., 2012, 48:305-312 doi: 10.1016/j.ejmech.2011.12.032
-
[28]
Motswainyana W M, Onani M O, Madiehe A M. Polyhedron, 2012, 41:44-51 doi: 10.1016/j.poly.2012.04.010
-
[29]
Kaluđerović G N, Paschke R, Prashar S, et al. J. Organomet. Chem., 2010, 695:1883-1890 doi: 10.1016/j.jorganchem.2010.04.029
-
[1]
-
表 1 化合物的晶体学数据
Table 1. Crystallographic data of the compounds
Compound 1 2 Empirical formula C50H92O8Sn4 C52H98N2O8Sn4 Formula weight 1 296.00 1 354.08 Crystal system Monoclinic Monoclinic Space group P21/n P21/n a / nm 1.359 54(6) 1.347 88(8) b/ nm 1.391 80(5) 1.391 05(9) c / nm 1.644 11(6) 1.745 35(11) β/(°) 106.775(2) 107.310(3) V/ nm3 2.978 6(2) 3.124 3(3) Z 2 2 Dc/(Mg·m-3) 1.445 1.439 Absorption coefficient / mm-1 1.701 1.626 F(000) 1312 1376 Limiting indices (h, k, l, ) -8~16, -13-16, -19-19 -16-17, -18-14, -22-22 Reflections collected 16 591 20 755 Unique reflections (Rint) 5 245 (0.039 3) 7 070 (0.023 7) Data with I>2σ(I) 2 978 5 140 Data, restraints, parameters 5 245, 138, 281 7 070, 20, 298 Goodness of fit on F2 1.276 1.062 Completeness 0.998 0.99 R1, wR2 [I>2σ(I)] 0.067 9, 0.201 5 0.038 1, 0.099 7 R1, wR2(all data) 0.118 4, 0.230 9 0.058 9, 0.118 1 (△ρ)max,(△ρ) min/ (e·nm-3) 763, -641 580, -542 表 2 化合物的部分键长和键角
Table 2. Selected bond lengths (nm) and angles (°) for 1 and 2
1 2 1 2 Sn1-C1 0.209 7(11) 0.211 6(6) Sn2-O3 0.203 5(4) 0.203 3(3) Sn1-C5 0.199 6(10) 0.210 8(6) Sn2-O4 0.212 8(5) 0.213 0(3) Sn2-C9 0.207 6(10) 0.210 9(6) Sn2-O3A 0.213 1(4) 0.212 9(3) Sn2-C13 0.203 3(9) 0.211 9(6) Sn2A-O3 0.213 1(4) 0.212 9(3) Sn1-O1 0.213 4(5) 0.213 2(3) C18-O1 0.125 5(10) 0.131 5(5) Sn1-O3 0.200 9(4) 0.202 7(3) C18-O2 0.121 3(10) 0.122 2(6) Sn1-O4 0.224 1(5) 0.226 9(3) C17-O4 0.145 6(10) 0.142 6(6) O3-Sn1-C1 112.8(4) 110.8(2) C13-Sn2-C9 116.0(4) 120.8(3) O3-Sn1-O1 81.87(19) 81.31(12) O3-Sn2-O4 72.64(18) 73.48(12) C1-Sn1-O1 102.2(3) 102.2(2) C13-Sn2-O4 98.9(4) 97.8(2) O3-Sn1-C5 118.1(4) 112.3(2) C9-Sn2-O4 98.7(3) 97.8(2) C1-Sn1-C5 125.3(5) 132.8(3) O3-Sn2-O3A 73.96(19) 73.39(12) O1-Sn1-C5 103.4(4) 102.4(2) C13-Sn2-O3A 99.4(3) 98.4(2) O3-Sn1-O4 70.71(18) 70.65(11) C9-Sn2-O3A 98.0(3) 98.4(2) C1-Sn1-O4 87.8(4) 87.98(19) O4-Sn2-O3A 146.59(19) 146.87(12) O1-Sn1-O4 152.6(2) 151.96(12) Sn1-O3-Sn2 114.46(19) 114.27(13) C5-Sn1-O4 90.9(4) 88.8(2) Sn1-O3-Sn2A 139.5(2) 139.12(14) O3-Sn2-C13 122.0(3) 118.9(2) Sn2-O3-Sn2A 106.05(19) 106.61(12) O3-Sn2-C9 121.9(3) 120.4(2) Symmetry codes: A:-x+1, -y+2, -z for 1; A:-x, -y+2, -z+2 for 2 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 1
- 文章访问数: 1230
- HTML全文浏览量: 169


 下载:
下载:


 下载:
下载:

