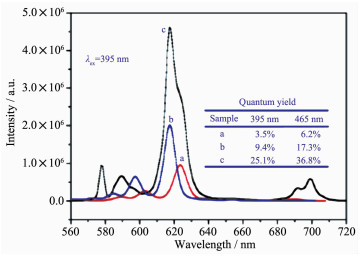
 图 1
三种荧光粉的发射光谱[13]
Figure 1.
Photoluminescence comparison of three phosphors[13]
图 1
三种荧光粉的发射光谱[13]
Figure 1.
Photoluminescence comparison of three phosphors[13]

Citation: LI Shuo, GUO Ning, LIANG Qi-Meng, DENG Hong-Xiao. Red Phosphors Doped by Eu Used in White LED[J]. Chinese Journal of Inorganic Chemistry, 2017, 33(4): 543-549. doi: 10.11862/CJIC.2017.044

白光LED用Eu掺杂红色荧光粉
English
Red Phosphors Doped by Eu Used in White LED
-
0 引言
1993年GaN蓝光发光二极管[1-2]成功研制并产业化, 促进了LEDs向前发展。比起传统照明光源,白光LED因其具有亮度高、体积小、寿命长、高效节能、绿色环保等优点,使得它在交通运输、电子产品、医疗器械许多领域都有了广泛地应用[3-6]。目前,能够使LEDs发出白光的方法主要有2种:一种是黄色荧光粉在GaN蓝光芯片激发下发出白光;另一种是蓝、绿、红荧光粉在近紫外光GaN芯片激发下发出白光[7-8]。但是目前缺少能够被近紫外光或者蓝光有效激发的荧光粉,尤其缺乏高效红色荧光粉,导致白光LED的显色指数偏低。现今,荧光粉转换白光LED仍是主流方案,其中因为高效荧光粉决定了LED的光转换效率、流明效率、相关色温等重要参数而使其成为关键因素[9]。因此LED用高效红色荧光粉的研制已成为当今研究热点。
1 Eu3+掺杂的线状红光发射荧光粉
近年来,Eu3+的荧光发光特性被广泛地研究。Eu3+是红色荧光粉常用的稀土掺杂元素。Eu3+(4f 6) 的发射谱线位于红色区域,它的谱线对应于4f 6电子组态内从激发态5D0能级到7FJ能级的跃迁。Eu3+的f-f跃迁,跃迁电子为外层5s25p6电子所屏蔽,因此跃迁电子不受晶体场等环境影响,故其发射光谱为线状发射光谱[10]。
1.1 基质敏化系列荧光粉
基质敏化有2种情况:一种是基质阳离子将吸收的能量通过共振方式传递给发光离子;另一种是基质发生能带跃迁,产生激子,激子再通过共振方式将能量传递给发光离子。钨钼酸盐、钒酸盐以及钛酸盐因其独特的结构可以将能量有效地传递给Eu3+,进而提高的Eu3+掺杂的荧光粉的发光效率以及发光强度,是优异的基质敏化材料, 因此一直是发光材料领域的研究热点。
Chiu等[11]用高温固相法成功地制备了一系列Li、Eu共掺杂的LiEu (WO4)2-x(MoO4)x钨/钼酸盐荧光粉,研究了Na、K不同碱金属对荧光粉发光性能的影响。LiEu (WO4)2-x(MoO4)x荧光粉可以被394 nm的近紫外光激发,发射615 nm的红光。Dalal等[12]通过燃烧法合成了SrZn1-xEuxV2O7荧光粉,并研究了Eu3+离子浓度对发光强度、CIE色度指数及光致发光寿命的影响。在395nm近紫外光激发下,此荧光粉发出616 nm的红光。最佳燃烧温度为700 ℃,Eu3+离子最佳浓度为0.04(物质的量分数),且浓度淬灭机理是偶极偶极相互作用。当Eu3+离子掺杂浓度为0.04时,荧光粉的色度坐标为 (0.636 6,0.362 9),其荧光寿命为2.54 ms。Zhang等[13]研究了Li+电荷补偿对双钙钛矿结构Sr3Ti2O7:Eu3+荧光粉发光性能的影响。研究表明Li+电荷补偿可以提高荧光粉的发光强度、量子效率以及显色性能。如图 1所示,在395 nm激发光的激发下,(Sr0.9Eu0.1Li0.1)3Ti2O7荧光粉的发光效率分别是Y2O2S:Eu0.05荧光粉和CaMoO4:Eu0.3荧光粉的5倍和3倍;并且 (Sr0.9Eu0.1Li0.1)3 Ti2O7荧光粉的量子效率为25.1%,远远高于Y2O2S:Eu0.05荧光粉和CaMoO4:Eu0.3荧光粉。其色坐标为 (0.654,0.336),接近于NTSC的标准值 (0.670, 0.330)。
尽管钨钼酸盐、钒酸盐以及钛酸盐体系荧光粉因为基质敏化而具有优异发光性能,但总体而言,其光效仍未达到当今白光LED用红色荧光粉的使用要求。因此需要通过寻找不同基质和掺杂不同稀土离子,同时研究其热稳定性,提高荧光粉发光效率,以更好的适用于白光LED。
1.2 Ce3+→Tb3+→Eu3+敏化体系荧光粉
Ce3+可以被近紫外光激发,是一种良好的敏化剂,而且可以转移一部分的能量到其他激活离子[14-18],如Eu3+、Tb3+;而Tb3+可以作为Eu3+、Mn2+的敏化剂。Ce3+→Tb3+→Eu3+敏化体系荧光粉基质主要有硼酸盐基质、硅酸盐基质、磷酸盐基质以及氯化物基质。Zhang等[14]用高温固相法合成了Gd2SiO5:Ce3+,Tb3+,Eu3+系列荧光粉,并对其激发、发射光谱,衰减曲线以及Tb3+和Eu3+浓度比进行了研究。其结果表明:Ce3+吸收近紫外光,然后把能量传递给Tb3+, 并产生强烈的绿光,随后Tb3+把能量传递Eu3+,最后发出强烈的614nm的红色线状光谱,由此可知Gd2SiO5:Ce3+,Tb3+,Eu3+系列荧光粉的能量传递形式为Ce3+→Tb3+→Eu3+。Zhang等[15]还用高温固相法合成了一系列新型的宽带激发线状红色荧光粉Ba2Y (BO3)2Cl:Ce3+,Tb3+,Eu3+,此类荧光粉在近紫外区有强烈的宽带吸收,因Eu3+的敏化而发出红光。Ce3+,Tb3+的发射衰减曲线表明在Ce3+、Tb3+和Eu3+之间存在电荷转移。
因此,此类荧光粉的能量传递方式一般为能量转移与金属金属电荷转移。其他此类荧光粉及其发光性能如表 1所示。
 表 1
Ce3、Tb3+、Eu3+敏化体系荧光粉的发光性能
Table 1.
Luminescence performance of sensitization system phosphors by Ce3, Tb3+ and Eu3+
表 1
Ce3、Tb3+、Eu3+敏化体系荧光粉的发光性能
Table 1.
Luminescence performance of sensitization system phosphors by Ce3, Tb3+ and Eu3+
Phosphor composition Excitation peak / nm Emission peak / nm Ref. LuBO3:Ce3+,Tb3+,Eu3+ 360 580, 592, 613-624, 650 [19] GdBO3:Ce3+,Tb3+,Eu3+ 356 592, 612, 624 [16] La5Si2BO13:Ce3+,Tb3+,Eu3+ 280 591, 614, 620 [20] Y2SiO5:Ce3+,Tb3+,Eu3+ 355 592, 612, 624 [21] NaYF4:Ce3+,Tb3+,Eu3+ 248 590, 614, 691 [22] 表 1 Ce3、Tb3+、Eu3+敏化体系荧光粉的发光性能
Table 1. Luminescence performance of sensitization system phosphors by Ce3, Tb3+ and Eu3+1.3 共掺Bi3+敏化体系荧光粉
Bi3+的6s2电子结构使其既可以做激活剂也可以做敏化剂,共掺Bi3+可以使激发峰向长波方向移动,使荧光粉更好地被近紫外光或者蓝光激发[23-25]。
Kim等[26]通过对 (Ca,Eu) MoO4、(Ca,Eu,Bi) MoO4荧光粉发射光谱的研究,探讨了共掺Bi3+以及电荷补偿对CaMoO4:Eu3+荧光粉发射强度的促进作用。研究表明当Bi3+共掺到CaMoO4:Eu3+荧光粉之后,Bi3+会破坏Eu3+附近晶体场的对称性,进而破坏Eu3+内部的4f跃迁禁阻,提高发射强度。由表 2可知电荷补偿对CaMoO4:Eu3+荧光粉的发射强度的促进作用更显著,因为电荷补偿对荧光粉的结晶度以及共价键都有影响。
Rambabu等[27]从主体成分 (Gd,Y和Gd/Y)、共掺Bi3+和SiO2涂层3个方面对LnVO4荧光粉进行了系统研究。研究表明共掺Bi3+后荧光粉内能量转移为VO43+→Bi3+→Eu3+,共掺Bi3+不仅可以提高发光强度还可以拓宽荧光粉的激发光谱,Y0.949VO4:Bi0.001,Eu0.05荧光粉的发光强度是Y0.95VO4:Eu0.05荧光粉的1.6倍;SiO2涂层有明显清洁和光滑表面,可以减少表面的能量损失来提高发光性能,Y0.949VO4:Bi0.001,Eu0.05@SiO2荧光粉的发光强度是Y0.95VO4:Eu0.05荧光粉的2.2倍。
Bi3+离子作为敏化剂能有效吸收能量并传递给邻近的激活剂离子,提高荧光粉的发光强度。Eu3+对近紫外光吸收不是十分有效,而Bi3+能够有效捕获近紫外光,增强并拓宽位于400 nm附近的紫外光吸收波长,将所吸收的能量有效地传递给Eu3+,使Eu3+发光性能得到改善。
1.4 共掺Sm3+敏化体系荧光粉
Sm3+被认为是Eu3+的良好的敏化剂是因为它们特定能级之间的能量差小,可以实现能量转移。
Bouzidi等[28]研究了Sm3+、Eu3+掺杂的BaWO4荧光粉,研究表明共掺Sm3+之后BaWO4:Eu3+荧光粉的发光寿命延长,量子效率提高24%。BaWO4:Eu3+, Sm3+荧光粉色度坐标为 (0.660,0.334),色纯度为82.90%,而BaWO4:Eu3+荧光粉色度坐标为 (0.640,0.361),色纯度为57.78%;BaWO4:Sm3+荧光粉色度坐标为 (0.602,0.396),色纯度为65.72%,数据表明共掺Sm3+之后BaWO4:Eu3+荧光粉红光性能更优异。
Sun等[29]用固相法合成了Ca14Mg2(SiO4)8荧光粉,并研究了掺杂Eu3+、Sm3+和共掺Eu3+和Sm3+对荧光粉性能的影响。研究表明:Ca14Mg2(SiO4)8:Eu3+可以在394 nm光的激发下发射614 nm的红光且其浓度淬灭机理为偶极偶极相互作用;Ca14Mg2(SiO4)8:Sm3+可以在405nm光的激发下,发射602 nm的红光,其浓度淬灭机理为相邻原子的能量转移;而共掺Eu3+和Sm3+之后,由于Sm3+→Eu3+之间的能量转移,Ca14Mg2(SiO4)8荧光粉在400~410 nm的吸收带增加,Eu3+的发射强度增强。
共掺Sm3+可以扩宽Eu3+掺杂红色荧光粉的吸收波长范围,使荧光粉能被蓝光激发,同时由于Sm3+→Eu3+之间的能量转移,共掺Sm3+可以提高红色荧光粉的发光性能。
2 Eu2+掺杂的带状红光发射荧光粉
二价铕离子 (Eu2+) 是一种重要的激活剂;Eu2+的发光是由基态的4f 7能级到激发态4f 65d能级跃迁引起的[30]。4f-5d跃迁是电偶极允许跃迁,因此Eu2+在许多基质中的吸收和发光效率都比较高。
2.1 硫化物系列荧光粉
硫化物体系是一类用途广泛的发光基质材料。目前使用的硫化物体系主要为 (Ca1-x,Srx) S:Eu2+体系。该类荧光粉可以被蓝光激发而发射红光。
Yang等[31]研究表明,加入Mg、Ga取代Ca可以显著提高CaS:Eu荧光粉的发光效率,但是单独添加效果不明显。研究表明, 在185 ℃条件下,Ca0.89Mg0.01Ga0.1S:Eu荧光粉的发射强度随温度升高而下降的概率减少37%;室温下,其发射强度比未掺杂前提高23.9%。
Hu等[32]研究了以硫化物为原料的 (Ca1-x,Srx) S:Eu2+红色荧光粉。研究表明,以硫化物为原料合成的红色荧光粉的纯度高于硫酸盐原料。(Ca1-x,Srx) S:Eu2+荧光粉可以被430~450 nm的蓝光激发发射红光,Eu2+取代Ca/Sr作为发光中心。可以通过调整Ca和Sr比例来获取不同发射波长的荧光粉。
硫化物荧光粉最大的问题是物理化学稳定性较差,易潮解形成硫化物污染环境。因此Avci等[33]在CaS:Eu2+荧光粉的表面涂覆一层氧化铝薄膜来增强其抗水性。实验表明,涂覆氧化铝薄膜后CaS:Eu2+荧光粉的抗水性得到明显改善。
2.2 氮化物系列荧光粉
与目前商用的硫化物红色荧光粉相比,氮化物荧光粉 (特别是硅基氮 (氧) 化物、硅铝基氮化物荧光转换材料) 具有优异的热和化学稳定性以及优良的荧光性能,成为白光LED的理想转换荧光材料。
Li等[34]用高温固相法合成了一系列M2Si5N8:Eu2+(M=Ca,Sr,Ba) 荧光粉。研究表明在395nm光激发下,随着Eu2+掺杂浓度的增加M2Si5N8:Eu2+(M=Ca,Sr) 表现为典型的宽带激发,发射波长为600~680 nm;而Ba2Si5N8:Eu2+的发射波长为580~680 nm。在465 nm光的激发下,Ca1.98Eu0.02Si5N8,Sr1.98Eu0.02Si5N8和Ba1.98Eu0.02 Si5N8荧光粉的相对发射强度分别为71%,87%和84%,且其量子效率分别为50%~55%,75%~80%和75%~80%。Sr2Si5N8:Eu2+荧光粉的色坐标值更加接近于标准样品 (Sr1-xCaxS:Eu2+) 而在Eu掺杂M2-xEuxSi5N8(M=Ca,Sr,Ba) 荧光粉中,Sr2Si5N8:Eu2+荧光粉具有最优性能,是优异的WLED用荧光粉。
改善氮化物系列荧光粉合成条件仍然是未来研究的主要方向。Chen等[35-36]以M (NO3)2(M=Ca,Sr),α-Si3N4和Eu (NO3)3为原材料,在90%N2+10%H2(体积分数) 的气氛中,于1 200 ℃和常压下用硝酸盐法合成了M2Si5N8:Eu2+(M=Ca,Sr) 荧光粉。此类荧光粉在465 nm光激发下,可以在580~670 nm处产生强烈的发射光。与传统的合成方法相比,此合成方法温度降低了约200 ℃,且为常压反应,为未来工业以及科研发展提供了新思路。
Kim等[37]用氮化法在常压加热条件下合成了 (Sr,Ca) AlSiN3:Eu2+荧光粉,此类荧光粉可以在450 nm蓝光的激发下,发射635~655 nm的红光;并且随着Sr浓度的增加,荧光粉的发射峰向短波方向移动。根据温度衰减曲线,(Sr0.42Ca0.56) AlSiN3:Eu2+(2%,原子百分数) 荧光粉在150 ℃下的发射强度依然保持室温下发射强度的86%,而YAG:Ce3+荧光粉在150 ℃下的发射强度仅为室温下的68%,说明此类荧光粉具有良好的热稳定性,是优异的WLED用荧光粉。
由于氮化物的相对惰性,传统氮化物荧光粉的合成通常需要高温、高压等苛刻条件,对生产设备的要求很高,不利于工业化生产,这极大地制约了该系列荧光粉的应用。因此,优化氮化物荧光粉的合成工艺对新型氮化物荧光粉的研制开发具有重要意义。
2.3 磷酸盐系列荧光粉
磷酸盐系列荧光粉因为其制备温度低、亮度高、物理化学稳定性好、晶粒大小易于控制等优点成为重要的发光材料。
目前研究较多的近紫外激发磷酸盐体系荧光粉是用Eu3+作为激活剂,在近紫外光激发下能发射红光。但是Deng等[38]用固相法合成了Eu2+激发的红色Ca4(PO4)2O荧光粉,此荧光粉可以被460 nm的蓝光激发,发射半峰宽FWHM≈154 nm,665 nm的宽带红光。且其斯托克斯位移为6 354.5 cm-1,大于Eu2+掺杂的其他氧化物红色荧光粉:Sr3SiO5:Eu2+(3 402 cm-1),Sr3Al2O6:Eu2+(4 846.6 cm-1) 和LiSrBO3:Eu2+(5 557.9 cm-1)。当其用于WLED时其电流为20 mA, 色坐标为 (0.313 5, 0.331 6),且其相关色温为6 446 K,显色指数为90.5。
2.4 Eu2+掺杂的窄带红光发射荧光粉
Eu2+掺杂的宽带激发、窄带发射荧光粉,具有较高显色指数 (CRI),较高光谱光视效率,窄带发射使其发光集中在人眼可以识别的范围内,发光集中且易于控制,较低相关色温 (CCT < 4 000 K) 以及较高的流明效率,是一种优异的新型荧光粉,因此引起了人们的高度关注。
Sebastian等[39]制备的Sr[Mg3SiN4]:Eu2+荧光粉可以被450 nm的蓝光激发,发射615 nm的红光,且半峰宽为43 nm。M[Mg3SiN4](M=Ca,Sr,Eu) 的高对称的立方体结构会产生小的斯托克斯位移,Eu2+的激发态的结构弛豫是禁阻的,这就是可以产生窄带发射特性的原因。其研究还表明,Sr[Mg3SiN4]:Eu2+荧光粉性能易受温度影响:温度降低时其发射强度增大,当温度达到6 K时,相对量子效率几乎达到100%。由于窄带隙引起的其他能量损失 (例如光致电离) 可能是导致高温时发光效率降低的原因。Sebastian等[40]还合成了立方晶系结构的Ba[Mg3SiN4]荧光粉,此荧光粉的发射波长为670 nm,半峰宽为1 970 cm-1。研究表明其有序结构是窄带发射的重要原因,可以通过优化结构组织关系来合成和优化目标产物。
Pust等[41]成功合成了Ca[LiAl3N4]:Eu2+荧光粉,此荧光粉可以被470 nm的蓝光激发,发射668 nm的红光,且半峰宽为60 nm。Ca[LiAl3N4]:Eu2+的色坐标为 (0.720,0.280),其色度较深。Ca[LiAl3N4]:Eu2+荧光粉这种特殊的宽带激发窄带发射发光性能源自于其高度压缩的AlN、LiN、SiN和MgN4四方晶系。为了能得到短波长的窄带发射光谱,Pust等[5]还研究了用Sr部分代替Ca,并成功合成了Sr[LiAl3N4]:Eu2+荧光粉,此荧光粉可以被440 nm的蓝光激发,发射650 nm的红光,且半峰宽为50 nm。Sr[LiAl3N4]:Eu2+荧光粉具有较低的热淬灭性,在200 ℃下依然保持95%的相对量子效率,且其流明效率比目前商用CaAlSiN3:Eu2+荧光粉提高14%,是优异的宽带激发窄带发射新型荧光粉。
Peter等[42]利用高温高压反应合成了Ca18.75Li10.5[Al39N55]:Eu2+荧光粉。此荧光粉因其独特的T5超四面体的结构 (四面体AlN4单位组成和相连的附加AlN4部分组成) 吸引了人们的注意,也证明了不仅仅立方晶系结构可以实现Eu2+的窄带发射。此荧光粉的发射波长为647 nm,半峰宽为1 280 cm-1,是优异的窄带发射红色荧光粉。
因此,Eu2+掺杂的窄带红光发射荧光粉的高对称性以及刚性的晶体结构可以诱发Eu2+激发中心微弱的电子声子相互作用,显著地减少非辐射跃迁过程的发生,从而减少能量损失,提高其流明效率。其他此类荧光粉及其发光性能见表 3。
Phosphor composition Excitation peak / nm Emission peak / nm FWHM /nm Ref. Ba[Mg2Al2N4]:Eu2+ 450~480 666 43 [43] Sr[Mg2Al2N4]:Eu2+ 450~480 612 54 [43] Ca[Mg2Al2N4]:Eu2+ 450~480 607 55 [43] Ba[Mg2Za2N4]:Eu2+ 440 649 46 [43] Ba3Ga3Ns:Eu2+ 365 638 47 [44] (Sr,Ba)2Si5Nj:Eu2+ 450 590~625 38~49 [45] (Ca,Sr) AlSiN3:Eu2+ 450 610~660 40~48 [46] 表 3 Eu2+掺杂的窄带光谱荧光粉的发光性能
Table 3. Luminescence performance of Eu2+ doped narrow band phosphors2.5 Eu2+作为敏化剂的红色荧光粉
Eu2+不仅可以作为激活剂,同时也可以作为过渡金属离子的敏化剂。Mn2+由于自旋禁阻跃迁,导致对紫外吸收很弱,直接激发的发光也较弱,因此常常选择使用合适的敏化剂来提高Mn2+的发光效率。一些稀土离子如Ce3+、Eu2+、Pr3+等均对Mn2+的发光有很强的敏化作用,其中以Eu2+对Mn2+的敏化效果最好。由于Mn2+的4T1→6A1为禁阻跃迁,使得Mn2+掺杂的荧光粉的发光强度弱,而共掺Eu2+之后,Eu2+-Mn2+之间的能量传递大大增强了Mn2+的发光强度。共掺Eu2+、Mn2+可以增强荧光粉对紫外或者近紫外光的吸收,使荧光粉能够更好的被紫外或者近紫外激发。
本课题组[47-50]主要研究了Eu2+、Mn2+共掺白磷钙矿类型荧光粉,如Ca9Gd (PO4)7:Eu2+,Mn2+、Ca9Lu (PO4)7:Eu2+,Mn2+和Ca9MgK (PO4)7:Eu2+,Mn2+荧光粉,研究表明在近紫外光的激发下,固定Eu2+浓度,通过调节Mn2+浓度可以使荧光粉发射光谱实现蓝绿光到红光的转变,最终荧光粉可以发射645 nm的红光。Eu2+的发射光谱与Mn2+的激发光谱的重叠为Eu2+-Mn2+之间的能量传递提供了理论基础。根据所得的能量衰减曲线以及能量传递效率,Eu2+-Mn2+之间的能量传递属于电偶极电多级相互作用。
3 问题与展望
Eu3+掺杂的线状红光发射荧光粉存在发光效率低、稳定性差等问题,并且其只能被近紫外光或者紫外光激发。钨钼酸盐、钒酸盐以及钛酸盐因其独特的结构可以将能量有效地传递给Eu3+,而被认为是优异的基质敏化材料,但其光效仍未达到当今白光LED用红色荧光粉的使用要求。因此需要通过寻找不同基质和掺杂不同稀土离子,同时研究其热稳定性,提高其发光效率,使其更好的适用于白光LED。Ce3+→Tb3+→Eu3+体系荧光粉因其离子之间存在能量传递,提高了荧光粉的发光效率以及发光强度;而共掺Bi3+、Sm3+等离子则可以使Eu3+的激发波长向长波方向移动,使得荧光粉能被近紫外光或者蓝光激发,并且共掺离子间的能量传递可以提高荧光粉的发光效率。
对于Eu2+掺杂的硫化物系列荧光粉,其物理化学稳定性较差,易潮解,因此需要采取包覆或者玻璃化措施来改善其稳定性。Eu2+掺杂的氮化物荧光粉发射光谱的半峰宽较宽,其长波部分到达远红外区,不易被人眼识别,使得其流明效率损失,因此需要对其合成方法进行改进;而且氮化物系列荧光粉具有合成条件苛刻等不足,则需要寻找简单有效的合成工艺;Eu2+掺杂的宽带激发、窄带红光发射荧光粉,因其半峰宽较窄使得其发光效率提高,但是其合成方法比较单一,可以通过优化结构组织关系来合成和优化目标产物。对于Eu2+掺杂化合物的研究应不仅仅拘泥于将其作为发光离子,还应该研究其作为敏化剂的作用。
-
-
[1]
Nakamura S, Mukai T, Senoh M, et al. Appl. Phys. Lett., 1994, 64(13):1687-1689 doi: 10.1063/1.111832
-
[2]
Nakamura S, Senoh M, Iwasa N, et al. Appl. Phys. Lett., 1995, 67(13):1668-1670
-
[3]
Li X, Budai J D, Liu F, et al. Light Sci. Appl., 2013, 2:50-57 doi: 10.1038/lsa.2013.6
-
[4]
Oh J H, Yang S J, Do Y R. Light Sci. Appl., 2014, 3:141-149 doi: 10.1038/lsa.2014.22
-
[5]
Pust P, Weiler V, Hecht C, et al. Nat. Mater., 2014, 13(9):891-896 doi: 10.1038/nmat4012
-
[6]
Zhang D, Duan L, Zhang Y, et al. Light Sci. Appl., 2015, 4:232-238 doi: 10.1038/lsa.2015.5
-
[7]
Guo C F, Huang D X, Su Q. Mater. Sci. Eng. B, 2006, 130(1/2/3):189-193
-
[8]
Xie R J, Hiroeaki N. Sci. Technol. Adv. Mater., 2007(7/8):588-600
-
[9]
Mueller M R, Mueller G, Krames M R, et al. Phys. Status Solidi A, 2005, 202(9):1727-1732 doi: 10.1002/pssa.v202:9
-
[10]
Ronda C R, Justel T, Nikol H. J. Alloys Compd., 1998, 275:669-676
-
[11]
Chiu C RH, Wang MF, Lee C S et al. J. Solid State Chem., 2007, 180(2):619-627 doi: 10.1016/j.jssc.2006.11.015
-
[12]
Dalal M, Taxak V B, Lohra S, et al. J. Lumin., 2015, 161:63-70 doi: 10.1016/j.jlumin.2014.12.056
-
[13]
Zhang L, Sun, B H, Liu Q, et al. J. Alloys Compd., 2016, 657:27-31 doi: 10.1016/j.jallcom.2015.10.096
-
[14]
Zhang X, Chen Y, Zhou L, et al. Ind. Eng. Chem. Res., 2014, 53(16):6694-6698 doi: 10.1021/ie404312n
-
[15]
Zhang X, Zhou L, Pang Q, et al. J. Am. Ceram. Soc., 2014, 97(7):2124-2129 doi: 10.1111/jace.2014.97.issue-7
-
[16]
Zhang X, Zhou L, Pang Q, et al. Opt. Mater., 2014, 36(7):1112-1118 doi: 10.1016/j.optmat.2014.02.009
-
[17]
Zhang X, Zhou L, Pang Q, et al. J. Phys. Chem. C, 2014, 118(14):7591-7598 doi: 10.1021/jp412702g
-
[18]
Zhang Y, Zhu Z, Qiao Y. Mater. Lett., 2013, 93:9-11 doi: 10.1016/j.matlet.2012.11.068
-
[19]
Zhang X G, Fu X H, Song J H, et al. Mater. Res. Bull., 2016, 80:77-85
-
[20]
Zhang X G, Zhang J L, Gong M L. Mater. Lett., 2015, 143:71-74 doi: 10.1016/j.matlet.2014.12.056
-
[21]
Zhang X G, Zhou L Y, Pang Q, et al. J. Phys. Chem. C, 2014, 118(14):7591-7598 doi: 10.1021/jp412702g
-
[22]
Ding M Y, Zhang H L, Chen D Q, et al. J. Alloys Compd., 2016, 672:1117-1124
-
[23]
Chen Y C, Wu Y C, Wang D Y, et al. J. Mater. Chem., 2012, 22(16):7961-7969 doi: 10.1039/c2jm30756a
-
[24]
Guan A, Mo F, Chen P, et al. J. Disp. Technol., 2016, 12(2):136-142
-
[25]
Ma Y, Ran W, Li W, et al. Luminescence, 2016, 31(3):665-670 doi: 10.1002/bio.v31.3
-
[26]
Kim E O, Jeong J H, Kim J H. J. Korean Phys. Soc., 2016, 68(4):578-82 doi: 10.3938/jkps.68.578
-
[27]
Rambabu U, Munirathnam N R, Chatterjee S, et al. Ceram. Int., 2013, 39(5):4801-4811 doi: 10.1016/j.ceramint.2012.11.070
-
[28]
Bouzidi C, Ferhi M, Elhouichen H, et al. J. Lumin., 2015, 161:448-455 doi: 10.1016/j.jlumin.2015.01.053
-
[29]
Sun W, Pang R, Li H, et al. J. Rare Earths, 2015, 33(8):814-819 doi: 10.1016/S1002-0721(14)60489-0
-
[30]
Zhang Z H, Wang Y H. Mater. Lett., 2007, 61(19/20):4128-4130
-
[31]
Yang L, Zhang N, Zhang R, et al. Mater. Lett., 2014, 129:134-136 doi: 10.1016/j.matlet.2014.05.041
-
[32]
Hu Y S, Zhuang W D, Ye H Q, et al. J. Lumin., 2005, 111(3):139-145 doi: 10.1016/j.jlumin.2004.07.005
-
[33]
Avci N, Cimieri I, Smet P F, et al. Opt. Mater., 2011, 33(7):1032-1035 doi: 10.1016/j.optmat.2010.07.021
-
[34]
Li Y Q, Van Steen J E J, Van Krevel J W H, et al. J. Alloys Compd., 2006, 417(1/2):273-279
-
[35]
Chen C, Chen W, Rainwater B, et al. Opt. Mater., 2011, 33(11):1585-1590 doi: 10.1016/j.optmat.2011.04.014
-
[36]
Chen C, Xie E. Sci. China Ser. G, 2014, 57(3):433-436 doi: 10.1007/s11433-013-5204-4
-
[37]
Kim H S, Machida K I, Itoh M, et al. J. Sol-Gel Sci. Technol., 2014, 3(12):R234-R237
-
[38]
Deng D G, Yu H, Li Y Q, et al. J. Mater. Chem. C, 2013, 1(19):3194-3199 doi: 10.1039/c3tc30148f
-
[39]
Schmiechen S, Schneider H, Wagatha P, et al. Chem. Mater., 2014, 26(8):2712-2719 doi: 10.1021/cm500610v
-
[40]
Schmiechen S, Strobel P, Hecht C, et al. Chem. Mater., 2015, 27(5):1780-1785 doi: 10.1021/cm504604d
-
[41]
Pust P, WochnikA S, Baumann E, et al. Chem. Mater., 2014, 26(11):3544-3549 doi: 10.1021/cm501162n
-
[42]
Wagatha P, Pust P, Weiler V, et al. Chem. Mater., 2016, 28(4):1220-1226 doi: 10.1021/acs.chemmater.5b04929
-
[43]
Pust P, Hintze F, Hecht C, et al. Chem. Mater., 2014, 26(21):6113-6119 doi: 10.1021/cm502280p
-
[44]
Hintze F, Hummel F, Schmidt P J, et al. Chem. Mater., 2012, 24(2):402-407 doi: 10.1021/cm203323u
-
[45]
Zeuner M, Schmidt P J, Schnick W. Chem. Mater., 2009, 21(12):2467-2473 doi: 10.1021/cm900341f
-
[46]
Uheda K, Hirosaki N, Yamamoto Y, et al. Electrochem. Solid-State Lett., 2006, 9(4):H22-H25 doi: 10.1149/1.2173192
-
[47]
Guo N, You H, Jia C, et al. Dalton Trans., 2014, 43(32):12373-12379 doi: 10.1039/C4DT01021C
-
[48]
Guo N, Huang Y, You H, et al. Inorg. Chem., 2010, 49(23):10907-10913 doi: 10.1021/ic101749g
-
[49]
Guo N, Li S, Chen J S, et al. J. Lumin., 2016, 179:328-333 doi: 10.1016/j.jlumin.2016.07.015
-
[50]
Guo N, You H, Song Y, et al. J. Mater. Chem., 2010, 20(41):9061-9067 doi: 10.1039/c0jm01860k
-
[1]
-
表 1 Ce3、Tb3+、Eu3+敏化体系荧光粉的发光性能
Table 1. Luminescence performance of sensitization system phosphors by Ce3, Tb3+ and Eu3+
Phosphor composition Excitation peak / nm Emission peak / nm Ref. LuBO3:Ce3+,Tb3+,Eu3+ 360 580, 592, 613-624, 650 [19] GdBO3:Ce3+,Tb3+,Eu3+ 356 592, 612, 624 [16] La5Si2BO13:Ce3+,Tb3+,Eu3+ 280 591, 614, 620 [20] Y2SiO5:Ce3+,Tb3+,Eu3+ 355 592, 612, 624 [21] NaYF4:Ce3+,Tb3+,Eu3+ 248 590, 614, 691 [22] 表 2 不同激发波长下的相对发射强度表[26]
Table 2. Relative emission intensity under different excitation wavelength[26]
Phosphor composition Excitation peak /nm 397.5 330 290 Ca0.95Eu0.05MoO4 1 1 1 Ca0.925Eu0.05MoO4 3.5 3.3 3.2 Ca0.94Eu0.05Bi001MoO4 2.7 350 2.5 Ca0.91Eu0.05Bi0.01MoO4 6.2 560 3.3 表 3 Eu2+掺杂的窄带光谱荧光粉的发光性能
Table 3. Luminescence performance of Eu2+ doped narrow band phosphors
Phosphor composition Excitation peak / nm Emission peak / nm FWHM /nm Ref. Ba[Mg2Al2N4]:Eu2+ 450~480 666 43 [43] Sr[Mg2Al2N4]:Eu2+ 450~480 612 54 [43] Ca[Mg2Al2N4]:Eu2+ 450~480 607 55 [43] Ba[Mg2Za2N4]:Eu2+ 440 649 46 [43] Ba3Ga3Ns:Eu2+ 365 638 47 [44] (Sr,Ba)2Si5Nj:Eu2+ 450 590~625 38~49 [45] (Ca,Sr) AlSiN3:Eu2+ 450 610~660 40~48 [46] -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 16
- 文章访问数: 4577
- HTML全文浏览量: 419


 下载:
下载:
 下载:
下载:

