 图 1
不同温度下水热处理24 h所得不同样品的XRD图
Figure 1.
XRD patterns of the different samples obtained at different hydrothermal treatment temperature for 24 h
图 1
不同温度下水热处理24 h所得不同样品的XRD图
Figure 1.
XRD patterns of the different samples obtained at different hydrothermal treatment temperature for 24 h

Citation: LIU Bing, FU Rong-Rong, GAO Shan-Min, HUANG Bai-Biao, DAI Ying. Preparation of Ti3+ Self-Doped TiO2(A)/TiO2(R)/In2O3 Nanoheterojunctions with Enhanced Visible-Light-Driven Photocatalytic Properties[J]. Chinese Journal of Inorganic Chemistry, 2016, 32(2): 223-232. doi: 10.11862/CJIC.2016.045

Ti3+自掺杂的TiO2(A)/TiO2(R)/In2O3纳米异质结的制备与可见光催化性能
English
Preparation of Ti3+ Self-Doped TiO2(A)/TiO2(R)/In2O3 Nanoheterojunctions with Enhanced Visible-Light-Driven Photocatalytic Properties
-
Key words:
- Ti3+ self-doped
- / TiO2
- / In2O3
- / nanoheterojunctions
- / visible-light photocatalysis
-
0 引言
近年来,利用光激发半导体产生电子 (e-) 和空穴 (h+) 来降解水中污染物和分解水制氢引起广泛关注,是解决环境污染和生产氢能源的潜在手段[1]。其中TiO2因光化学性质稳定、无污染和来源广等优点,成为重要的光催化材料之一。但是纯的TiO2存在禁带宽度大 (锐钛矿TiO2:3.2 eV,金红石TiO2:3.0 eV) 和电子迁移率低 (10-4~10-5 cm2·V·s-1) 的问题,导致其低的可见光利用率和量子效率,不能满足实际需要[2]。虽然已经将离子掺杂、贵金属修饰、染料敏化以及微结构调控等技术应用于TiO2的改性[3],但是金属或非金属元素的掺杂会降低TiO2的稳定性,而且若掺杂量控制不当,这种异类原子会成为光生e-和h+的复合中心,降低TiO2的光催化性能。而表面光敏化虽然能有效拓展TiO2光响应范围,但是许多敏化剂制备困难,价格昂贵,同时敏化剂本身会被TiO2降解而失去活性。因此,制备能被可见光激发、快速的光生e-和h+传输的TiO2光催化剂,成为值得深入研究的课题[2-3]。
研究表明,纳米异质结具有比单一相催化剂更佳的光催化性能,这主要归因于提高的光生e-和h+分离效率[4]。In2O3是一种n-型、间接带隙的半导体,其间接带隙为2.8 eV,能够被可见光激发[5],因此In2O3常用来作为敏化剂和宽带隙半导体复合,扩展复合光催化材料的光吸收范围[6-12],这类复合材料具有良好的光催化降解有机染料或分解水产氢性能。
In2O3的导带 (CB) 位于-0.62 V,价带 (VB) 位于2.18 V (vs NHE)[13],锐钛矿相TiO2的CB和VB分别位于-0.29和+2.91 V[14],二者具有交错的能带结构,因此In2O3和TiO2能够形成有效的异质结[15-16]。Mu等采用静电纺丝结合水热处理技术,制备了一维结构的In2O3/TiO2异质结,并具有良好的可见光催化降解RhB的性能[17]。Li等采用浸渍法制备了负载In2O3的TiO2纳米催化剂,并在紫外光激发下催化降解甲基橙,研究了光生载流子的分离效率,结果表明负载有In2O3的复合光催化剂比纯的TiO2具有更佳的光催化降解性能[18]。这种经In2O3敏化的TiO2不仅能够被可见光激发,而且形成的异质结结构能够加快光生e-和h+的分离,降低复合几率,因此具有提高的光催化性能[15-18]。但是异质结中只有In2O3能够吸收可见光,TiO2仅起到接受光生电子、促进光生e-和h+的分离作用,因此对可见光的利用率仍然较低。另外,TiO2存在不同的晶体结构,随着研究的深入,锐钛矿相TiO2(A) 和金红石相TiO2(R) 的复合研究越来越受到重视[19],这是因为二者的VB和CB带边不同,复合后能形成异相结,从而加快光生e-和h+的分离,提高光电转换效率。
因此,为了充分利用可见光并提高光生e-和h+的分离效率,本文在无还原剂的条件下,以TiCl3和InCl3为Ti源和In源,制备了Ti3+自掺杂的TiO2(A)/TiO2(R)/In2O3纳米异质结,研究了产物的可见光催化降解RhB和苯酚的性能,结果表明所得产物具有较强的可见光吸收性能和较高的光生e-和h+分离效率。不同于传统的异类原子掺杂,通过在TiO2中引入Ti3+,可在TiO2的CB下方形成局域态,从而使TiO2的光吸收范围延伸至可见光区甚至红外光区[20-21],因此Ti3+自掺杂的TiO2成为近期的研究热点[20]。进一步研究表明,Ti3+还能提高TiO2的导电性,加快光生e-和h+的传输速率,进而提高TiO2的光电转换效率[22-24]。
1 实验部分
1.1 样品的制备
Ti3+自掺杂的TiO2/In2O3异质结的制备过程如下:首先,将60 mg In2O3溶解在10 mL浓度为6 mol·L-1的HCl溶液中,然后加入15 mL质量分数为20%的TiCl3溶液,在室温、搅拌的情况下,用浓度为5 mol·L-1的NaOH溶液调节混合液的pH值到6,生成蓝紫色沉淀。将混合物过滤、洗涤后,所得固体置于50 ℃的真空干燥箱中干燥,得深蓝色前驱体。将深蓝色前驱体分散在40 mL用高纯N2鼓泡的去离子水中,然后移入容积为50 mL的内衬聚四氟乙烯的反应釜中,用高纯N2鼓泡10 min后密封,分别在160、180和200 ℃下水热处理24 h,待自然冷却到室温后,经后续分离、洗涤、干燥后得到样品。不同水热处理温度下所得样品分别命名为IT-160,IT-180和IT-200。为了对比,采用类似的方法,以TiCl3为Ti源,在不加InCl3的条件下于180 ℃水热处理制备纯的Ti3+自掺杂纳米TiO2,所得浅蓝色粉末命名为T-180;并以TiCl4和InCl3为原料制备纯的TiO2和In2O3纳米粉体。
光电极的制作:分别称取0.02 g粉末样品,加入0.2 mL聚乙二醇2000和4 mL无水乙醇,经超声分散后,取600 μL悬浮液,在SYSC-100S型旋涂仪上,采用完全相同的转速进行旋转涂膜,将样品均匀涂覆在2.0 cm×2.0 cm的FTO玻璃上,然后在120 ℃下干燥30 min,再在260 ℃下热处理2 h。
1.2 样品的表征
物相组成表征在Rigaku DMax-2500型X射线衍射 (XRD) 仪上进行,Cu Kα(λ=0.154 18 nm) 辐射,Ni滤波片,扫描速度0.02°·min-1,广角衍射测量范围20°~70°。通过JEOL JEm-2100型高分辨透射电子显微镜 (HRTEM) 对样品的形貌和粒度进行观测。用ESCA 3000型X射线光电子能谱 (XPS) 仪对样品中元素的存在状态进行分析,Mg Kα(1 253.6 eV) 为辐射源,以C1s的284.6 eV结合能作标准。在岛津UV-2550型紫外-可见分光光度计测量样品的紫外-可见漫反射光谱 (UV-Vis DRS),以标准BaSO4为参比。在Perkin Elmer LS 55型荧光分光光度计上进行荧光光谱测试,激发波长为320 nm。配制浓度分别为5×10-4 mol·L-1和2×10-3 mol·L-1的对苯二甲酸与NaOH的混合溶液并加入40 mg催化剂,光照一段时间后取悬浊液离心,取上层清液并经2倍稀释后测溶液的荧光强度。样品的瞬态光电流测试在CHI660C型电化学工作站上进行,采用标准的三电极体系。在完全相同的电极制备和测试条件下,自制的光电极作为工作电极,铂丝和Ag/AgCl电极分别作为对电极和参考电极,浓度为0.1 mol·L-1的硫酸钠水溶液作电解质溶液。
1.3 样品的光催化性能
采用对RhB水溶液的吸附和降解来评价材料的光催化性能,将40 mg样品超声分散在80 mL浓度为1.0×10-5 mol·L-1的RhB水溶液中,先避光搅拌30 min,然后用北京泊菲莱科技有限公司生产的带有λ≥400 nm滤波片的PLS-SXE300型氙灯光照,光源与溶液的距离为30 cm,采用恒温水浴保持催化反应过程中温度在25 ℃左右。光催化反应过程中,每间隔10 min,取出2~3 mL溶液高速离心,然后用721型分光光度计测定溶液在不同光照时间下的吸光度A,用公式 (1) 计算光催化降解率[17]:
其中,A0为RhB溶液的初始吸光度值,At为催化反应过程中t时刻时溶液的吸光度值。
可见光下对苯酚水溶液的光催化降解实验流程与之类似,将40 mg催化剂样品加入浓度为6×10-5 mol·L-1的苯酚溶液中,在可见光下进行光照,每隔20 min取样,经高速离心分离后,采用4-氨基氨替吡啉比色法,在510 nm处测定溶液中苯酚的浓度。
2 结果与讨论
2.1 样品的表征
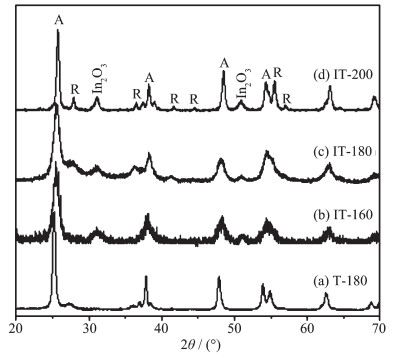
采用XRD研究不同水热处理温度下所得样品的物相结构,图 1是样品的XRD图。在不加InCl3的情况下,采用TiCl3为Ti源,在180 ℃下水热处理24 h所得样品为纯的TiO2,而且基本为TiO2(A),仅出现微弱的TiO2(R) 衍射峰 (图 1a)。在反应原料中加入InCl3后,当水热处理温度为160 ℃时,样品由TiO2(A) 和In2O3组成,在2θ=25.6°,38.1°,48.4°,54.3°和63.0°处的衍射峰对应TiO2(A) 的 (101)、(004)、(200)、(105) 和 (204) 晶面 (JCPDS No.21-1272),在2θ=30.6°和51.0°处的衍射峰对应In2O3的 (222) 和 (440) 晶面 (JCPDS No.88-2160)(图 1b)。由于In3+的半径 (0.081 nm) 远大于Ti4+的半径 (0.068 nm),因此In3+很难取代TiO2晶格中的Ti4+形成In3+掺杂的TiO2[25],而通常形成In2O3和TiO2的复合物[15, 26]。样品中In2O3的衍射峰非常弱,说明In2O3的颗粒尺寸非常小,而且高度弥散分布在TiO2中,或者结晶差造成的。随水热处理温度的升高,样品的结晶性变好,而且出现了金红石相TiO2(R)(图 1c,d)。在2θ=27.9°,36.5°,41.6°,44.3°,55.4°,56.6°处的衍射峰分别对应TiO2(R) 的 (110)、(101)、(111)、(210)、(211) 和 (220) 晶面 (JCPDS No.21-1276)。
 图 1
不同温度下水热处理24 h所得不同样品的XRD图
Figure 1.
XRD patterns of the different samples obtained at different hydrothermal treatment temperature for 24 h
图 1
不同温度下水热处理24 h所得不同样品的XRD图
Figure 1.
XRD patterns of the different samples obtained at different hydrothermal treatment temperature for 24 h
通过TEM和HRTEM来观察样品的颗粒尺寸、形貌和微结构。图 2是不同水热处理温度下所得样品的TEM和HRTEM照片,结果说明水热处理温度对材料的形貌有重要影响。从图 2可以看出,IT-160主要由大小较均匀的小颗粒组成,但存在一定的团聚现象 (图 2a),这可能是因为样品的结晶性较差,存在部分非晶成分造成的。当水热处理温度为180 ℃时,样品的形貌更为规则,团聚程度降低,而且出现了少量的短棒状结构 (图 2b)。HRTEM结果表明,样品主要TiO2(A) 颗粒组成,其中包含少量的In2O3颗粒 (图 2c)。晶格条纹间距d=0.348 nm的颗粒对应TiO2(A) 的 (101) 面,晶格条纹间距d=0.289 nm的颗粒对应In2O3的 (222) 面。当水热处理温度为200 ℃时,样品主要由纳米棒和纳米颗粒组成 (图 2d)。对IT-200样品进行HRTEM观测 (图 2e),纳米棒的晶格条纹间距为0.32 nm,对应TiO2(R) 的 (110) 晶面。紧紧负载在纳米棒上的纳米颗粒的晶格间距分别为0.348 nm和0.288 nm,分别对应TiO2(A) 的 (101) 和In2O3的 (222) 晶面,说明负载在纳米棒上的颗粒为TiO2(A) 和In2O3。这种一维结构的纳米棒为光生e-和h+的快速传输提供了通道,并有足够的空间用于光生e-和h+的分离,从而可以有效抑制光生载流子的复合[27]。
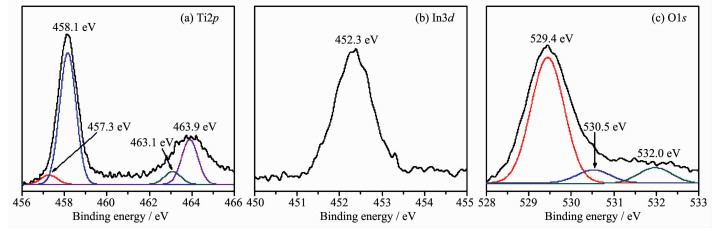
采用XPS对样品中Ti、In和O的化学态进行了分析,图 3a是样品IT-180中Ti2p的高分辨XPS谱及拟合结果。纯TiO2的Ti2p3/2和Ti2p1/2电子结合能为459.4和464.7 eV[28],与纯的TiO2相比,样品中Ti4+的Ti2p3/2和Ti2p1/2的结合能分别位于458.1和463.9 eV处,拟合后位于457.3和463.1 eV处的峰对应Ti3+的Ti2p3/2和Ti2p1/2的结合能,说明样品中的Ti以Ti4+和Ti3+ 2种价态存在[29],而Ti3+可以在TiO2的CB底形成局域态,从而使TiO2能够被可见光激发,同时Ti3+能够提高TiO2的导电性,促进e-迅速转移,有效抑制光生e--h+的复合[30]。图 3b是In3d的高分辨XPS谱,在452.3 eV的峰归于In3d3/2的电子结合能,证明铟以+3氧化态形成存在[17],但是样品中In3d3/2的结合能向高能方向移动,说明In2O3和TiO2之间存在强烈的相互作用,即二者之间形成了良好的异质结结构[18]。图 3c是O1s的XPS谱及拟合结果。样品中存在3种状态的氧,位于529.5,530.9和532 eV处的结合能峰分别归于Ti-O-Ti、In-O晶格氧和表面羟基氧[31-32]。
以上结果表明,将TiCl3和InCl3的混合溶液进行沉淀反应所得蓝紫色前驱体经水热处理后,能够制备得到Ti3+自掺杂的TiO2 /In2O3纳米异质结。水热处理温度影响产物的物相、结晶性和形貌。在较低的水热处理温度下,所得样品为Ti3+自掺杂的TiO2(A)/In2O3异质结,随水热处理温度的升高,样品的结晶性变好,而且为Ti3+自掺杂的TiO2(A)/TiO2(R)/In2O3异质结,并且TiO2(R) 为纳米棒结构。
在样品的制备过程中,当向TiCl3和InCl3的混合液中滴加NaOH溶液时,OH-和Ti3+、In3+发生沉淀反应,形成含有大量-OH的前驱体,由于Ti (OH)3和In (OH)3的Ksp⊖分别为1.0×10-40和1.3×10-37,而且溶液中Ti3+的浓度远大于In3+的浓度,因此首先形成Ti (OH)3沉淀,随后生成In (OH)3沉淀,即In (OH)3可能沉积在Ti (OH)3的表面。在水热处理过程中,非晶态的前驱体沉淀通过重结晶或原位转换生成晶态的氧化物[33]。当水热温度较低时,前驱体沉淀发生脱水缩合反应形成颗粒细小的TiO2(A) 和弥散分布的In2O3颗粒,从而得到Ti3+自掺杂的TiO2(A)/In2O3异质结。而在TiO2晶体生长过程中,一些金属离子和他们的含氧化合物能充当催化剂的角色,降低形成TiO2(R) 的活化能,促进TiO2的晶型转化,并且有利于形成TiO2(R) 纳米棒结构[34-37]。因此,随水热处理温度的升高,TiO2(A) 纳米颗粒逐渐形成TiO2(R) 纳米棒,没有转化的TiO2(A) 纳米颗粒和In2O3负载在TiO2(R) 纳米棒上,从而得到Ti3+自掺杂的TiO2(A)/TiO2(R)/In2O3纳米异质结。
2.2 样品光吸收和催化性能
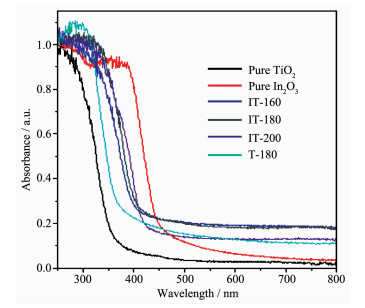
图 4给出了不同水热处理温度下所得复合样品以及纯的Ti3+自掺杂TiO2、TiO2和In2O3的UV-Vis DRS谱图,纯的TiO2禁带宽度大,因此在可见光区没有吸收,纯In2O3的吸收边位于450 nm附近,这与In2O3的带隙一致。与纯的TiO2相比,Ti3+自掺杂的TiO2和复合样品的吸收阈值向长波长方向移动,并且在400~800 nm的可见光范围内均有一定程度的吸收,显示了优良的光吸收特性。与单一的Ti3+自掺杂TiO2相比,复合后样品的吸收红移程度更大,这是因为In2O3的敏化作用引起的[6, 9-10]。Ti3+自掺杂的TiO2和与In2O3复合后材料在可见光区有明显的吸收,这一方面是因为Ti3+在TiO2的CB下方0.75~1.18 eV范围内形成局域态[22, 38],从而使材料能被可见光激发;另一方面是In2O3为窄带隙半导体,可以直接被可见光激发[6, 9-10],对TiO2起到敏化作用。样品在可见光区有吸收,说明样品能够被可见光激发产生e-和h+,从而能够表现出可见光催化性能。
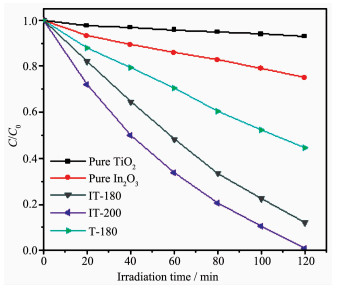
RhB水溶液经常被用来作为模拟废水检验半导体的光催化性能。图 5a是纯TiO2、In2O3、Ti3+自掺杂TiO2以及Ti3+自掺杂TiO2/In2O3异质结对RhB的吸附和可见光催化降解性能。在光照前,样品对RhB都有一定的吸附能力,其中IT-160的吸附性能最好,30 min对RhB的吸附率达到28.4%,这跟IT-160的结晶性差、颗粒尺寸小有关 (图 1b,图 2a)。打开光源进行辐照后,与纯的TiO2和In2O3相比,Ti3+自掺杂的TiO2以及复合后的IT样品具有优良的可见光催化降解RhB的活性,其中IT-200的光催化性能最好,50 min内几乎将RhB完全降解。
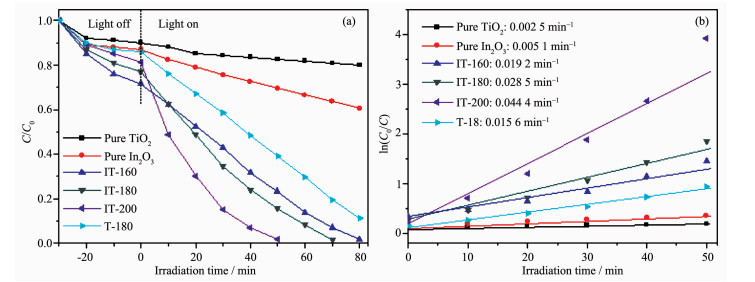 图 5
(a) 可见光下不同复合样品、Ti3+自掺杂TiO2及纯TiO2和In2O3对RhB的吸附和降解曲线; (b) 光催化降解RhB一级动力学曲线
Figure 5.
(a) Adsorption and photodegradation of RhB solutions by using Ti3+ self-doped TiO2, pure TiO2, In2O3, and Ti3+ self-doped TiO2/In2O3 heterojunctions as photocatalyst under visible light irradiation; (b) Variation in the normalized ln (C0/C) of the RhB concentration as a function of irradiation time
图 5
(a) 可见光下不同复合样品、Ti3+自掺杂TiO2及纯TiO2和In2O3对RhB的吸附和降解曲线; (b) 光催化降解RhB一级动力学曲线
Figure 5.
(a) Adsorption and photodegradation of RhB solutions by using Ti3+ self-doped TiO2, pure TiO2, In2O3, and Ti3+ self-doped TiO2/In2O3 heterojunctions as photocatalyst under visible light irradiation; (b) Variation in the normalized ln (C0/C) of the RhB concentration as a function of irradiation time
通过比较光催化降解反应速率常数来定量评估材料的光催化性能,悬浮液中有机污染物的光催化氧化反应服从Langmuir-Hinshelwood模型 (公式2)[17]:
其中,Ct是RhB水溶液在反应t时刻的浓度,C0是RhB的初始浓度,kapp是一级速率常数,kapp可以从ln (C0/C) 与时间的线性关系中获得。如图 5b所示,样品IT-200、IT-180、IT-160、T-180、纯TiO2和In2O3的反应速率常数分别为0.044 4、0.028 5、0.019 2、0.015 6、0.002 5和0.005 1 min-1,说明水热处理温度对异质结的光催化性能有很大影响。在所有样品中,IT-200的催化反应速率常数最大,分别是纯TiO2和In2O3的17.76倍和8.71倍。Ti3+自掺杂TiO2与In2O3形成异质结后,光催化降解性能明显高于单一的Ti3+自掺杂TiO2样品,说明形成异质结更有利于光催化反应的进行,这是因为异质结有助于光生e-和h+的快速分离, 降低e-和h+的复合几率[6-7, 9, 17]。
对光催化剂来说,样品的稳定性是影响其性能的重要因素,而Ti3+自掺杂的TiO2容易被空气和水中的溶解氧氧化而失去活性[22]。采用样品的重复使用实验来考察样品的稳定性,每次催化实验完成后将悬浊液进行高速离心分离,所得固体经洗涤后于80 ℃下干燥,然后重新加入RhB溶液进行光催化降解实验,所得结果如图 6所示。经5次重复使用后,纯的Ti3+自掺杂TiO2和200 ℃下水热处理24 h所得异质结样品的光催化降解性能没有明显下降,而且仍保持浅蓝色,说明样品有良好的稳定性,可以被重复利用。
在光催化降解研究中,作为有机染料的RhB常被用来作为模拟废水,考察样品的催化降解性能[10, 17, 39]。但考虑到作为有色染料的RhB可能具有敏化作用而使不能被可见光激发的半导体材料也具有可见光催化降解性能,我们进一步选取无色的苯酚作为模拟污染物,对样品的光催化性能进行研究。图 7为纯的TiO2、In2O3、Ti3+自掺杂TiO2以及复合样品IT-180、IT-200在可见光下对苯酚的光催化降解结果。从中可以看出,和纯的TiO2、In2O3相比,Ti3+自掺杂TiO2以及复合后的样品对苯酚的可见光催化降解性能明显提高,但复合后的降解性能更好,这和光催化降解RhB的结果一致,说明样品良好的光催化降解性能是由Ti3+的自掺杂和异质结的形成双重效应引起的。
2.3 光催化反应机理
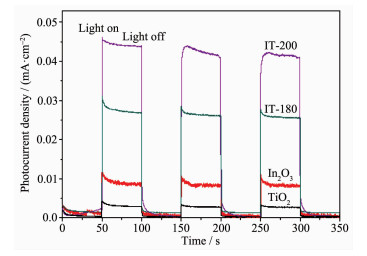
光电流可为确定光生e-和h+的分离效率提供直接的证据,电极产生的光电流越大,e-和h+的分离效率越高[40]。为了验证Ti3+自掺杂TiO2/In2O3异质结具有高的光生e-和h+的分离效率,在相同的条件下测试了可见光下由样品IT-180、IT-200和纯TiO2、In2O3制作的光电极的光电流密度随时间的响应曲线,结果于图 8表示。从中可以看出,由样品IT-180和IT-200所制备的光电极的光电流密度响应是可逆的和稳定的,纯的In2O3能产生一定的光电流,而纯TiO2的光电流密度非常小。这是由于Ti3+自掺杂的TiO2/In2O3异质结增强了材料的可见光响应性能并有助于光生e-和h+的分离,因此具有较大的光电流密度。
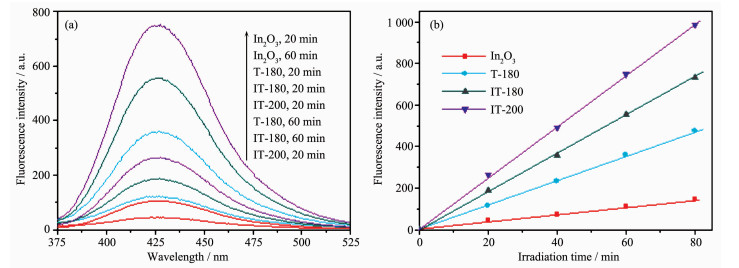
在液相光催化降解反应过程中,被普遍接受的催化降解机理是光生电子迁移到催化剂的表面与溶解氧结合形成超氧离子自由基·O2-,·O2-与H2O作用,经过一系列反应得到强氧化性的·OH,然后·OH将染料分子矿化分解[17, 35, 41]。为了验证不同催化剂在光催化过程中·OH的产率,采用对苯二甲酸光致发光探测技术 (TA-PL) 检测光催化反应过程中·OH的浓度[42-43]。在可见辐照下,对苯二甲酸 (TA) 捕获·OH生成2-羟基对苯二甲酸 (TAOH),TAOH的荧光强度与溶液中·OH的浓度成正比,荧光强度越强,说明产生的·OH越多,即光生e--h+越易分离,光催化活性越高[43]。图 9(a)为TA捕获由纯In2O3、Ti3+自掺杂TiO2(样品T-180) 以及复合样品IT-180、IT-200在光照20和60 min时的荧光光谱;图 9(b)是相应样品的荧光强度随光照时间的变化曲线。从图 9可以明显看出,随光照时间的延长,荧光强度逐渐加强,说明反应生成的·OH逐渐增多。在相同的条件下,异质结样品的荧光强度明显高于单一的Ti3+自掺杂TiO2,更高于纯的In2O3,说明复合后更有利于光生e-和h+的分离,这与光催化降解结果以及瞬态光电流响应结果一致。
以上结果表明Ti3+的自掺杂拓展了TiO2的光响应范围,使TiO2能被可见光激发,In2O3属于窄带隙半导体,可直接被可见光激发,而由Ti3+自掺杂的TiO2和In2O3组成的异质结加快了光生e-和h+的分离,有效抑制e--h+的复合,此外,材料表面的羟基基团可促进光催化反应进程,因此,Ti3+自掺杂的TiO2/In2O3异质结具有良好的可见光催化降解性能。
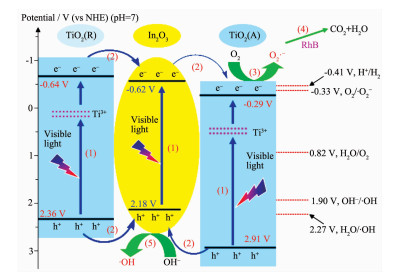
In2O3的CB和VB分别位于-0.62和2.18 V[13],锐钛矿相TiO2的CB和VB分别位于-0.29和2.91 V[14]。Deák等曾报道TiO2(R) 的CB比TiO2(A) 的CB高~0.35 eV,而VB高~0.55 eV[44-45],这种交错的能带结构使TiO2(A)、TiO2(R)、In2O3三者之间能够形成有效的异质结。而Ti3+在TiO2的CB底0.75~1.18 eV范围内形成局域态,因此TiO2能够响应可见光[38],据此,我们给出了如图 10所示的光生e-和h+的转移分离示意图。
在可见光激发下,电子分别从TiO2的VB跃迁至由Ti3+形成的局域态中,然后再跃迁至CB,并在VB留下h+;同时In2O3的VB上的e-被激发至In2O3的CB (图 10(1))[17, 35]。由于三者之间相互交错的能带结构,光生e-迅速从TiO2-x(R) 的CB转移至In2O3的CB,继而转移至TiO2-x(A) 的CB,同时h+分别从TiO2(R) 和TiO2(A) 的VB转移至In2O3的VB (图 10(2)),使光生e-和h+得到有效分离,这种电荷的定向迁移使光生e-和h+的复合几率降低,从而提高光催化活性和光电转换性能[6, 10, 18]。处于TiO2(A) 的CB上的e-和反应体系中溶解的氧反应生成·O2-,继而通过一系列反应将RhB降解 (图 10(3), (4)),位于In2O3的VB上的h+与-OH反应生成·OH (图 10(5)),这些活性基团 (·O2-,·OH) 进一步将有机污染物分子氧化降解。
3 结论
以TiCl3为钛源,InCl3为铟源,在不使用还原剂的条件下,水热处理前驱体沉淀并通过控制水热处理温度,得到Ti3+自掺杂的TiO2(A)/In2O3和TiO2(A)/TiO2(R)/In2O3纳米异质结。水热处理温度影响产物的物相、结晶性和形貌。在较低的水热处理温度下,所得样品为Ti3+自掺杂的TiO2(A)/In2O3异质结,随水热处理温度的升高,样品的结晶性变好,而且为Ti3+自掺杂的TiO2(A)/TiO2(R)/In2O3异质结,并且TiO2(R) 为纳米棒结构。可见光催化降解RhB和苯酚的结果表明材料具有良好的可见光催化活性,电化学测试结果表明材料具有快速的光生e-和h+的分离效率。Ti3+的自掺杂和In2O3的敏化拓展了异质结的光响应范围,不同晶相的TiO2和In2O3组成的异质结结构加快了光生e-和h+的分离,有效抑制e--h+的复合,此外,材料表面的羟基基团促进光催化反应的进行。
-
-
[1]
Kubacka A, Fernández-García M, Colón G. Chem. Rev., 2012, 112(3):1555-1614 doi: 10.1021/cr100454n
-
[2]
Liu G, Wang L Z, Yang H G, et al. J. Mater. Chem., 2010, 20(5):831-843 doi: 10.1039/B909930A
-
[3]
付荣荣, 李延敏, 高善民, 等.无机化学学报, 2014, 30(10):2231-2245 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?flag=1&file_no=20141001&journal_id=wjhxxbcnFU Rong-Rong, LI Yan-Min, GAO Shan-Min, et al. Chinese J. Inorg. Chem., 2014, 30(10):2231-2245 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?flag=1&file_no=20141001&journal_id=wjhxxbcn
-
[4]
Kudo A, Miseki Y. Chem. Soc. Rev., 2009, 38(1):253-278 doi: 10.1039/B800489G
-
[5]
Gai L G, Ma L, Jiang H H, et al. CrystEngComm, 2012, 4 (21):7479-7486
-
[6]
Liu H R, He X, Hu Y C, et al. Mater. Lett., 2014, 131:104-107 doi: 10.1016/j.matlet.2014.05.182
-
[7]
Zhao F, Lu Q F, Liu S W, et al. Mater. Lett., 2015, 139:19-21 doi: 10.1016/j.matlet.2014.10.028
-
[8]
Yu L H, Huang Y, Xiao G C, et al. J. Mater. Chem. A, 2013, 1 (34):9637-9640 doi: 10.1039/c3ta12207g
-
[9]
Xu L L, Guan J G, Gao L, et al. Catal. Commun., 2011, 12 (6):548-552 doi: 10.1016/j.catcom.2010.11.027
-
[10]
何霞, 刘海瑞, 董海亮, 等.无机材料学报, 2014, 29(3): 264-268HE Xia, LIU Hai-Rui, DONG Hai-Liang, et al. J. Inorg. Mater., 2014, 29(3): 264-268
-
[11]
Wang Z Y, Huang B B, Dai Y, et al. J. Phys. Chem. C, 2009, 113(11):4612-4617 doi: 10.1021/jp8107683
-
[12]
Lü J, Kako T, Li Z S, et al. J. Phys. Chem. C, 2010, 114(13): 6157-6162 doi: 10.1021/jp906550t
-
[13]
Zhu G Q, Hojamberdiev M, Katsumata K, et al. Adv. Powder Technol., 2014, 25(4):1292-1303 doi: 10.1016/j.apt.2014.03.008
-
[14]
Skorb E V, Antonouskaya L I, Belyasova N A, et al. Appl. Catal. B: Environ., 2008, 84(1/2):94-99
-
[15]
Shchukin D, Poznyak S, Kulak A, et al. J. Photochem. Photobiol. A: Chem., 2004, 162(2/3):423-430
-
[16]
Skorb E V, Ustinovich E A, Kulak A I, et al. J. Photochem. Photobiol. A: Chem., 2008, 193(2/3):97-102
-
[17]
Mu J B, Chen B, Zhang M Y, et al. ACS Appl. Mater. Interfaces, 2012, 4(1):424-430 doi: 10.1021/am201499r
-
[18]
Zhong J B, Li J Z, Zeng J, et al. Appl. Phys. A, 2014, 115 (4):1231-1238 doi: 10.1007/s00339-013-7965-z
-
[19]
Tian G H, Fu H G, Jiang L Q, et al. J. Phys. Chem. C, 2008, 112(8):3083-3089 doi: 10.1021/jp710283p
-
[20]
Su J, Zou X X, Chen J S. RSC Adv., 2014, 4(27):13979-13988 doi: 10.1039/c3ra47757f
-
[21]
孙杰, 孙鹤, 孙文彦.无机化学学报, 2014, 30(10):2308-2314 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?flag=1&file_no=20141010&journal_id=wjhxxbcnSUN Jie, SUN He, SUN Wen-Yan. Chinese J. Inorg. Chem., 2014, 30(10):2308-2314 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?flag=1&file_no=20141010&journal_id=wjhxxbcn
-
[22]
Hamdy M S, Amrollahi R, Mul G. ACS Catal., 2012, 2(12): 2641-2647 doi: 10.1021/cs300593d
-
[23]
Liu X, Gao S M, Xu H, et al. Nanoscale, 2013, 5(5):1870-1875 doi: 10.1039/c2nr33563h
-
[24]
Wang X T, Li Y M, Liu X, et al. Chinese J. Catal., 2015, 36 (3):389-399 doi: 10.1016/S1872-2067(14)60234-5
-
[25]
Yu Y L, Wang E J, Yuan J X, et al. Appl. Surf. Sci., 2013, 273:638-644 doi: 10.1016/j.apsusc.2013.02.098
-
[26]
Rodriguez-González V, Moreno-Rodriguez A, May M, et al. J. Photochem. Photobiol. A: Chem., 2008, 193(2/3):266-270
-
[27]
Tian J, Leng Y H, Zhao Z H, et al. Nano Energy, 2015, 11: 419-427 doi: 10.1016/j.nanoen.2014.10.025
-
[28]
Saha N C, Tompkins H G. J. Appl. Phys., 1992, 72(7):3072-3079 doi: 10.1063/1.351465
-
[29]
Espinós J P, Fernández A, González-Elipe A R. Surf. Sci., 1993, 295(3):402-410 doi: 10.1016/0039-6028(93)90287-T
-
[30]
Szczepankiewicz S H, Moss J A, Hoffmann M R. J. Phys. Chem. B, 2002, 106(11):2922-2927 doi: 10.1021/jp004244h
-
[31]
Guerrero M, Altube A, García-Lecina E, et al. ACS Appl. Mater. Interfaces, 2014, 6(16):13994-14000 doi: 10.1021/am5033549
-
[32]
Gurlo A, Barsan N, Weimar U, et al. Chem. Mater., 2003, 15 (23):4377-4383 doi: 10.1021/cm031114n
-
[33]
Li S F, Ye G L, Chen G Q. J. Phys. Chem. C, 2009, 113(10): 4031-4037 doi: 10.1021/jp8076936
-
[34]
Yanagisawa K, Ovenstone J. J. Phys. Chem. B, 1999, 103 (37):7781-7787 doi: 10.1021/jp990521c
-
[35]
Fu R R, Gao S M, Xu H, et al. RSC Adv., 2014, 4(70):37061-37069 doi: 10.1039/C4RA06152G
-
[36]
Xu C K, Shin P H, Cao L L, et al. Chem. Mater., 2009, 22 (1):143-148
-
[37]
Guo W X, Xu C, Wang X, et al. J. Am. Chem. Soc., 2012, 134(9):4437-4441 doi: 10.1021/ja2120585
-
[38]
Prokes S M, Gole J L, Chen X, et al. Adv. Funct. Mater., 2005, 15(1):161-167 doi: 10.1002/(ISSN)1616-3028
-
[39]
吴子伟, 吕晓萌, 沈佳宇, 等.无机化学学报, 2014, 30(3):492-498 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?flag=1&file_no=20140304&journal_id=wjhxxbcnWU Zi-Wei, LÜ Xiao-Meng, SHEN Jia-Yu, et al. Chinese J. Inorg. Chem., 2014, 30(3):492-498 http://www.wjhxxb.cn/wjhxxbcn/ch/reader/view_abstract.aspx?flag=1&file_no=20140304&journal_id=wjhxxbcn
-
[40]
Xiang Q J, Yu J G, Jaroniec M. J. Phys. Chem. C, 2011, 115 (15):7355-7363 doi: 10.1021/jp200953k
-
[41]
Murphy S, Saurel C, Morrissey A, et al. Appl. Catal. B: Environ., 2012, 119-120:156-165 doi: 10.1016/j.apcatb.2012.02.027
-
[42]
Guldi D M, Rahman G A, Sgobba V, et al. J. Am. Chem. Soc., 2006, 128(7):2315-2323 doi: 10.1021/ja0550733
-
[43]
Hu Y, Gao X H, Yu L, et al. Angew. Chem., 2013, 125(21): 5746-5749 doi: 10.1002/ange.201301709
-
[44]
Deák P, Aradi B, Frauenheim T. J. Phys. Chem. C, 2011, 115(8):3443-3446 doi: 10.1021/jp1115492
-
[45]
Carneiro J T, Savenije T J, Moulijn J A, et al. J. Phys. Chem. C, 2011, 115(5):2211-2217 doi: 10.1021/jp110190a
-
[1]
-
图 5 (a) 可见光下不同复合样品、Ti3+自掺杂TiO2及纯TiO2和In2O3对RhB的吸附和降解曲线; (b) 光催化降解RhB一级动力学曲线
Figure 5 (a) Adsorption and photodegradation of RhB solutions by using Ti3+ self-doped TiO2, pure TiO2, In2O3, and Ti3+ self-doped TiO2/In2O3 heterojunctions as photocatalyst under visible light irradiation; (b) Variation in the normalized ln (C0/C) of the RhB concentration as a function of irradiation time
-

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 1
- 文章访问数: 1388
- HTML全文浏览量: 148




 下载:
下载:









 下载:
下载:

