 图式 1
醛的氧化
Scheme1.
Oxidation of aldehyde
图式 1
醛的氧化
Scheme1.
Oxidation of aldehyde

Citation: Tian Qingqiang, Wang Huajun, Yuan Jianyong. Oxidation of Aromatic Aldehydes by Sodium Chlorite and Hydrogen Peroxide under Neutral Conditions[J]. Chemistry, 2017, 80(12): 1143-1147.

中性条件下亚氯酸钠和双氧水氧化芳香醛
English
Oxidation of Aromatic Aldehydes by Sodium Chlorite and Hydrogen Peroxide under Neutral Conditions
-
Key words:
- Sodium chlorite
- / Hydrogen peroxide
- / Neutral condition
- / Oxidation
- / Aldehyde
-
广泛用于药物合成的羧酸主要通过醛氧化获得[1, 2]。目前,工业上芳香酸主要由芳香醛通过高锰酸钾或者双氧水氧化制得。事实上,通过高锰酸钾氧化制备会产生大量锰渣,不仅浪费资源,还会造成严重的环境污染,工业化难度大[3]。通过双氧水氧化制备,反应剧烈,反应过程不易控制,容易引起安全事故,工业化难度大[4, 5]。探索一种安全性高、成本低廉、适合工业化的制备芳香酸的方法十分必要。NaClO2是广泛使用的废水净化剂和氧化消毒剂[6, 7],在有机合成中可用于醛的氧化,但常规条件要使用酸。在此,我们探究了在中性条件下使用NaClO2和H2O2对芳香族醛和α, β-不饱和醛进行氧化,可以高产率得到目标产物,该方法具有良好的工业化应用前景。
为了最大程度地提高收率、节省能源、降低成本、提高反应效率,本文以3, 4-二甲氧基苯甲醛为原料优化出溶剂、亚氯酸钠-双氧水的投入量、温度等反应条件。在此基础上进一步拓展了反应的底物适应范围(图式 1)。
1 实验部分
1.1 实验仪器和试剂
WRS-1B数字熔点仪(上海精密仪器科学仪器有限公司);核磁共振谱仪(德国Bruker公司);1-2-S电热恒温鼓风干燥箱(上海博讯实业有限公司);安捷伦(Agilent)1260高效液相色谱仪(安捷伦科技有限公司);高效液相C18反相色谱柱WondaCract ODS-2(上海岛津技迩商贸有限公司)。
4, 5-二甲氧基-2-硝基苯甲醛(纯度大于99%,自制);3, 4-二甲氧基苯甲醛(藜芦醛)、苯甲醛、3-甲基苯甲醛、4-甲基苯甲醛、2-氟苯甲醛、2-溴苯甲醛、3-氯苯甲醛、4-氯苯甲醛、2-噻吩甲醛、1-萘甲醛、2-萘甲醛、3-硝基苯甲醛、α-甲基肉桂醛、α-氯代肉桂醛、苯丙炔醛、对甲氧基苯甲醛、对乙酰氨基苯甲醛、对甲硫基苯甲醛、反式己烯醛等均为市售国产分析纯级试剂。
1.2 实验步骤
1.2.1 醛的氧化
将1mmol醛(1)和2.5mL乙醇加到25mL三口瓶中加热到40℃,依次加入2mmol双氧水和1.1mmol亚氯酸钠,用薄层色谱跟踪显示反应完全,降至室温,缓慢加入亚硫酸氢钠直到使淀粉碘化钾试纸不变蓝为止,抽滤得滤饼,水洗3次,粗产物经200目的硅胶色谱柱纯化得目标产物2。
3, 4-二甲氧基苯甲酸(2a):白色固体,收率99%,熔点179~180℃(文献值[8]179~181℃);1H NMR (400MHz,CDCl3) δ:7.72(dd,J=8.4、2.0 Hz,1H),7.60(d,J=2.0Hz,1H),7.13(d,J=8.4 Hz,1H),3.99(s,3H),3.90(s,3H);13C NMR(101MHz,CDCl3)δ:147.71,133.60,128.83,103.73,103.34,92.4,91.5,36.1,35.9。
4, 5-二甲氧基-2-硝基苯甲酸(2b):淡黄色固体,收率98%,熔点189~190℃(文献值[9]185℃);1H NMR (400MHz,CDCl3)δ:7.63(s,1H),6.95(s,1H),3.91(s,3H),3.86(s,3H);13C NMR(101MHz,CDCl3) δ:171.40,153.75,148.71,124.60,121.63,112.33,110.34,56.09,56.03。
3-甲基苯甲酸(2c):白色固体,收率99%,熔点109~112℃(文献值[10]109~111℃);1H NMR(400MHz,CDCl3) δ:8.07~7.68 (m,2H),7.65~7.16 (m,2H),2.44(s,3H);13C NMR(101MHz,CDCl3) δ:169.8,138.30,134.55,130.74,129.34,128.38,127.40,21.26。
4-甲基苯甲酸(2d):白色固体,收率99%,熔点180~182℃(文献值[10]180~182℃);1H NMR(400MHz,CDCl3)δ:7.85(d,J=8.2 Hz,2H),7.20(d,J=8.0 Hz,2H),2.3(s,3H);13C NMR (101MHz,CDCl3) δ:172.10,144.61,130.27,129.22,126.64,21.77。
2-氟苯甲酸(2e):白色固体,收率98%,熔点122~124℃(文献值[10]122~125℃);1H NMR(400MHz,CDCl3)δ:8.05(t,J=6.9Hz,1H),7.59(dd,J=12.3、6.5Hz,1H),7.25(dd,J=9.5、5.5Hz,1H),7.22~7.14(m,1H);13C NMR(101MHz,CDCl3)δ:169.38,163.95,161.34,135.61,132.78,124.13,117.18。
2-溴苯甲酸(2f):白色固体,收率95%,熔点144~148℃(文献值[11]147~149℃);1H NMR(400MHz,CDCl3)δ:8.07~8.00(m,1H),7.77~7.70(m,1H),7.48~7.37(m,2H);13CNMR(101MHz,CDCl3)δ:170.94,134.88,133.54,132.45,130.44,127.30,122.59。
3-氯苯甲酸(2g):白色固体,收率94%,熔点150~152℃(文献值[10]151~152℃);1H NMR (400MHz,CDCl3) δ:8.07(d,J=18.4Hz,1H),8.00(d,J=7.0Hz,1H),7.59(d,J=7.7Hz,1H),7.51~7.38(m,1H);13C NMR(101MHz,CDCl3) δ:170.90,134.73,133.90,131.02,130.28,129.86,128.33。
4-氯苯甲酸(2h):白色固体,收率99%,熔点237~238℃(文献值[10]236~237℃);1H NMR(400MHz,CDCl3)δ:8.06(d,J=8.5Hz,2H),7.48(d,J=8.5Hz,2H);13C NMR(101MHz,CDCl3)δ:169.44,131.58,131.58,128.92,128.92。
2-噻吩甲酸(2i):白色固体,收率95%,熔点124~126℃(文献值[11]125~129℃);1H NMR(400MHz,CDCl3)δ:7.93(dd,J=3.8、1.2Hz,1H),7.68(dd,J=5.0,1.2Hz,1H),7.17(dd,J=4.9、3.8Hz,1H);13C NMR(101MHz,CDCl3)δ:167.54,135.02,134.01,132.90,128.09。
1-萘甲酸(2j):白色固体,收率85%,161~162℃(文献值[12]160~162℃);1H NMR(400MHz,CDCl3)δ:9.09(d,J=8.7Hz,1H),8.42(dd,J=7.3、1.2Hz,1H),8.10(d,J=8.2Hz,1H),7.92(d,J=8.1Hz,1H),7.60~7.53(m,3H);13C NMR(101MHz,CDCl3)δ:172.92,134.64,133.96,131.85,131.66,128.73,128.13,126.35,125.93,125.61,124.56。
2-萘甲酸(2k):白色固体,收率98%,熔点186~187℃(文献值[12]186~187℃)。1H NMR(400MHz,CDCl3)δ:8.79~8.69(m,1H),8.13(dd,J=8.6、1.7Hz,1H),8.00(d,J=8.0Hz,1H),7.95~7.88(m,2H),7.60(dddd,J=22.1、8.0、6.9、1.3Hz,2H);13C NMR(101MHz,CDCl3) δ:171.80,135.98,132.47,132.16,129.56,128.68,128.35,127.84,126.80,126.52,125.41。
苯甲酸(2l):白色固体,收率99%,熔点120~123℃(文献值[13]121~123℃);1H NMR(400MHz,CDCl3)δ:8.16~8.10(m,2H),7.66~7.58(m,1H),7.51~7.45(m,2H);13C NMR(101MHz,CDCl3)δ:172.27,133.84,130.24,129.33,128.51。
3-硝基苯甲酸(2m):淡黄色固体,收率93%,熔点141~142℃(文献值[14]140~142℃);1H NMR(400MHz,CDCl3)δ:9.06~8.79(m,1H),8.48(ddd,J=16.3、8.8、4.5Hz,2H),7.72(t,J=8.0Hz,1H);13CNMR(101MHz,CDCl3)δ:168.84,148.41,135.77,131.00,129.87,128.23,125.25。
α-甲基肉桂酸(2n):白色固体,收率94%,熔点99~102℃(文献值[15]98~99℃);1H NMR(600MHz,CDCl3)δ:7.87(s,1H),7.52~7.21(m,5H),2.18(s,3H);13CNMR(151MHz,CDCl3) δ:174.32,141.13,135.60,129.86,128.46,127.58,13.74。
α-氯代肉桂酸(2o):淡黄色固体,收率95%,熔点139~143℃(文献值[16]143~144℃);1H NMR(600MHz,CDCl3)δ:8.06(s,1H),7.94~7.89(m,2H),7.51~7.45(m,3H);13C NMR(151MHz,CDCl3)δ:168.03,139.23,132.61,130.94,130.75,128.64,120.98。
苯丙炔酸(2p):白色固体,收率95%,熔点135~136℃(文献值[17]131~133℃);1H NMR(600MHz,DMSO-d6)δ:12.68(s,1H),10.24(s,1H),7.88(d,J=8.6Hz,2H),7.69(d,J=8.6Hz,2H);13CNMR(151MHz,DMSO-d6)δ:169.31,167.39,143.79,130.83,125.33,118.61,24.61。
对甲氧基苯甲酸(2q):浅绿色固体,收率91%,熔点179~182℃(文献值[18]181~182℃);1H NMR (600MHz,DMSO-d6)δ:7.91(d,J=8.6Hz,2H),6.95(d,J=8.3Hz,2H),3.79(s,3H);13CNMR(151MHz,DMSO-d6)δ:169.4,164.9,131.69,123.8,113.89,55.79。
对乙酰氨基苯甲酸(2r):白色固体,收率97%,熔点255~256℃(文献值[19]262℃);1H NMR(600MHz,DMSO-d6)δ:10.24(s,1H),7.88(d,J=8.6Hz,2H),7.69(d,J=8.6Hz,2H),2.08(s,3H);13C NMR(151MHz,DMSO-d6)δ:169.31,167.39,143.79,130.83,125.33,118.61,24.61。
对甲硫基苯甲酸(2s):白色固体,收率94%,熔点198~199℃(文献值[20]199~200℃);1H NMR(600MHz,DMSO-d6) δ:7.84 (d,J=8.4Hz 2H),7.34 (d,J=8.4Hz 2H),2.50(s,3H);13C NMR(151MHz,DMSO-d6)δ:167.61,144.87,130.46,127.92,125.12,14.53。
己烯酸(2t):白色固体,收率91%,熔点31~33℃(文献值[21]32.8~33℃);1H NMR (600MHz,CDCl3)δ:7.13~6.99(m,1H),5.83(d,J=15.6Hz,1H),2.20(q,J=7.1Hz,2H),1.56~1.44(m,2H),0.95(q,J=7.3Hz,3H);13C NMR(151MHz,CDCl3)δ:172.39,151.74,121.15,34.26,21.15,13.63。
1.2.2 亚氯酸钠和双氧水氧化醛的放大实验
在3000mL的三口瓶中加入600mL乙醇、100g(0.47mol)4, 5-二甲氧基-2-硝基苯甲醛和246mL H2O2(30(wt)%,2.4mol)溶液,滴加135g NaClO2溶液(80(wt)%,1.2mol),于40℃条件下搅拌5h。向混合物中加入NaHSO3以淬灭反应,将乙醇减压蒸馏回收,然后滤出不溶物,将其用40%的NaOH水溶液溶解,用H2SO4调节pH至1,有沉淀析出。将沉淀物过滤并水洗滤饼,真空箱干燥4h,得黄色固体产物(2b)99.3g,收率为93%,通过高效液相色谱测定纯度为99.5%。
2 结果与讨论
2.1 溶剂对收率的影响
以3, 4-二甲氧基苯甲醛为底物探究溶剂对亚氯酸钠/双氧水氧化醛的影响。由表 1可知,乙醇为最佳反应溶剂,在该体系中产物收率可达94%,而且反应时间短。
 表 1
溶剂对亚氯酸钠和双氧水氧化3, 4-二甲氧基苯甲醛的影响
Table 1.
Effect of solvents on oxidation of 3, 4-dimethoxybenzaldehyde by NaClO2 and H2O2
表 1
溶剂对亚氯酸钠和双氧水氧化3, 4-二甲氧基苯甲醛的影响
Table 1.
Effect of solvents on oxidation of 3, 4-dimethoxybenzaldehyde by NaClO2 and H2O2
序号 溶剂 时间/h 产率a/% 1 乙醇 2 94 2 甲醇 3 89 3 异丙醇 2 83 4 甲基叔丁基醚 6 80 5 氯仿 6 56 6 四氢呋喃 4 86 7 乙酸乙酯 5 65 8 二氯甲烷 6 60 a分离产率 2.2 温度对收率的影响
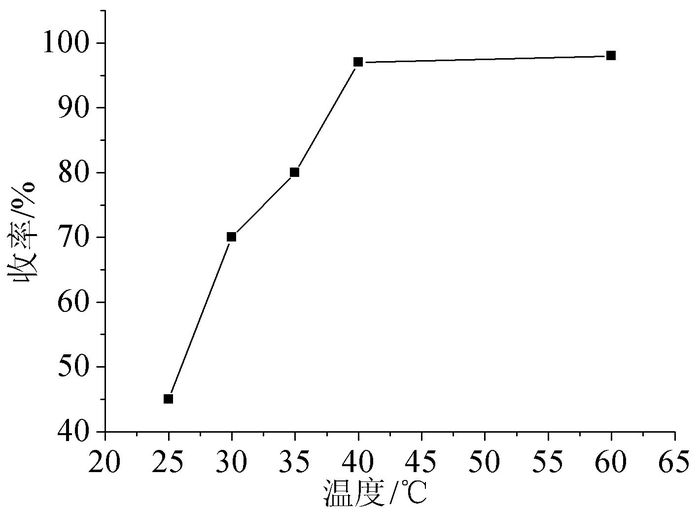
氧化反应在较温和的条件下即可发生,同时温度是影响双氧水分解的重要因素。以3, 4-二甲氧基苯甲醛为底物探究温度对收率的影响。由图 1可知,温度较低时反应不完全,收率较低;高于40℃后再提高温度产率无明显上升,同时可能会导致双氧水分解。所以40℃是较优的反应温度,此条件下反应的收率为97%。
2.3 亚氯酸钠和双氧水的用量对收率的影响
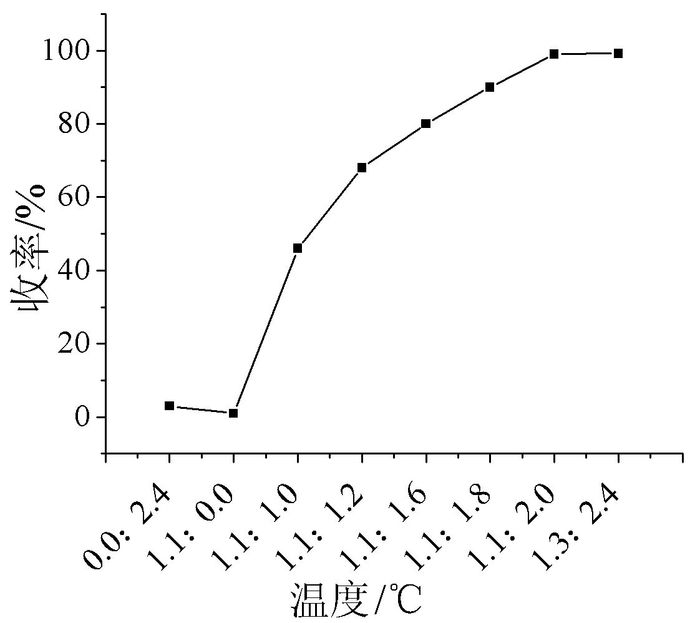
亚氯酸钠和双氧水的用量可以影响到醛的氧化效果,以3, 4-二甲氧基苯甲醛为底物探究了亚氯酸钠和双氧水的用量对醛氧化的收率影响。由图 2可知,n(NaClO2):n(H2O2)=1.1:2时产率最高,继续增加双氧水的量产率没有明显变化。
2.4 中性条件下亚氯酸钠和双氧水对醛的氧化
利用上述优化工艺条件。以乙醇为溶剂、亚氯酸钠:双氧水:醛=1.1:2:1,考察了不同取代基对反应的影响。从表 2可以看出,底物取代基的不同对氧化反应的收率和反应时间也有着不同的影响。实验结果表明,α, β-不饱和醛、芳香族杂环醛、芳族醛和脂族醛在该体系中都表现出良好的反应性。

条目 R 产物 反应时
间/h产率a
/%1 3, 4-dimethoxyphenyl 2a 2 99 2 4, 5-dimethoxy-2-nitrophenyl 2b 2 98 3 3-MeC6H4 2c 3 99 4 4-MeC6H4 2d 3 99 5 2-FC6H4 2e 3 98 6 2-BrC6H4 2f 3 95 7 3-ClC6H4 2g 1 94 8 4-ClC6H4 2h 3 99 9 2-thiophene 2i 3 95 10 1-naphthyl 2j 3 85 11 2-naphthyl 2k 3 98 12 Ph 2l 3 99 13 3-NO2C6H4 2m 1 93 14 C6H5CH=C(CH3) 2n 3 94 15 C6H5CH=C(Cl) 2o 3 95 16 C6H5CC 2p 3 95 17 p-CH3OC6H4 2q 4 91 18 p-CH3CONHC6H4 2r 7 97 19 p-CH3SC6H4 2s 4 94 20 CH3CH2CH2CH=CH 2t 3 91 a分离产率 3 结论
亚氯酸钠和双氧水的混合体系可以高产率、高选择性、清洁和安全地将醛氧化成羧酸,并且在中性条件下对醛可以选择性氧化,该体系对α, β-不饱和醛、芳香族杂环醛、芳族醛和脂族醛表现出良好的反应性。此外,该体系还对具有较大空间位阻的醛也显示出良好的反应性。其副产物是清洁无污染的氧和钠盐。在此基础上,使用4, 5-二甲氧基-2-硝基苯甲醛作为底物进行放大实验,4, 5-二甲氧基-2-硝基苯甲酸的产率为93%,表明该氧化体系具有良好工业应用前景。
-
-
[1]
E Dalcanale, F Montanari. J. Org. Chem., 1986, 51:567~569. doi: 10.1021/jo00354a037
-
[2]
B S Bal. W E Childers, H WPinnick. Tetrahedron, 1981, 37:2091~2096.
-
[3]
J Sedelmeier, S V Ley, I R Baxendale et al. Org. Lett., 2010, 12:3618~3621. doi: 10.1021/ol101345z
-
[4]
李泽江.精细与专用化学品, 2010, (11):1~5. doi: 10.3969/j.issn.1008-1100.2010.11.001
-
[5]
王玉强.广东化工, 2006, (01):45~46. doi: 10.3969/j.issn.1007-1865.2006.01.019
-
[6]
黄云翔.广州化工, 1997, (03):15~20. http://www.cnki.com.cn/Article/CJFDTotal-GZHA199703004.htm
-
[7]
周重道, 龙军, 徐培芳.化学世界, 1993, (01):40~42. http://www.cnki.com.cn/Article/CJFDTotal-HXSS199301013.htm
-
[8]
X A Wu, P Ying, J Y Liu. Synth. Commun., 2009, 39(19):3459~3470. doi: 10.1080/00397910902778001
-
[9]
H L Goering, A C Backus, C S Chang et al. J. Org. Chem., 1975, 40(11):1533~1535. doi: 10.1021/jo00899a002
-
[10]
P Marcé, J Lynch, A J Blacker et al. Chem. Commun., 2016, 52(5):1013~1016. doi: 10.1039/C5CC08681G
-
[11]
X Y Wang, Z P Shang, G F Zha. Tetrahed. Lett., 2016, 57(50):5628~5631. doi: 10.1016/j.tetlet.2016.11.002
-
[12]
R Zheng, Q Z Zhou, H N Gu. Tetrahed. Lett., 2014, 55(41):5671~5675. doi: 10.1016/j.tetlet.2014.08.090
-
[13]
BBarati, M Moghadam, A Rahmati et al. Synlett, 2013, 24(1):90~96.
-
[14]
S Battula, A Kumar, Q N Ahmed. Org. Biomol. Chem., 2015, 13(39):9953~9956. doi: 10.1039/C5OB01615K
-
[15]
V VPatil, G S Shankarling. J. Org. Chem., 2015, 80(16):7876~7883. doi: 10.1021/acs.joc.5b00582
-
[16]
A H A Youssef, H M Abdel-Maksoud. J. Org. Chem., 1975, 40(22):3227~3229. doi: 10.1021/jo00910a014
-
[17]
X H Wei, S J Yang, N Liang et al. Molecules, 2013, 18(1):1325~1336. doi: 10.3390/molecules18011325
-
[18]
O Marvi, M Talakoubi. Orient. J. Chem., 2016, 32(1):359~365. doi: 10.13005/ojc
-
[19]
A N Manin, A P Voronin, K V Drozd et al. Eur. J. Pharm. Sci., 2014, 65:56~64. doi: 10.1016/j.ejps.2014.09.003
-
[20]
A Correa, R Martin. J. Am. Chem. Soc., 2009, 131(44):15974~15975. doi: 10.1021/ja905264a
-
[21]
F Tellier, R Sauvetre. Tetrahed. Lett., 1993, 34(34):5433~5436. doi: 10.1016/S0040-4039(00)73927-X
-
[1]
-
表 1 溶剂对亚氯酸钠和双氧水氧化3, 4-二甲氧基苯甲醛的影响
Table 1. Effect of solvents on oxidation of 3, 4-dimethoxybenzaldehyde by NaClO2 and H2O2
序号 溶剂 时间/h 产率a/% 1 乙醇 2 94 2 甲醇 3 89 3 异丙醇 2 83 4 甲基叔丁基醚 6 80 5 氯仿 6 56 6 四氢呋喃 4 86 7 乙酸乙酯 5 65 8 二氯甲烷 6 60 a分离产率 表 2 不同的醛氧化成酸的结果
Table 2. Results of the oxidation of different aldehydes into acids

条目 R 产物 反应时
间/h产率a
/%1 3, 4-dimethoxyphenyl 2a 2 99 2 4, 5-dimethoxy-2-nitrophenyl 2b 2 98 3 3-MeC6H4 2c 3 99 4 4-MeC6H4 2d 3 99 5 2-FC6H4 2e 3 98 6 2-BrC6H4 2f 3 95 7 3-ClC6H4 2g 1 94 8 4-ClC6H4 2h 3 99 9 2-thiophene 2i 3 95 10 1-naphthyl 2j 3 85 11 2-naphthyl 2k 3 98 12 Ph 2l 3 99 13 3-NO2C6H4 2m 1 93 14 C6H5CH=C(CH3) 2n 3 94 15 C6H5CH=C(Cl) 2o 3 95 16 C6H5CC 2p 3 95 17 p-CH3OC6H4 2q 4 91 18 p-CH3CONHC6H4 2r 7 97 19 p-CH3SC6H4 2s 4 94 20 CH3CH2CH2CH=CH 2t 3 91 a分离产率 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 0
- HTML全文浏览量: 0


 下载:
下载:


 下载:
下载:

