 图1
ARDF(a)和NRDF(b)样品的照片
Figure1.
Pictures of ARDF(a) and NRDF(b)
图1
ARDF(a)和NRDF(b)样品的照片
Figure1.
Pictures of ARDF(a) and NRDF(b)

Citation: LIN Jun-heng, YANG Wen-shen, YIN Xiu-li, WU Chuang-zhi. Release of HCl and H2S during pyrolysis of aged refuse derived-fuels[J]. Journal of Fuel Chemistry and Technology, 2018, 46(2): 152-160.

矿化垃圾衍生燃料热解过程HCl与H2S析出规律
English
Release of HCl and H2S during pyrolysis of aged refuse derived-fuels
-
Key words:
- HCl
- / H2S
- / aged refuse derived-fuels
- / normal refuse derived-fuels
- / pyrolysis
-
“十三五”规划报告中的调研结果显示,2015年中国仍有约3.0×107 t生活垃圾未得到无害化处理[1]。现阶段,垃圾无害化处理方式主要包括堆肥、热处理和卫生填埋三种。堆肥具有处理成本低和环境友好等优势,但其处理量和处理效率相对较低;热处理是现阶段最具前景的垃圾无害化处理方式,但存在较高的设备技术要求和昂贵的投资成本等问题,大规模推广仍需一定的时间;卫生填埋是中国现阶段最主要的垃圾处理方式,2015年卫生填埋处理量占总处理量的66.2%[1],其具有技术要求低和处理效率高等优势,但同样存在占地面积大和环境不友好等缺陷。同时越发严格的建厂标准和土地资源的限制也使得投资成本越来越高。一个中大型填埋场的建成需要4.0×107元资金和3-5年时间,可使用年限仅为20年,而后需要30-50年进行保养恢复[2],周期漫长。因此,亟需开发高效的填埋垃圾处理方式,进而实现填埋场库容的动态循环利用和土地复原。
填埋垃圾经若干年降解后,基本上达到稳定状态,极少产生渗滤液和气体,且生物可降解组分含量在3%以下,因此, 又被称为矿化垃圾[3]。赵由才等[3, 4]研究发现,矿化垃圾具有渗透性好、结构松散、重金属含量合格及不含致病菌等特点,可安全开采,具备较好的应用前景。欧盟早在1999年的矿化垃圾处理指南中便指出,通过建设多座垃圾发电厂以利用矿化垃圾,进而减少其存量和实现填埋场的复原[5]。Bosmans等[6]研究发现,矿化垃圾经过必要的分类和预处理可制备成RDF(Refuse Derived-Fuels),可有效提高其运输和能源利用效率。矿化垃圾制成的RDF热值可达到10-20 MJ/kg,而且在焚烧发电等热处理利用过程中符合相关污染物的排放标准[7]。Chalermcharoenrat等[8]利用下吸式气化反应器研究了矿化垃圾中RPF(Refuse Plastic and Paper Fuel)的气化特性,发现在空气当量比为0.144时,燃气热值达到4.41 MJ/m3。而添加Ni-Mg-La/Al2O3催化剂后,燃气热值可提高至15-19 MJ/m3[9]。由此可见,矿化垃圾的能源化利用不仅对填埋场土地复原和垃圾减容等方面具有显著意义,而且具有一定的经济性。
垃圾可通过焚烧、热解和气化等热处理技术得以高效利用。其中, 热解处理技术可实现垃圾快速减容目标,同时也提供高热值燃气,具有较好的工业应用前景[10]。但在热解过程中,垃圾含有的元素Cl和S易以HCl和H2S的形式进入热解气,进而加速了设备的高温腐蚀[11]。如何有效地减少腐蚀性气氛的释放和减缓设备的腐蚀,已成为垃圾热解利用方向的研究重点。近年来,前人关于热解过程中生活垃圾的HCl和H2S释放规律也开展了一些相关研究[12-15],但多针对其慢速热解或单组分热解过程。在实际热处理过程中,垃圾基本能在较短时间内达到较高的热解温度,而这一快速热解过程中HCl和H2S的析出多受二次反应的影响,造成其析出规律不同于慢速热解过程[16]。同时,多组分间的相互作用也不可忽略。单组分PVC在400 ℃时热解,其所含Cl的90%便以HCl的形式析出[17],而在相同条件下,混合塑料的HCl析出率则为80%左右[16];而相比于慢速热解,PVC在快速热解条件下析出更少的HCl,以及更多的含Cl焦油[18];热解过程中,更多的挥发分含量有利于垃圾中的有机S以H2S形式析出[12];较高的热解温度能促使原料中的S向较稳定的固相S转化,使得固相S含量升高[19, 20]。另外,矿化垃圾形成过程的特殊性,也会造成其HCl和H2S的释放规律有别于常规垃圾,而该方面的研究却很少报道。
本研究分别以常规垃圾衍生燃料(Normal Refuse Derived-Fuel,NRDF)和填埋场矿化垃圾成型燃料(Aged refuse Derived-Fuel,ARDF)为原料,利用热重分析仪-傅里叶红外光谱-质谱(TG-FTIR-MS)在线联用分析法和水平固定床管式炉反应器,分析了热解温度及热解类型对析出行为的影响,并对热解固相产物腐蚀性元素的赋存特点进行了考察。
1 实验部分
1.1 实验原料
本研究所用实验样品见图 1。
ARDF由广西省阳朔市葡萄镇某矿化垃圾成型厂提供;而NRDF样品原料采集自广西省桂林市葡萄镇某垃圾回收站,由废纸、废塑料、废草木和纺织废品等组成,原料经烘干、按特定比例混合[21]及破碎(粒径3 mm以下)后,通过电子万能试验机(WD-100KE,Guangzhou YDYQ Precision Instruments Co., LTD.,China)制得直径为10 mm的NRDF颗粒,成型条件为130 ℃和75 MPa。ARDF和NRDF样品经粉碎和筛分,得粒径为150 μm以下的物料,并于105 ℃下干燥至恒重后备用。
1.2 分析仪器及表征方法
采用元素分析仪(Vario EL cube,Elementaranalyse,Germany)对样品中C、H、N和S元素含量进行定量测定;参照JIS Z7302-6-1999标准,使用氧弹量热仪(WZR-1T-CII,Changsha Bente Intrusments Co. Ltd.,China)和分光光度计(DR3900,HACH,USA),采用高温燃烧-硫氰酸汞分光光度法测得样品中总Cl含量。在搅拌条件下,将样品浸渍于去离子水中6 h,并采用硫氰酸汞分光光度法(DR3900,HACH,USA)测定所得滤液中的Cl-离子含量,计算得到样品中的无机Cl元素含量。同时,采用离子色谱仪(883 IC,Metrohm,Swiss)测定所得滤液中的SO42-含量,计算得到样品中硫酸盐含量。以高纯N2为载气,在密闭环境中将样品溶解于1:10磷酸溶液中,并将所产生的尾气通入醋酸锌溶液中。反应持续20 min后,采用亚甲基蓝法在分光光度计测定醋酸锌溶液中的S2-浓度,计算得到样品中硫化物的含量。O元素含量则通过差减法求得。参照GB/T 28731—2012标准,采用箱式气氛炉(MX1100-30,Shmicrox Co.,Ltd.,China)分别对干基样品中的挥发分(V)、固定碳(FC)和灰分(A)含量进行测定。实验采用热重分析仪(STA 449F3,Netzsch,Germany)、傅里叶红外光谱仪(TENSOR 27,Bruker,Germany)和质谱仪(Omnistar,Pfeiffer-Vacuum,Germany)在线联用分析样品的慢速热解过程(200-900 ℃),定性考察慢速热解过程中HCl和H2S的释放规律,升温速率为30 ℃/min,热解终温为900 ℃,N2流量为40 mL/min。以2798 cm-1作为HCl的特征吸收波长[14];H2S的特征质荷比为34[22]。根据前人的研究[14, 23],强度-温度/时间积分可以表达相对析出量,但两种样品中的Cl和S含量并不相同,无法直接通过对比积分得出样品慢速热解过程中HCl和H2S析出率的高低,因此, 本研究引入RHCl和RH2S表示HCl和H2S的相对析出率,其计算公式如下:
式中,AHCl和AH2S分别表示TG-FTIR-MS结果中HCl和H2S析出峰峰面积,wCl和wS分别表示样品中Cl和S元素的含量,RHCl和RH2S均为无量纲值。
1.3 实验装置及分析方法
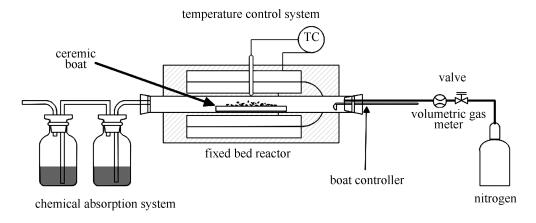
快速热解实验在炉长为60 cm的水平管式炉上进行,实验装置见图 2。
热解反应器为长1200 mm、内径44 mm的石英管,通过热电偶对电加热系统精确控温。每次实验均将精确称量的3.00 g原料平铺于陶瓷样品舟中,并将样品舟置于石英管的常温区域。反应器密封后,以400 mL/min的流量通入纯度为99.9%的N2,并在反应前持续吹扫30 min,以确保实验在惰性气氛下进行。目标热解温度分别设定为450、550、650、750和850 ℃,稳定升至设定温度后,将样品舟迅速推入管式炉中心反应区,持续热解30 min后,将样品舟拉至常温区冷却。实验过程中,尾气导入两组串联的分别装有100 mL NaOH(0.05 mol/L)溶液和100 mL NaAc-ZnAc(0.05 mol/L)缓冲溶液的孟氏洗瓶中,以确保热解气中的HCl和H2S被充分吸收,并分别采用硫氰酸汞分光光度法(GB/T 13580.9—1992)和亚甲基蓝分光光度法(GB/T 16489—1996)定量检测吸收液中Cl-和S2-含量。样品舟中固相产物冷却至室温后称重,并采用氧弹量热仪、分光光度计和元素分析仪分别检测固相中的Cl和S含量。每组实验平行进行2次或3次,标准偏差不大于5%。通过公式(3)-(6)计算两种样品的HCl(YHCl-Cl)和H2S(YH2S)析出率以及固相产物中固相Cl(Ysolid-Cl)和固相S(Ysolid-S)含量。
2 结果与讨论
2.1 样品特性分析
城市生活垃圾中的Cl含量为0.3%-1.5%,S含量为0.05%-0.4%[7, 24],具体见表 1,本实验中所用NRDF样品中的Cl和S含量分别为1.37%和0.15%,说明本实验样品具有一定的代表性。常规生活垃圾中大部分的Cl来源于塑料的聚氯乙烯(PVC),且多以有机Cl的形式存在;而S则多存在于纸张、橡胶和布料中,主要以硫酸盐和有机硫形式存在[24]。经过长时间降解,矿化垃圾中的Cl多以无机盐形式存在[25]。因此,相较于样品NRDF,ARDF中具有较低的Cl含量(0.95%)和较高的无机Cl含量(0.46%),以及较高的总S含量(0.65%)和无机S含量(0.103%),同时,ARDF样品含有较高的灰分(41.68%)和较低的挥发分(40.75%)。因此,在相同的热解条件下,相较于样品NRDF,ARDF具有产气量低和残渣量高的特点。
Sample Ultimate analysis wdb*/% Proximate analysis wdb*/% C H N O** total
Sinorganic
Stotal
Clinorganic
ClA V FC ARDF 35.95 2.56 0.85 18.29 0.65 0.103 0.95 0.46 41.68 40.75 17.57 NRDF 57.26 6.23 0.87 22.64 0.15 0.007 1.37 0.14 11.48 75.96 12.56 *: dried basis;**: calculated by difference 2.2 慢速热解的HCl和H2S释放特性
2.2.1 RDF慢速热解特征
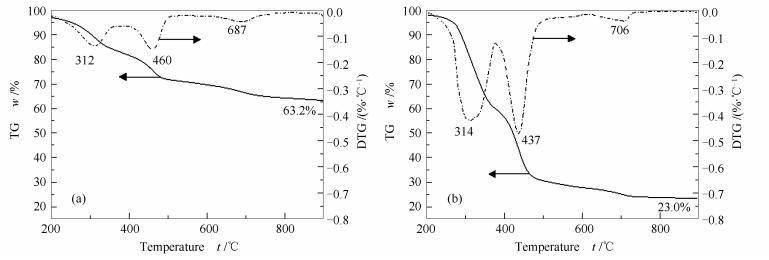
为准确分析样品的热解失重特性,对样品进行了热重实验分析,结果见图 3。
ARDF与NRDF具有相似的热失重特性,均包括三个反应阶段,温度分别为200-375、375-505和600-760 ℃。第一阶段主要为生物质类组分和少部分塑料类组分热解,析出CO2、H2O和C2-5轻质烃等物质;第二阶段主要为塑料类组分热解,析出CO、H2和CH4等小分子气体;第三阶段,垃圾中的含氧酸盐达到分解温度,析出CO2和CO等气体[22, 26]。根据原料特性,由于矿化垃圾长期处于填埋场中降解,可分解组分含量降低,导致ARDF的热解失重率(36.8%)明显低于NRDF(77.0%),该结论与工业分析中的ARDF高灰分和低挥发分特性相互印证。
2.2.2 慢速热解过程中HCl释放特性
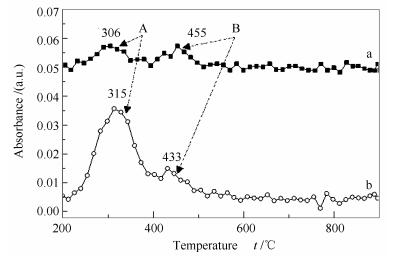
通过TG-FTIR定性考察样品慢速热解过程中HCl的析出特性,结果见图 4。
由图 4可知,在慢速热解过程中,两种样品H2S的析出均分两个阶段,结合前人的研究结果可知[13, 17]:第一段析出温度为200-400 ℃,垃圾样品中的塑料、纺织废物和生物质组分热解产生一定量的HCl;第二段析出温度为400-520 ℃,样品发生碳骨架重构环化反应,再次析出一定量的HCl。表 2为样品ARDF和NRDF的HCl红外吸收峰峰面积及HCl相对析出率计算值RHCl。
 表 2
ARDF和NRDF的HCl红外吸收峰峰面积及HCl相对析出率计算值RHCl
Table 2.
Absorbance area of HCl and RHCl of HCl from ARDF and NRDF
表 2
ARDF和NRDF的HCl红外吸收峰峰面积及HCl相对析出率计算值RHCl
Table 2.
Absorbance area of HCl and RHCl of HCl from ARDF and NRDF
Sample Area of
peak AArea of
peak BResult
of RHClARDF 0.6632 0.4344 115.5 NRDF 2.973 0.7283 270.2 由表 2可知,NRDF的RHCl值是ARDF的2.3倍,说明在慢速热解过程中NRDF的HCl析出率明显高于ARDF。由表 1可知,相较于样品NRDF,ARDF原料Cl含量较低(0.95%),同时含有大量的无机Cl(0.46%),而在慢速热解过程中,无机Cl盐向HCl的转化主要通过无机Cl盐与挥发分和无机氧化物(如SiO2、CO2)发生氢交换反应完成[15],ARDF较低的挥发分含量明显降低了热解过程中氢交换反应发生的几率,从而造成ARDF相对较低的HCl析出率。
2.2.3 慢速热解过程中H2S释放特性
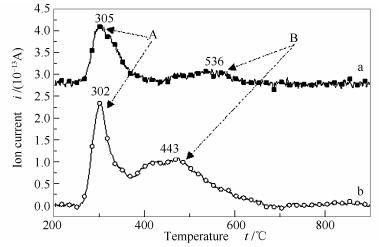
通过TG-MS定性考察样品慢速热解过程中H2S的析出特性,结果见图 5。
由图 5可知,在慢速热解过程中,两种样品H2S的析出均分两个阶段:第一段析出温度为230-370 ℃,主要为脂肪硫化合物分解产生的H2S;第二段析出温度为380-670 ℃,主要为芳香硫和杂环硫分解产生的H2S[27]。同时可发现,ARDF的第二析出峰(536 ℃)比NRDF(443 ℃)延后,说明相较于样品NRDF,ARDF中芳香硫和杂环硫的芳构化程度较高[20],导致分解析出H2S温度较高。表 3为样品ARDF及NRDF的H2S离子吸收峰峰面积及H2S相对析出率计算值RH2S。
 表 3
ARDF及NRDF的H2S离子吸收峰峰面积及H2S相对析出率计算值RH2S值
Table 3.
Ion current area of H2S and RH2S of ARDF and NRDF
表 3
ARDF及NRDF的H2S离子吸收峰峰面积及H2S相对析出率计算值RH2S值
Table 3.
Ion current area of H2S and RH2S of ARDF and NRDF
Sample Area of
peak A
/ 1×10-11Area of
peak B
/ 1×10-11Result of
RH2S
/ 1×10-9ARDF 0.861 0.316 1.811 NRDF 1.276 1.792 20.453 由表 3可知,NRDF的RH2S值是ARDF的11倍,说明在慢速热解过程中NRDF的H2S相对析出率明显大于ARDF。相较于ARDF,NRDF中的挥发分含量高,热解时产生的大量氢自由基,能明显促进其S元素向H2S转化[12]。ARDF虽然S含量相对较高,但挥发分含量低,且其无机硫组分含量较高(0.103%),有机硫又多为稳定的芳香S化合物,因此, ARDF的S元素向H2S转化较为困难。
2.3 快速热解腐蚀性元素气相释放和固相赋存特性
2.3.1 快速热解过程中样品的Cl元素气相释放和固相赋存特性
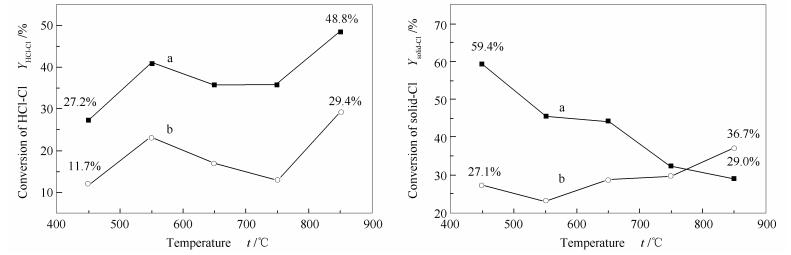
为进一步对比研究实际热解过程中ARDF和NRDF的HCl释放规律,本研究进行了快速热解实验,并对样品中HCl的析出量和固相Cl含量进行了定量分析,结果见图 6。
由图 6可知,样品ARDF和NRDF在快速热解过程中具有相似的HCl析出规律。当热解温度为450 ℃时,样品ARDF和NRDF的HCl析出率均为最低值(27.2%和11.7%);当热解温度在450-850 ℃时,HCl析出率随时间成S型变化(先高后低再高)的趋势,并在850 ℃时,HCl析出率达到最高(48.8%和29.4%)。但样品ARDF和NRDF的固相Cl含量变化规律趋势并不相同。当热解温度由450 ℃升高至550 ℃时,两种样品热解后的固相Cl含量均有所下降;当热解温度在550-850 ℃时,ARDF中的固相Cl含量随热解温度的升高而降低,而NRDF却随热解温度的升高而升高。当热解温度450 ℃时,ARDF的固相Cl含量最高(59.4%);而当热解温度为850 ℃时,NRDF的固相Cl含量最高(36.7%)。
由表 1可知,ARDF和NRDF的原料中无机Cl和有机Cl含量比例各不相同,因而两者会在快速热解过程中表现出不同的热解析出特性。随热解温度的升高,两种样品的HCl析出率和固相Cl含量表现出了不同的变化趋势。根据慢速热解实验结果可知,ARDF和NRDF的第二阶段HCl析出均在400-520 ℃完成,可见在450 ℃的快速热解试验中仍有部分存在于PVC中的Cl并未析出,因此, 当热解温度升至550 ℃时,两种样品均出现HCl析出率增高和固相Cl含量降低的现象。样品NRDF中有机Cl比例较高(89.8%),因此, 在快速热解过程中表现出明显的有机Cl反应规律,当热解温度在550-850 ℃,较快的升温速率导致样品NRDF中的有机Cl还未完成脱氯反应便以焦油Cl的形式进入气相;且较快的升温速率还会导致样品析出较多的多环芳烃[28],其易与析出的HCl反应形成氯代芳烃,进而导致样品的HCl析出率下降[18];而当热解温度为850 ℃时,热解过程中形成的含Cl焦油开始裂解并析出HCl,同时高温挥发的无机Cl盐也会与挥发分反应生成一定量的HCl,从而使得NRDF样品的HCl析出率在温度升至850 ℃有所提高;随着温度升高,高温使一部分含Cl焦油在样品表面进一步碳化形成固相C-Cl键,且该趋势随热解温度的升高而越加明显,从而导致NRDF中固相Cl含量随热解温度的升高而增加。
ARDF则因含有较高量的无机Cl(48.4%),在快速热解过程中同时表现出无机Cl和有机Cl的反应规律,当热解温度在550-850 ℃,无机Cl盐转化为HCl的量随热解温度的升高而增高[29],因此, 随热解温度的升高,ARDF热解固相产物中无机Cl含量不断减少,且减少量明显高于焦油Cl吸附于样品表面形成的固相Cl,从而造成ARDF中总固相Cl含量下降。与NRDF中同样的原理,由于快速热解下挥发分更容易形成多环芳香化合物,当热解温度在550-750 ℃,ARDF热解析出的HCl亦有一部分转化为含Cl焦油,导致HCl析出率下降。通过对比ARDF和NRDF的固相Cl含量,可以发现,ARDF的最高固相Cl含量(59.4%)比NRDF(36.7%)要高,说明在矿化垃圾在热解利用过程中,Cl元素不易释放进入气相,有利于固相赋存。
2.3.2 快速热解过程中样品的S元素气相释放和固相赋存特性
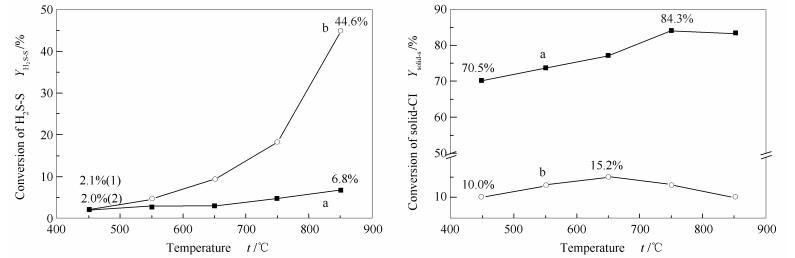
本研究对样品ARDF和NRDF在快速热解过程中H2S的析出量和固相S含量定量分析,以对比研究热解温度对H2S释放规律的影响,实验结果见图 7。
在快速热解过程中,ARDF和NRDF的H2S析出率随热解温度的升高而升高,当热解温度为850 ℃时,析出率达到最高(6.8%和44.6%),此时ARDF和NRDF的最大H2S析出量分别为668和442 μg/g。随热解温度升高,ARDF和NRDF中固相S含量呈先升高后降低的趋势。当热解温度为750 ℃时,ARDF固相S含量达到最高(84.3%);而NRDF则在热解温度为650 ℃时,固相S含量达到最高(15.2%)。
在快速热解过程中,样品除析出的H2S和产生的固相S组分外,还会产生一定量的含S焦油化合物,其中的部分含S焦油化合物以气态形式析出,并可进一步裂解生成H2S,且转化率随热解温度的升高而升高;同时,有部分含S焦油组分吸附于样品表面并进一步碳化形成有机固相S[19]。随着热解温度的升高,样品在快速热解过程中会产生更多的含S焦油化合物,进而在一定程度上增加了样品的固相S含量。吸附于样品表面的含S焦油组分亦可进一步裂解生成H2S,根据所形成的含S焦油化合物的稳定性不同,所需要的裂解温度不同。由慢速热解实验结果可知,ARDF中芳香硫的芳构化程度较高,其快速热解过程中产生的含S焦油化合物更加稳定,分解产生H2S所需热解温度更高,所以ARDF在快速热解中在750 ℃以上才表现出明显的H2S析出率增长。因此,相较于样品NRDF,ARDF在较高的热解温度下达到最高固相S含量。通过对比ARDF和NRDF的固相S含量,可以发现,ARDF的最高固相S含量(84.3%)明显高于NRDF(15.2%),说明在矿化垃圾在热解利用过程中,S元素不易释放进入气相,有利于固相赋存。
3 结论
样品ARDF和NRDF具有相似的慢速热解特性,主要包括三个反应阶段,分别为200-375、375-505和600-760 ℃。但由于ARDF具有较高的灰分含量(41.68%),造成其热失重率相对较低(36.8%)。在慢速热解过程中,样品均以两个温度段析出HCl(200-400和420-500 ℃)和H2S(230-370和380-670 ℃)。样品ARDF具有较高的无机Cl含量和较低的挥发分含量,而所含S又多以无机S和稳定的芳香S化合物形式存在,因此, 相较于样品NRDF,ARDF在慢速热解过程中表现出较低的HCl和H2S析出率。
在快速热解过程中,ARDF和NRDF的HCl析出率随温度的升高呈S型变化(先升高后降低再升高)的趋势,而H2S的析出率与温度呈正相关,两种样品的HCl、H2S析出率均在850℃达到峰值,HCl析出率分别为48.8%(ARDF)和29.4%(NRDF),H2S析出率分别为6.8%(ARDF)和44.6%(NRDF)。
ARDF的Cl和S元素最高赋存率分别可达59.4%(450 ℃)和84.3%(750 ℃),而NRDF的Cl和S元素最高赋存率分别仅为36.7%(850 ℃)和15.2%(650 ℃),ARDF的Cl和S元素明显高于NRDF。说明在合适的热解条件下,相比NRDF,样品ARDF的腐蚀性元素不易释放进入气相,倾向于固相赋存。
-
-
[1]
"十三五"全国城镇生活垃圾无害化处理设施建设规划[R]. 北京: 国家发展改革委住房城乡建设部, 2016."The 13th Five-Year Plan" construction planning for harmless treatment facilities of national municipal wastes[R]. Beijing: Ministry of Housing and Urban-Rural Development of the People's Republic of China, 2016.
-
[2]
李华, 赵由才. 填埋场稳定化垃圾的开采、利用及填埋场土地利用分析[J]. 环境卫生工程, 2000,8,(2): 56-57+61. LI Hua, ZHAO You-cai. The exploitation of stabilizing solid waste and the utilization analysis for the land of landfill site[J]. Environ Sanit Eng, 2000, 8(2): 56-57+61.
-
[3]
赵由才, 柴晓利, 牛冬杰. 矿化垃圾基本特性研究[J]. 同济大学学报(自然科学版), 2006,34,(10): 1360-1364. doi: 10.3321/j.issn:0253-374X.2006.10.017ZHAO You-cai, CHAI Xiao-li, NIU Dong-jie. Characteristics of aged refuse in closed refuse landfill in Shanghai[J]. J Tongji Univ (Nat Sci), 2006, 34(10): 1360-1364. doi: 10.3321/j.issn:0253-374X.2006.10.017
-
[4]
ZHAO Y C, WANG L C, HUA R H, XU D M, GU G W. A comparison of refuse attenuation in laboratory and field scale lysimeters[J]. Waste Manage, 2002, 22(1): 29-35. doi: 10.1016/S0956-053X(01)00028-9
-
[5]
COMMISSION E. Council Directive 99/31/EC of 26 April 1999 on the landfill of waste (Landfill Directive)[EB]. 1999.
-
[6]
BOSMANS A, VANDERREYDT I, GEYSEN D, HELSEN L. The crucial role of Waste-to-Energy technologies in enhanced landfill mining:a technology review[J]. J Clean Prod, 2013, 55(14): 10-23.
-
[7]
ROTHEUT M, QUICKER P. Energetic utilisation of refuse derived fuels from landfill mining[J]. Waste Manage, 2017, 62: 101-117. doi: 10.1016/j.wasman.2017.02.002
-
[8]
CHALERMCHAROENRAT S, LAOHALIDANOND K, KERDSUWAN S. Optimization of combustion behavior and producer gas quality from reclaimed landfill through highly densify RDF-gasification[J]. Energy Procedia, 2015, 79: 321-326.
-
[9]
KAEWPENGKROW P, ATONG D, SRICHAROENCHAIKUL V. Pyrolysis and gasification of landfilled plastic wastes with Ni-Mg-La/Al2O3 catalyst[J]. Environ Technol, 2012, 33(22/24): 2489-2495.
-
[10]
袁浩然, 鲁涛, 熊祖鸿, 黄宏宇, 小林敬幸, 陈勇, 黎志强. 城市生活垃圾热解气化技术研究进展[J]. 化工进展, 2012,31,(2): 421-427. YUAN Hao-ran, LU Tao, XIONG Zu-hong, HUANG Hong-yu, KOBAYASHI Noriyuki, CHEN Yong, LI Zhi-qiang. Advance in pyrolysis and gasification of municipal solid waste study[J]. Chem Ind Eng Prog, 2012, 31(2): 421-427.
-
[11]
PAN T J, GESMUNDO F, NIU Y. Corrosion behavior of three iron-based model alloys in reducing atmospheres containing HCl and H2S at 600℃[J]. Corros Sci, 2007, 49(3): 1362-1377. doi: 10.1016/j.corsci.2006.06.014
-
[12]
HU H, FANG Y, LIU H, YU R, LUO G, LIU W, LI A, YAO H. The fate of sulfur during rapid pyrolysis of scrap tires[J]. Chemosphere, 2014, 97(1): 102-107.
-
[13]
YUAN G, CHEN D, YIN L, WANG Z, ZHAO L, WANG J Y. High efficiency chlorine removal from polyvinyl chloride (PVC) pyrolysis with a gas-liquid fluidized bed reactor[J]. Waste Manage, 2014, 34(6): 1045-1050. doi: 10.1016/j.wasman.2013.08.021
-
[14]
ZHU H M, JIANG X G, YAN J H, CHI Y, CEN K F. TG-FTIR analysis of PVC thermal degradation and HCl removal[J]. J Anal Appl Pyrolysis, 2008, 82(1): 1-9.
-
[15]
LANE D J, VAN EYK P J, ASHMAN P J, KWONG C W, DE NYS R, ROBERTS D A, COLE A J, LEWIS D M. Release of Cl, S, P, K, and Na during thermal conversion of algal biomass[J]. Energy Fuels, 2015, 29(4): 2542-2554. doi: 10.1021/acs.energyfuels.5b00279
-
[16]
WILLIAMS E A, WILLIAMS P T. The pyrolysis of individual plastics and a plastic mixture in a fixed bed reactor[J]. J Chem Technol Biot, 1997, 70(1): 9-20. doi: 10.1002/(ISSN)1097-4660
-
[17]
YU J, SUN L, MA C, QIAO Y, YAO H. Thermal degradation of PVC:A review[J]. Waste Manage, 2016, 48: 300-314. doi: 10.1016/j.wasman.2015.11.041
-
[18]
ZHOU H, WU C, ONWUDILI J A, MENG A, ZHANG Y, WILLIAMS P T. Influence of process conditions on the formation of 2-4 ring polycyclic aromatic hydrocarbons from the pyrolysis of polyvinyl chloride[J]. Fuel Process Technol, 2016, 144(Supplement C): 299-304.
-
[19]
MENG N, JIANG D, LIU Y, GAO Z, CAO Y, ZHANG J, GU J, HAN Y. Sulfur transformation in coal during supercritical water gasification[J]. Fuel, 2016, 186: 394-404. doi: 10.1016/j.fuel.2016.08.097
-
[20]
XU L, YANG J L, LI Y M, LIU Z Y. Behavior of organic sulfur model compounds in pyrolysis under coal-like environment[J]. Fuel Process Technol, 2004, 85(8/10): 1013-1024.
-
[21]
阮松宾. 广西县级城镇生活垃圾处理方式和工艺探讨[J]. 环境卫生工程, 2008,16,(1): 27-30. RUAN Song-bin. Discussion about means and process of country towns domestic waste treatment in Guangxi[J]. Environ Sanit Eng, 2008, 16(1): 27-30.
-
[22]
SINGH S, WU C, WILLIAMS P T. Pyrolysis of waste materials using TGA-MS and TGA-FTIR as complementary characterisation techniques[J]. J Anal Appl Pyrolysis, 2012, 94: 99-107. doi: 10.1016/j.jaap.2011.11.011
-
[23]
HOTOV G, SLOV K V. Quantitative TG-MS analysis of evolved gases during the thermal decomposition of carbon containing solids[J]. Thermochim Acta, 2016, 632(Supplement C): 23-28.
-
[24]
GUO X E, YANG X L, LI H, WU C Z, CHEN Y, LI F, XIE K C. Release of hydrogen chloride from combustibles in municipal solid waste[J]. Environ Sci Technol, 2001, 35(10): 2001-2005. doi: 10.1021/es991208r
-
[25]
钱小青, 牛东杰, 楼紫阳, 赵由才. 填埋场矿化垃圾资源综合利用研究进展[J]. 环境卫生工程, 2006,14,(2): 62-64. QIAN Xiao-qing, NIU Dong-jie, LOU Zi-yang, ZHAO You-cai. Development of resource comprehensive application study on mineralized waste in landfill Site[J]. Environ Sanit Eng, 2006, 14(2): 62-64.
-
[26]
S RUM L, GR NLI M G, HUSTAD J E. Pyrolysis characteristics and kinetics of municipal solid wastes[J]. Fuel, 2001, 80(9): 1217-1227.
-
[27]
WANG X, SI J, TAN H, MA L, POURKASHANIAN M, XU T. Nitrogen, sulfur, and chlorine transformations during the pyrolysis of straw[J]. Energy Fuels, 2010, 24(9): 5215-5221. doi: 10.1021/ef1007215
-
[28]
EFIKA E C, ONWUDILI J A, WILLIAMS P T. Products from the high temperature pyrolysis of RDF at slow and rapid heating rates[J]. J Anal Appl Pyrolysis, 2015, 112(Supplement C): 14-22.
-
[29]
杜胜磊, 陈汉平, 杨海平, 胥广富, 王贤华, 张世红.生物质热解过程中F和Cl的迁徙行为研究[J].中国电机工程学报, 2010, 30(14):115-120.DU Sheng-Lei, CHEN Hai-ping, XU Guang-fu, WNAG Xian-hua, ZHANG Shi-hong. Transformation behavior of F and Cl during biomass pyrolysis[J]. Proc CSEE, 2010, 30(14):115-120.
-
[1]
-
表 1 ARDF和NRDF的元素分析与工业分析
Table 1. Ultimate and proximate analysis of ARDF and NRDF
Sample Ultimate analysis wdb*/% Proximate analysis wdb*/% C H N O** total
Sinorganic
Stotal
Clinorganic
ClA V FC ARDF 35.95 2.56 0.85 18.29 0.65 0.103 0.95 0.46 41.68 40.75 17.57 NRDF 57.26 6.23 0.87 22.64 0.15 0.007 1.37 0.14 11.48 75.96 12.56 *: dried basis;**: calculated by difference 表 2 ARDF和NRDF的HCl红外吸收峰峰面积及HCl相对析出率计算值RHCl
Table 2. Absorbance area of HCl and RHCl of HCl from ARDF and NRDF
Sample Area of
peak AArea of
peak BResult
of RHClARDF 0.6632 0.4344 115.5 NRDF 2.973 0.7283 270.2 表 3 ARDF及NRDF的H2S离子吸收峰峰面积及H2S相对析出率计算值RH2S值
Table 3. Ion current area of H2S and RH2S of ARDF and NRDF
Sample Area of
peak A
/ 1×10-11Area of
peak B
/ 1×10-11Result of
RH2S
/ 1×10-9ARDF 0.861 0.316 1.811 NRDF 1.276 1.792 20.453 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 0
- HTML全文浏览量: 0


 下载:
下载:






 下载:
下载:

