 图 1
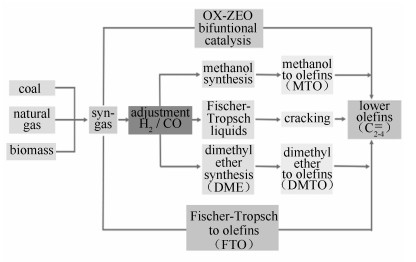
合成气转化制备低碳烯烃路径示意图
Figure 1.
Various routes for the production of lower olefins via syngas
图 1
合成气转化制备低碳烯烃路径示意图
Figure 1.
Various routes for the production of lower olefins via syngas

Citation: YU Fei, LI Zheng-jia, AN Yun-lei, GAO Peng, ZHONG Liang-shu, SUN Yu-han. Research progress in the direct conversion of syngas to lower olefins[J]. Journal of Fuel Chemistry and Technology, 2016, 44(7): 801-814.

合成气催化转化直接制备低碳烯烃研究进展
English
Research progress in the direct conversion of syngas to lower olefins
-
Key words:
- lower olefins
- / syngas
- / Fischer-Tropsch reaction
- / bifunctional catalysis
- / reaction mechanism
- / nanometer catalysis
-
低碳烯烃(乙烯、丙烯、丁烯) 是重要的有机化工原料,其产业发展水平和市场供需平衡情况直接影响整个石化工业的发展水平和产业规模。随着国民经济的快速增长,中国对低碳烯烃的需求急速增长,低碳烯烃的生产研发也受到了越来越多的关注。在传统工业中,乙烯主要通过石脑油、石油气和凝析油裂解得到[1]。丙烯可从石脑油蒸汽裂解制乙烯副产物或流化催化裂化过程的裂化气中得到。在蒸汽裂解工艺中,通过调整裂解深度可以改变丙烯和乙烯的比例,轻度裂解可产生更多丙烯[2]。由于石油资源的日益减少和C1化学的迅速发展,为缓解对石油资源的依赖,世界各国的研究主要以非石油路线为主,即利用煤炭、天然气、生物质等含碳资源通过合成气直接或间接制备烯烃,路径示意图见图 1。以合成气制备得到的甲醇为原料,通过甲醇或二甲醚路线是发展非石油资源生产乙烯、丙烯等产品的核心技术[3]。该技术包括两个步骤,即合成气经铜基催化剂合成甲醇,甲醇再经分子筛催化剂转化为低碳烯烃。如果能减少反应步骤,将合成气直接高选择性合成低碳烯烃,将体现出流程更短、能耗更低的优势,有较强的竞争力,未来发展前景更为良好[4, 5]。综述的目的是对近年来合成气催化转化制备低碳烯烃(尤其是费托反应路线直接制备低碳烯烃) 的相关进展进行简要的评述。
1 合成气间接制备低碳烯烃
从合成气出发间接制取低碳烯烃技术主要是指MTO (Methanol to Olefins) 工艺[3]。MTO工艺是指由合成气首先制备甲醇,再由甲醇脱水生成二甲醚,二甲醚与甲醇混合物继续脱水生成以乙烯、丙烯为主的低碳烯烃产物。其主反应为:
甲醇制取低碳烯烃的研究主要集中在催化剂的设计以及工艺改进。20世纪80年代,中国科学院大连化学物理研究所研发了ZSM-5及其改性MTO催化剂,并成功应用于固定床反应器;而后他们又开发了应用于流化床的小孔径SAPO-34分子筛催化剂[6-10],目前,该技术已比较成熟并已实现了商业化。
近年来,由于丙烯的应用不断扩大,全球丙烯需求增大率一直高于乙烯。与传统的MTO工艺同时生产乙烯和丙烯不同,甲醇制丙烯(MTP) 工艺主要生产丙烯,丙烯选择性可达80%以上。目前,MTP工艺的关键在于催化剂选择性和稳定性的提高以及相应的工艺流程设计,代表性技术有德国鲁奇公司(Lurgi) 的MTP,清华大学FMTP及大连化学物理研究所开发的DMTP工艺,其中,后两者皆采用流化床技术。德国鲁奇公司采用改性ZSM-5分子筛催化剂并应用于MTP生产,这种催化剂具有较好的稳定性,采用固定床进行反应,在425 ℃以及1.5 ×105 Pa条件下,甲醇转化率为97%、丙烯的收率可以达到70%[11]。
2 合成气直接制备低碳烯烃
2.1 双功能催化路线
尽管MTO过程具有较高的低碳烯烃选择性及转化率,但需先将合成气转化为甲醇,再经由分子筛催化得到低碳烯烃,其两步法工业化成本较高,经济效益较低。科学家们一直致力于制备含两种组元的双功能催化剂,试图将上述两个步骤耦合在一起,合并为一步法,这样可以简化工业过程。该类双功能复合催化剂中的一种组分用于活化CO并将其转化为甲醇或类似甲醇的中间产物,而另一种组分为具有MTO性能的分子筛。由于合成气制甲醇受热力学限制,较低温度和较高压力将有利于甲醇的生成,但是,MTO反应则通常在高温进行。如果将这两个反应耦合进行合成气直接转化制低碳烯烃,鉴于两者最佳反应条件不重合,需要从催化体系的选择以及组分调配入手。由于低温下MTO反应几乎无任何活性,目前, 该类双功能复合催化剂一般采用较高的反应温度。传统的Cu-Zn-Al甲醇催化剂在高温下甲醇选择性极低,而其Zn与其他过度金属复合氧化物如ZnZr以及ZnCr可以在高温下高选择性合成甲醇,故经常被考虑作为耦合催化剂进行研究。尽管高温下甲醇合成催化剂明显受热力学限制,但如果生成的甲醇能够迅速在分子筛孔道内发生MTO反应,则可拉动合成气制甲醇反应往右进行,进而实现较高的CO转化率。
Chen等[12]将传统的CuZnAl甲醇合成催化剂与MTO催化剂SAPO-34进行物理混合作为双功能催化剂,在400 ℃、3.0×106 Pa压力下,其CO转化率约60%,虽然低碳烃类占总烃类选择性可达96.5%,但几乎都是烷烃。由于两种催化剂反应条件的差别,其双功能催化剂性能不佳,低碳烯烃选择性及CO转化率均不如MTO过程。Li等[13]以ZnCr高温甲醇催化剂为核,外层包覆SAPO-34,低碳烃类选择性可以达到66.9%,但其CO转化率较低,仅为4.2%,且生成较多烷烃。
最近,Cheng等[14]报道了一种由合成气直接制备低碳烯烃的ZnZr二元氧化物与SAPO-34分子筛物理混合的双功能催化剂,在400 ℃下,低碳烯烃选择性可以达到74%,CO转化率为11%,具体见图 2。由图 2可知,ZrO2表面的氧空位可以活化CO,在H2存在下可以通过甲酸盐形成表面甲氧基物种,但是ZrO2对H2的解离能力较弱,所以需要加入ZnO增强对H2的解离,而分子筛用来进行C-C键耦合形成C2-4的烯烃。通过调节Zn含量来改变高温甲醇催化剂的反应温度,使之与分子筛MTO反应温度相适应,然后通过两种催化剂的物理混合达到合成气直接制备低碳烯烃的目的。由图 2还可知,弱酸性位以及氧化物与分子筛之间合适的距离有利于低碳烯烃的产生。
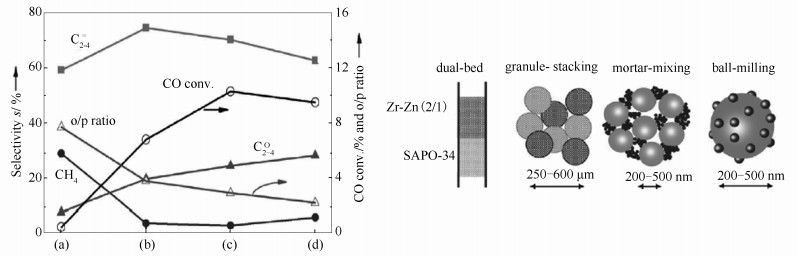 图 2
Zr-Zn氧化物与SAPO-34分子筛不同结合方式对反应性的影响[14]
Figure 2.
Effect of integration manner on the catalytic behaviors of the composite catalysts containing Zr-Zn (Zr/Zn=2:1) oxide and SAPO-34
图 2
Zr-Zn氧化物与SAPO-34分子筛不同结合方式对反应性的影响[14]
Figure 2.
Effect of integration manner on the catalytic behaviors of the composite catalysts containing Zr-Zn (Zr/Zn=2:1) oxide and SAPO-34
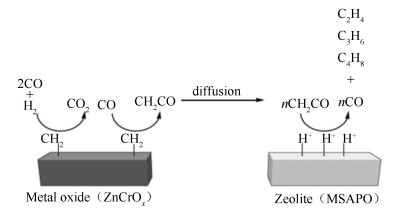
Jiao等[5]则提出了全新的OX-ZEO过程,即采用氧化物-分子筛物理混合催化剂,OX (复合氧化物) 用来活化CO分子并形成相应中间体,这些中间体可以在ZEO (分子筛) 的酸性位上形成相应的烯烃。制备的ZnCrOx/MSAPO催化剂在400 ℃、2.5×106 Pa和H2/CO (体积比)=1.5的反应条件下,CO转化率可达17%,低碳烯烃选择性则高达80%(图 3)。该双功能催化剂是由部分还原的金属氧化物(ZnCrOx) 和介孔分子筛(Meso-SAPO-34) 组成。认为,CO和H2由具有大量氧缺陷的ZnCrOx金属复合氧化物活化,形成CH2物种,随后与CO结合生产乙烯酮中间体(CH2CO)。该中间体经气相扩散至分子筛孔道中,经酸性位作用,转化为低碳烯烃(图 4)。通过详细的质谱表征,证实了ZnCrOx氧化物气相产物中确实存在着乙烯酮中间体;而且单独采用乙烯酮中间体进料,出口气体中可以检测到烃类物质,说明乙烯酮中间体可以通过分子筛催化生成低碳烃类。与传统MTO过程相比,该双功能催化剂具有较高的寿命,经过650 h反应后催化剂无明显失活。
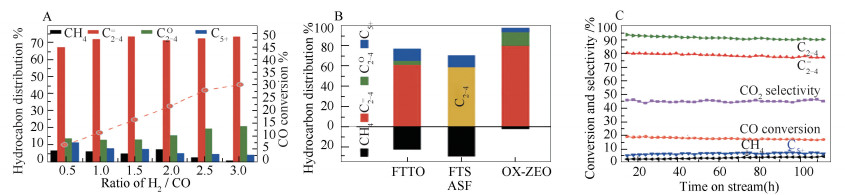 图 3
OX-ZEO双功能催化剂的催化性能[5]
Figure 3.
Performance of the bifunctional OX-ZEO catalyst in the conversion of syngas to olefins[5] (a) CO conversion and product distribution at different H2/CO volume ratios over ZnCrOx/MSAPO; (b) hydrocarbon distribution over OX-ZEO in comparison with that reported for FTTO and that in FTS predicted by the ASF model at a chain growth probability of 0.46; (c) stability test of the ZnCrOx/MSAPO catalyst[5] FTTO or FTO, Fischer-Tropsch to olefin
图 3
OX-ZEO双功能催化剂的催化性能[5]
Figure 3.
Performance of the bifunctional OX-ZEO catalyst in the conversion of syngas to olefins[5] (a) CO conversion and product distribution at different H2/CO volume ratios over ZnCrOx/MSAPO; (b) hydrocarbon distribution over OX-ZEO in comparison with that reported for FTTO and that in FTS predicted by the ASF model at a chain growth probability of 0.46; (c) stability test of the ZnCrOx/MSAPO catalyst[5] FTTO or FTO, Fischer-Tropsch to olefin
2.2 费托反应路线
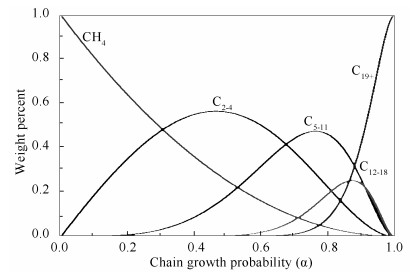
由合成气经费托(Fischer-Tropsch,FT) 反应一步法直接制备低碳烯烃过程被称作FTO (Fischer-Tropsch to Olefins) 过程。在C1化学研究中,合成气直接制备烯烃一直以来是费托合成的重要研究方向之一,其主要难点在于如何有效控制产物分布从而提高低碳烯烃选择性[2]。FT合成过程中,一般认为,先进行碳氧键断裂形成C吸附中间物种,再发生碳-碳耦合形成不同碳链长度的产物[16, 17]。针对经典FT机理,一般认为,产物的链增长服从聚合机理[18-22],产物选择性近似遵循Anderson-Schulz-Flory (ASF) 分布。ASF分布的数学表达式如下:
或者采用对数形式:
根据其对数形式的数学表达式,通过ln (Wn/n) 对n作图可以得到一条直线,这条直线的斜率即为α。式中的α为链增长因子,表示碳链增长和终止的速率之比;此值越大,表示链增长能力越大,产物中长链有机物(烃类以及含氧化合物) 含量越多,反之亦然[21]。依据式(1) 作图,以α(链增长因子) 为横坐标,以Wn(不同组分质量分数) 为纵坐标,可以得到费托合成的产物分布曲线,具体见图 5。由图 5可知,如果要在产物中得到更多的低碳烯烃,那么需要将α控制在0.45-0.55,在这个范围内CH4的选择性为25%-35%,而CH4一直是FT反应中不希望出现的副产物。一般来说,α对温度变化比较敏感,受温度影响较大;α会随着反应温度增加而减小。在FT反应体系中,可以通过升高温度使产物向低碳方向移动,产生更多的C2-4产物,但同时CH4选择性也会随之增加,而且较高温度下烯烃容易发生二次加氢反应,进一步降低了低碳烯烃选择性。优异的FTO催化剂性能首先应体现在产物选择性方面,即同时具备较高的低碳烯烃选择性及较低的甲烷选择性,而这与ASF分布相矛盾。
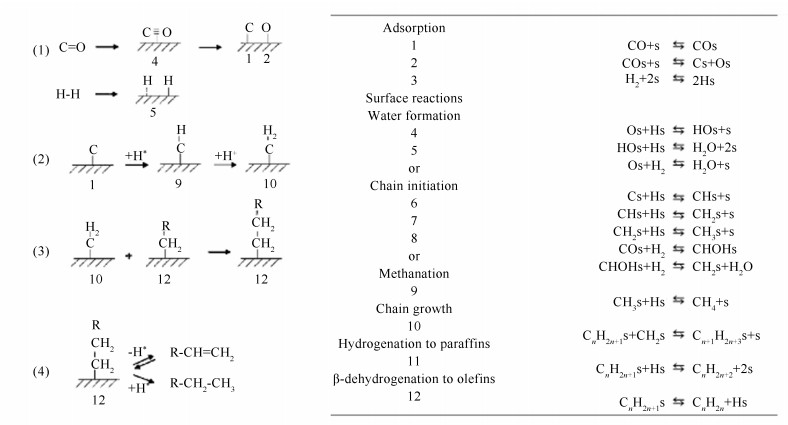
2.2.1 FTO反应机理
FTO反应仍属于FT反应范畴,其反应机理与传统FT反应机理类似。Fischer和Tropsch于1926年提出了碳化物机理[23, 24],之后几十年的时间里,研究人员对FT活性金属进行了进一步地探究,并通过动力学模型的构建、探针分子选定、同位素示踪实验等办法,采用先进的表征手段检测反应中间物种,对碳化物机理进行补充和完善,逐步发展成了一套系统的理论(图 6)。选定的FT活性金属都可以吸附CO并对C-O键进行活化进而使其断裂,这是反应的第一步。当合成气与催化剂表面接触时,CO在金属表面发生解离,C原子与表面金属结合并形成相应的金属碳化物[25-27]。金属表面活化的C原子可以逐级加氢形成次甲基(CH)、亚甲基(CH2) 以及甲基(CH3) 中间体,甲基进一步加氢可以形成甲烷[28]。同位素标记、表面反应以及有机金属的研究都证实了CO在金属表面吸附活化并形成了相应的表面碳化物[29-33]。
一般认为,CH2中间体为聚合单体,碳链增长符合亚甲基聚合机理,也就是说,在FT合成的反应条件下,游离的亚甲基采用表面插入方式逐步聚合,聚合达到一定程度,从催化剂表面脱附形成不同链长的烃类[18, 19]。由于CH2N2在FT反应条件下容易解离成为CH2中间体,所以常常被选作探针分子进行FT反应机理研究。Brady等[20, 21]采用CH2N2作为探针分子对催化剂表面聚合情况进行研究;发现当采用CH2N2作为唯一的反应物时,产物中只有CH4、C2H6、C2H4、C2H2和HCN,说明亚甲基单体在催化剂表面会发生C-C键耦合。当采用CH2N2和H2共同进料,产物与CO加氢反应的产物组成类似,可以检测到C1-18产物,这说明亚甲基发生了聚合反应。当聚合达到一定程度,碳链从催化剂表面脱离并形成相应的烷烃或者烯烃,基于不同的脱附机理,碳链终止方式也会有差别。Brady等[20, 21]认为,如果金属-烷基键采用β-消除方式断裂,那么就会生成α-烯烃;如果金属-烷基键采用加氢还原方式断裂,那么就会生成相应的烷烃。在反应体系中,CH2聚合速率与碳链终止以及烃类脱附速率为竞争反应,两者的速率决定了产物分布偏向低碳还是高碳方向;α-烯烃的脱附与二次加氢反应为一对竞争反应,这两者的反应速率决定了产物中烯烃与烷烃的比例。在FTO反应中,应该尽量采用较低的反应压力以抑制烯烃二次加氢反应,提高烯烃产量。
2.2.2 FTO催化剂研究进展
FTO反应与FT反应类似,传统FT催化剂均被用于FTO的改性研究。能够用于CO加氢反应的催化剂主要有Fe、Co、Ni、Ru元素,其中,Ni的加氢能力过强,反应中主要生成甲烷,并不适合用来做FT反应的催化剂。Ru具有较高的低温活性,其长链烃类选择性较高,并且易于在低温下还原得到金属相,是比较理想的FT合成催化剂[34-41];但是,Ru元素受全球储量以及价格限制,并不能用于大规模工业生产。从产物分布、元素含量以及经济性考虑,Fe和Co是最适合进行FT反应的两种金属,而这两类催化剂也常被选作FTO催化剂进行研究。
2.2.2.1 铁基FTO催化剂
Fe基催化剂在低温以及高温费托反应中都有较好的性能,能够适用于不同来源的合成气,是目前应用比较成熟的FT催化剂。与Co相比,Fe的链增长能力较弱,产物中烯/烷比较高,所以被广泛用于FTO反应的研究中。由于较高反应温度下可以减小链增长因子,使产物向低碳烃类移动,用于生产低碳烯烃的Fe基催化剂一般采用高温FT合成。工业应用的Fe基催化剂一般由沉淀法或者熔铁法制备,Sasol公司在流化床反应器上使用的熔铁催化剂,是将Fe的氧化物、结构助剂和化学助剂熔融制备而成;这种催化剂的低碳烯烃选择性并不高(24%),而且甲烷选择性过高[42]。之后德国鲁尔公司(Ruhrchemie) 将氧化铁和其他金属氧化物(如Ti、V、Mo、W、Mn的氧化物) 混合,可以得到较高的CO转化率(50%),低碳烯烃选择性可以达到70%,同时甲烷选择性不到10%[43, 44]。与此同时,Büssemeier研究小组报道了烧结的Fe、Ti、Zn和K的氧化物催化剂,CO转化率为87%,低碳烯烃和甲烷的选择性分别为75%和10%[45]。尽管见诸报道的催化体系可以达到较好的催化效果,但是反应温度高,催化剂的寿命只有几百个小时,而且催化剂还有积炭严重、可重复性差等缺陷;因此,需要添加适当的电子助剂以及结构助剂以优化催化剂性能。
2.2.2.2 Co基FTO催化剂
相比于Fe基费托合成催化剂,Co基催化剂具有更强的链增长能力及加氢能力,一般难以实现较高的低碳烯烃选择性。与Fe基FTO研究相比,目前报道的Co基FTO文献并不多。Chen等[99]研究Co-Mo双金属催化剂,发现Mo的添加抑制了甲烷生成,且轻质烃的生成活化能较Co基催化剂降低了10%-15%,同时烯烃含量增加。Fraenkel等[100]利用Cd气体还原法在A型分子筛笼内负载Co团簇,发现该催化剂在151 ℃下产物几乎以丙烯为主,但笼内的Co团簇很不稳定,随着反应进行,易于迁移至笼外并发生团聚长大,最终体现出传统Co基费托性能。
Mn常常作为电子助剂或者结构助剂被引进Co基催化剂中;Mn可以有效地改变Co的还原性以及表面电子结构,增加催化剂表面碱性,并促进烯烃脱附。Feyzi等[101]曾系统研究CoMn基催化剂在FTO中的应用,发现负载在TiO2上的CoMn催化剂在常压及250 ℃下表现出最好的FTO性能,低碳烯烃选择性为30%-40%。Zhou等[102]采用1,4-丁二醇为溶剂制备了Co/MnOx催化剂,低碳烯烃选择性可以达到42.2%,而相应的水溶液制备的Co/MnOx低碳烯烃选择性只有26.5%,这主要归于1,4-丁二醇对催化剂孔结构的调变作用改变了Co的还原性以及MnO载体表面电子状态。Tang等[103]以CNTs为载体负载CoMn催化剂并研究Mn对FTO催化剂性能的影响,他们指出少量Mn加入(0.3%) 可以明显抑制甲烷生成并提高低碳烯烃选择性,在Mn含量更多的情况下,甲烷选择性进一步减少,但C5+选择性显著升高。
2.2.2.1.1 电子助剂的影响
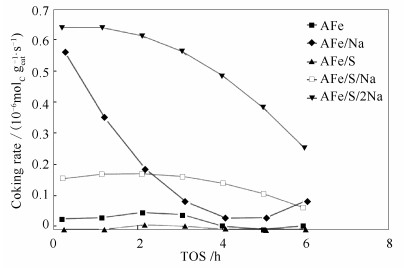
电子助剂是铁基催化剂中不可缺少的成分,可以明显地改变Fe基催化剂的反应性能。碱金属是典型的给电子助剂,可有效调节铁催化剂表面酸碱性、降低铁的电子亲和力、促进对CO的吸附和减弱对H2的吸附,从而可以提高催化剂的活性,减弱烯烃二次加氢反应、抑制亚甲基聚合,提高低碳烯烃的收率[46-53]。但过高的碱金属含量容易造成催化剂的过度碳化和积炭反应[54-58],降低催化剂的稳定性。Torres Galvis等[59]系统研究了Na含量对Fe基催化剂性能的影响;指出,在催化体系中加入少量Na可以降低甲烷选择性,提高链增长能力。但是,热重(TGA) 以及锥形元件震荡微天平(TEOM) 的测试结果表明(图 7),过量Na加入会加速炭在催化剂表面沉积,发生严重的积炭反应。
碱金属助剂的加入对催化剂活性以及产物选择性的影响高度依赖于碱金属浓度、催化剂制备方法以及反应条件。Kang等[60]研究了制备方法对Fe-Cu-Al-K催化剂FTO性能的影响,分别用溶胶-凝胶法以及共沉淀法制备了两种组成相同的非负载型催化剂,还分别用浸渍法与沉淀法制备了负载型催化剂,在300 ℃、1.0×106 Pa和H2/CO (体积比)=2条件下评价运行了70 h。结果表明,溶胶-凝胶法制备的催化剂具有最高的C2-4烯烃选择性(21%),低碳烯烃收率为11%,甲烷选择性低至7%,CO转化率为96%。还发现,随着催化剂表面酸性增加,低碳烯烃选择性随之降低。Hoffer等[61]采用Na浸渍的Fe纳米颗粒催化剂在340 ℃、2.3×106 Pa和H2/CO (体积比)=1反应条件下,低碳烯烃选择性可达44%,甲烷选择性为15%,转化率高达98%。Wang等[62]分别采用氧化还原法和共沉淀法制备了碳纳米管负载的Fe基催化剂Fe/MnK-CNTs和FeMnK/CNTs,发现采用氧化还原法制备的Fe/MnK-CNTs催化剂表现出更好的催化活性以及稳定性,并且低碳烯烃选择性高于共沉淀法制备的催化剂;认为氧化还原法制备的催化剂可以得到均一的小粒径颗粒,并且提供更多的碳纳米管表面缺陷,降低载体与活性相的相互作用。
硫作为助剂同样也可以提高低碳烯烃选择性。众所周知,硫容易导致费托催化剂中毒;但是一些研究发现,对于铁基催化剂,在特定反应条件下,少量硫的加入可以作为助剂提高低碳烯烃选择性、减少甲烷生成和增加催化剂的反应活性[63-69]。Zhou等[70]在研究中指出,S的加入还可以抑制积炭生成;制备的Fe/Al2O3-H-8S催化剂不仅表现出高活性和烯烃选择性,同时还具有良好的抑制积炭能力。Crous等[71]在一篇专利中介绍了一种铁基催化剂,采用碱金属为第一助剂,并加入少量的Be、Ge、N、P、As、Sb、S、Se和Te作为第二助剂;这种催化剂在330 ℃、2.0×106 Pa和H2/CO (体积比)=4反应条件下有着良好的性能,低碳烯烃选择性为39%,合成气转化率为41%,而且甲烷选择性很低(9%)。此外,Hadadzadeh等[72]研发了Fe-Mn负载型双金属催化剂,分别采用氧化铝、氧化钛、二氧化硅、氧化镁以及分子筛作为载体,并将催化剂暴露在H2S气体中进行毒化处理;发现经过毒化处理的催化剂表现出更高的乙烯和丙烯选择性以及很低的甲烷选择性。最近,Torres Galvis等[4]发现, 在适量Na及S促进下,负载在惰性载体(如CNF、α-Al2O3和β-SiC等) 上的Fe基催化剂低碳烯烃选择性高达60%以上。少量S添加可以抑制甲烷生成并提高低碳烯烃选择性(表 1);认为S可以选择性屏蔽催化剂加氢活性位,从而抑制烯烃二次加氢反应,减少饱和烷烃生成[59]。同时,还深入考察了FeCx粒径对催化性能的影响,发现当粒径从7 nm减低至2 nm时,改进Fe基FTO催化剂表观TOF值升高2倍,但甲烷选择性升高而低碳烯烃选择性减低。据此,提出甲烷及低碳烯烃的生成位点有所不同,认为甲烷主要生成于配位数较低的纳米颗粒的顶点及棱边处,而低碳烯烃则形成于台阶处[73]。
 表 1
S和Na对负载铁催化剂性能的影响[59]
Table 1.
Effect of S and Na promoters on the catalytic performance of supported iorn catalysts in FT synthesis[59]
表 1
S和Na对负载铁催化剂性能的影响[59]
Table 1.
Effect of S and Na promoters on the catalytic performance of supported iorn catalysts in FT synthesis[59]
Catalyst Fischer-Tropsch yield/(10-5 molCO·gFe-1·s-1) Product selectivity s/% CH4 C2-4 olefins C2-4 paraffins C5+ Fe/Al2O3 0.14 54 42 3 2 Fe/Al2O3 + 0.2% Na 0.08 50 43 5 3 Fe/Al2O3 + 0.03% S 1.70 33 58 3 5 Fe/Al2O3 + 0.2% Na + 0.03% S 0.57 15 64 2 19 Fe/Al2O3 + 0.4% Na + 0.03% S 0.16 23 51 3 22 Fe 0.02 78 13 2 7 Fe + 0.4% Na + 0.4% S 0.30 21 60 3 16 另外,一些过渡金属如Mn、Ti、V等,由于对CO的亲和力高于Fe,也可用作助剂改善产物中烯烃选择性。Mn可以同时起到电子助剂和结构助剂的作用[46, 47, 52, 54, 62, 72-77],Mn助剂一方面通过与Fe强相互作用提高铁物种分散度; 另一方面, 有一定的给电子能力,促进CO离解、提高对烯烃产物的选择性。Yang等[78]制备了不同K、Mn含量的碳纳米管负载Fe催化剂,发现Mn可以使FeCxN1-x在反应条件下稳定存在,并促进CO表面吸附;Mn含量为1%的催化剂表现出很好的低碳烯烃选择性,但是催化剂活性较低。Liu等[79]制备了MnOx修饰的Fe3O4微球催化剂,将MnOx纳米颗粒镶在Fe3O4微球表面(图 8);Mn助剂的加入可以有效地调节表面碳化铁的性质,抑制烯烃二次加氢反应,提高低碳烯烃选择性(60.1%)。他们通过XAFS表征发现,Mn可以促进球状θ-Fe3C颗粒生成,而θ-Fe3C可能有利于提高产物烯/烷比,促进低碳烯烃生成。DFT计算表明,在Fe3C表面的Fe-C活性位上,H2可以十分容易的解离成吸附态原子,进而形成亚甲基(CH2) 物种,同时,Fe3C较弱的加氢能力可以提高产物烯/烷比[80]。
 图 8
(a) Mn/Fe3O4结构模型;(b) Fe3O4微球的扫描电镜照片;(c) 还原后Mn/Fe3O4催化剂的TEM照片;(d) Mn/Fe3O4催化剂的STEM照片;(e) 相应的STEM-EDX元素分析[79]
Figure 8.
(a) Structural model for the Mn/Fe3O4 catalyst; (b) SEM images of the Fe3O4 microspheres; (c) TEM images of theMn/Fe3O4 catalyst after reduction; (d) original STEM image of Mn/Fe3O4 catalyst as prepared; (e) corresponding STEM-EDX elemental mapping of Fe, O and Mn on the catalyst[79]
图 8
(a) Mn/Fe3O4结构模型;(b) Fe3O4微球的扫描电镜照片;(c) 还原后Mn/Fe3O4催化剂的TEM照片;(d) Mn/Fe3O4催化剂的STEM照片;(e) 相应的STEM-EDX元素分析[79]
Figure 8.
(a) Structural model for the Mn/Fe3O4 catalyst; (b) SEM images of the Fe3O4 microspheres; (c) TEM images of theMn/Fe3O4 catalyst after reduction; (d) original STEM image of Mn/Fe3O4 catalyst as prepared; (e) corresponding STEM-EDX elemental mapping of Fe, O and Mn on the catalyst[79]
2.2.2.1.2 结构助剂的影响
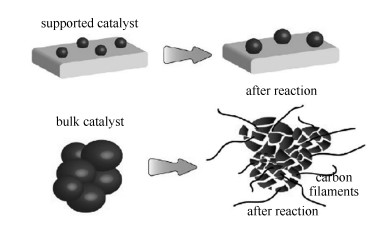
在Fe基FTO催化剂中,结构助剂主要作为活性组分载体,起着有效分散活性组分的作用。载体材料一般需要具备较大的比表面积,传统载体包括γ-氧化铝和二氧化硅均满足这一条件。采用浸渍法将无机铁盐负载在高比表面积的载体上,很容易获得高分散度的铁纳米颗粒,这些铁纳米颗粒具有相对较窄的颗粒分布,均匀的空间分布,从而尽可能降低颗粒团聚(图 9)。然而,铁与大多数氧化物载体之间有着强烈的相互作用,容易在接触处形成难还原的新物种(如铝酸铁和硅酸铁等)[69, 81-86],进而抑制了具有催化活性的碳化铁的生成。因此,相对惰性载体,以γ-氧化铝或二氧化硅为载体所得的催化剂活性有所下降[4]。与之相反,活性组分与载体之间的弱相互作用有利于激活活性位,但这种较弱的相互作用无法忍受FTO反应所需的条件,以至于在反应一段时间后活性组分发生聚集结焦,进而导致催化剂失活。因此,需要合理调整活性组分与载体之间的相互作用。
Bruce等[87]分别以硝酸盐和羰基金属化合物为前驱体,采用浸渍法制备了氧化硅负载Fe、Fe-Mn、Fe-K和Fe-Mn-K催化剂,在300 ℃、2×105-5×105 Pa和H2/CO (体积比)=1.5条件下进行合成反应,以羰基金属复合物为前驱体的催化剂低碳烯烃选择性为64%,甲烷选择性为25%,但是转化率低于5%。Van Dillen等[88]认为以羰基金属复合物为前体的催化剂抑制了二次加氢反应,有机金属复合物可能会促进金属快速结晶,增加铁的分散度,从而提高了低碳烯烃选择性。Smith等[89]也做了类似研究;采用羰基金属化合物为前驱体,所得的Fe/SiO2低碳烯烃选择性可达69%,但CO转化率低于5%。Stoop等[90]报道了氧化硅负载Ru/Fe (3:1) 双金属催化剂,在277 ℃、1×105 Pa和H2/CO (体积比)=2反应条件下,CO转化率小于3%,甲烷选择性低于10%,但具有较高的烯烷比(乙烯/乙烷=3;丙烯/丙烷=6)。Ru-Fe合金结合了Fe的高选择性与Ru的高活性,但这种双金属催化剂的炭沉积速率高于Fe/SiO2,当反应温度高于402 ℃时,催化剂失活显著。
此外,很多研究人员对氧化铝载体也进行了系统研究。Baker团队[91, 92]制备了一种铁基催化剂,将前躯体负载在经稀土元素氧化物修饰且热处理后的γ-氧化铝上;此催化剂上低碳烯烃选择性为63%,甲烷选择性为7%(280 ℃、8×105 Pa、H2/CO (体积比)=0.5)。不过这种结构的催化剂容易积炭结焦,使用寿命较短。Zhou等[70]制备了一种分层的α-Al2O3负载Fe基催化剂;与传统商品α-Al2O3相比,这种材料可以使Fe纳米颗粒更好地固定在载体表面。
碳纳米材料如活性炭[46, 48, 93-95]、碳纳米管[62, 78, 96]、碳纳米纤维[4, 59]以及石墨烯[97]等多孔材料,由于具有很大的比表面积、可调变的孔径与孔结构,而且通过表面修饰改性可以调节金属前躯体与载体的相互作用强度,常常被用作载体进行FTO反应研究。Venter等[46]采用高比表面积(1 400 m2/g) 的无定形炭黑作为载体,选择含K的Fe、Mn羰基化物为浸渍前躯体制备了一种负载Fe催化剂K[MnFe (CO)9]/C;在采用275-290 ℃、常压、H2/CO (体积比)=3反应条件下,低碳烯烃选择性可以高达76%。后续的催化剂稳定性测试中发现,反应100 h之后,催化剂活性降低了55%。指出,失活主要是由于严重的积炭所造成的[48]。围绕作为载体的碳纳米材料,研究人员常掺杂N、O等元素对其进行改性,而掺杂的元素起到了明显的助剂作用。Lu等[96]采用N掺杂的碳纳米管作为载体负载Fe基催化剂,N掺杂可以增强碳纳米管表面的锚定效应,Fe纳米粒子可以很容易地固定在载体表面。这种催化剂的低碳烯烃选择性可以达到46.7%,高于相应的非掺杂碳纳米管负载Fe催化剂,而且表现出更好的催化活性以及稳定性。此外,N掺杂碳纳米管可以提高催化剂表面的固有碱性,促进CO吸附解离以及烯烃脱附,进而提高烯烃选择性;同时N掺杂的助剂效应有助于Fe的还原以及活性相χ-Fe5C2生成,使催化剂的活性增加。由图 10还可知,锚定效应抑制了Fe纳米颗粒团聚烧结,从而提高了催化剂的稳定性。
Chen等[97]以Li3N和CCl4为前躯体,采用溶剂热法制备了一种N掺杂的石墨烯材料,通过加入三聚氯氰调控N掺杂量,并采用超声辅助浸渍法将Fe负载在N掺杂石墨烯上。这种催化剂的低碳烯烃选择性为50%,优于传统的炭黑负载Fe催化剂(30%)。结合XAS与XRD表征结果,指出N掺杂的助剂效应可以使Fe物种更容易被还原。Schulte等[98]对碳纳米管进行改性制备了N-功能化及O-功能化碳纳米管,并以柠檬酸铁氨为前躯体将Fe负载在改性的纳米管上进行高温FT反应。与传统块状Fe催化剂相比,制备的催化剂表现出良好的稳定性(>80 h) 以及反应活性(81.9%),并且产物中低碳烯烃含量较高。认为,N或O-功能化碳纳米管可以提供锚定位点,使Fe纳米颗粒固定在载体表面,在还原及反应过程中可以抑制活性相Fe2C5纳米颗粒长大。
3 结论与展望
合成气转化制备低碳烯烃,无论采取间接合成路线还是直接合成路线,与传统石油裂解路线相比,可以在一定程度上缓解目前石油供不应求的现状,而且产物中几乎不含硫氧化物和氮氧化物,从而减少了对环境的危害以及后续废弃处理费用。由于具有流程更短、能耗更低的优势,直接合成路线越来越受到研究人员的关注。针对双功能催化路线(如OX-ZEO体系),为了保证甲醇或类似甲醇的中间产物在分子筛孔道内发生类似MTO反应以生成低碳烯烃,反应温度一般都需要在400 ℃以上。另一功能组分(即用于活化CO的氧化物组分) 也处在同样的高温反应条件下,这要求该组分具备较好的高温稳定性。同时,由于分子筛的稳定性有限,易发生积炭失活,如何通过分子筛孔道结构的设计抑制积炭发生,是该合成路线的一大挑战。
合成气转化经费托反应路线直接制备低碳烯烃已有多年的研究历史,但尚存在众多瓶颈问题以待进一步攻克。综合分析FTO研究的历史及现状,可认为其研究主要是基于Fe基费托或Co基费托的改进。为了尽可能提高低碳烯烃的选择性,主要采用引入助剂及优化反应条件的策略。合适的助剂加入可一定程度减低加氢能力并控制碳链增长能力。此外,为实现较高的低碳烯烃选择性,一般采用较高的反应温度;之所以采用高温,其主要原因在于高温利于降低碳链增长能力,使产物往低碳数移动,促进低碳烯烃选择性的提高。同时,为了降低加氢能力,则采用较低的压力。此外,原料气的H2/CO (体积比) 对产物分布也有一定影响,一般来说,采用较低的H2/CO (体积比),产物的烯烷比较高,烯烃的选择性较高。通过分析产物分布,可认为绝大部分报道所涉及的产物分布皆服从ASF分布,与传统FT相比,尽管C2-4选择性有所提高,但甲烷选择性亦明显升高,即整体而言只是链增长因子从高值(0.8-0.9) 移向较低值(0.5左右)。因此,可认为目前FTO的研究尚未摆脱FT的范畴,ASF分布还起着重要作用,其原因在于其催化活性位结构与常规费托合成的无异;即,Fe基FTO的活性位与Fe基费托一致,皆为FeCx,而Co基FTO活性位则与Co基费托一致,皆为金属态Co。由于活性位主要决定催化性能,助剂的影响或反应条件的优化只是一定程度改变催化性能,因此,目前的FTO研究从某种程度上可视为链增长因子偏低的FT反应。
这种链增长因子偏低的FT反应显然难以满足FTO的工业应用,其原因有以下两点:第一点为产物选择性尚不够理想,如果认为低碳烯烃选择性尚可接受(50%左右),其接近20%的甲烷选择性则属过高;第二点为稳定性难以满足要求。由于多采用高温,而高温下催化剂颗粒更易发生团聚长大,同时Boudouard反应加剧,所产生的积炭将覆盖活性位点,这两者皆导致催化剂活性不断降低且产物选择性不断恶化。为了实现很好的FTO催化性能,应设法摆脱ASF分布的限制。要实现这点,则应从活性位结构出发,即采用全新的活性位结构,而非传统的费托反应活性位,开发全新的催化活性位结构。此外,为了得到优异的FTO催化性能,还应从催化反应工程的角度考虑FTO催化剂的设计。与大部分多相催化反应一致,FTO反应也包括以下五个步骤:(1) 反应物分子往催化剂孔内扩散;(2) 反应物分子在催化剂表面吸附;(3) 吸附在催化剂表面的分子发生活化及反应;(4) 产物从催化剂表面发生脱附;(5) 产物分子向催化剂周围扩散。设计FTO催化剂时应全面考虑上述五个步骤,避免发生短板效应。如果活性位结构决定步骤(2)-步骤(4),那么,活性位结构所处的介观环境则决定步骤(1) 及步骤(5)。传质对FTO最终催化性能起着关键作用,如果整个反应受扩散限制,除反应活性受到抑制外,由于H2分子扩散速率明显大于CO,反应活性位的局部环境处H2/CO体积比将明显大于催化剂颗粒外部环境,而过高的H2浓度将促进CH4及其他饱和烷烃的生成,降低目标产物低碳烯烃的选择性。
此外,与饱和烷烃相比,低碳烯烃热力学方面并不稳定,生成并扩散至气相中后还有可能发生再次吸附,进而发生二次加氢反应生成饱和烷烃,或参与碳链增长生成更高碳数的产物,这也将降低低碳烯烃的选择性。为避免烯烃二次加氢,需要保证低碳烯烃一旦生成便可尽快扩散至催化剂外部。因此,需要构筑强化传质、传热介观结构,最大程度优化活性位所处的微区环境,实现高活性、高选择性及高稳定性。
总之,一种好的FTO催化剂要求同时具备合适的活性位结构及利于强化传质的介观结构环境。同时,为深化对FTO反应网络及催化机理的深入,有必要开展更深入的构效关系研究,尤其是原位条件下构效演变规律研究,从而澄清催化剂表面C-O键活化及断裂、碳链增长及终止机理,揭示其与传统费托活性组分催化性能区别的本质原因,为新型FTO催化剂的设计提供理论依据。
-
-
[1]
CORMA A, MELO F V, SAUVANAUD L, ORTEGA F. Light cracked naphtha processing: Controlling chemistry for maximum propylene production[J]. Catal Today, 2005, 107-108: 699-706. doi: 10.1016/j.cattod.2005.07.109
-
[2]
TORRES GALÜIS H M, DE JONG K P. Catalysts for production of lower olefins from synthesis gas: A review[J]. ACS Catal, 2013, 3(9): 2130-2149. doi: 10.1021/cs4003436
-
[3]
TIAN P, WEI Y X, YE M, LIU Z M. Methanol to olefins (MTO): From fundamentals to commercialization[J]. ACS Catal, 2015, 5(3): 1922-1938. doi: 10.1021/acscatal.5b00007
-
[4]
TORRES GALÜIS H M, BITTER J H, KHARE C B, RUITENBEEK M, DUGULAN A I, DE JONG K P. Supported iron nanoparticles as catalysts for sustainable production of lower olefins[J]. Science, 2012, 335(6070): 835-838. doi: 10.1126/science.1215614
-
[5]
JIAO F, LI J J, PAN X L, XIAO J P, LI H B, MA H, WEI M M, PAN Y, ZHOU Z Y, LI M R, MIAO S, LI J, ZHU Y F, XIAO D, HE T, YANG J H, QI F, FU Q, BAO X H. Selective conversion of syngas to light olefins[J]. Science, 2016, 351(6277): 1065-1068. doi: 10.1126/science.aaf1835
-
[6]
陈腊山. MTO/MTP技术的研发现状及应用前景[J]. 化肥设计, 2008,46,(1): 3-6. CHEN La-shan. Present situation of MTO/MTP technology development and its application perspective[J]. Chem Fert Des, 2008, 46(1): 3-6.
-
[7]
何长青, 刘中民, 蔡光宇, 杨立新, 常颜君, 王作周, 姜增全, 石仁敏, 易林林, 孙承林.以双模板剂合成磷酸硅铝分子筛的方法:CN, 1106715[P].1995-08-16.HE Chang-qing, LIU Zhong-min, CAI Guang-yu, YANG Li-xin, CHANG Yan-jun, WANG Zuo-zhou, JIANG Zeng-quan, SHI Ren-min, YI Lin-lin, SUN Cheng-lin.A method to synthesize silicoaluminophosphatezeolite via dual-template: CN, 1106715[P]. 1995-08-16.
-
[8]
刘中民, 蔡光宇, 何长青, 杨立新, 王作周, 罗静慎, 常彦君, 石仁敏, 姜增全, 孙承林.一种以三乙胺为模板剂的合成硅磷铝分子筛及其制备:CN, 1088483[P].1994-06-29.LIU Zhong-min, CAI Guang-yu, HE Chang-qing, YANG Li-xin, WANG Zuo-zhou, LUO Jing-shen, CHANG Yan-jun, SHI Ren-min, JIANG Zeng-quan, SUN Cheng-lin. A method to synthesize silicoaluminophosphate zeolite with triethylaminetemplate: CN, 1088483[P]. 1994-06-29.
-
[9]
蔡光宇, 刘中民, 何长青, 孙承林, 扬立新, 常彦君, 石仁敏, 姜增全, 易林林, 王作周.金属改性小孔磷硅铝型分子筛催化剂及其制备方法和应用:CN, 1167654[P].1997-12-17.CAI Guang-yu, LIU Zhong-min, HE Chang-qing, SUN Cheng-lin, YANG Li-xin, CHANG Yan-jun, SHI Ren-min, JIANG Zeng-quan, YI Lin-lin, WANG Zuo-zhou. Preparationand application of metal-modified silicoaluminophosphate zeolite catalyst: CN, 1167654[P]. 1997-12-17.
-
[10]
李宏愿, 许磊, 刘中民, 孙承林, 杨立新.一种制备SAPO-17和SAPO-44分子筛的方法:CN, 1299775[P].2001-06-20.LI Hong-yuan, XU Lei, LIU Zhong-min, SUN Cheng-lin, YANG Li-xin. A method to synthesize SAPO-17 and SAPO-44zeolite: CN, 1299775[P]. 2001-06-20.
-
[11]
ČEJKA J, CORMA A, ZONES S. Zeolites and Catalysis: Synthesis, Reactions and Applications[M]. Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA, 2010: 1056.
-
[12]
CHEN Y P, XU Y M, CHENG D G, CHEN Y C, CHEN F Q, LU X Y, HUANG Y P, NI S B. C2-C4 hydrocarbons synthesis from syngas over CuO-ZnO-Al2O3/SAPO-34 bifunctional catalyst[J]. J Chem Technol Biotechnol, 2015, 90(3): 415-422. doi: 10.1002/jctb.2015.90.issue-3
-
[13]
李津京, 潘秀莲, 包信和. 核壳结构催化剂Cr-Zn@SiO2@SAPO-34催化合成气直接转化制低碳烃的性能[J]. 催化学报, 2015,36,(7): 1131-1135. doi: 10.1016/S1872-2067(14)60297-7LI Jin-jing, PAN Xiu-lian, BAO Xin-he. Direct conversion of syngas into hydrocarbons over a core-shell Cr-Zn@SiO2@SAPO-34 catalyst[J]. Chin J Catal, 2015, 36(7): 1131-1135. doi: 10.1016/S1872-2067(14)60297-7
-
[14]
CHENG K, GU B, LIU X L, KANG J C, ZHANG Q H, WANG Y. Direct and highly selective conversion of synthesis gas to lower olefins: Design of a bifunctional catalyst combining methanol synthesis and carbon-carbon coupling[J]. Angew Chem Int Ed, 2016, 55(15): 4725-4728. doi: 10.1002/anie.201601208
-
[15]
DE JONG K P. Surprised by selectivity[J]. Science, 2016, 351(6227): 1030-1031.
-
[16]
SCHULZ H. Short history and present trends of Fischer-Tropsch synthesis[J]. Appl Catal A:Gen, 1999, 186(1/2): 3-12.
-
[17]
ZHANG Q H, KANG J C, WANG Y. Development of novel catalysts for Fischer-Tropsch synthesis: Tuning the product selectivity[J]. ChemCatChem, 2010, 2(9): 1030-1058. doi: 10.1002/cctc.201000071
-
[18]
BILOEN P. On the mechanism of the Fischer-Tropsch synthesis[J]. J Roy Neth Chem Soc, 1980, 99(2): 33-38.
-
[19]
BILOEN P, SACHTLER W M H. Mechanism of hydrocarbon synthesis over Fischer-Tropsch catalysts[J]. Adv Catal, 1981, 30: 165-216.
-
[20]
BRADY Ⅲ R C, PETTIT R. Reactions of diazomethane on transition-metal surfaces and their relationship to the mechanism of the Fischer-Tropsch reaction[J]. J Am Chem Soc, 1980, 102(19): 6181-6182. doi: 10.1021/ja00539a053
-
[21]
BRADY Ⅲ R C, PETTIT R. Mechanism of the Fischer-Tropsch reaction. The chain propagation step[J]. J Am Chem Soc, 1981, 103(5): 1287-1289. doi: 10.1021/ja00395a081
-
[22]
VAN DER LAAN G P, BEENACKERS A A C M. Kinetics and selectivity of the Fischer-Tropsch synthesis: A literature review[J]. Catal Rev, 1999, 41(3/4): 255-318.
-
[23]
FISCHER F, TROPSCH H. Synthesis of petroleum at atmospheric pressure from gasification products of coal[J]. Brennstoff-Chem, 1926, 7: 97-104.
-
[24]
FISCHER F, TROPSCH H. Direct synthesis of petroleum hydrocarbons at ordinary pressure. Ⅰ. Ⅱ.[J]. Ber Dtsch Chem Ges, 1926, 59B: 830-831.
-
[25]
WENTRCEK R, WOOD B J, WISE H. The role of surface carbon in catalytic methanation[J]. J Catal, 1976, 43(1/3): 363-366.
-
[26]
BILOEN P, HELLE J N, SACHTLER W M H. Incorporation of surface carbon into hydrocarbons during Fischer-Tropsch synthesis: Mechanistic implications[J]. J Catal, 1979, 58(1): 95-107. doi: 10.1016/0021-9517(79)90248-3
-
[27]
RABO J A, RISCH A P, POUTSMA M L. Reactions of carbon monoxide and hydrogen on Co, Ni, Ru, and Pd metals[J]. J Catal, 1978, 53(3): 295-311. doi: 10.1016/0021-9517(78)90102-1
-
[28]
KAMINSKY M C, WINOGRAD N, GEOFFROY G L, VANNICE M A. Direct SIMS observation of methylidyne, methylene, and methyl intermediates on a nickel (Ⅲ) methanation catalyst[J]. J Am Chem Soc, 1986, 108(6): 1315-1316. doi: 10.1021/ja00266a042
-
[29]
ARAKI M, PONEC V. Methanation of carbon monoxide on nickel and nickel-copper alloys[J]. J Catal, 1976, 44(3): 439-448. doi: 10.1016/0021-9517(76)90421-8
-
[30]
SHRIVER D F, SAILOR M J. Transformations of carbon monoxide and related ligands on metal ensembles[J]. Acc Chem Res, 1988, 21(10): 374-379. doi: 10.1021/ar00154a004
-
[31]
BRADLEY J S. The chemistry of carbidocarbonyl clusters[J]. Adv Organomet Chem, 1983, 22: 1-58.
-
[32]
CHISHOLM M H, HAMMOND C E, JOHNSON V J, STREIB W E, HUFFMAN J C. Metal alkoxides: Models for metal oxides. 17. Reductive cleavage of carbon monoxide to carbide and oxide by ditungsten and tetratungsten alkoxides. Crystal and molecular structures of W4(μ4-C)(OCH2-c-Pen)14, W4(μ4-C)(O)(OCH2-t-Bu)12 and W4(μ4-C)(O)(O-i-Pr)12[J]. J Am Chem Soc, 1992, 114(18): 7056-7065.
-
[33]
VANNICE M A. The catalytic synthesis of hydrocarbons from H2/CO mixtures over the group Ⅷ metals: Ⅰ. The specific activities and product distributions of supported metals[J]. J Catal, 1975, 37(3): 449-461. doi: 10.1016/0021-9517(75)90181-5
-
[34]
BHASIN M M, BARTLEY W J, ELLGEN P C, WILSON T P. Synthesis gas conversion over supported rhodium and rhodium-iron catalysts[J]. J Catal, 1978, 54(2): 120-128. doi: 10.1016/0021-9517(78)90035-0
-
[35]
ICHIKAWA M. Catalysis by supported metal crystallites from carbonyl clusters. II. Catalytic ethanol synthesis from CO and H2 under atmospheric pressure over supported rhodium crystallites prepared from Rh carbonyl clusters deposited on TiO2, ZrO2, and La2O3[J]. Bull Chem Soc Jpn, 1978, 51(8): 2273-2277. doi: 10.1246/bcsj.51.2273
-
[36]
ICHIKAWA M. Catalysis by supported metal crystallites prepared from metal carbonyl clusters: III. Catalytic vapor-phase hydroformylation of olefins over Rh, bimetallic Rh-Co, and Co crystallites prepared from the carbonyl cluster compounds dispersed on zinc oxide[J]. J Catal, 1979, 56(1): 127-129. doi: 10.1016/0021-9517(79)90096-4
-
[37]
ICHIKAWA M. Catalytic hydroformylation of olefins over the rhodium, bimetallic Rh-Co, and cobalt carbonyl clusters supported with some metal oxides[J]. J Catal, 1979, 59(1): 67-78. doi: 10.1016/S0021-9517(79)80046-9
-
[38]
WATSON P R, SOMORJAI G A. The hydrogenation of carbon monoxide over rhodium oxide surfaces[J]. J Catal, 1981, 72(2): 347-363. doi: 10.1016/0021-9517(81)90018-X
-
[39]
WATSON P R, SOMORJAI G A. The formation of oxygen-containing organic molecules by the hydrogenation of carbon monoxide using a lanthanum rhodate catalyst[J]. J Catal, 1982, 74(2): 282-295. doi: 10.1016/0021-9517(82)90034-3
-
[40]
KIP B J, HERMANS E G F, VAN WOLPUT J H M C, HERMANS N M A, VAN GRONDELLE J, PRINS R. Hydrogenation of carbon monoxide over rhodium/silica catalysts promoted with molybdenum oxide and thorium oxide[J]. Appl Catal, 1987, 35(1): 109-139. doi: 10.1016/S0166-9834(00)82426-4
-
[41]
LAVALLEY J C, SAUSSEY J, LAMOTTE J, BREAULT R, HINDERMANN J P, KIENNEMANN A. Infrared study of carbon monoxide hydrogenation over rhodium/ceria and rhodium/silica catalysts[J]. J Phys Chem, 1990, 94(15): 5941-5947. doi: 10.1021/j100378a061
-
[42]
DRY M E, DE W, ERASMUS H B. Update of the sasol synfuels process[J]. Ann Rev Energy, 1987, 12: 1-46. doi: 10.1146/annurev.eg.12.110187.000245
-
[43]
BUSSEMEIER B, FROHNING C D, CORNILS B. Lower olefins via Fischer-Tropsch[J]. Hgdrocarbon Process, 1975, 55(11): 105-112.
-
[44]
BUESSEMEIER B, FROHNING C D, HORN G, KLUY W. Process for the production of unsaturated hydro-carbons: US, 4455395[P]. 1984-6-19.
-
[45]
BUESSEMEIER B, FROHNING C D, HORN G, KLUY W. Process for the manufacture of unsaturated hydrocarbons: US, 4564642[P]. 1986-01-14.
-
[46]
VENTER J, KAMINSKY M, GEOFFROY G L, VANNICE M A. Carbon-supported Fe-Mn and K-Fe-Mn clusters for the synthesis of C2-C4 olefins from CO and H2: Ⅰ. Chemisorption and catalytic behavior[J]. J Catal, 1987, 103(2): 450-465. doi: 10.1016/0021-9517(87)90136-9
-
[47]
沈兴, 王蕾, 张永锋, 李增喜, 张香平, 张锁江. 合成气直接制取低碳烯烃的铁基负载型催化剂的制备与性能[J]. 过程工程学报, 2009,9,(6): 1178-1185. SHEN Xing, WANG Lei, ZHANG Yong-feng, LI Zeng-xi, ZHANG Xiang-ping, ZHANG Suo-jiang. Preparation and performance of supported iron-based catalysts for conversion of synthesis gas to light olefins[J]. Chin J Process Eng, 2009, 9(6): 1178-1185.
-
[48]
VENTER J, KAMINSKY M, GEOFFROY G L, VANNICE M A. Carbon-supported Fe-Mn and K-Fe-Mn clusters for the synthesis of C2-C4 olefins from CO and H2: Ⅱ. Activity and selectivity maintenance and regenerability[J]. J Catal, 1987, 105(1): 155-162. doi: 10.1016/0021-9517(87)90015-7
-
[49]
DRY M E, OOSTHUIZEN G J. The correlation between catalyst surface basicity and hydrocarbon selectivity in the Fischer-Tropsch synthesis[J]. J Catal, 1968, 11(1): 18-24. doi: 10.1016/0021-9517(68)90004-3
-
[50]
YANG Y, XIANG H W, XU Y Y, BAI L, LI Y W. Effect of potassium promoter on precipitated iron-manganese catalyst for Fischer-Tropsch synthesis[J]. Appl Catal A: Gen, 2004, 266(2): 181-194. doi: 10.1016/j.apcata.2004.02.018
-
[51]
LI J B, MA H F, ZHANG H T, SUN Q W, YING W Y, FANG D Y. Sodium promoter on iron-based catalyst for direct catalytic synthesis of light alkenes from syngas[J]. Fuel Process Technol, 2014, 125: 119-124. doi: 10.1016/j.fuproc.2014.03.017
-
[52]
LI J B, MA H F, ZHANG H T, SUN Q W, YING W Y, FANG D Y. Direct production of light olefins from syngas over potassium modified Fe-Mn catalyst[J]. React Kinet Mech Cat, 2014, 112(2): 409-423. doi: 10.1007/s11144-014-0716-0
-
[53]
陈嘉宁, 刘永梅. K、Mn助剂协同效应对Fe基催化剂上CO加氢制低碳烯烃反应性能的影响[J]. 燃料化学学报, 2013,41,(12): 1488-1494. CHEN Jia-ning, LIU Yong-mei. Effects of Mn-K synergistic action on iron-based catalyst for CO hydrogenation to light olefins[J]. J Fuel Chem Technol, 2013, 41(12): 1488-1494.
-
[54]
LOHITHARN N, GOODWIN JR J G. Effect of K promotion of Fe and FeMn Fischer-Tropsch synthesis catalysts: Analysis at the site level using SSITKA[J]. J Catal, 2008, 260(1): 7-16. doi: 10.1016/j.jcat.2008.08.011
-
[55]
RANKIN J L, BARTHOLOMEW C H. Effects of potassium and calcination pretreatment on the adsorption and chemical/physical properties of Fe/SiO2[J]. J Catal, 1986, 100(2): 533-540. doi: 10.1016/0021-9517(86)90126-0
-
[56]
TIHAY F, ROGER A C, KIENNEMANN A, POURROY G. Fe-Co based metal/spinel to produce light olefins from syngas[J]. Catal Today, 2000, 58(4): 263-269. doi: 10.1016/S0920-5861(00)00260-1
-
[57]
TIHAY F, POURROY G, RICHARD-PLOUET M, ROGER A C, KIENNEMANN A. Effect of Fischer-Tropsch synthesis on the microstructure of Fe-Co-based metal/spinel composite materials[J]. Appl Catal A: Gen, 2001, 206(1): 29-42. doi: 10.1016/S0926-860X(00)00595-0
-
[58]
KALAKKAD D S, SHROFF M D, KÖHLER S, JACKSON N, DATYE A K. Attrition of precipitated iron Fischer-Tropsch catalysts[J]. Appl Catal A: Gen, 1995, 133(2): 335-350. doi: 10.1016/0926-860X(95)00200-6
-
[59]
TORRES GALÜIS H M, KOEKEN A C J, BITTER J H, DAVIDIAN T, RUITENBEEK M, DUGULAN A I, DE JONG K P. Effects of sodium and sulfur on catalytic performance of supported iron catalysts for the Fischer-Tropsch synthesis of lower olefins[J]. J Catal, 2013, 303: 22-30. doi: 10.1016/j.jcat.2013.03.010
-
[60]
KANG S H, BAE J W, SAI PRASAD P S, PARK S J, WOO K J, JUN K W. Effect of preparation method of Fe-based Fischer-Tropsch catalyst on their light olefin production[J]. Catal Lett, 2009, 130(3): 630-636.
-
[61]
HOFFER B W, BUNZEL S, NEUMANN D, BAY K, SCHWAB E, GRAESSLE U, STEINER J. Method for producing olefins through reaction of carbon monoxide with hydrogen: WO 2009013174[P]. 2009-01-29.
-
[62]
WANG D, ZHOU X P, JI J, DUAN X Z, QIAN G, ZHOU X G, CHEN D, YUAN W K. Modified carbon nanotubes by KMnO4 supported iron Fischer-Tropsch catalyst for the direct conversion of syngas to lower olefins[J]. J Mater Chem A, 2015, 3(8): 4560-4567. doi: 10.1039/C4TA05202A
-
[63]
VAN DIJK W L, NIEMANTSVERDRIET J W, VAN DAR KRAAN A M, VAN DER BAAN H S. Effects of manganese oxide and sulphate on the olefin selectivity of iron catalysts in the Fischer-Tropsch reaction[J]. Appl Catal, 1982, 2(4/5): 273-288.
-
[64]
BROMFIELD T C, COVILLE N J. The effect of sulfide ions on a precipitated iron Fischer-Tropsch catalyst[J]. Appl Catal A: Gen, 1999, 186(1/2): 297-307.
-
[65]
BROMFIELD T C, COVILLE N J. Surface characterization of sulfided precipitated-iron Fischer-Tropsch catalysts by X-ray photoelectron spectroscopy[J]. Appl Surf Sci, 1997, 119(1/2): 19-24.
-
[66]
WU B S, BAI L, XIANG H W, LI Y W, ZHANG Z X, ZHONG B. An active iron catalyst containing sulfur for Fischer-Tropsch synthesis[J]. Fuel, 2004, 83(2): 205-212. doi: 10.1016/S0016-2361(03)00253-9
-
[67]
MCCUE A J, ANDERSON J A. Sulfur as a catalyst promoter or selectivity modifier in heterogeneous catalysis[J]. Catal Sci Technol, 2014, 4(2): 272-294. doi: 10.1039/C3CY00754E
-
[68]
KRITZINGER J A. The role of sulfur in commercial iron-based Fischer-Tropsch catalysis with focus on C2-product selectivity and yield[J]. Catal Today, 2002, 71(3/4): 307-318.
-
[69]
PARK J Y, LEE Y J, KHANNA P K, JUN K W, BAE J W, KIM Y H. Alumina-supported iron oxide nanoparticles as Fischer-Tropsch catalysts: Effect of particle size of iron oxide[J]. J Mol Catal A, 2010, 323(1/2): 84-90.
-
[70]
ZHOU X P, JI J, WANG D, DUAN X Z, QIAN G, CHEN D, ZHOU X G. Hierarchical structured α-Al2O3 supported S-promoted Fe catalysts for direct conversion of syngas to lower olefins[J]. Chem Commun, 2015, 51(42): 8853-8856. doi: 10.1039/C5CC00786K
-
[71]
CROUS R, BROMFIELD T C, BOOYENS S. Olefin selective FT catalyst composition and preparation thereof: US, 2012029096[P]. 2012-02-02.
-
[72]
HADADZADEH H, MIRZAEI A A, MORSHEDI M, RAEISI A, FEYZI M, ROSTAMIZADEH N. The effect of H2S on the selectivity of light alkenes in the Fe-Mn-catalyzed Fischer-Tropsch synthesis[J]. Petrol Chem, 2010, 50(1): 78-86. doi: 10.1134/S0965544110010123
-
[73]
TORRES GALÜIS H M, BITTER J H, DAVIDIAN T, RUITENBEEK M, DUGULAN A I, DE JONG K P. Iron particle size effects for direct production of lower olefins from synthesis gas[J]. J Am Soc Chem, 2012, 134(39): 16207-16215. doi: 10.1021/ja304958u
-
[74]
马利海, 张建利, 范素兵, 赵天生. 水热法Fe-Mn催化剂制备及其合成气制低碳烯烃催化活性[J]. 燃料化学学报, 2013,41,(11): 1356-1360. MA Li-hai, ZHANG Jian-li, FAN Su-bing, ZHAO Tian-sheng. Preparation of Fe-Mn catalyst by hydrothermal method and its catalytic activity for the synthesis of light olefins from CO hydrogenation[J]. J Fuel Chem Technol, 2013, 41(11): 1356-1360.
-
[75]
刘意, 刘勇, 陈建峰, 张燚. 不同氧化锰载体对费托钴基催化剂合成低碳烯烃的影响[J]. 化工学报, 2015,66,(9): 3413-3420. LIU Yi, LIU Yong, CHEN Jian-feng, ZHANG Yi. Effects of MnOx supports on light olefin synthesis using cobalt catalyst in Fischer-Tropsch reaction[J]. J Chem Ind Eng, 2015, 66(9): 3413-3420.
-
[76]
戴薇薇, 刘达, 付东龙, 张征湃, 张俊, 徐晶, 韩一帆. MnOx助剂对Fe/SiO2催化剂费-托合成制低碳烯烃动力学的影响[J]. 化工学报, 2015,66,(9): 3444-3455. DAI Wei-wei, LIU Da, FU Dong-long, ZHANG Zheng-pai, ZHANG Jun, XU Jing, HAN Yi-fan. Kinetics study of Fischer-Tropsch reaction to lower olefins over MnOx-promoted Fe/SiO2 catalysts[J]. J Chem Ind Eng, 2015, 66(9): 3444-3455.
-
[77]
汪根存, 张侃, 刘平, 惠海涛, 李文怀, 谭猗生. Fe-Mn催化剂浆态床合成低碳烯烃的反应性能[J]. 石油化工, 2012,41,(11): 1234-1238. WANG Gen-cun, ZHANG Kan, LIU Ping, HUI Hai-tao, LI Wen-huai, TAN Yi-sheng. Performance of Fe-Mn catalyst for preparation of light olefins in slurry bed reactor[J]. Petrochem Technol, 2012, 41(11): 1234-1238.
-
[78]
YANG Z Q, PAN X L, WANG J H, BAO X H. FeN particles confined inside CNT for light olefin synthesis from syngas: Effects of Mn and K additives[J]. Catal Today, 2012, 186(1): 121-127. doi: 10.1016/j.cattod.2011.11.034
-
[79]
LIU Y, CHEN J F, BAO J, ZHANG Y. Manganese-modified Fe3O4 microsphere catalyst with effective active phase of forming light olefins from syngas[J]. ACS Catal, 2015, 6(6): 3905-3909.
-
[80]
HUO C F, LI Y W, WANG J G, JIAO H J. Insight into CH4 formation in iron-catalyzed Fischer-Tropsch synthesis[J]. J Am Soc Chem, 2009, 131(41): 14713-14721. doi: 10.1021/ja9021864
-
[81]
PERRICHON V, CHARCOSSET H, BARRAULT J, FORQUY C. Influence of a partial dissolution of alumina during the preparation of iron catalysts on their catalytic properties for Fischer-Tropsch synthesis[J]. Appl Catal, 1983, 7(1): 21-29. doi: 10.1016/0166-9834(83)80235-8
-
[82]
RAO K R P M, HUGGUNS F E, MAHAJAN V, HUFFMAN G P, RAO V U S, BHATT B L, BUKUR D B, DAVIS B H, O'BRIEN R J. MÖssbauer spectroscopy study of iron-based catalysts used in Fischer-Tropsch synthesis[J]. Top Catal, 1995, 2(1): 71-78.
-
[83]
WAN H J, WU B S, TAO Z C, LI T Z, AN X, XIANG H W, LI Y W. Study of an iron-based Fischer-Tropsch synthesis catalyst incorporated with SiO2[J]. J Mol Catal A, 2006, 260(1/2): 255-263.
-
[84]
SUO H Y, WANG S G, ZHANG C H, XU J, WU B S, YANG Y, XIANG H W, LI Y W. Chemical and structural effects of silica in iron-based Fischer-Tropsch synthesis catalysts[J]. J Catal, 2012, 286: 111-123. doi: 10.1016/j.jcat.2011.10.024
-
[85]
位健, 马现刚, 方传艳, 葛庆杰, 徐恒泳. Fe /SiO2纳米复合物上合成气制低碳烯烃催化性能研究[J]. 燃料化学学报, 2014,42,(7): 827-832. WEI Jian, MA Xian-gang, FANG Chuan-yan, GE Qing-jie, XU Heng-yong. Iron-silica nanocomposites as a catalyst for the selective conversion of syngas to light olefins[J]. J Fuel Chem Technol, 2014, 42(7): 827-832.
-
[86]
李剑锋, 陶跃武, 周晓峰, 陈庆龄, 袁渭康. 负载型铁基催化剂上合成气制低碳烯烃[J]. 化学反应工程与工艺, 2010,26,(6): 486-493. LI Jian-feng, TAO Yue-wu, ZHOU Xiao-feng, CHEN Qing-ling, YUAN Wei-kang. Performance of supported Fe based catalyst for synthesis of light alkenes from syngas[J]. Chem React Eng Technol, 2010, 26(6): 486-493.
-
[87]
BRUCE L, HOPE G, TURNEY T W. Light olefin production from CO/H2 over silica supported Fe/Mn/K catalysts derived from a bimetallic carbonyl anion, [Fe2Mn (CO)12]-[J]. React Kinet Catal Lett, 1982, 20(1): 175-180.
-
[88]
VAN DILLEN A J, TERÖRDE R J A M, LENSVELD D J, GEUS J W, DE JONG K P. Synthesis of supported catalysts by impregnation and drying using aqueous chelated metal complexes[J]. J Catal, 2003, 216(1/2): 257-264.
-
[89]
SMITH A K, THEOLIER A, BASSET J M, UGO R, COMMEREUC D, CHAUVIN Y. Hydrocarbon formation from metal carbonyl clusters supported on highly divided oxides[J]. J Am Chem Soc, 1978, 100(8): 2590-2591. doi: 10.1021/ja00476a076
-
[90]
STOOP F, VAN DER WIELE K. Formation of olefins from synthesis gas over silica-supported RuFe bimetallic catalysts[J]. Appl Catal, 1986, 23(1): 35-47. doi: 10.1016/S0166-9834(00)81450-5
-
[91]
BAKER B G, CLARK N J. Selective Fischer-Tropsch catalysts containing iron and lanthanide oxides[J]. Stud Surf Sci Catal, 1987, 31: 455-465. doi: 10.1016/S0167-2991(08)65428-2
-
[92]
BAKER B G, PARK T, CLARK N J, MCARTHUR H, SUMMERVILLE E. Catalysts and methods of their manufacture: US, 4610975[P]. 1986-09-09.
-
[93]
SOMMEN A P B, STOOP F, VAN DER WIELE K. Synthesis gas conversion on carbon supported iron catalysts and the nature of deactivation[J]. Appl Catal, 1985, 14: 277-288. doi: 10.1016/S0166-9834(00)84360-2
-
[94]
JONES V K, NEUBAUER L R, BARTHOLOMEW C H. Effects of crystallite size and support on the carbon monoxide hydrogenation activity/selectivity properties of iron/carbon[J]. J Phys Chem, 1986, 20(20): 4832-4839.
-
[95]
张敬畅, 卫国宾, 曹维良. 合成气制低碳烯烃用Fe/AC催化剂的制备及性能表征[J]. 催化学报, 2003,24,(4): 259-264. ZHANG Jing-chang, WEI Guo-bin, CAO Wei-liang. Preparation and characterization of Fe/AC catalysts for synthesis of light olefins via carbon monoxide hydrogenation[J]. Chin J Catal, 2003, 24(4): 259-264.
-
[96]
LU J Z, YANG L J, XU B L, WU Q, ZHANG D, YUAN S J, ZHAI Y, WANG X Z, FAN Y N, HU Z. Promotion effects of nitrogen doping into carbon nanotubes on supported iron Fischer-Tropsch catalysts for lower olefins[J]. ACS Catal, 2014, 4(2): 613-621. doi: 10.1021/cs400931z
-
[97]
CHEN X Q, DENG D H, PAN X L, HU Y F, BAO X H. N-doped graphene as an electron donor of iron catalysts for CO hydrogenation to light olefins[J]. Chem Commun, 2014, 51(1): 217-220.
-
[98]
SCHULTE H J, GRAF B, XIA W, MUHLER M. Nitrogen-and oxygen-functionalized multiwalled carbon nanotubes used as support in iron-catalyzed, high-temperature Fischer-Tropsch synthesis[J]. 2012, 4(3): 350-355.
-
[99]
CHEN H, ADESINA A A. Improved alkene selectivity in carbon monoxide hydrogenation over silica supported cobalt-molybdenum catalyst[J]. Appl Catal A: Gen, 1994, 112(2): 87-103. doi: 10.1016/0926-860X(94)80211-4
-
[100]
FRAENKEL D, GATES B C. Shape-selective Fischer-Tropsch synthesis catalyzed by zeolite-entrapped cobalt clusters[J]. J Am Chem Soc, 1980, 102(7): 2478-2480. doi: 10.1021/ja00527a067
-
[101]
FEYZI M, HASSANKHANI A. TiO2 supported cobalt-manganese nano catalysts for light olefins production from syngas[J]. J Energy Chem, 2013, 22(4): 645-652. doi: 10.1016/S2095-4956(13)60085-6
-
[102]
ZHOU W G, LIU J Y, WU X, CHEN J F, ZHANG Y. An effective Co/MnOx catalyst for forming light olefins via Fischer-Tropsch synthesis[J]. Catal Commun, 2015, 60: 76-81. doi: 10.1016/j.catcom.2014.10.027
-
[103]
TANG L P, SONG C L, YANG X L, LI M L, HU B. Promotion of Mn doped Co/CNTs catalysts for CO hydrogenation to light olefins[J]. Chin J Chem, 2013, 31(6): 826-830. doi: 10.1002/cjoc.v31.6
-
[1]
-
图 2 Zr-Zn氧化物与SAPO-34分子筛不同结合方式对反应性的影响[14]
Figure 2 Effect of integration manner on the catalytic behaviors of the composite catalysts containing Zr-Zn (Zr/Zn=2:1) oxide and SAPO-34
(a): dual-bed configuration; (b): stacking of granules with sizes of 250-600 mm; (c): simple mixing of the two components in an agate mortar; (d): ball-milling of two components together for 24 h the o/p ratio denotes the ratio of C2-4 olefin/paraffin[14]
图 3 OX-ZEO双功能催化剂的催化性能[5]
Figure 3 Performance of the bifunctional OX-ZEO catalyst in the conversion of syngas to olefins[5] (a) CO conversion and product distribution at different H2/CO volume ratios over ZnCrOx/MSAPO; (b) hydrocarbon distribution over OX-ZEO in comparison with that reported for FTTO and that in FTS predicted by the ASF model at a chain growth probability of 0.46; (c) stability test of the ZnCrOx/MSAPO catalyst[5] FTTO or FTO, Fischer-Tropsch to olefin
图 8 (a) Mn/Fe3O4结构模型;(b) Fe3O4微球的扫描电镜照片;(c) 还原后Mn/Fe3O4催化剂的TEM照片;(d) Mn/Fe3O4催化剂的STEM照片;(e) 相应的STEM-EDX元素分析[79]
Figure 8 (a) Structural model for the Mn/Fe3O4 catalyst; (b) SEM images of the Fe3O4 microspheres; (c) TEM images of theMn/Fe3O4 catalyst after reduction; (d) original STEM image of Mn/Fe3O4 catalyst as prepared; (e) corresponding STEM-EDX elemental mapping of Fe, O and Mn on the catalyst[79]
表 1 S和Na对负载铁催化剂性能的影响[59]
Table 1. Effect of S and Na promoters on the catalytic performance of supported iorn catalysts in FT synthesis[59]
Catalyst Fischer-Tropsch yield/(10-5 molCO·gFe-1·s-1) Product selectivity s/% CH4 C2-4 olefins C2-4 paraffins C5+ Fe/Al2O3 0.14 54 42 3 2 Fe/Al2O3 + 0.2% Na 0.08 50 43 5 3 Fe/Al2O3 + 0.03% S 1.70 33 58 3 5 Fe/Al2O3 + 0.2% Na + 0.03% S 0.57 15 64 2 19 Fe/Al2O3 + 0.4% Na + 0.03% S 0.16 23 51 3 22 Fe 0.02 78 13 2 7 Fe + 0.4% Na + 0.4% S 0.30 21 60 3 16 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 0
- HTML全文浏览量: 0



 下载:
下载:









 下载:
下载:

