 图1
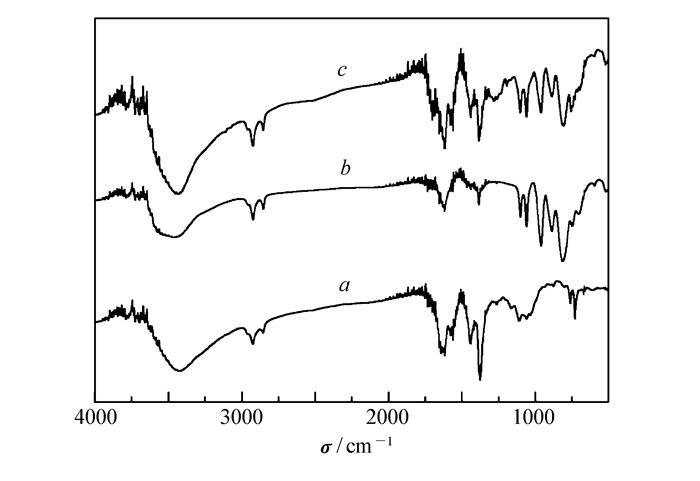
HKUST-1(a)、CuPW11@HKUST-1(b)和催化后回收CuPW11@HKUST-1(c)的红外谱图
Figure1.
FT-IR spectra of HKUST-1(a), CuPW11@HKUST-1(b) and CuPW11@HKUST-1 after catalysis(c)
图1
HKUST-1(a)、CuPW11@HKUST-1(b)和催化后回收CuPW11@HKUST-1(c)的红外谱图
Figure1.
FT-IR spectra of HKUST-1(a), CuPW11@HKUST-1(b) and CuPW11@HKUST-1 after catalysis(c)

Citation: XU Kerui, ZHONG Zhiming, XU Huidong, WANG Xuan, ZHAO Min, WU Chuande. Highly Efficient Aerobic Oxidation of Arylalkanes with a Biomimetic Catalyst Platform[J]. Chinese Journal of Applied Chemistry, 2017, 34(9): 1079-1085. doi: 10.11944/j.issn.1000-0518.2017.09.170191

复合仿生催化体系的构建与高效有氧氧化芳基烷烃
English
Highly Efficient Aerobic Oxidation of Arylalkanes with a Biomimetic Catalyst Platform
-
酶是一类具有特异催化性质的生物催化剂,能够高效催化一些传统催化剂无法在温和条件下催化的化学反应[1]。例如,生物酶可以在温和条件下活化氧气,实现常温、常压催化氧化惰性有机物分子,而传统催化剂则需要在高温、高压的反应条件下催化反应,并且反应物转化率相对较低以及产物选择性相对较差[2-3]。为了实现在温和条件下的催化化学反应,研究人员根据生物酶的活性中心、结构以及催化机理等设计合成了大量模拟酶催化剂,实现了在相对温和条件下类似酶催化的高效率与高选择性[4-5]。
杂多酸(Polyoxometalates,简写为POMs)是一类具有纳米尺寸大小的阴离子型金属氧化物簇合物,具有结构多样、功能齐全与性质可调控等特点。在杂多酸中引入具有氧化还原活性的金属杂原子,杂多酸往往表现出类似生物酶的催化性质[6-7]。金属-有机框架材料(metal-organic frameworks,简称MOFs),是一类由多齿有机配体桥联金属离子形成的多孔框架材料[8-9]。MOFs具有孔隙率高、比表面积大、结构与性质易于调控等特点,是一类理想的模拟酶催化剂载体。许多不同类型的分子催化剂,包括POMs,分别被选择负载在MOFs孔道中,形成了不同类型的复合催化剂材料,实现了高活性以及高选择性催化反应[10-17]。其局限性在于无法在温和条件下活化氧气分子,实现惰性C—H键的高效活化氧化[18]。根据过渡金属取代的缺位杂多酸往往具有特殊催化性质,我们合成了由Keggin-型缺位杂多酸[CuPW11O39H5](简写为CuPW11)与MOF材料HKUST-1(HKUST=Hong Kong University of Science and Technology)形成的复合材料CuPW11@HKUST-1,并研究了其催化性质[19-20]。实验结果表明,CuPW11@HKUST-1在温和条件下无法直接活化氧气实现催化需氧氧化芳基烷烃。为了达到在温和条件下直接活化O2分子的目的,我们引入了N-羟基邻苯二甲酰亚胺(N-hydroxyphthalimide, 简写为NHPI)作为助催化剂,与CuPW11@HKUST-1一起形成复合仿生催化体系。复合仿生催化体系在催化芳基烷烃的氧化反应中,通过模拟生物酶的氧化中心、还原中心以及催化机理,实现了温和条件下以氧气为氧化剂高效催化氧化芳基烷烃,表现出了类似生物酶催化的性质。
1 实验部分
1.1 试剂和仪器
杂多酸K5CuPW11O39参照文献[21]的方法合成。其它试剂及原料均为市售分析纯,未经纯化处理,直接使用。
FTS-40 spectrophotomete型红外光谱仪(IR,美国Bio-RAD公司,KBr压片法);D/MAX 2550/PC型X射线粉末衍射仪(PXRD, 日本RIGAKU公司,CuKα);X-series-Ⅱ型电感耦合等离子体质谱仪(ICP-MS,美国Thermo Scientific公司);GCMS-QP2010型气相质谱联用色谱仪(GC-MS,日本SHIMADZU公司)。
1.2 CuPW11@HKUST-1的合成
在菌种瓶(2 mL)中加入K5CuPW11O39(6.5 mg, 0.002 mmol),Cu(NO3)·3H2O(75 mg, 0.31 mmol)和1 mL水,超声溶解后加入均苯三酸(45 mg, 0.21 mmol),磁力搅拌反应20 min后加入(CH3)4NOH(42 mg, 0.46 mmol),继续搅拌20 min,在65 ℃烘箱中反应7 d。将深蓝色晶体离心分离,用饱和KCl溶液(2 mL)和去离子水(2 mL)分别洗涤3次,晾干(产率89%)。FT-IR(KBr), σ/cm-1:1654(m), 1617(s), 1383(m), 1111(s), 1058(s), 960(s), 887(s), 801(s), 744(m), 711(m), 520(m)。
1.3 催化实验
将芳基烷烃(0.3 mmol), CuPW11@HKUST-1(0.1 μmol, 根据杂多酸计算), NHPI(0.03 mmol)溶解在乙腈溶剂(2 mL)中,在1.013×105 Pa O2气气氛(气球)、50 ℃下反应24 h。当反应混和液冷却到室温后,离心回收催化剂,用CH3CN多次洗涤固体催化剂。用GC-MS分析离心液中反应物与产物含量,并计算反应物转化率、产物产率与选择性。其它参比催化剂如CuPW11、HKUST-1和HKUST-1/CuPW11的用量与CuPW11@HKUST-1中各组分的含量相一致。
1.4 吸附实验
将经过除去溶剂活化的CuPW11@HKUST-1(10 mg)分别浸泡在乙基苯和苯乙酮(1.0 mL)中,室温搅拌6 h后离心分离,用乙醚洗涤固体除去表面吸附的乙基苯或苯乙酮。将所得固体浸泡在乙腈中,室温搅拌18 h释放出孔道中吸附的乙基苯或苯乙酮,然后离心分离。用GC-MS分析所得离心液,计算乙基苯和苯乙酮的吸附量。
2 结果与讨论
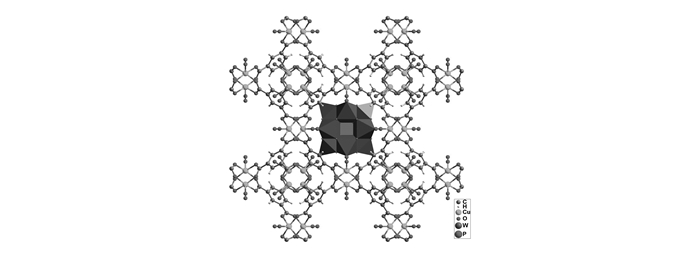
参考文献[20]方法,但杂多酸用量约为其1/7,合成了CuPW11@HKUST-1,即将均三苯甲酸、硝酸铜、四甲基氢氧化铵和杂多酸CuPW11溶解在水中,在65 ℃反应7 d。通过红外以及PXRD等手段表征所得深蓝色块状晶体(图 1和图 2),并与文献[19-20]结果进行了比较。ICP-MS分析结果表明,CuPW11@HKUST-1的分子式为[Cu3(C9H3O6)2][(CH3)4N]0.14[CuPW11O39H]0.035。其中,杂多酸[CuPW11O39H5]位于HKUST-1的孔道内,而其余孔道相互连通,有利于反应分子的传输以及产物分子从孔道中排出,进而提高催化效率(图 3)。
 图1
HKUST-1(a)、CuPW11@HKUST-1(b)和催化后回收CuPW11@HKUST-1(c)的红外谱图
Figure1.
FT-IR spectra of HKUST-1(a), CuPW11@HKUST-1(b) and CuPW11@HKUST-1 after catalysis(c)
图1
HKUST-1(a)、CuPW11@HKUST-1(b)和催化后回收CuPW11@HKUST-1(c)的红外谱图
Figure1.
FT-IR spectra of HKUST-1(a), CuPW11@HKUST-1(b) and CuPW11@HKUST-1 after catalysis(c)
直接活化氧气氧化碳氢化合物具有重要的工业价值[22-23],因此,我们以催化有氧氧化芳基烷烃作为模板反应研究了CuPW11@HKUST-1的模拟酶催化性质。由于芳基烷烃中的C—H键非常稳定,单组份CuPW11@HKUST-1催化剂无法在温和反应条件下(50 ℃和1.013×105 Pa O2)活化氧气氧化乙基苯(表 1, entry 1),这主要是因为,与生物酶催化比较,缺少能提供电子的还原助催化剂。根据N-羟基邻苯二甲酰亚胺(NHPI)在金属离子的作用下会形成苯二甲酰亚氨基—NO·(phthalimido-N-oxyl,简写为PINO)自由基,并生成一个具有还原性质的H·[24]。H·可以作为电子给体促进氧气活化,起到类似还原辅酶的作用,促进温和条件下高效模拟酶催化氧化反应。如表 1中entry 2所示,在NHPI助催化剂的协同作用下,复合催化体系在温和反应条件下(50 ℃和11.013×105 Pa O2)实现了高效催化有氧氧化乙基苯。其中,苯乙酮的产率为88%,选择性为97%。在相同催化反应条件下,单组分如CuPW11和NHPI以及它们简单混合物的催化效率远远低于复合催化体系(表 1, entries 3~7),说明催化反应是在不同组分间的协同作用下完成的,而不是简单催化结果的加和。仿生催化体系具有很好的普适性,能在温和条件下催化氧化一系列芳基烷烃化合物(表 1, entries 8~10)。二苯甲烷的转化率较低,可能是由于其尺寸较大,导致其与位于孔道中杂多酸活性中心接触困难(表 1, entry 11)。
 表 1
选择催化有氧氧化芳基烷烃反应a
Table 1.
Selective aerobic oxidation of alkylbenzenes for the formation of phenylketonesa
表 1
选择催化有氧氧化芳基烷烃反应a
Table 1.
Selective aerobic oxidation of alkylbenzenes for the formation of phenylketonesa

Entry Substrate Catalyst Product Yield/%b 1 
CuPW11@HKUST-1 
trace 2 
CuPW11@HKUST-1/NHPI 
88 3 
NHPI 
trace 4 
CuPW11 
trace 5 
HKUST-1/NHPI 
trace 6 
NHPI/CuPW11 
33 7 
HKUST-1/CuPW11/NHPI 
11 8 
CuPW11@HKUST-1/NHPI 
86 9 
CuPW11@HKUST-1/NHPI 
99 10 
CuPW11@HKUST-1/NHPI 
93 11 
CuPW11@HKUST-1/NHPI 
59 a.Alkylbenzene(0.3 mmol), CuPW11@HKUST-1(0.1 μmmol, based on POM) and NHPI(0.03 mmol) in acetonitrile(2 mL) were stirred under an O2 atmosphere(balloon) at 50 ℃ for 24 h; b.yield% was determined by GC-MS. 为了证明催化反应主要是在复合材料CuPW11@HKUST-1孔道内进行,我们研究了CuPW11@HKUST-1对反应物乙基苯和产物苯乙酮的吸附性质。将活化后的CuPW11@HKUST-1分别在乙基苯和苯乙酮中室温浸泡6 h,然后通过GC分析反应物及产物的吸附量。分析与计算结果表明,每摩尔CuPW11@HKUST-1的孔道可吸附反应物乙基苯的量为7.5摩尔,而产物苯乙酮的吸附量为1.0摩尔。当将CuPW11@HKUST-1加入到乙基苯与苯乙酮(1:1摩尔比)的混合溶液中,CuPW11@HKUST-1表现出对反应物乙基苯优先选择吸附与富集的性质。在CuPW11@HKUST-1孔道中,乙基苯和苯乙酮的比例为1.7:1(摩尔比)。为了进一步证明CuPW11@HKUST-1对反应物分子具有富集能力,将催化反应进行12h后的反应体系离心,收集固体催化剂。GC-MS分析结果表明,从固体催化剂中释放的乙基苯与苯乙酮比例为2.7:1(摩尔比)。总之,上述研究结果说明,CuPW11@HKUST-1在催化反应过程中通过富集作用保持了孔道中高反应物浓度、低产物浓度,最大限度提高了复合催化体系的催化效率。
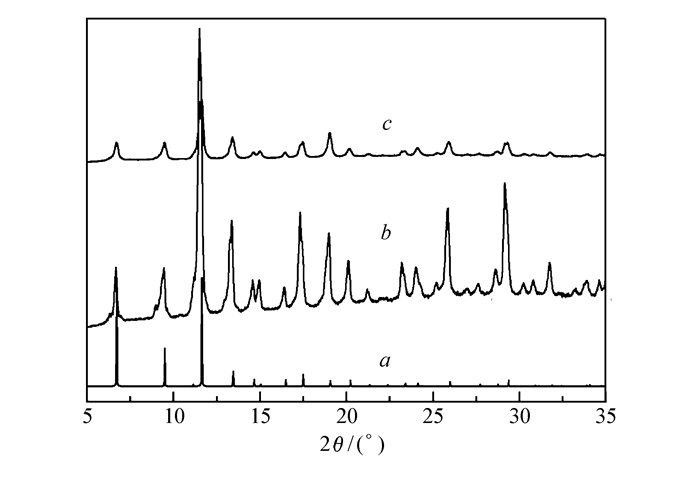
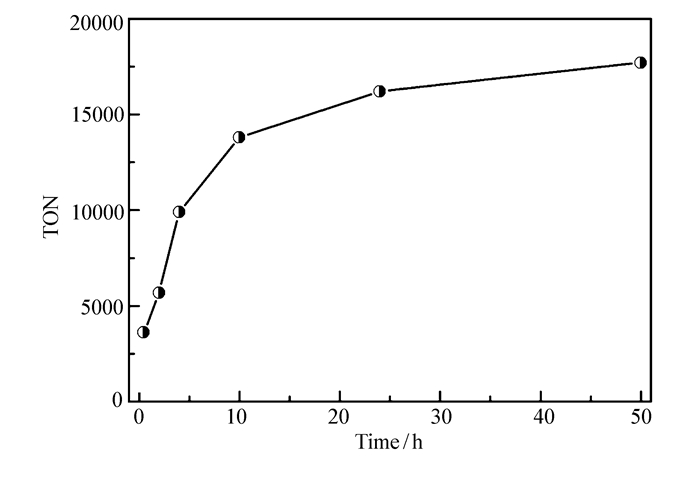
为了证实CuPW11@HKUST-1的非均相催化性质,我们首先在不加反应物的情况下,将CuPW11@HKUST-1和NHPI的混合物在乙腈溶剂中、50 ℃和O2气气氛下搅拌24 h,然后将混合物离心分离。在分离的上清液中加入反应物乙基苯,然后在如前所述的相同条件下催化反应24 h。GC分析结果表明,乙基苯的转化率与NHPI单组分催化的结果几乎是相同的,证实了CuPW11@HKUST-1催化反应的非均相催化性质。通过比较CuPW11@HKUST-1在催化反应前后的PXRD图谱(图 2)可以看出,CuPW11@HKUST-1的结构未发生明显的改变,证实了CuPW11@HKUST-1在上述催化反应条件下的稳定性。但由于是在搅拌条件下的催化反应,CuPW11@HKUST-1在催化反应后颗粒减小,使得PXRD图谱中的衍射峰强度明显减弱。我们还通过增大乙基苯与催化剂的比例,研究了复合催化体系的催化动力学性质。如图 4所示,其转化数(TON)可以高达17700,并能持续保持高催化活性。
众所周知,生物酶催化氧化反应主要是在催化氧化还原中心与还原辅酶的协同作用下完成的[5]。其中氧化还原中心与O2配位结合,再通过还原辅酶提供电子实现活化O2分子。与生物酶比较,固载在HKUST-1孔道中的杂多酸表面金属CuⅡ离子起到了模拟酶氧化还原活性中心的作用,NHPI在形成PINO时提供一个H·作为电子与质子的组合供体,起到了类似还原辅酶的作用[24]。在催化反应过程中,POM CuⅡ位点首先与O2分子配位结合,然后从NHPI得到一个H·形成过氧化物中间体,再经过NHPI二次还原形成高价金属氧化物中间体,实现了分子氧活化。金属高价氧化物中间体非常活泼,很容易将氧原子插入到乙基苯的亚甲基C—H键之间,实现乙基苯氧化反应。另外,PINO也非常活泼,容易从有机物分子中夺取H原子回到NHPI,并形成一个活泼自由基进一步活化氧气,同时实现有机物分子的氧化[24]。综上所述,复合仿生催化体系通过POM促进NHPI形成PINO自由基实现氧气活化,NHPI通过提供H·促进POM活化O2分子。也就是说,通过多组分的协同作用提高了单组分的催化效率,实现了高效有氧氧化芳基烷烃。
3 结论
为了实现高效模拟酶催化活化氧气氧化芳基烷烃,我们以CuPW11@HKUST-1孔道中的杂多酸组分作为氧化还原活性中心,以NHPI作为供电子的助催化剂,形成复合模拟酶催化体系。该模拟酶催化体系在催化活化氧气氧化芳基烷烃反应中表现出了类似生物酶催化的性质,具有反应条件温和、转化率高、转化数高和选择性高等特点。本文的研究结果表明,使用多催化活性中心复合催化体系,通过不同组分间的协同催化,是一条切实可行的模拟酶高效催化反应路线,为在温和条件下实现高效活化惰性反应物分子提供了一个有效途径。
-
-
[1]
Hughes M D, Xu Y J, Jenkins P. Tunable Gold Catalysts for Selective Hydrocarbon Oxidation Under Mild Conditions[J]. Nature, 2005, 437(7062): 1132-1135. doi: 10.1038/nature04190
-
[2]
Liese A, Seelbach K, Eds. Industrial Biotransformations[M]. Wandrey, C. Wiley-VCH, Weinhiem, 2006.
-
[3]
Faber K. Biotransformations in Organic Chemistry[M]. Springer-Verlag, Berlin, 5th ed, 2004.
-
[4]
Kadish K M, Smith K M, Guilard R, Eds. The Porphyrin Handbook[M]. Academic Press, San Diego, 2000.
-
[5]
Sheldon R A. Metalloporphyrins in Catalytic Oxidation[M]. Marcel Dekker, Basel, 1994.
-
[6]
Wang S S, Yang G Y. Recent Advances in Polyoxometalate-Catalyzed Reactions[J]. Chem Rev, 2015, 115(11): 4893-4962. doi: 10.1021/cr500390v
-
[7]
Ye J J, Wu C D. Immobilization of Polyoxometalates in Crystalline Solids for Highly Efficient Heterogeneous Catalysis[J]. Dalton Trans, 2016, 45(25): 10101-10112. doi: 10.1039/C6DT01378C
-
[8]
Zhou H C, Long J R, Yaghi O M. Metal-Organic Frameworks Special Issue[J]. Chem Rev, 2012, 112(2): 673-1268. doi: 10.1021/cr300014x
-
[9]
Zhou H C, Kitagawa S. Themed Issues on Metal-Organic Frameworks[J]. Chem Soc Rev, 2014, 43(16): 5415-6172. doi: 10.1039/C4CS90059F
-
[10]
Zhao M, Ou S, Wu C D. Porous Metal-Organic Frameworks for Heterogeneous Biomimetic Catalysis[J]. Acc Chem Res, 2014, 47(4): 1199-1207. doi: 10.1021/ar400265x
-
[11]
Zou C, Zhang Z, Xu X. A Multifunctional Organic-Inorganic Hybrid Structure Based on MnⅢ-Porphyrin and Polyoxometalate as a Highly Effective Dye Scavenger and Heterogenous Catalyst[J]. J Am Chem Soc, 2012, 134(1): 87-90. doi: 10.1021/ja209196t
-
[12]
Yang X L, Xie M H, Zou C. Porous Metalloporphyrinic Frameworks Constructed from Metal 5, 10, 15, 20-Tetrakis(3, 5-biscarboxylphenyl)porphyrin for Highly Efficient and Selective Catalytic Oxidation of Alkylbenzenes[J]. J Am Chem Soc, 2012, 134(25): 10638-10645. doi: 10.1021/ja303728c
-
[13]
Liu J, Chen L, Cui H. Applications of Metal Organic Frameworks in Heterogeneous Supramolecular Catalysis[J]. Chem Soc Rev, 2014, 43(16): 6011-6061. doi: 10.1039/C4CS00094C
-
[14]
Ou S, Wu C D. Rational Construction of Metal-Organic Frameworks for Heterogeneous Catalysis[J]. Inorg Chem Front, 2014, 1(10): 721-734. doi: 10.1039/C4QI00111G
-
[15]
Wu C D, Zhao M. Incorporation of Molecular Catalysts in Metal Organic Frameworks for Highly Efficient Heterogeneous Catalysis[J]. Adv Mater, 2017, 29(14): 1605446. doi: 10.1002/adma.v29.14
-
[16]
Liu Y, Liu S, He D. Crystal Facets Make a Profound Difference in Polyoxometalate-Containing Metal-Organic Frameworks as Catalysts for Biodiesel Production[J]. J Am Chem Soc, 2015, 137(39): 12697-12703. doi: 10.1021/jacs.5b08273
-
[17]
Sun C Y, Liu S X, Liang D D. Highly Stable Crystalline Catalysts Based on a Microporous Metal-Organic Framework and Polyoxometalates[J]. J Am Chem Soc, 2009, 131(5): 1883-1888. doi: 10.1021/ja807357r
-
[18]
Zhao M, Ou S, Wu C D. Biomimetic Activation of Molecular Oxygen with a Combined Metalloporphyrinic Framework and Co-catalyst Platform[J]. ChemCatChem, 2017, 9(3): 1192-1196.
-
[19]
Chui S S Y, Lo S M F, Charmant J P H. A Chemically Functionalizable Nanoporous Material[J]. Science, 1999, 283(5405): 1148-1150. doi: 10.1126/science.283.5405.1148
-
[20]
Song J, Luo Z, Britt D K. A Multiunit Catalyst with Synergistic Stability and Reactivity:A Polyoxometalate Metal Organic Framework for Aerobic Decontamination[J]. J Am Chem Soc, 2011, 133(42): 16839-16846. doi: 10.1021/ja203695h
-
[21]
Tourn C M, Tourn G F, Malik S A. Triheteropolyanions Containing Copper(Ⅱ), Manganese(Ⅱ), or Manganese(Ⅲ)[J]. J Inorg Nucl Chem, 1970, 32(12): 3875-3890. doi: 10.1016/0022-1902(70)80566-8
-
[22]
Labinger J A, Bercaw J E. Understanding and Exploiting C-H Bond Activation[J]. Nature, 2002, 417(6888): 507-514. doi: 10.1038/417507a
-
[23]
Bäckvall J E. Modern Oxidation Methods[M]. John Wiley, Weinheim, 2011.
-
[24]
Recupero F C, Punta F. Free Radical Functionalization of Organic Compounds Catalyzed by N-Hydroxyphthalimide[J]. Chem Rev, 2007, 107(9): 3800-3842. doi: 10.1021/cr040170k
-
[1]
-
表 1 选择催化有氧氧化芳基烷烃反应a
Table 1. Selective aerobic oxidation of alkylbenzenes for the formation of phenylketonesa

Entry Substrate Catalyst Product Yield/%b 1 
CuPW11@HKUST-1 
trace 2 
CuPW11@HKUST-1/NHPI 
88 3 
NHPI 
trace 4 
CuPW11 
trace 5 
HKUST-1/NHPI 
trace 6 
NHPI/CuPW11 
33 7 
HKUST-1/CuPW11/NHPI 
11 8 
CuPW11@HKUST-1/NHPI 
86 9 
CuPW11@HKUST-1/NHPI 
99 10 
CuPW11@HKUST-1/NHPI 
93 11 
CuPW11@HKUST-1/NHPI 
59 a.Alkylbenzene(0.3 mmol), CuPW11@HKUST-1(0.1 μmmol, based on POM) and NHPI(0.03 mmol) in acetonitrile(2 mL) were stirred under an O2 atmosphere(balloon) at 50 ℃ for 24 h; b.yield% was determined by GC-MS. -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 1
- 文章访问数: 1038
- HTML全文浏览量: 120


 下载:
下载:



 下载:
下载:

