 图 图式 1
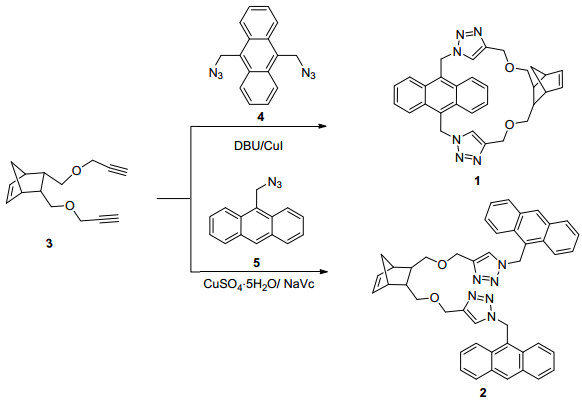
目标分子1和2的合成路线
Figure 图式 1.
Synthetic route of 1 and 2
图 图式 1
目标分子1和2的合成路线
Figure 图式 1.
Synthetic route of 1 and 2

Citation: Zhu Wenbin, Lü Xiaolan, Zhu Jianghua, Cao Qianyong. Norbornene-Based Triazoles for Fluorescent Sensing of Metal Ions[J]. Chinese Journal of Organic Chemistry, 2017, 37(3): 624-629. doi: 10.6023/cjoc201611004

降冰片烯荧光三唑化合物的合成及其金属离子识别
English
Norbornene-Based Triazoles for Fluorescent Sensing of Metal Ions
-
Key words:
- norbornene
- / anthracene
- / triazole
- / fluorescence
- / metal ions recognition
-
荧光识别过渡金属及重金属离子化学传感器的设计与合成, 由于其操作简便, 灵敏度高, 检测速度快等优点, 近年来引起了广泛的关注[1~4].其中, Zn2+与Cu2+是人体必需的微量元素, 参与人体的新陈代谢与多种酶的合成.而Hg2+为对人体有毒的一种重金属离子, 会导致消化系统、神经系统、心血管等一系列疾病; 铜离子摄入过量会导致铜中毒, 严重的导致肝脏疾病甚至死亡[5~7].因此, 对这些金属离子快速灵敏识别与检测具有重要的意义.
金属离子荧光化学传感器是指将荧光信号单元及金属离子识别单元通过共价键键合的功能分子.其中荧光信号单元包括稠环芳烃、罗丹明、丹酰氯、萘酰亚胺、荧光素等, 而识别基团则为O、S、N等杂原子.目前, 基于光致电子转移 (PET)、荧光共振能量转移 (FRET)、分子内电荷转移 (ICT) 及单分子聚激态发射转换的金属离子化学传感器已有大量文献报道[8~13].
2001年Sharpless等[14, 15]提出的Cu (Ⅰ) 催化的炔与叠氮化合物1, 3-偶极加成合成1, 2, 3-环三唑化合物, 即“点击反应”, 由于其反应条件温和、操作简单、反应产率高等优点在有机材料、生物及催化领域有着广泛应用.同时, “点击反应”生成的环三唑不仅是一个共价键间隔基, 同时是金属离子与阴离子的识别单元:其3-位N原子是金属离子的配位点, 而5-位CH能与阴离子发生氢键作用, 可用于设计合成不同阴/阳离子荧光化学传感器[16~25].笔者近期关注三唑化合物化学传感器的设计与合成.继续前期工作, 本文报道了以降冰片烯为骨架含蒽荧光团环状双三唑化合物1及其非环对应物2, 对其金属离子识别性质通过荧光、1H NMR及DFT计算进行了详细研究.
1 结果与讨论
1.1 合成目标化合物研究
目标化合物1和2的合成见Scheme 1.以蒽及降冰片烯二甲酸酐为起始原料, 首先根据文献方法[26~29]合成降冰片烯双炔化合物3、9, 10-二迭氮甲基蒽化合物4及9-叠氮甲基蒽化合物5.非环双三唑化合物2以典型的“点击反应”催化剂CuSO4/NaVc催化在N, N-二甲基甲酰胺 (DMF) 溶剂中合成, 而环双三唑化受体1以1, 8-二氮杂二环[5.4.0]十一碳-7-烯 (DBU)/CuI为催化剂在甲苯溶液中采用极度稀释法[21, 30]合成.其中环受体分子1的收率为39%, 而非环受体分子2的收率为80%, 与文献报道值相一致.同时研究还发现, 非环受体2在大部分有机溶剂中, 如CH2Cl2, CHCl3, CH3CN, EtOAc, MeOH, DMF及二甲基亚砜 (DMSO) 中都有很好的溶解性, 而环受体仅在强极性溶剂DMF及DMSO中才有好的溶解性.它们的结构通过了1H NMR, 13C NMR, ESI-TOF-MS及元素分析进行了表征.
1.2 阳离子的荧光光谱研究
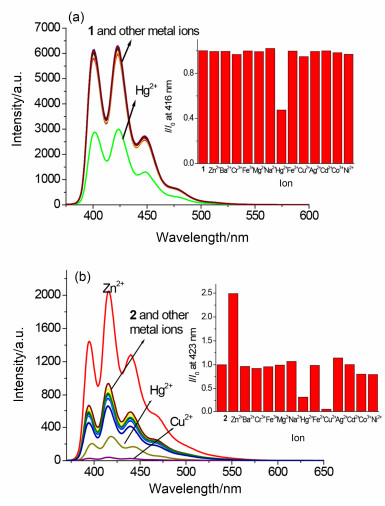
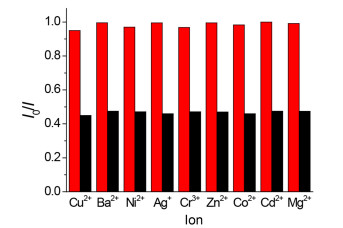
首先通过荧光光谱研究了受体分子1与2对不同金属离子的识别能力.在CH3CN-H2O (V:V=90:10) 溶液中, 以360 nm为激发波长, 受体分子1与2在具有基于蒽荧光团强的单体发射峰, 其中1的发射峰处于400, 423和449 nm, 而受体分子2的发射峰位于于394, 416和439 nm.受体分子1较2发射峰红移可能归因于1中两个缺电子三唑环对一个蒽生色团的强的吸电子效应, 而在受体2中则为一个三唑环对一个蒽环的吸电子效应.当滴加不同金属离子 (Na+, Mg2+, Ba2+, Hg2+, Cu2+, Cr3+, Zn2+, Fe2+, Ni2+, Co2+, Cd2+, Ag+) 于受体1或2时, 环状受体分子1仅对Hg2+有很好的荧光淬灭响应, 而非环受体分子2对Zn2+, Hg2+, Cu2+都表现出不同的荧光信号响应 (图 1).其中滴加Zn2+时使受体分子的荧光强度增大, 而滴加Hg2+和Cu2+时导致荧光淬灭响应.非环受体2差的金属离子选择性可能归因为其柔性可变的双足构型, 可容纳不同离子半径的金属离子配位.
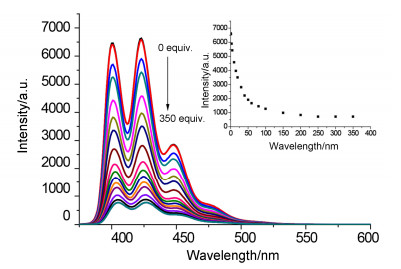
图 2为受体分子1中滴加不同当量Hg2+时荧光光谱变化图.随着Hg2+浓度增加, 化合物1基于蒽单分子发射峰强度逐渐减弱.当滴加约250 equiv.的Hg2+时, 其光谱强度变化达到饱和, 其荧光淬灭率 (I-I0)/I0达到89%.滴加Hg2+导致1荧光减弱可归因于金属离子Hg2+到蒽荧光团PET淬灭过程, 如同一些文献报道那样[11].根据荧光光谱滴定数据, 根据Benesi-Hilde-brand[31]方程线性拟合, 可得出1和Hg2+络合化学计量比为1:1.同时算得1-Hg2+的络合常数为2.03×103 L·mol-1 (R=0.998), 对Hg2+检测限为3.52×10-4 mol/L (R=0.989).
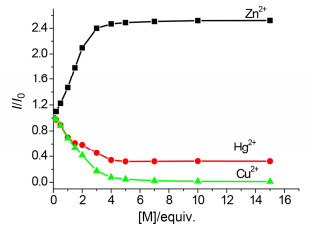
本文同时研究了受体2中分别滴加Zn2+, Cu2+与Hg2+时荧光光谱进行测定 (图 3), 其一些络合参数列于表 1. 2可与Zn2+, Cu2+与Hg2+形成稳定的1:1型络合物, 可通过荧光Job曲线证实.从图 3及表 1的数据可以发现, 2与Zn2+, Cu2+与Hg2+的络合常数分别为6.73×103, 1.40×104与1.97×103 L·mol-1, 荧光检测限分别为8.4×10-7, 4.1×10-7和1.2×10-5 mol/L, 表明2对这些离子荧光识别能力顺序为Cu2+>Zn2+>Hg2+.同时根据滴定数据可发现, 虽然环受体1较非环受体2有更好的荧光识别选择性, 而其荧光识别灵敏性却有很大的减弱, 就可能归因于受体分子1中大的刚性环结构, 使得其不能同时与1中的N, O配位原子发生强的配位键合.
1/ 2-M2+ Binding constant Limit of detection Saturated equivalent/equiv. 1-Hg2+
2-Zn2+
2-Hg2+
2-Cu2+2.03×103
6.73×103
1.40×104
1.97×1033.52×10-4
8.4×10-7
4.1×10-7
1.2×10-5250
5
5
5表 1 受体分子1/2与不同金属离子络合参数
Table 1. The binding parameters between 1/2 and metal ions笔者同时测定了受体环状1在其他竞争性金属离子存在时对Hg2+的荧光响应.从图 4可看出, 在其他金属离子存在时, 受体1对Hg2+仍然有很好的识别能力, 可用于Hg2+选择性识别的荧光探针.同时, 探针1在不同pH值时对Hg2+也进行了探讨, 受体分子在pH值4~9范围内对Hg2+都有很好的识别能力.
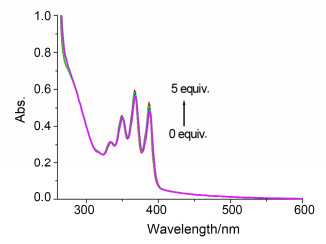
文章同时测定1/2中滴加不同金属离子时紫外光谱变化.不同于荧光光谱, 滴加Zn2+, Hg2+, Cu2+及其他金属离子时, 受体分子1/2的吸收光谱变化不大 (图 5), 表明受体分子与金属络合后对其基态电子光谱影响并不大.
1.3 识别机理研究
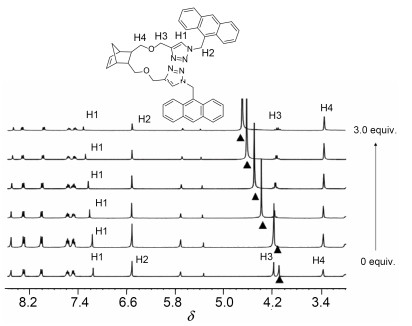
受体分子1/2对金属离子荧光响应可归因于受体分子中O及N原子与金属离子配位的结果.由于1的溶解性差, 本文以2为例通过1H NMR滴定来证实这一设想. 图 6为在CD3CN/CDCl3 (V:V=8:2) 溶液中受体分子2中滴加不同当量Hg2+时1H NMR变化图.随着Hg2+的加入, 受体分子三唑环上的氢H (1) 化学位移发生了从δ7.17到7.32的低场移动 (加入3 equiv. Hg2+), 同时烷氧键邻位亚甲基上的质子H (3) 发生了高场移动 (Δδ=0.05) 及从单峰裂分为四重峰的变化.这表明受体分子中O及N原子可能发生了金属离子配位.
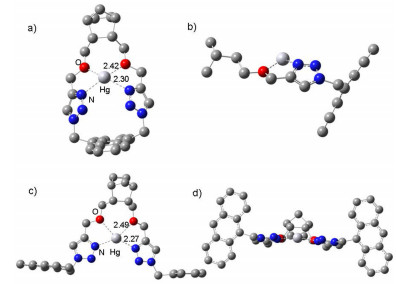
DFT计算结果也进一步证明了受体分子中N及O原子参与金属配位的合理性.配合物1-Hg2+与2-Hg2+的DFT计算最优构型见图 7.从图中看出, 受体分子1与2中的三唑环上的3-位N原子及醚氧键中的O原子与中心原子Hg2+参与了的配位.从键长数据可看出, 两受体分子中N原子的配位能力强于O原子.同时从图中还可看出, 虽然1与2中配位原子与中心离子配位键长相差不大, 但1-Hg2+中金属离子Hg2+位于环的侧面 (图 7b), 2-Hg2+则位于受体分子平面腔孔中.这种侧面配位 (1-Hg2+) 与平面配位差异可解释受体1较2更弱的与Hg2+络合能力结果.
2 结论
通过点击反应合成了一种以降冰片烯为骨架含蒽荧光团非环及环状双三唑化合物1和2, 并研究了其对金属离子荧光识别能力.在CH3CN-H2O (V:V=90:10) 中, 荧光光谱表明环受体1仅对Hg2+有荧光淬灭响应, 而2对Zn2+, Hg2+与Cu2+都有很好的荧光识别能力, 其荧光识别能力顺序为Cu2+>Zn2+>Hg2+.同时研究发现虽然1较2具有更好的金属离子识别选择性, 但其荧光识别灵敏度有很大减弱. 1H NMR滴定及DFT计算表明受体分子受体分子中的三唑环上的3位N原子及醚氧基团中的O原子参与了金属配位.同时DFT计算表明非环受体2较1有更好同Hg2+尺寸匹配, 导致其有更好的离子识别灵敏性.目前虽然大量文献报道环状受体分子由于好的预组织性及刚性结构较非环受体有更好的客体分子选择性与灵敏性识别[32], 本文的结果表明主客体间空间尺寸匹配性常有更大的影响.本文的研究为设计高选择性与灵敏度的环状受体具有一定的参考价值.
3 实验部分
3.1 仪器与试剂
化合物3, 4和5按文献方法合成, 其它试剂及药品 (分析纯) 购于国药集团化学试剂公司; 无水溶剂按文献方法纯化制备, 其他试剂均为分析纯, 使用前未作进一步纯化.
核磁共振仪 (德国Bruker公司, Bruker Vance 400 MHz, TMS为内标)、紫外可见光谱 (HITACHI U-3010型紫外可见分光光度计)、荧光光谱 (Hitachi F-4600型荧光光谱仪).滴定所用金属离子Na+, Mg2+, Ba2+, Hg2+, Cu2+, Cr3+, Zn2+, Fe2+, Ni2+, Co2+, Cd2+, Ag+等) 均为高氯酸盐.
3.2 实验方法
3.3 紫外及荧光光谱滴定实验
紫外及荧光光谱测定受体分子浓度为2×10-5 mol/ L乙腈-水 (V:V=90:10) 溶液, 金属离子配制成2× 10-3 mol/L溶液.荧光光谱测定时激发波长为360 nm.测试时用移液枪向1和2中滴加高氯酸盐的阳离子, 观察受体分子与阳离子结合后紫外及荧光光谱变化.
3.4 1H NMR滴定测试
Bruker Vance 400 MHz核磁共振仪, CD3CN溶液中化合物2 (2.0×10-4 mol/L) 中利用累积滴加法逐次加入高氯酸盐的阳离子, 观察受体分子2与Hg2+结合后活泼氢化学位移的变化.
3.5 量子化学结构计算
采用高斯09的B3LYP/6-31G*(d, p) 方法, 计算目标化合物1, 2与阳离子作用后的结构模型.
辅助材料 (Supporting Information) 化合物1和2与金属离子的紫外光谱图, 1H NMR、13C NMR及ESI-MS.这些材料可以免费从本刊网站 (http://sioc-journal.cn/) 上下载.
3.2.1 (14Z, 54Z, 91R, 93S, 94S)-11H, 51H-7, 11-二氧-1, 5 (1, 4)-二三唑-3(9, 10)-蒽-9(2, 3)-二环[2.2.1]庚烷环二十烷-95-烯 (1) 的合成
在氮气保护下, 将1.5 mL的1, 8-二氮杂二环[5.4.0]十一碳-7-烯 (DBU, 10 mmol) 及28.5 mg CuI (0.015 mmol) 加入到200 ml除水甲苯中, 并将溶液升温至70 ℃.同时化合物3 (115 mg, 0.5 mmol) 和4 (144 mg, 0.5 mmol) 溶于100 mL除水甲苯中, 并缓慢滴加到上述溶液.滴加约8 h, 滴加完毕后, 继续反应2 h.减压蒸馏除去溶剂, 残留物用CH2Cl2/MeOH (V:V=98:2) 过柱, 得到102 mg (0.18 mmol) 白色固体1, 收率39%. m.p. 198~199 ℃; 1H NMR (400 MHz, DMSO-d6)δ: 8.77 (s, 2H), 8.44 (s, 2H), 7.74 (s, 2H), 7.59 (s, 2H), 7.02 (s, 2H), 6.77 (q, J=15.4 Hz, 3H), 5.73 (s, 1H), 4.46 (d, J=13.8 Hz, 2H), 4.27 (s, 2H), 3.90 (d, J=13.3 Hz, 2H), 2.35 (s, 2H), 1.91 (s, 2H), 1.61 (s, 2H), 1.21 (s, 2H), 0.94 (s, 1H), 0.86 (s, 1H); 13C NMR (101 MHz, DMSO-d6) δ: 143.6, 134.5, 130.7, 130.17, 128.6, 127.6, 125.2, 124.8, 123.3, 67.1, 62.8, 45.7, 44.4, 40.5, 40.1, 39.9, 39.8, 39.5, 39.3~38.9 (m); ESI-MS m/z: 520.25 (M+1)+. Anal. calcd for C31H30N6O2: C 71.79, H 5.83, N 16.20; found C 71.65, H 5.85, N 16.32.
3.2.2 (1R, 4S, 5R)-5, 6-二{{[1-(蒽-9-亚甲基)-1H-1, 2, 3-三唑-4-亚]甲氧基}甲基}二环[2.2.1]庚烷-2-烯 (2) 的合成
在氮气保护下, 将115 mg (0.5 mmol) 化合物3、280 mg (1.2 mmol) 化合物5、25 mg五水硫酸铜、20 mg抗坏血酸钠溶于10 mL DMF中, 反应混合液室温下反应4 h.待反应结束后, 在反应液中加入氯化钠水溶液, 过滤, 取滤渣.干燥后粗产物用二氯甲烷-甲醇的混合液体 (V:V=98:2) 过柱, 减压蒸馏, 得到284 mg白色固体2, 产率80%. m.p. 145~146 ℃; 1H NMR (400 MHz, CDCl3) δ: 8.51 (s, 2H), 8.31 (d, J=8.8 Hz, 4H), 8.01 (d, J=8.0 Hz, 4H), 7.59~7.56 (m, 4H), 7.50~7.46 (m, 4H), 7.10 (s, 2H), 6.51 (s, 4H), 5.73 (s, 2H), 5.30 (s, 2H), 4.25~4.18 (m, 4H), 4.25~4.18 (m, 4H), 3.03 (t, J=13.2 Hz, 2H), 2.81 (t, J=15.4 Hz, 2H), 2.66 (s, 2H), 2.18 (s, 4H), 1.61~1.58 (m, 1H), 1.27 (d, J=16.2 Hz, 1H); 13C NMR (100 MHz, CDCl3) δ: 31.0, 41.2, 45.3, 46.3, 48.8, 53.5, 64.1, 70.5, 122.0, 123.0, 123.8, 125.4, 127.6, 129.4, 129.8, 129.8, 130.8, 131.4, 135.0, 145.3; ESI-MS m/z: 698.22 (M+1)+. Anal. calcd for C45H40N6O2: C 77.56, H 5.79, N 12.06; found C 77.72, H 5.83, N 12.14.
-
-
[1]
Masayuki, M.; Michael, M.; Peter, W.; Richard, A.; Kim, D. Org. Lett. 2005, 7, 4943. doi: 10.1021/ol051919w
-
[2]
Kallol, B.; Anand, K.; Moupriya, N.; Soumen, B. Anal. Chem. 2014, 86, 2740. doi: 10.1021/ac404160v
-
[3]
Zhang, X.; Guo, C.; Li, Z.; Shen, G.; Yu, R. Anal. Chem. 2002, 74, 821. doi: 10.1021/ac0109218
-
[4]
Seraphine, V.; Hasan, A.; Murat, S.; Jun, Y.; Chuan, H. J. Am. Chem. Soc. 2010, 132, 2567 doi: 10.1021/ja9097324
-
[5]
Wu, L.; Guo, Q.; Liu, Y.; Sun, Q. Anal. Chem. 2015, 87, 5318. doi: 10.1021/acs.analchem.5b00514
-
[6]
Koushik, G.; Sudipto, D.; Shibashis, H.; Aradhita, B.; Corrado, R.; Partha, R. J. Mol. Struct. 2016, 325, 1118.
-
[7]
Mehdi, A.; Roghayeh, S.; Soraia, M. Sens. Actuators, B 2016, 233, 355. doi: 10.1016/j.snb.2016.04.077
-
[8]
Ding, Y.; Zhu, W.-H.; Xie, Y. Chem. Rev. 2017, 117, 2203. doi: 10.1021/acs.chemrev.6b00021
-
[9]
Ding, Y.; Li, X.; Li, T.; Zhu, W.; Xie, Y. J. Org. Chem. 2013, 78, 5328. doi: 10.1021/jo400454e
-
[10]
Xie, Y.; Wei, P.; Li, X.; Hong, T.; Zhang, K.; Furuta, H. J. Am. Chem. Soc. 2013, 135, 19119. doi: 10.1021/ja4112644
-
[11]
Ding, Y.; Tang, Y.; Zhu, W.; Xie, Y. Chem. Soc. Rev. 2015, 44, 1101. doi: 10.1039/C4CS00436A
-
[12]
Tang, Y.; Ding, Y.; Li, X.; Ågren, H.; Li, T.; Zhang, W.; Xie, Y. Sen. Actuators, B 2015, 206, 291. doi: 10.1016/j.snb.2014.09.060
-
[13]
Martınez-Manez, R.; Sancenon, F. Chem. Rev. 2003, 103, 4419. doi: 10.1021/cr010421e
-
[14]
Kolb, H.; Finn, M.; Sharpless, B. Angew. Chem., Int. Ed. 2001, 40, 2004. doi: 10.1002/(ISSN)1521-3773
-
[15]
Lau, Y. H.; Rutledge, P. J.; Watkinson, M.; Todd, M. H. Chem. Soc. Rev. 2011, 40, 2848. doi: 10.1039/c0cs00143k
-
[16]
Ge, J.; Liu, Z.; Cao, Q.; Chen, Y; Zhu, J. Chem. Asian J. 2016, 11, 687. doi: 10.1002/asia.v11.5
-
[17]
Dai, B.; Cao, Q.; Wang, L.; Wang, Z.; Yang, Z. Inorg. Chim. Acta 2014, 423, 163. doi: 10.1016/j.ica.2014.08.015
-
[18]
Zhu, J.; Fan, X.; Cao, Q. Inorg. Chim. Acta 2016, 451, 111. doi: 10.1016/j.ica.2016.07.021
-
[19]
Wang, Z; Palacios, M.; Pavel, A. Anal. Chem. 2008, 80, 7451. doi: 10.1021/ac801165v
-
[20]
Wu, Y.; Tan, Y.; Wu, J.; Chen, S.; Chen, Y.; Zhou, X.; Jiang, Y.; Tan, C. ACS Appl. Mater. Interfaces 2015, 7, 6882. doi: 10.1021/acsami.5b00587
-
[21]
王智成, 戴博娜, 丘继芳, 曹迁永, 葛金柱, 有机化学, 2015, 35, 2383. doi: 10.6023/cjoc201506021Wang, Z.; Dai, B.; Qiu, J.; Cao, Q.; Ge, J. Chin. J. Org. Chem. 2015, 35, 2383 (in Chinese). doi: 10.6023/cjoc201506021
-
[22]
Emiliano, T.; Arna, K.; Lisa, M.; Matthew H. T.; Michael, W. Inorg. Chem. 2009, 48, 319. doi: 10.1021/ic8017634
-
[23]
Sui, B.; Kim, B.; Zhang, Y.; Frazer, A.; Belfield, K. ACS Appl. Mater. Inter. 2013, 5, 2920. doi: 10.1021/am400588w
-
[24]
Maity, D.; Govindaraju, T. Inorg. Chem. 2010, 49, 7229. doi: 10.1021/ic1009994
-
[25]
Xu, K.; Chen, Z.; Zhou, L.; Zheng, O.; Wu, X.; Guo, L.; Qiu, B.; Lin, Z.; Chen, G. Anal. Chem. 2015, 87, 816. doi: 10.1021/ac503958r
-
[26]
Banti, D.; North, M. Tetrahedron Lett. 2002, 43, 1561. doi: 10.1016/S0040-4039(02)00009-6
-
[27]
Zhou, L.; Sun, Q. Chem. Commun. 2015, 51, 16767. doi: 10.1039/C5CC07306E
-
[28]
Reuter, R.; Wegner, H. Chem. Commun. 2013, 49, 146. doi: 10.1039/C2CC35974J
-
[29]
Kumari, A.; Swamy, K. J. Org. Chem. 2016, 81, 1425. doi: 10.1021/acs.joc.5b02567
-
[30]
Caricato, M.; Olmo, A.; Gargiulli, C.; Gattuso, G.; Pasini, D. Tetrahedron 2012, 68, 7861. doi: 10.1016/j.tet.2012.07.038
-
[31]
Szejtli, J. Cyclodextrine Technology, Kluwer Academic Publishers, Dodrecht, The Netherlands, 1988.
-
[32]
Hua, Y.; Flood, A. H. Chem. Soc. Rev. 2010, 39, 1262. doi: 10.1039/b818033b
-
[1]
-
图 1 在CH3CN-H2O (V:V=90:10) 溶液中化合物1(a) 与2(b) 中滴加等量 (1为20 equiv., 2为5 equiv.) 不同金属离子荧光光谱变化图
Figure 1 Fluorescence spectra of 1(a) and 2(b) upon addition equiv. (20 equiv. for 1 and 5 equiv. for2) of metal ions in CH3CN-H2O (V:V=90:10) solution
c=2.0×10-5 mol/L, λex=360 nm. Inset: the bar graph of 1 at 423 nm or2 at 415 nm upon addition of various metal ions
表 1 受体分子1/2与不同金属离子络合参数
Table 1. The binding parameters between 1/2 and metal ions
1/ 2-M2+ Binding constant Limit of detection Saturated equivalent/equiv. 1-Hg2+
2-Zn2+
2-Hg2+
2-Cu2+2.03×103
6.73×103
1.40×104
1.97×1033.52×10-4
8.4×10-7
4.1×10-7
1.2×10-5250
5
5
5 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 5
- 文章访问数: 2147
- HTML全文浏览量: 172


 下载:
下载:







 下载:
下载:

