 图 1
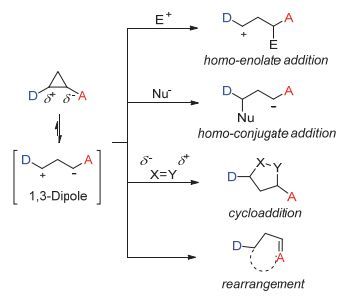
D-A环丙烷的反应性能
Figure 1.
Reactivity of D-A cyclopropanes.
图 1
D-A环丙烷的反应性能
Figure 1.
Reactivity of D-A cyclopropanes.

Citation: Yan Wen-Guang, Wang Pan, Wang Lijia, Sun Xiu-Li, Tang Yong. Copper Catalyzed[3+2] Annulation of Indoles with 1, 1, 2, 2-Tetrasubstituted Donor-Acceptor Cyclopropanes[J]. Acta Chimica Sinica, 2017, 75(8): 783-787. doi: 10.6023/A17040146

铜(Ⅱ)催化的吲哚与四取代D-A环丙烷[3+2]开环/环化反应
English
Copper Catalyzed[3+2] Annulation of Indoles with 1, 1, 2, 2-Tetrasubstituted Donor-Acceptor Cyclopropanes
-
Key words:
- Donor-Acceptor (D-A) cyclopropane
- / indole
- / annulation
- / quaternary center
- / bis-oxazoline
-
1 引言
Donor-Acceptor环丙烷(D-A环丙烷)是一类最小的饱和碳环, 由于其邻位供电子和拉电子基团之间的“推-拉”作用, 在Lewis酸的活化作用下, 可以形成1, 3-两性离子中间体, 发生多种形式的反应, 例如接受亲核试剂、亲电试剂的进攻, 与不饱和化合物发生[3+2]形式环加成反应, 重排反应等(图 1) [1].最重要的是, D-A环丙烷可以通过[3+n]环加成反应来构建多元碳(杂)环、并环结构, 使其成为有机反应中一类重要的合成砌块, 被广泛应用于天然产物的合成中[2].
近年来, 基于1, 1-偕二酯基-2位单取代的D-A环丙烷的合成方法学取得了飞速的发展, 为环状和杂环化合物的合成提供了一条简单、高效的合成途径, 但对于推电子基团位点双取代的D-A环丙烷(四取代D-A环丙烷)可能因位阻较大而研究较少[3b, 3p, 4].该类四取代的环丙烷与亲核试剂的开环反应, 可以产生新的季碳中心, 为季碳中心的构建提供新的途径.
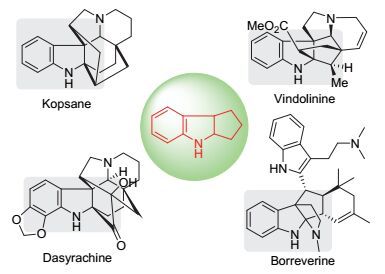
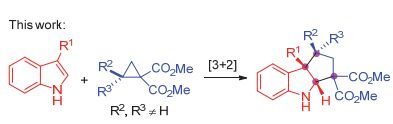
吲哚并五元碳环结构是一类非常重要生物碱的核心结构单元, 广泛存在于多种天然产物中[5](图 2).发展原子经济性好、催化的、立体选择性的方法来构建此类结构骨架一直受到合成化学家们的关注, 而通过吲哚与环丙烷开环/环化的策略具有简捷高效的特点[6].我们在D-A环丙烷的反应研究中, 实现了2-取代-1, 1-双酯基D-A环丙烷与吲哚的不对称[3+2]环加成反应, 以最高98%的产率, 大于50/1 dr和96% ee得到吲哚并五元碳环结构骨架的化合物[3f].在此研究基础上, 我们对吲哚与2, 2-二取代-1, 1-双酯基D-A环丙烷的[3+2]开环/环化反应进行了探索, 实现了一步构建吲哚并五元碳环结构, 在新形成的五元环上构建三个季碳中心(图 3).本文将报道初步的研究结果.
2 结果与讨论
2.1 反应条件优化
2.1.1 反应溶剂及四取代D-A环丙烷酯基大小对反应的影响
首先我们以N-苄基3-甲基吲哚(1a)和2, 2-二取代-1, 1-双酯基D-A环丙烷2为模板底物进行了反应条件的优化.在该反应中, 由于吲哚对环丙烷的傅-克开环反应为主要副产物, 且存在环丙烷自身开环聚合的副反应, 因此目标产物的产率较低.为了抑制副反应, 提高目标产物的产率和非对映选择性, 我们在进行了一系列初步尝试后, 选用较好的六氟锑酸铜为Lewis酸, 研究了反应的溶剂及四取代D-A环丙烷上酯基的大小对反应的影响(表 1).

Entrya R Solvent Time/h Conv.b/% Yieldc/% drd 1 Me DCM 19 >99 60 64/36 2 Me DCE 24 80 32 57/43 3 Me CHCl3 15 80 36 67/33 4 Me THF 20 >99 13 50/50 5 Me PhCH3 22 >99 46 63/37 6 Me PhCl 20 >99 61 62/38 7 Me CH3CN 22 38 trace — 8 Me CH3NO2 19 >99 29 66/34 9 Bn DCM 22 >99 68 67/33 10 CH2t-Bu DCM 24 >99 20 80/20 11 CH2CF3 DCM 21 91 79 70/30 12e CH2CF3 DCM 21 97 89 70/30 13e, f CH2CF3 DCM 21 >99 32 90/10 
aReaction conditions: 1a (0.30 mmol), 2 (0.20 mmol), CuBr2 (0.02 mmol), AgSbF6 (0.04 mmol), in 2.0 mL of solvent at room temperature under N2 atmosphere. bDetermined by 1H NMR spectroscopy of the crude reaction mixture with 1, 1, 2, 2-tetrachloroethane as internal standard. cIsolated yield. dThe diastereomeric ratio (dr) was determined by 1H NMR spectroscopy of the crude reaction mixture. eThe reaction was carried out at 0 ℃; f L was used as the ligand, M/L=1/1.2. 当使用二氯甲烷为溶剂时, 能取得60%的产率, dr值为64/36(表 1, Entry 1);使用1, 2-二氯乙烷和氯仿时, 反应的产率都明显降低, 但在氯仿中能取得67/33的dr值(Entries 2, 3);使用四氢呋喃时, 产率仅为13%, dr值仅为50/50 (Entry 4);使用甲苯时, 产率也并不理想(Entry 5);而当使用氯苯为反应溶剂时, 能取得61%的产率, 但非对映选择性相对于二氯甲烷为溶剂时略有降低(Entry 6);使用乙腈时, 反应速率太慢, 环丙烷转化率较低, 只有少量产物生成(Entry 7);使用硝基甲烷时, 产率也不理想(Entry 8).通过以上反应溶剂的研究确定卤代烷类溶剂二氯甲烷效果最好.
随后对环丙烷上的酯基进行了考察.将环丙烷上的酯基由甲酯换成苄酯时, 反应产率和非对映选择性都略有提高(Entry 9);当变为新戊酯时, 尽管能取得80/20的dr值, 但产率仅为20% (Entry 10);当使用三氟乙酯时, 反应的活性大幅度提高, 能取得79%的产率, 70/30的dr值(Entry 11).在使用三氟乙酯的环丙烷时, 通过进一步降低反应温度使傅-克反应得到进一步抑制, 反应产率可以提高至89%, dr值依然保持在70/30 (Entry 12);在加入消旋双噁唑啉配体L[7]后, 尽管只能取得32%的产率, 但能取得最好90/10的dr值(Entry 13).在此研究的基础上, 我们希望能够在保持较好的非对映选择性条件下, 通过改变吲哚上的保护基来提高产物的产率和选择性, 并抑制副产物的生成.
2.1.2 吲哚上不同保护基对反应的影响
当吲哚N上取代基由苄基变为甲基时, 在粗产物的NMR谱图中观察不到傅-克烷基化副产物, 反应的产率提高至76%, dr值保持在90/10(表 2, Entry 1 vs. 2).使用甲基保护的吲哚, 提高其用量至2当量时, 反应的产率也可提高到79%, dr值提高到91/9 (Entry 3);如果使用不带保护基的吲哚, 反应产率和dr值都不太理想(Entry 4).

Entrya R1 Conv.b/% Yieldc/% drd 1 Bn (1a) >99 32 90/10 2 Me (1b) >99 76 90/10 3e Me (1b) >99 79 91/9 4 H (1c) >99 65 70/30 aReaction conditions: 1/2=1.5/1, 1 (0.30 mmol), 2 (0.20 mmol), CuBr2 (0.02 mmol), AgSbF6 (0.04 mmol), L (0.024 mmol), in 2.0 mL of DCM at 0 ℃ under N2 atmosphere. bDetermined by 1H NMR spectroscopy of the crude reaction mixture with 1, 1, 2, 2-tetrachloroethane as internal standard.cIsolated yield. dThe diastereomeric ratio (dr) was determined by 1H NMR spectroscopy of the crude reaction mixture. e 1/2=2/1. 2.2 底物普适性研究
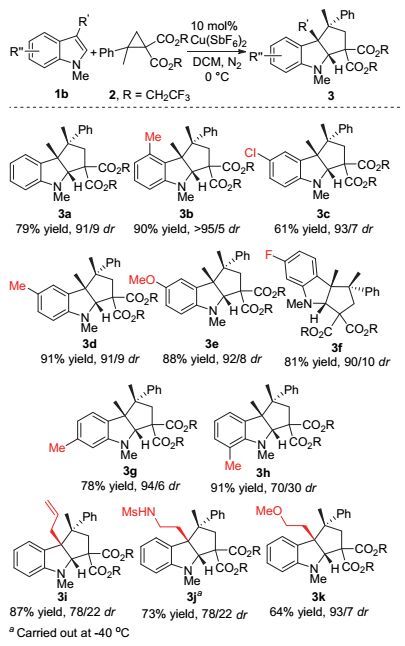
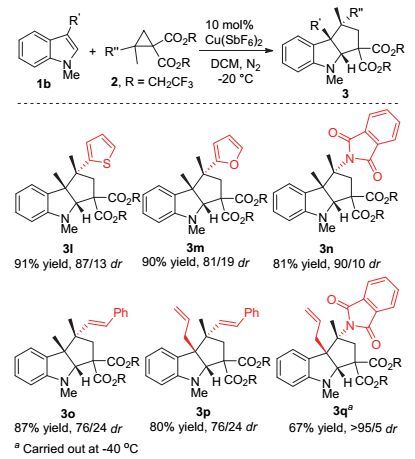
通过对反应条件的详细优化, 确定了吲哚与四取代D-A环丙烷[3+2]开环/环化反应的最优条件, 使用酯基为三氟乙酯的四取代D-A环丙烷, 现场生成的10 mol% Cu (SbF6)2/L为催化剂, 二氯甲烷为溶剂, 0 ℃条件下反应.在此最优条件下, 对底物普适性进行了研究.
首先, 对吲哚底物进行了普适性研究(图 4).相较于吲哚, 4-Me吲哚底物(3b)反应活性增加, dr值提高到大于95/5;当在吲哚5位引入氯时, 反应也能很好的进行(3c); 当在吲哚底物5位引入供电子基团5-Me, 5-OMe时, 反应速率加快, 可以取得优秀的产率和非对映选择性(3d, 3e); 当在吲哚6位引入吸电子、给电子基团时, 反应也能顺利进行(3f, 3g); 而当使用7-Me吲哚时, 可能由于反应过程中两个非对映异构体能垒相差不大, 非对映选择性降低, dr值仅为70/30 (3h).对于吲哚3位烯丙基取代的底物, 能够取得87%的产率, 78/22的dr值(3i); 色胺类底物在-40 ℃反应时, 能取得73%的产率, 78/22的dr值(3j); 保护的色醇类底物也能很好的适应该反应, 取得64%的产率和93/7的dr值(3k).
在完成了对吲哚底物普适性研究后, 接下来对不同取代的D-A环丙烷的普适性也进行了研究(图 5).这类富电子的四取代D-A环丙烷反应活性较高, 在0 ℃反应时副产物较多, 为了抑制副反应, 提高目标产物的产率, 将反应温度降低至-20~-40 ℃.对于噻吩基、呋喃基取代的D-A环丙烷, 反应都能非常顺利进行, 取得优秀的产率和中等的非对映选择性(3l, 3m); 对于邻苯二甲酰胺取代的环丙烷, 反应也能取得优秀的产率和非对映选择性(3n); 对于肉桂基取代的环丙烷, 也能取得87%的产率和76/24的dr值(3o); 同时吲哚三位烯丙基取代的吲哚底物(3p, 3q)都能与此类富电子环丙烷反应, 其中产物3q能取得>95/5的dr值.
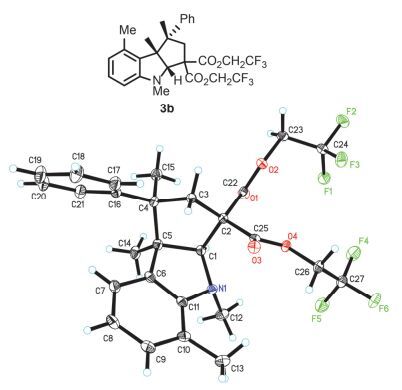
2.3 产物的单晶结构及相对构型的确定
为了确定产物的相对构型, 我们培养了产物3b的主要异构体的单晶.利用X射线单晶衍射的方法确定了产物的相对构型.单晶分析结果显示, 吲哚3位的甲基与2位的氢处于同侧(图 6).
3 结论
我们利用Cu (Ⅱ)/BOX作催化剂, 首次实现了吲哚与四取代D-A环丙烷的[3+2]环加成反应, 对芳环上含有不同取代基的吲哚、色胺、色醇和各类四取代D-A环丙烷, 都能以优秀的产率和中等到优秀的非对映选择性得到四氢吲哚的衍生物.该策略可以简单、高效、原子经济性地构建吲哚并五元碳环结构骨架, 在五元环上一次性地引入三个季碳中心, 为相关天然产物核心骨架的构建提供了新的方法.
-
-
[1]
For reviews on the transformations of D-A cyclopropanes, see: (a) Reissig, H.-U.; Zimmer, R. Chem. Rev. 2003, 103, 1151; (b) Yu, M.; Pagenkopf, B. L. Tetrahedron 2005, 61, 321; (c) Rubin, M.; Rubina, M.; Gevorgyan, V. Chem. Rev. 2007, 107, 3117; (d) Carson, C. A.; Kerr, M. A. Chem. Soc. Rev. 2009, 38, 3051; (e) Cavitt, M. A.; Phun, L. H.; France, S. Chem. Soc. Rev. 2014, 43, 804; (f) de Nanteuil, F.; De Simone, F.; Frei, R.; Benfatti, F.; Serrano, E.; Waser, J. Chem. Commun. 2014, 50, 10912; (g) Liao, S.; Sun, X.-L.; Tang, Y. Acc. Chem. Res. 2014, 47, 2260; (h) Schneider, T. F.; Kaschel, J.; Werz, D. B. Angew. Chem., Int. Ed. 2014, 53, 5504; (i) Grover, H. K.; Emmett, M. R.; Kerr, M. A. Org. Biomol. Chem. 2015, 13, 655. (j) Wang, Y.; Yu, Z.-X. Acc. Chem. Res. 2015, 48, 2288.
-
[2]
For selected examples, see: (a) Meyers, C.; Carreira, E. M. Angew. Chem., Int. Ed. 2003, 42, 694; (b) Carson, C. A.; Kerr, M. A. Angew. Chem., Int. Ed. 2006, 45, 6560; (c) Young, I. S.; Kerr, M. A. J. Am. Soc. Chem. 2007, 129, 1465; (d) Leduc, A. B.; Kerr, M. A. Angew. Chem., Int. Ed. 2008, 47, 7945; (e) Morales, C. L.; Pagenkopf, B. L. Org. Lett. 2008, 10, 157. (f) Campbell, M. J.; Johnson, J. S. J. Am. Soc. Chem. 2009, 131, 10370; (g) Karadeolian, A.; Kerr, M. A. Angew. Chem., Int. Ed. 2010, 49, 1133; (h) Han, Y.; Fu, Q.; Tang, W.; Yan, C. Chin. J. Chem. 2012, 30, 1867.
-
[3]
For recent selected examples, see: (a) Grover, H. K.; Emmett, M. R.; Kerr, M. A. Org. Lett. 2013, 15, 4838; (b) Haubenreisser, S.; Hensenne, P.; Schröder, S.; Niggemann, M. Org. Lett. 2013, 15, 2262; (c) Miyake, Y.; Endo, S.; Moriyama, T.; Sakata, K.; Nishibayashi, Y. Angew. Chem., Int. Ed. 2013, 52, 1758; (d) Ryabchuk, P.; Edwards, A.; Gerasimchuk, N.; Rubina, M.; Rubin, M. Org. Lett. 2013, 15, 6010; (e) Wales, S. M.; Walker, M. M.; Johnson, J. S. Org. Lett. 2013, 15, 2558; (f) Xiong, H.; Xu, H.; Liao, S.; Xie, Z.; Tang, Y. J. Am. Soc. Chem. 2013, 135, 7851; (g) Zhou, Y.-Y.; Li, J.; Ling, L.; Liao, S.-H.; Sun, X.-L.; Li, Y.-X.; Wang, L.-J.; Tang, Y. Angew. Chem., Int. Ed. 2013, 52, 1452; (h) Chakrabarty, S.; Chatterjee, I.; Wibbeling, B.; Daniliuc, C. G.; Studer, A. Angew. Chem., Int. Ed. 2014, 53, 5964; (i) de Nanteuil, F.; Serrano, E.; Perrotta, D.; Waser, J. J. Am. Soc. Chem. 2014, 136, 6239; (j) Garve, L. K. B.; Barkawitz, P.; Jones, P. G.; Werz, D. B. Org. Lett. 2014, 16, 5804; (k) Hashimoto, T.; Kawamata, Y.; Maruoka, K. Nat. Chem. 2014, 6, 702; (l) Lin, S.; Li, L.; Liang, F.; Liu, Q. Chem. Commun. 2014, 50, 10491; (m) Novikov, R. A.; Tarasova, A. V.; Korolev, V. A.; Timofeev, V. P.; Tomilov, Y. V. Angew. Chem., Int. Ed. 2014, 53, 3187; (n) Talukdar, R.; Tiwari, D. P.; Saha, A.; Ghorai, M. K. Org. Lett. 2014, 16, 3954; (o) Zhang, H.-H.; Luo, Y.-C.; Wang, H.-P.; Chen, W.; Xu, P.-F. Org. Lett. 2014, 16, 4896; (p) Kang, Q.-K.; Wang, L.; Zheng, Z.-B; Li, J.-F.; Tang, Y. Chin. J. Chem. 2014, 32, 669; (q) Liu, H.; Zheng, C.; You, S.-L. Chin. J. Chem. 2014, 32, 709; (r) Chen, H.; Zhang, J.; Wang, D. Z. Org. Lett. 2015, 17, 2098; (s) Rakhmankulov, E. R.; Ivanov, K. L.; Budynina, E. M.; Ivanova, O. A.; Chagarovskiy, A. O.; Skvortsov, D. A.; Latyshev, G. V.; Trushkov, I. V.; Melnikov, M. Y. Org. Lett. 2015, 17, 770; (t) Xia, Y.; Liu, X.; Zheng, H.; Lin, L.; Feng, X. Angew. Chem., Int. Ed. 2015, 54, 227; (u) Xu, H.; Hu, J.-L.; Wang, L.; Liao, S.; Tang, Y. J. Am. Soc. Chem. 2015, 137, 8006; (v) Wang, L.-N.; Cui, Q.; Yu, Z.-X. J. Org. Chem. 2016, 81, 10165; (w) Bose, S.; Yang, J.; Yu, Z.-X. J. Org. Chem. 2016, 81, 6757; (x) Liu, C.-H.; Yu, Z.-X. Org. Biomol. Chem. 2016, 14, 5945; (y) Liu, C.-H.; Zhuang, Z.; Bose, S.; Yu, Z.-X. Tetrahedron 2016, 72, 2752.
-
[4]
For examples on transformations of 1, 1, 2, 2-tetrasubstituted Donor-Acceptor Cyclopropanes, see: (a) Sibi, M. P.; Ma, Z.; Jasperse, C. P. J. Am. Chem. Soc. 2005, 127, 5764; (b) Carson, C. A.; Kerr, M. A. Org. Lett. 2009, 11, 777; (c) Sherry, B. D.; Furstner, A. Chem. Commun. 2009, 7116; (d) Xing, S.; Pan, W.; Liu, C.; Ren, J.; Wang, Z. Angew. Chem., Int. Ed. 2010, 49, 3215; (e) Smith, A. G.; Slade, M. C.; Johnson, J. S. Org. Lett. 2011, 13, 1996; (f) Yu, Q.; Ma, S. Chem. Commun. 2012, 48, 11784; (g) Wenz, D. R.; Read de Alaniz, J. Org. Lett. 2013, 15, 3250; (h) Zhu, W.; Fang, J.; Liu, Y.; Ren, J.; Wang, Z. Angew. Chem., Int. Ed. 2013, 52, 2032; (i) Mackay, W. D.; Fistikci, M.; Carris, R. M.; Johnson, J. S. Org. Lett. 2014, 16, 1626; (j) Shiba, T.; Kuroda, D.; Kurahashi, T.; Matsubara, S. Synlett 2014, 25, 2005.
-
[5]
(a) Dewick, P. M. Medicinal Natural Products: A Biosynthetic Approach, 2nd ed., Wiley, New York, 2002; (b) Fattorusso, E.; Taglialatela Scafati, O. Modern Alkaloids, Wiley-VCH, Weinheim, Germany, 2008.
-
[6]
For selected annulations of indoles with cyclopropanes, see: (a) Harrington, P.; Kerr, M. A. Tetrahedron Lett. 1997, 38, 5949; (b) Kerr, M. A.; Keddy, R. G. Tetrahedron Lett. 1999, 40, 5671; (c) England, D. B.; Kuss, T. D. O.; Keddy, R. G.; Kerr, M. A. J. Org. Chem. 2001, 66, 4704; (d) Bajtos, B.; Yu, M.; Zhao, H.; Pagenkopf, B. L. J. Am. Soc. Chem. 2007, 129, 9631.
-
[7]
For selected examples of using L as ligand: (a) Yasuhara, S.; Sasa, M.; Kusakabe, T.; Takayama, H.; Kimura, M.; Mochida, T.; Kato, K. Angew. Chem., Int. Ed. 2011, 50, 3912; (b) Zhou, J.-L.; Liang, Y.; Deng, C.; Zhou, H.; Wang, Z.; Sun, X.-L.; Zheng, J.-C.; Yu, Z.-X.; Tang, Y. Angew. Chem., Int. Ed. 2011, 50, 7874; (c) Karyakarte, S. D.; Smith, T. P.; Chemler, S. R. J. Org. Chem. 2012, 77, 7755; (d) Miller, Y.; Miao, L.; Hosseini, A. S.; Chemler, S. R. J. Am. Chem. Soc. 2012, 134, 12149; (e) Qu, J.-P.; Liang, Y.; Xu, H.; Sun, X.-L.; Yu, Z.-X.; Tang, Y. Chem.-Eur. J. 2012, 18, 2196; (f) Del Bel, M.; Rovira, A.; Guerrero, C. A. J. Am. Chem. Soc. 2013, 135, 12188.
-
[1]
-
表 1 反应溶剂及四取代D-A环丙烷酯基大小对反应的影响
Table 1. Effects of ester groups in cyclopropane

Entrya R Solvent Time/h Conv.b/% Yieldc/% drd 1 Me DCM 19 >99 60 64/36 2 Me DCE 24 80 32 57/43 3 Me CHCl3 15 80 36 67/33 4 Me THF 20 >99 13 50/50 5 Me PhCH3 22 >99 46 63/37 6 Me PhCl 20 >99 61 62/38 7 Me CH3CN 22 38 trace — 8 Me CH3NO2 19 >99 29 66/34 9 Bn DCM 22 >99 68 67/33 10 CH2t-Bu DCM 24 >99 20 80/20 11 CH2CF3 DCM 21 91 79 70/30 12e CH2CF3 DCM 21 97 89 70/30 13e, f CH2CF3 DCM 21 >99 32 90/10 
aReaction conditions: 1a (0.30 mmol), 2 (0.20 mmol), CuBr2 (0.02 mmol), AgSbF6 (0.04 mmol), in 2.0 mL of solvent at room temperature under N2 atmosphere. bDetermined by 1H NMR spectroscopy of the crude reaction mixture with 1, 1, 2, 2-tetrachloroethane as internal standard. cIsolated yield. dThe diastereomeric ratio (dr) was determined by 1H NMR spectroscopy of the crude reaction mixture. eThe reaction was carried out at 0 ℃; f L was used as the ligand, M/L=1/1.2. 表 2 吲哚上不同保护基对反应的影响
Table 2. Effect of protecting groups on the indole substrate

Entrya R1 Conv.b/% Yieldc/% drd 1 Bn (1a) >99 32 90/10 2 Me (1b) >99 76 90/10 3e Me (1b) >99 79 91/9 4 H (1c) >99 65 70/30 aReaction conditions: 1/2=1.5/1, 1 (0.30 mmol), 2 (0.20 mmol), CuBr2 (0.02 mmol), AgSbF6 (0.04 mmol), L (0.024 mmol), in 2.0 mL of DCM at 0 ℃ under N2 atmosphere. bDetermined by 1H NMR spectroscopy of the crude reaction mixture with 1, 1, 2, 2-tetrachloroethane as internal standard.cIsolated yield. dThe diastereomeric ratio (dr) was determined by 1H NMR spectroscopy of the crude reaction mixture. e 1/2=2/1. -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 16
- 文章访问数: 4585
- HTML全文浏览量: 351


 下载:
下载:





 下载:
下载:

