 图 1
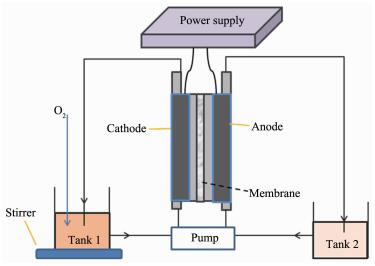
双室电芬顿反应装置图
Figure 1.
Schematic diagram of electro-Fenton in the divided cell
图 1
双室电芬顿反应装置图
Figure 1.
Schematic diagram of electro-Fenton in the divided cell

Citation: LIU Yong, CUI Le-Le, WANG Jia-Cheng, JING Wen-Heng. Transition Metal Oxides Modified Graphite Felt and Its Electrochemical Oxidation Performance[J]. Chinese Journal of Inorganic Chemistry, 2016, 32(9): 1552-1558. doi: 10.11862/CJIC.2016.196

过渡金属氧化物修饰石墨毡阴极及电催化氧化性能测试
English
Transition Metal Oxides Modified Graphite Felt and Its Electrochemical Oxidation Performance
-
Key words:
- graphite felt
- / modification
- / transition metal oxide
- / electro-Fenton
- / cathode
-
0 引言
电芬顿技术利用电化学原位产生H2O2,与溶液中的Fe2+相互作用产生羟基自由基(OH), 其在溶液中具有很强的氧化电势(E0=2.80 V),因此,可以无选择性有效地去除水生环境中难降解、有毒和非生物降解的有机微污染物[1]。电芬顿系统内H2O2的持续生成避免了H2O2异地制备、运输、储存、添加等过程中存在的安全问题,并有效节约了处理成本[2]。近年来,电芬顿方法已在有机合成染料、活性药物成分、有毒有机物质、工业污染物和个人护理产品污染物处理方面取得了显著的进展[3-5]。
电芬顿处理有机废水的反应机理非常复杂,主要描述为以下5个过程[6-7]:
其中,阴极材料的性能直接决定了H2O2的原位生成,进而影响到电芬顿处理有机污染物的能效,因此高性能阴极材料的开发一直是该领域研究的热点。石墨毡因具有较高比表面积,耐腐蚀,抗氧化,良好的机械完整性,强吸附能力,Fe2+的高效再生性等突出优势,而被作为电芬顿中理想的电催化阴极材料。然而,未处理的石墨毡电催化活性并不高。为此研究人员尝试对其表面进行处理,主要方法有化学处理、热处理、等离子体处理等。Gao用芬顿试剂处理石墨毡,增加了石墨毡的含氧集团[8],Wang把KOH处理过的石墨毡用于电芬顿中提高了染料有机废水的处理效果[9],Miao在硫酸中对石墨毡进行电化学修饰,并作为电芬顿的阴极对饮用水进行预处理,取得较好的效果[10],Assumpcao等釆用较低含量的过渡金属Ce的氧化物颗粒修饰碳材料,改善了炭电极的催化活性,显著提高了过氧化氢的产量[11]。但是由于石墨毡表面光滑,且疏水性较强,因此过渡金属氧化物在其表面的负载量通常较低。为此,本文采用H2O2对石墨毡进行了预处理,然后将CeO2负载到其表面,制备出改性石墨毡电极。通过扫描电镜(SEM),X射线衍射仪(XRD),接触角测试仪和循环伏安(CV),电化学阻抗谱(EIS)和线性扫描(LSV)等方法对改性石墨毡进行了表征。并将改性后石墨毡作为阴极,用于电芬顿反应降解染料废水测试。
1 实验部分
1.1 实验材料
本实验所用药品NaCl、FeSO4·7H2O、K3[Fe(CN)6]、CeCl3和Na2SO4·5H2O(国药集团化学试剂有限公司),HCl、H2SO4、KCl、H2O2(上海凌峰化学试剂有限公司),乙醇(99.7%),染料甲基橙MO(天津化学试剂研究所),含碳量99.9%的石墨毡(上海弘竣实业有限公司),纯度为99.5%的氧气(江苏天鸿化工有限公司),TiO2陶瓷膜(孔径5 nm)和双室电芬顿反应器均是实验室自制,实验用水均为去离子水。
1.2 分析测试仪器
UV759型紫外可见分光光度计(上海仪分析仪器有限公司);TOC-VCPH型总有机碳仪(日本岛津有限公司);扫描电子显微电镜(Hitachi S4800);X射线衍射仪(Miniflex 600X,日本理学);电子天平(北京赛多利斯仪器有限公司);电化学工作站Instruments Reference3000(德国GAMRY公司);傅里叶红外光谱仪(Thermo Nicolet 8700,美国);三电极系统(天津艾达恒晟科技发展有限公司)。
1.3 改性石墨毡阴极材料的制备
1.4 改性石墨毡形态表征和电化学测试
通过FTIR分析GF和GF-g官能团的变化,利用SEM(加速电压5.0 kV)和XRD(Cu Kα射线,λ=0.154 18 nm,工作电压40 kV,电流30 mA,扫描范围10°~80°)观察石墨毡改性前后的表面形态,用接触角测试考察电极亲水性的变化。电极的电化学性能测试采用三电极体系进行,工作电极是改性前后石墨毡电极,辅助电极是铂电极,参比电极是Ag/AgCl电极,循环伏安(CV)和电化学阻抗谱(EIS)测试的电解液均为对炭类电极敏感的10 mmol·L-1 K3[Fe(CN)6]和1 mol·L-1 KCl的溶液,线性扫描(LSV)的电解液是pH=3,饱和溶解氧的50 mmol·L-1 Na2SO4溶液:测试结果均是通过电化学工作站得到。所有电化学测试的石墨毡大小均为0.5 cm×0.5 cm×1 cm。
1.5 电芬顿反应降解甲基橙
实验采用的反应器为双室电芬顿反应装置如图 1所示,它由电压系统、氧气供给、蠕动泵、隔膜、电极、搅拌器、阴阳两极电解液储液罐等组成。
阳极电解液:10 mmol·L-1 HCl和50 mmol·L-1 NaCl溶液100 mL[12]。阴极电解液:100 mg·L-1 MO,0.2 mmol·L-1 Fe2+,pH=2的溶液100 mL,采用较低浓度的Fe2+是由于其在电芬顿过程中可以再生,降低了铁离子对水的污染[13]。如方程(5)和(6),实验中采用机械强度好,抗化学腐蚀的陶瓷膜作为隔膜,将反应器的阴阳两室隔开,阻止两极电解液的直接混合, 避免阴极产生的H2O2在阳极发生分解[7]。阴极电极为改性前后的石墨毡电极,阳极为未改性石墨毡电极,施加电压为-1.5 V,阴阳极电解液的流速均为1.7 mL·min-1。为了使阴极溶液达到饱和溶解氧浓度,加入电压前往阴极液贮槽通入纯氧气10 min,转子的搅拌速率为100 r·min-1。MO的浓度通过紫外可见分光光度计在λ=464 nm,反应时间为0、10、20、30、40、50和60 min时测其吸光度。染料废水的TOC在反应时间为0、30、60、90和120 min由TOC分析器测定。实验过程中温度均是室温25 ℃。
1.3.1 石墨毡的成型清洗
将石墨毡切割成厚度为5 mm,半径为10 mm圆片状,把成型石墨毡放在无水水乙醇进行超声清洗,后用去离子水冲洗烘干[10],此时的石墨毡标记为GF。
1.3.3 石墨毡的稀土元素Ce的氧化物修饰
将相同大小GF和GF-g浸泡在5% CeCl3溶液中24 h后再500 ℃下N2气氛炉中煅烧2 h,分别将这2种处理后石墨毡标记为GF-c和GF-gc。
1.3.2 石墨毡的H2O2化学预处理
将清洗烘干的石墨毡在H2O2溶液中恒温80 ℃加热2 h后用去离子水冲洗烘干,将此石墨毡标记为GF-g。
2 结果与讨论
2.1 石墨毡形态表征
2.2 石墨毡电化学性能测试
电芬顿中电极的电化学性能的评价主要有3个指标:电极材料的电荷传输阻力,表面电活性,过氧化氢产生能力[17]。
3.3 改性石墨毡阴极对MO催化氧化
2.1.2 石墨毡的SEM表征
图 3所示改性前后石墨毡的SEM图,从图 2可见,原石墨毡单根碳纤维表面光滑成沟壑状,单根直径约为9 μm,H2O2预处理石墨毡表面变得有些粗糙,主要原因是强氧化性的H2O2对石墨毡有氧化作用,增加了表面含氧基团[14]。由(c)和(d)可知CF-gc表面的纳米颗粒远多于CF-c,可能由于H2O2对石墨毡化学处理之后,刻蚀表面有利于CeO2的沉积负载。
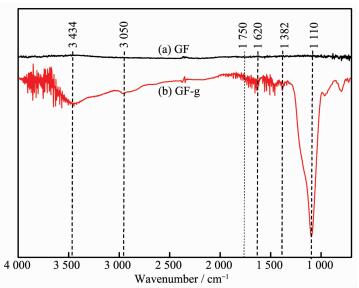
2.1.1 石墨毡的FTIR表征
如图 2所示为H2O2预处理前后石墨毡的红外光谱图,由图 2可知,清洗后石墨毡的FTIR图并没有明显的吸收峰,这是由于石墨毡的石墨化程度较高,几乎没有其他元素存在。而H2O2处理之后的石墨毡出现明显的红外吸收峰,3 434和1 382 cm-1附近为-OH的伸缩振动峰和弯曲振动峰,1 110 cm-1附近为C-O的伸缩振动峰,1 750 cm-1附近为C=O伸缩振动峰,-OH基团(C=C-OH)的拉伸振动峰出现在1 620 cm-1附近,3 050 cm-1附近为的C-H的伸缩振动峰[8]。对比特征峰的峰面积,发现H2O2预处理后石墨毡的含氧基团显著增加。
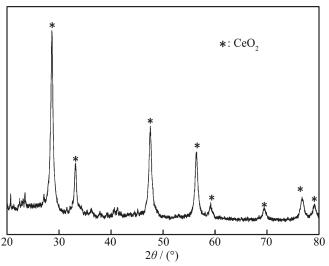
2.1.3 石墨毡的XRD表征
图 4为改性石墨毡的XRD图,由图 4知2θ角在28.5°、33.2°、46.6°、56.2°处出现了明显的XRD衍射峰,属于CeO2特征峰,是典型的“萤石型”单晶相结构,CeO2成功负载在石墨毡的表面。它具有较高的储氧能力,释放氧的能力以及较强的氧化还原性能,石墨毡阴极负载二氧化铈催化剂可以增加局部氧气浓度,而二氧化铈维持局部氧气浓度的主要作用是基于下面的反应[15]:
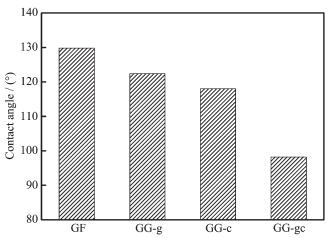
图 5所示为改性前后石墨毡的接触角,用以讨论石墨毡的亲水性变化。从图 5可见,GF、GF-g、GF-c和GF-gc的接触角分别为129°、122°、118°和98°,原石墨毡和处理后的石墨毡均呈疏水性,改性前后石墨毡的亲水性强弱:GF < GF-g < GF-c < GF-gc,由于H2O2的氧化作用增加了材料表面的羟基和羧基(-COH和-COOH),亲水性改善,减少水溶液润湿石墨毡的时间,进而可以提高CeO2在石墨毡表面的负载量。由图 5同样可知,Ce氧化物负载过程也提高了石墨毡的亲水性。对于高度疏水的原石墨毡,提高其表面亲水性可以促进阴极和电解质之间的电子传输和溶解氧的转移,有利于加速电极表面电化学过程,从而电极的电催化性能得到改善[16]。
2.2.2 石墨毡的表面电活性
图 7所示为改性前后的石墨毡电极CV曲线,电解液为含有[Fe(CN)6]3-溶液,铁氰化物系统的循环伏安法是监测电极表面电活性高效简便的方法[20],越大的[Fe(CN)6]3-/[Fe(CN)6]4-氧化还原峰电流密度反应出电极表面越高的电活性[21]。由图可见GF-gc、GF-g和GF-c的氧化还原峰电流密度的大小分别为GF的21.63、8.64和2.88倍。
电极的活性表面积可由Randles-Sevcik方程[17]计算得到
Ip为峰电流,A为工作电极表面积(cm2),C为电活性物质本体的物质的量浓度(mol·cm-3),D为扩散系数(cm-2·s-1),v为扫描速度(V·s-1)。由方程(8)可知电极的表面积与峰电流成正比,得到GF、GF-g、GF-c和GF-gc的表面积分别如表 1,由表 1可知GF-gc的电极活性表面积最大,更适合作为电芬顿的阴极材料。
Graphite felt A/cm2 GF 2.28 GF-g 5.71 GF-c 17.13 GF-gc 49.32 2.2.3 石墨毡的过氧化氢产生能力
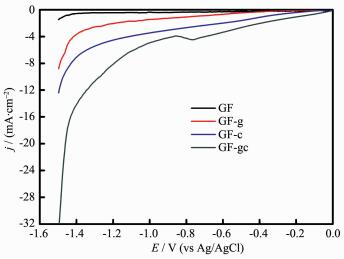
为考察改性石墨毡阴极氧还原(方程1)的电催化活性,对石墨毡进行线性扫描,如图 8为改性前后石墨毡的线性扫描曲线,由图 8可知所有改性石墨毡相对于原石墨毡的氧还原电流响应均有所增强,说明H2O2化学预处理和CeO2修饰均可提高原的催化能力。而且GF-gc在氧还原过程中的电流响应最为强烈。电流响应越强烈,方程(1)就越容易进行,说明溶解氧还原生成过氧化氢的电催化性能越强[17],可能是由于石墨毡负载的氧化铈提高电极表面局部的氧含量,填补了溶解氧沿电解液扩散至电极表面所需的时间,氧还原过程可以持续有效地在电极表面上进行,可以解释GF-gc的氧还原电流响应较强的原因,电极的催化性能显著提高。
2.2.1 石墨毡的导电性
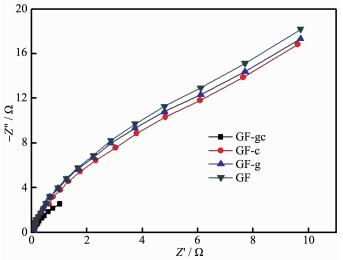
交流阻抗谱方法是一种以小振幅的正弦波电位为扰动信号的电测量方法, 以小振幅的电信号对体系进行扰动,一方面可避免对体系产生大的影响,另一方面也使得扰动与体系的响应之间近似呈线性关系,这就使得测量结果的数学处理变得简单[18]。EIS是研究电极表面电子传输的能力的有效手段。电极表面的电荷传输阻力(Rct)可以通过EIS测定,其大小可以由Nyquist图实轴半圆的截距推算得到。该截距的降低相对于界面电阻变小,从而有助于电极电荷传输[19]。图 6为改性前后石墨毡的电化学阻抗图。由图 6可推测得GF、GF-g、GF-c和GF-gc的Rct分别是23.4、21.2、20.1和7.1 Ω,GF-gc的Rct是原石墨毡Rct的三分之一,电极表面的电荷传输阻力显著降低。可能是因为过渡金属氧化铈存在电子空穴,多种价态共存的情况有助于电子自由迁移(方程7),以及介质和电极的电子传输面积增大,降低了电极表面的电子传输阻力。复合石墨毡相对于其他两种单一方法修饰的电极表现出较小的表面电荷传输阻力,体现出优良的导电性能。
3.3.1 MO的脱色降解
图 9为改性前后的石墨毡作为双室电芬顿的阴极对MO的降解矿化情况。由图 9可知,随反应时间的推移,脱色和TOC去除速率趋势变缓,改性后的石墨毡均加快MO的脱色和TOC去除速率,GF-gc对MO降解效果最为明显,20 min去除率已经达到96.8%,相对于原石墨毡去除率提高133.2%,30 min时MO溶液基本完全脱色,120 min时TOC去除速率达到69.2%,相对于未改性的石墨毡(28.3%)提高144.4%,说明复合石墨毡具有最高的电催化氧化活性,这与前述的表征结果所呈现的亲水性、氧还原能力和电荷传输阻力等优势密切相关。而且由图 9可知,单一的过渡金属氧化铈修饰石墨毡的性能优于单一H2O2化学预处理石墨毡的性能,说明氧化铈负载的碳材料能提高过氧化氢的产量[11],促进染料废水的降解。此外甲基橙的脱色是由于分子偶氮键断裂导致,由图 9两幅图对比得知MO脱色进度较TOC去除较快,与参考文献[22]中甲基红脱色降解情况相一致。这是由于显色基团-N=N-相关的n→π*跃迁需要较低能量吸收带,因此-N=N-很容易被攻击断开,自毁长共轭π系统,进而甲基橙的脱色进度较快[23]。
3 结论
(1) H2O2的预处理增加了石墨毡的含氧基团,亲水性增强,使改性石墨毡表面负载密集的CeO2,在一定程度上H2O2处理对于CeO2在石墨毡表面的沉积过程有一定的调控性。
(2) CV、EIS和LSV曲线表明所有改性石墨毡表面积增大,表面电子传输阻力减小,以及ORR过程响应电流密度变大等可以增大过氧化氢的生产率,进而加快电芬顿催化氧化反应,提高染料甲基橙的脱色降解速率。
(3) 相对于单一的H2O2化学处理和Ce氧化物修饰的石墨毡,复合石墨毡表现出较好的催化氧化能力,对甲基橙的氧化处理效果较好,更适合做为电芬顿的阴极,GF-gc阴极处理100 mg·L-1甲基橙染料废水时,30 min基本完全脱色,2 h的矿化率也提高一倍多,与形态表征和电化学性能测试的分析结果相一致。
-
-
[1]
Brillas E, Sirés I, Oturan M A. Chem Rev., 2009, 109:6570-6631 doi: 10.1021/cr900136g
-
[2]
Yu F K, Zhou M H, Yu X M. Electrochim. Acta, 2015, 163: 182-189 doi: 10.1016/j.electacta.2015.02.166
-
[3]
Yu X M, Zhou M H, Ren G B, et al. Chem. Eng. J., 2015, 263: 92-100 doi: 10.1016/j.cej.2014.11.053
-
[4]
Sirés I, Garrido J A, Rodríguez R M, et al. Appl. Catal. B, 2007, 72(3/4):382-394 http://www.sciencedirect.com/science/article/pii/S0926337306004668
-
[5]
Wang Y J, Li X Y, Zhen L M, et al. J. Hazard. Mater., 2012, 229-230:115-121 doi: 10.1016/j.jhazmat.2012.05.108
-
[6]
Hammami S, Bellakhal N, Oturan N, et al. Chemosphere, 2008, 73(5):678-684 doi: 10.1016/j.chemosphere.2008.07.010
-
[7]
Sirés I, Brillas E, Oturan M A, et al. Environ. Sci. Pollut. Res. Int., 2014, 21(14):8336-8367 doi: 10.1007/s11356-014-2783-1
-
[8]
Gao C, Wang N F, Peng S, et al. Electrochim. Acta, 2013, 88:193-202 doi: 10.1016/j.electacta.2012.10.021
-
[9]
Wang Y, Liu Y H, Wang K, et al. Appl. Catal., B, 2015, 165:360-368 doi: 10.1016/j.apcatb.2014.09.074
-
[10]
Miao J, Zhu H, Tang Y, et al. Chem. Eng. J., 2014, 250:312-318 doi: 10.1016/j.cej.2014.03.043
-
[11]
Assumpção M H M T, Moraes A, De Souza R F B, et al. Appl. Catal., A, 2012, 411-412:1-6 doi: 10.1016/j.apcata.2011.09.030
-
[12]
Alberto A G, Pletcher D. et al. Electrochim. Acta, 1998, 44 (5):853-861 doi: 10.1016/S0013-4686(98)00242-4
-
[13]
Wang Y, Liu Y H, Liu T F, et al. Appl. Catal., B, 2014, 156-157:1-7 doi: 10.1016/j.apcatb.2014.02.041
-
[14]
李晓刚, 黄可龙, 刘素琴, 等.中南工业大学学报, 2007, 1:51-56 doi: 10.3969/j.issn.1672-7207.2007.01.010LI Xiao-Gang, HUANG Ke-Long, LIU Su-Qin, et al. J. Cent. South Univ. Technol., 2007, 1:51-56 doi: 10.3969/j.issn.1672-7207.2007.01.010
-
[15]
Yu H B, Kim J H, Lee H I, et al. J. Sources, 2005, 140(1): 59-65 doi: 10.1016/j.jpowsour.2004.08.015
-
[16]
Zhou L, Zhou M H, Hu Z X, et al. Electrochim. Acta, 2014, 140:376-383 doi: 10.1016/j.electacta.2014.04.090
-
[17]
Le T X H, Bechelany M, Lacour S, et al. Carbon, 2015, 94: 1003-1011 doi: 10.1016/j.carbon.2015.07.086
-
[18]
Bard A J, Faulknler L R, Translated by SHAO Yuan-Hua(邵元华), ZHU Guo-Yi(朱果逸), DONG Xian-Dui(董献堆). Electrochemical Methods Fundamentals and Applications(电化学方法原理和应用). Beijing: Chemical Industry Press, 2005.
-
[19]
Wang C Y, Ye F C, Wu H F, et al. Int. J Electrochem. Sci., 2013, 8:2440-2448 https://www.researchgate.net/publication/283827485_Depositing_Au_Nanoparticles_onto_Graphene_Sheets_for_Simultaneous_Electrochemical_Detection_Ascorbic_Acid_Dopamine_and_Uric_Acid
-
[20]
Liu C B, Wang K, Luo S L, et al. Small, 2011, 7(9):1203-1206 doi: 10.1002/smll.v7.9
-
[21]
Liu J, Qiao Y, Guo C X, et al. Bioresour. Technol., 2012, 114: 275-280 doi: 10.1016/j.biortech.2012.02.116
-
[22]
Zhou M H, Yu Q H, Lei L C, et al. Sep. Purif. Technol., 2007, 57(2):380-387 doi: 10.1016/j.seppur.2007.04.021
-
[23]
El-Desoky H S, Ghoneim M M, Zidan N M. Desalination., 2010, 264(1-2):143-150 doi: 10.1016/j.desal.2010.07.018
-
[1]
-
表 1 不同石墨毡电极的活性表面积
Table 1. Electroactive surface area of the different graphite felt electrodes
Graphite felt A/cm2 GF 2.28 GF-g 5.71 GF-c 17.13 GF-gc 49.32 -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 29
- 文章访问数: 3885
- HTML全文浏览量: 888





 下载:
下载:








 下载:
下载:

