 图 7
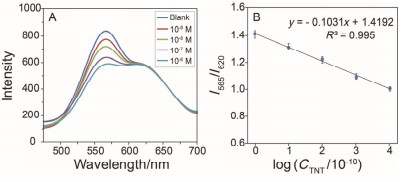
(A) (BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5薄膜对不同浓度的TNT溶液的荧光响应谱图. (B)荧光强度比值I565/I620随log (CTNT/10-10)的变化图
Figure 7.
(A) The fluorescence response profiles of the (BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5 ultrathin film to TNT with different concentrations. (B) The linear relationship between fluorescence intensity ratios (I565/I620) and log (CTNT/10-10)
图 7
(A) (BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5薄膜对不同浓度的TNT溶液的荧光响应谱图. (B)荧光强度比值I565/I620随log (CTNT/10-10)的变化图
Figure 7.
(A) The fluorescence response profiles of the (BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5 ultrathin film to TNT with different concentrations. (B) The linear relationship between fluorescence intensity ratios (I565/I620) and log (CTNT/10-10)

Citation: Guan Weijiang, Zhou Wenjuan, Lü Chao. Ultrathin Luminescence Film Based on Gold Nanoclusters with Aggregation-Induced Emission[J]. Acta Chimica Sinica, 2016, 74(11): 929-934. doi: 10.6023/A16080427

基于聚集诱导发光金纳米簇构筑发光超薄膜
English
Ultrathin Luminescence Film Based on Gold Nanoclusters with Aggregation-Induced Emission
-
Key words:
- gold nanocluster
- / aggregation-induced emission
- / luminescent film
- / layer-by-layer assembly
- / explosive
-
1 引言
荧光探针对待测物的测定是基于荧光团与待测物的相互作用, 导致其光学性质发生改变, 以荧光强度的变化进行定性及定量检测.溶液状态下的荧光探针具有灵敏度高、选择性好、检测范围广等优点, 但其存在污染待检测体系、无法重复使用和难以器件化等缺点[1~3].相比而言, 将荧光探针制成固态的薄膜传感器后, 则可实现在检测的过程中不污染待测体系、能够重复使用和回收、方便储存和运输, 这为制备真正器件化的传感设备打下坚实的基础[4~6].目前, 荧光高分子薄膜和荧光小分子掺杂的高分子薄膜是薄膜传感器的主流[6].但是, 大多数荧光材料被制作成固体薄膜后, 就不再是溶液中的单体分散状态, 而呈现出高度聚集的状态, 从而导致荧光强度减弱甚至猝灭, 使得荧光探针的检测灵敏度大大降低[7].为了解决聚集荧光猝灭(ACQ)的问题, 可以在荧光团上结合大体积的环状单元、减少荧光分子的负载量或将荧光分子掺杂到枝状聚合物中来抑制荧光分子之间的聚集[8, 9].采用这些方法往往需要增加薄膜的厚度以保证薄膜传感器的荧光强度.随着膜厚度的增加, 待测物分子在膜中扩散速度变慢, 传感薄膜的响应速度、灵敏度变差[6].因此, 在发光薄膜的制备中, 急需一种与ACQ截然相反的新型荧光材料, 不仅能避免聚集导致猝灭的发生, 还能使发光薄膜的厚度更薄.
2001年, 唐本忠课题组发现了一种具有聚集诱导发光(AIE)现象的荧光体系[10], 聚集状态下这类荧光分子的分子内运动(包括旋转和振动)会受到限制, 从而阻断非辐射跃迁方式, 导致荧光增强[11~13].这一有趣而重大的发现引起了全球研究人员的关注, 并迅速成为当前的研究热点[14~17].基于AIE分子的传感薄膜也陆续出现, 并被用于检测爆炸物、金属离子、环境有害物质等[18~21].层层组装技术由于能够对所制备的膜结构和组成进行精确控制而成为复合膜制备不可或缺的重要方法[22].到目前为止, 包括聚电解质、生物大分子、纳米粒子、聚电解质复合物以及带电小分子在内的多种类型的带电荷物质都可以作为层层组装的构筑基元实现复合膜的制备, 进而获得功能丰富的薄膜材料.
通常, AIE有机分子需要繁杂的合成步骤(往往需要有专业的有机合成技巧).相比之下, AIE无机纳米簇制备简单, 大多采用一锅法合成[23, 24].同时, 由于有机荧光分子中带有苯环、双键等共轭结构, 被光激发后容易引起自身结构的分解而使荧光强度迅速降低, 既不利于对待测物质的长时间检测, 也可能对荧光猝灭反应的检测结果造成干扰.而无机荧光纳米簇则具有极佳的光稳定性[20].根据有关报道, 其在激发光下照射2 h后, 依旧能保持80%以上的荧光强度[25].
本工作将带负电的谷胱甘肽包裹的金纳米簇(GSH-AuNCs)和牛血清白蛋白包裹的金纳米簇(BSA-AuNCs)与带正电荷的聚烯丙胺(PAH)通过静电作用以层层组装的方式分别制备了发黄色荧光的GSH-AuNCs/PAH薄膜和发红色荧光的BSA-AuNCs/PAH薄膜.紫外-可见吸收光谱和荧光光谱显示, 荧光金纳米簇在组装过程中没有出现荧光猝灭的现象, 吸收峰与发射峰位置均保持不变, 其吸光度和荧光强度随组装层数均匀增加.比较组装过程中薄膜荧光强度增加的速率发现, 具有AIE效应的GSH-AuNCs远远大于BSA-AuNCs, 且GSH-AuNCs/PAH薄膜的荧光绝对量子产率是GSH-AuNCs的2倍, 表明AIE荧光体系能够在更少层数(薄膜厚度)下制备出高荧光强度的发光薄膜.此外, 我们还发现, 相比于BSA-AuNCs/PAH薄膜, GSH-AuNCs/PAH薄膜的荧光更容易被爆炸物猝灭.基于此, 我们设计并构筑了以BSA-AuNCs/PAH薄膜为底, GSH-AuNCs/PAH薄膜为面的新型比率荧光传感薄膜.
2 结果与讨论
2.1 荧光金纳米簇的表征
2.2 荧光金纳米簇/聚电解质薄膜的表征
2.3 荧光金纳米簇/聚电解质复色薄膜的比率荧光传感
分别将GSH-AuNCs/PAH薄膜和BSA-AuNCs/PAH薄膜浸入到不同浓度的TNT溶液中, GSH-AuNCs/PAH薄膜的荧光强度随着TNT浓度的增加而减小, 而BSA-AuNCs/PAH薄膜的荧光强度几乎不变.根据已有报道, GSH的化学结构中具有富电子的伯胺基团, 可以与缺电子的TNT形成Meisenheimer复合物, 通过电荷转移相互作用淬灭GSH-AuNCs的荧光[28].基于同样的机理, 溶液中的BSA-AuNCs也可以被淬灭, 但是与PAH共组装成BSA-AuNCs/PAH薄膜后与TNT接触10 min并无响应, 可能由于以下三种原因:一是BSA-AuNCs/PAH薄膜层数(25层)较多, 使得TNT难以快速与BSA-AuNCs/PAH薄膜中的BSA-AuNCs相互作用[6]; 二是BSA-AuNCs/PAH薄膜的单层荧光强度较弱, 荧光发生改变时难以被检测到; 三是BSA-AuNCs在与PAH组装的过程中产生聚集, 使得大量的大分子BSA包裹在AuNCs周围, 这些BSA大分子聚集在一起后对TNT分子的扩散起到了抑制作用, 且大量BSA会在外层消耗掉大量的TNT, 使得薄膜内部的BSA-AuNCs不被淬灭[28].
考虑到单一荧光团的荧光强度变化易受到检测环境、仪器因素等的影响, 直接导致测量结果与真实值之间出现较大差距[29].比率型荧光探针含有两个荧光团, 通常选择较为稳定的荧光团作为参比, 另一个则与待测物作用, 荧光强度发生变化, 利用二者荧光强度的比值来标定待测物的浓度, 从而在一定程度上消除了测量中一些因素的影响[29].于是, 我们利用对TNT溶液惰性的BSA-AuNCs/PAH薄膜为底面、对TNT溶液敏感的GSH-AuNCs/PAH薄膜为表面, 构建了一种比率荧光传感薄膜, 并研究了其对TNT溶液的传感性能.图 7A为(BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5复色薄膜对不同浓度的TNT溶液的荧光响应谱图.结果显示, 随着TNT浓度(CTNT)的增加, 620 nm处的荧光强度基本不变, 565 nm处的荧光强度呈现逐级降低的趋势.图 7B为检测体系荧光强度比值I565/I620随log (CTNT/10-10)的变化图.在TNT浓度10-6~10-9 mol/L范围内, I565/I620与log (CTNT/10-10)呈现良好的线性关系, 其检出限达到1.0×10-10 mol/L.上述结果表明, 所构建的比率荧光传感薄膜可以实现对TNT的荧光比率检测.此外, 我们将本文的TNT检测方法与已有的其他检测手段进行了比较, 并总结在表 1.
 图 7
(A) (BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5薄膜对不同浓度的TNT溶液的荧光响应谱图. (B)荧光强度比值I565/I620随log (CTNT/10-10)的变化图
Figure 7.
(A) The fluorescence response profiles of the (BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5 ultrathin film to TNT with different concentrations. (B) The linear relationship between fluorescence intensity ratios (I565/I620) and log (CTNT/10-10)
图 7
(A) (BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5薄膜对不同浓度的TNT溶液的荧光响应谱图. (B)荧光强度比值I565/I620随log (CTNT/10-10)的变化图
Figure 7.
(A) The fluorescence response profiles of the (BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5 ultrathin film to TNT with different concentrations. (B) The linear relationship between fluorescence intensity ratios (I565/I620) and log (CTNT/10-10)
检测方法 检出限 特点 文献 本方法 10-10 mol/L 可用于液体检测, 制备简单, 便于携带, 检出限低 - 质谱(MS) 10-9 mol/L 可用于气体、液体检测, 一般与高效液相色谱、气相色谱联用, 选择性和灵敏度较好, 但仪器昂贵, 携带不便 [30] 化学发光(CL) 10-6 mol/L 可用于液体检测, 可与高效液相色谱技术联用提高选择性 [31] 表面增强拉曼光谱(SERS) 10-12 mol/L 可用于液体检测, 制备简单, 便于携带, 检出限低 [32] 离子迁移率谱仪(IMS) 10-12 mol/L 可用于气体检测, 擦拭取样效果好但过程繁琐, 吸气取样难度大但快速便捷 [30] 表 1 不同TNT检测方法比较
Table 1. Comparison of current methods for the detection of TNT2.1.1 谷胱甘肽包裹的金纳米簇
采用一锅法, 选用GSH同时作为还原剂和稳定剂, 制备出具有AIE性质的金纳米簇(GSH-AuNCs)[23], 其表面由GSH包裹, 带有负电荷.通过透射电镜(TEM)对合成的GSH-AuNCs进行形貌表征, 如图 1A, 其呈现出良好的分散性, 且尺寸分布较为均一, 直径约为1.9 nm.接着, 对生成的GSH-AuNCs进行紫外-可见吸收光谱和荧光发射光谱的表征, 结果如图 1B所示.其吸收光谱在约400 nm出现肩峰, 荧光最大发射波长在565 nm处(黄色荧光), 与文献报道一致[23].
2.1.2 牛血清白蛋白包裹的金纳米簇
利用牛血清白蛋白(BSA)在强碱性溶液中的还原性, 一步法制备BSA包裹的金纳米簇(BSA-AuNCs)[26].由于合成条件下pH值控制为约12.0, 处于BSA的等电点(5.1)以上, 因此合成的BSA-AuNCs表面带有大量负电荷, 能够稳定存在.BSA-AuNCs的TEM形貌表征如图 2A所示, 直径约1.6 nm, 分布均一, 且分散性良好.BSA-AuNCs的紫外-可见吸收光谱和荧光发射光谱如图 2B所示, 在约500 nm出现较宽的吸收峰, 最大发射波长约为620 nm (红色荧光).
2.2.2 荧光金纳米簇/聚电解质薄膜的形貌表征
以组装层数为5的GSH-AuNCs/PAH薄膜为例对薄膜的表面形貌进行表征.从(GSH-AuNCs/PAH)5的原子力显微镜(AFM)俯视图(图 6A)可以看出, GSH-AuNCs在薄膜中呈现球状聚集形态, 相比于溶液中的单分散颗粒, 聚集体的尺寸明显增加; 薄膜表面呈现均一连续的形貌, 与荧光照片所显示的均匀的橙黄色光相一致, 说明GSH-AuNCs发光团(聚集体)在薄膜内呈均匀连续分布.
同样的, 组装层数为25的BSA-AuNCs/PAH薄膜展现出类似的表面形貌.图 6B为(BSA-AuNCs/PAH)25的AFM俯视图, 与GSH-AuNCs薄膜相比, BSA-AuNCs在薄膜中的球状聚集体尺寸明显增大, 这可能是由多方面原因造成的:包括BSA的蛋白质结构、表面带电量的差异、组装层数不同等[6].从图中可以看到, 这种聚集体在薄膜表面呈现均一连续的分布, 与荧光照片所显示的均匀的红色荧光相一致.
2.2.1 荧光金纳米簇/聚电解质薄膜的光学性质
图 3A为不同组装层数的(GSH-AuNCs/PAH)n(n=1~5)薄膜的紫外-可见吸收光谱图.400 nm处的吸收峰与GSH-AuNCs溶液的吸收峰位置相同, 峰强度随组装层数均匀增加, 表明薄膜在组装过程中具有较强的有序性.同时, 薄膜的荧光光谱强度(最大荧光发射峰位于565 nm)随着组装层数的增长也呈现逐渐递增的趋势(如图 3B所示), 此现象也可通过不同层数薄膜在紫外光照射条件下的发光亮度进行观测:图 3B插图显示, 组装层数从1到5的GSH-AuNCs/PAH薄膜在365 nm紫外灯下发出均一的橙黄色荧光, 其亮度随层数增加逐渐增强.在紫外-可见吸收和荧光光谱图中, 不同层数薄膜的最大吸收和发射峰的位置并没有发生明显的移动和宽化, 表明整个组装过程中GSH-AuNCs的聚集并不影响其光学特性.此外, 经过与PAH层层组装成为(GSH-AuNCs/PAH)5薄膜后, GSH-AuNCs的荧光量子产率由水溶液中的9.30%增加到17.57%, 这主要归因于GSH-AuNCs的聚集诱导发光增强效应[23, 27].
图 4A为不同组装层数的(BSA-AuNCs/PAH)n(n=5~25)薄膜的紫外-可见吸收光谱图.与BSA-AuNCs溶液相比, 薄膜的吸收峰位置(500 nm)没有明显的变化, 随着组装层数的增加峰强度逐渐增加, 表明薄膜组装过程中的有序性.同时, 薄膜的荧光强度(620 nm处)随着层数的增长也呈现逐渐递增的趋势(如图 4B所示).同样, 在紫外光照下也可观测到不同层数薄膜荧光亮度的变化:图 4B插图显示, 组装层数从5到25的BSA-AuNCs/PAH薄膜在365 nm紫外灯下发出均一的红色荧光, 其亮度随层数增加逐渐增强.不同层数BSA-AuNCs/PAH薄膜的最大吸收和发射峰位置都没有发生明显的移动和宽化, 表明在组装过程中BSA-AuNCs的光学特性不受影响[27].此外, 我们对BSA-AuNCs/PAH薄膜与BSA-AuNCs溶液的荧光量子产率进行了测定, 发现BSA-AuNCs/PAH薄膜的荧光量子产率(7.52%)比BSA-AuNCs溶液的(5.01%)略高.两种AuNCs制成薄膜后呈现不同的发光行为, 可能的原因如下: GSH-AuNCs在PAH层间聚集后使得AuNCs间的Au‒Au相互作用增强, 并抑制其振动运动(减少非辐射跃迁), 导致荧光效率大大增强; 对于BSA-AuNCs, 由于配体是大分子BSA (空间位阻较大), 使得其聚集前后的Au‒Au相互作用变化不大, 其振动运动的减弱并不明显, 因此荧光效率增加较少[23].
图 5为(GSH-AuNCs/PAH)5和(BSA-AuNCs/PAH)25发光薄膜归一化后的发射光谱强度随紫外光照射时间的变化图.结果表明, 在365 nm氙灯(150 W)连续照射2 h后, 荧光强度近似的(GSH-AuNCs/PAH)5薄膜和(BSA-AuNCs/PAH)25薄膜, 它们的归一化荧光强度均保持在80%以上, 充分证明了荧光金纳米簇/聚电解质薄膜具有极好的光稳定性.
3 结论
本文成功制备了发黄色荧光的GSH-AuNCs/PAH层层组装薄膜和发红色荧光的BSA-AuNCs/PAH层层组装薄膜.在(GSH-AuNCs/PAH)5薄膜中, 具有AIE效应的GSH-AuNCs的荧光量子产率相比于水溶液中提高两倍.在保证荧光强度的前提下, 采用GSH-AuNCs能够大幅度的降低薄膜厚度, 有利于提高传感薄膜的响应速度和灵敏度.此外, 我们成功构建了一种新型的比率荧光薄膜传感体系:以BSA-AuNCs/PAH薄膜作为参比层, GSH-AuNCs/PAH薄膜作为响应层, 实现了对TNT的荧光比率检测.
4 实验部分
4.1 实验药品
谷胱甘肽(GSH)购自梯希爱(上海)化成工业发展有限公司(TCI Shanghai).牛血清白蛋白(BSA)、氯金酸(HAuCl4•3H2O)、聚烯丙胺盐酸盐(PAH)、2, 4, 6-三硝基甲苯(TNT)购自百灵威科技有限公司(J & K).过氧化氢、浓硫酸、氢氧化钠购自北京化工厂, 均为分析纯, 无需纯化, 可直接使用.
4.2 测试仪器
采用日本Shimadzu UV-3600型分光光度计在透射模式下对样品进行紫外-可见吸收光谱进行检测, 狭缝设置为1.0 nm.采用日本Hitachi F-7000型荧光分光光度计(扫描速度1200 nm/min, 激发和发射狭缝5 nm)对样品荧光特性进行研究.采用英国Edinburgh的FLS980型分光光度计对样品进行荧光量子产率的测量.采用日本JEM-3010高电压透射电子显微镜对样品形貌进行表征.采用德国Bruker Dimension FastScan原子力显微镜对薄膜进行表面形貌表征.
4.3 金纳米簇的制备
向2 mL 20 mmol/L的HAuCl4溶液中加入17.2 mL的超纯水, 充分搅匀后, 边搅拌边逐滴加入0.8 mL 100 mmol/L的GSH水溶液, 70 ℃下搅拌反应24 h, 得到谷胱甘肽包裹的荧光金纳米簇溶液(GSH-AuNCs), 在4 ℃下避光保存.
向5 mL 10 mmol/L的HAuCl4溶液中(37 ℃)边搅拌边逐滴加入5 mL 50 mg/mL BSA水溶液(37 ℃), 搅拌反应2 min后, 用1 mol/L的NaOH溶液调节反应液的pH值到12.0, 37 ℃搅拌过夜反应, 得到牛血清白蛋白包裹的荧光金纳米簇溶液(BSA-AuNCs), 在4 ℃下避光保存.
4.4 荧光金纳米簇/聚电解质薄膜的制备
将石英片放入过氧化氢和浓硫酸的混合溶液(体积比为3:7)中浸泡3 h, 然后用超纯水冲洗石英片并吹干, 即得到表面带负电的石英片.
将上述处理好的带负电的石英片浸入到1.0 g/L的PAH水溶液中, 10 min后取出, 用超纯水漂洗、吹干后, 再浸入到荧光纳米簇溶液中, 10 min后取出, 用超纯水漂洗、吹干; 重复以上步骤n次, 即得到具有n层的金纳米簇/聚电解质荧光薄膜:(GSH-AuNCs/PAH)n和(BSA-AuNCs/PAH)n.
在构建的(BSA-AuNCs/PAH)25薄膜上继续组装5层(GSH-AuNCs/PAH), 即得到复色的金纳米簇/聚电解质荧光薄膜:(BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5.
4.5 比率荧光检测TNT
以1 mg/mL的TNT甲醇溶液为储备液, 用超纯水稀释得到一系列不同浓度的TNT待测溶液.将制备好的(BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5复色薄膜浸入到不同浓度的TNT待测溶液中, 10 min后取出并吹干, 测定薄膜的荧光发射光谱, 以565 nm与620 nm处的荧光强度的比值(I565/I620)与TNT的对数浓度作图.激发波长设为365 nm, 发射和激发狭缝宽度均为5 nm.
-
-
[1]
Basabe-Desmonts, L.; Reinhoudt, D. N.; Crego-Calama, M. Chem. Soc. Rev. 2007, 36, 993. doi: 10.1039/b609548h
-
[2]
Li, X. H.; Gao, X. H.; Shi, W.; Ma, H. M. Chem. Rev. 2014, 114, 590. doi: 10.1021/cr300508p
-
[3]
Thomas Ⅲ, S. W.; Joly, G. D.; Swager, T. M. Chem. Rev. 2007, 107, 1339. doi: 10.1021/cr0501339
-
[4]
Ding, L.; Fang, Y. Chem. Soc. Rev. 2010, 39, 4258. doi: 10.1039/c003028g
-
[5]
Stich, M. I. J.; Fischer, L. H.; Wolfbeis, O. S. Chem. Soc. Rev. 2010, 39, 3102. doi: 10.1039/b909635n
-
[6]
Guan, W. J.; Zhou, W. J.; Lu, J.; Lu, C. Chem. Soc. Rev. 2015, 44, 6981. doi: 10.1039/C5CS00246J
-
[7]
Zhao, Z. J.; Lu, P.; Lam, J. W. Y.; Wang, Z. M.; Chan, C. Y. K.; Sung, H. H. Y.; Williams, I. D.; Ma, Y. G.; Tang, B. Z. Chem. Sci. 2011, 2, 672. doi: 10.1039/C0SC00521E
-
[8]
McQuade, D. T.; Pullen, E. A.; Swager, T. M. Chem. Rev. 2000, 100, 2537. doi: 10.1021/cr9801014
-
[9]
Zhu, C. L.; Liu, L. B.; Yang, Q.; Lv, F. T.; Wang, S. Chem. Rev. 2012, 112, 4687. doi: 10.1021/cr200263w
-
[10]
Luo, J. D.; Xie, Z. L.; Lam, J. W. Y.; Cheng, L.; Chen, H. Y.; Qiu, C. F.; Kwok, H. S.; Zhan, X. W.; Liu, Y. Q.; Zhu, D. B.; Tang, B. Z. Chem. Commun. 2001, 1740.
-
[11]
Guan, W. J.; Zhou, W. J.; Lu, C.; Tang, B. Z. Angew. Chem., Int. Ed. 2015, 54, 15160. doi: 10.1002/anie.201507236
-
[12]
李昱达, 张恒, 王迅昶, 汪锋, 夏养君, 化学学报, 2015, 73, 1055. doi: 10.6023/A15040282Li, Y. D.; Zhang, H.; Wang, X. C.; Wang, F.; Xia, Y. J. Acta Chim. Sinica 2015, 73, 1055. doi: 10.6023/A15040282
-
[13]
夏志清, 邵安东, 李强, 朱世琴, 朱为宏, 化学学报, 2016, 74, 351. doi: 10.6023/A16010001Xia, Z. Q.; Shao, A. D.; Li, Q.; Zhu, S. Q.; Zhu, W. H. Acta Chim. Sinica 2016, 74, 351. doi: 10.6023/A16010001
-
[14]
Mei, J.; Leung, N. L. C.; Kwok, R. T. K.; Lam, J. W. Y.; Tang, B. Z. Chem. Rev. 2015, 115, 11718. doi: 10.1021/acs.chemrev.5b00263
-
[15]
Guan, W. J.; Wang, S.; Lu, C.; Tang, B. Z. Nat. Commun. 2016, 7, 11811. doi: 10.1038/ncomms11811
-
[16]
褚衍环, 韩辉, 李维, 刘振涛, 韩相恩, 有机化学, 2016, 36, 336. doi: 10.6023/cjoc201508023Chu, Y. H.; Han, H.; Li, W.; Liu, Z. T.; Han, X. E. Chin. J. Org. Chem. 2016, 36, 336. doi: 10.6023/cjoc201508023
-
[17]
牛艳芳, 钱鹰, 胡秀东, 有机化学, 2016, 36, 555. doi: 10.6023/cjoc201509045Niu, Y. F.; Qian, Y.; Hu, X. D. Chin. J. Org. Chem. 2016, 36, 555. doi: 10.6023/cjoc201509045
-
[18]
Ghosh, K. R.; Saha, S. K.; Gao, J. P.; Wang, Z. Y. Chem. Commun. 2014, 50, 716. doi: 10.1039/C3CC47934J
-
[19]
Zhang, Y. Q.; Li, X. D.; Gao, L. J.; Qiu, J. H.; Heng, L. P.; Tang, B. Z.; Jiang, L. ChemPhysChem 2014, 15, 507. doi: 10.1002/cphc.v15.3
-
[20]
Zhao, N.; Lam, J. W. Y.; Sung, H. H. Y.; Su, H. M.; Williams, I. D.; Wong, K. S.; Tang, B. Z. Chem.-Eur. J. 2014, 20, 133. doi: 10.1002/chem.201303251
-
[21]
孙静波, 张恭贺, 贾小宇, 薛鹏冲, 贾俊辉, 卢然, 化学学报, 2016, 74, 165. doi: 10.6023/A15090628Sun, J. B.; Zhang, G. H.; Jia, X. Y.; Xue, P. C.; Jia, J. H.; Lu, R. Acta Chim. Sinica 2016, 74, 165. doi: 10.6023/A15090628
-
[22]
Li, Y.; Wang, X.; Sun, J. Q. Chem. Soc. Rev. 2012, 41, 5998. doi: 10.1039/c2cs35107b
-
[23]
Luo, Z. T.; Yuan, X.; Yu, Y.; Zhang, Q. B.; Leong, D. T.; Lee, J. Y.; Xie, J. P. J. Am. Chem. Soc. 2012, 134, 16662. doi: 10.1021/ja306199p
-
[24]
杨维涛, 郭伟圣, 张兵波, 常津, 化学学报, 2014, 72, 1209. doi: 10.6023/A14080568Yang, W. T.; Guo, W. S.; Zhang, B. B.; Chang, J. Acta Chim. Sinica 2014, 72, 1209. doi: 10.6023/A14080568
-
[25]
Tian, R.; Zhang, S. T.; Li, M. W.; Zhou, Y. Q.; Lu, B.; Yan, D. P.; Wei, M.; Evans, D. G.; Duan, X. Adv. Funct. Mater. 2015, 25, 5006. doi: 10.1002/adfm.v25.31
-
[26]
Xie, J. P.; Zheng, Y. G.; Ying, J. Y. J. Am. Chem. Soc. 2009, 131, 888. doi: 10.1021/ja806804u
-
[27]
Guan, W. J.; Lu, J.; Zhou, W. J.; Lu, C. Chem. Commun. 2014, 50, 11895. doi: 10.1039/C4CC06080F
-
[28]
Sun, X. C.; Wang, Y.; Lei, Y. Chem. Soc. Rev. 2015, 44, 8019, doi: 10.1039/C5CS00496A
-
[29]
王魁, 刘自力, 蒋凯, 化学学报, 2014, 72, 590. doi: 10.6023/A14030192Wang, K.; Liu, Z. L.; Jiang, K. Acta Chim. Sinica 2014, 72, 590. doi: 10.6023/A14030192
-
[30]
Makinen, M.; Nousiainen, M.; Sillanpaa, M. Mass Spectrom. Rev. 2011, 30, 940.
-
[31]
Capka, L.; Vecera, Z.; Mikuska, P.; Sestak, J.; Kahle, V. J. Chromatogr. A 2015, 1388, 167. doi: 10.1016/j.chroma.2015.02.041
-
[32]
Dasary, S. S. R.; Singh, A. K.; Senapati, D.; Yu, H. T.; Ray, P. C. J. Am. Chem. Soc. 2009, 131, 13806. doi: 10.1021/ja905134d
-
[1]
-
图 7 (A) (BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5薄膜对不同浓度的TNT溶液的荧光响应谱图. (B)荧光强度比值I565/I620随log (CTNT/10-10)的变化图
Figure 7 (A) The fluorescence response profiles of the (BSA-AuNCs/PAH)25/(GSH-AuNCs/PAH)5 ultrathin film to TNT with different concentrations. (B) The linear relationship between fluorescence intensity ratios (I565/I620) and log (CTNT/10-10)
表 1 不同TNT检测方法比较
Table 1. Comparison of current methods for the detection of TNT
检测方法 检出限 特点 文献 本方法 10-10 mol/L 可用于液体检测, 制备简单, 便于携带, 检出限低 - 质谱(MS) 10-9 mol/L 可用于气体、液体检测, 一般与高效液相色谱、气相色谱联用, 选择性和灵敏度较好, 但仪器昂贵, 携带不便 [30] 化学发光(CL) 10-6 mol/L 可用于液体检测, 可与高效液相色谱技术联用提高选择性 [31] 表面增强拉曼光谱(SERS) 10-12 mol/L 可用于液体检测, 制备简单, 便于携带, 检出限低 [32] 离子迁移率谱仪(IMS) 10-12 mol/L 可用于气体检测, 擦拭取样效果好但过程繁琐, 吸气取样难度大但快速便捷 [30] -

 扫一扫看文章
扫一扫看文章
计量
- PDF下载量: 0
- 文章访问数: 2727
- HTML全文浏览量: 772








 下载:
下载:






 下载:
下载:

