The Performance Degradation Study of Vehicle Fuel Cell under Start-Stop Operating Mode
质子交换膜燃料电池(Proton exchange membrane fuel cell,PEMFC)是一种高效、零排放与高功率密度的新型发电装置,经过世界范围内二十余年的持续研发,目前PEMFC在能量效率、功率密度、比功率、低温启动等性能指标方面已经取得了突破性进展[1, 2, 3],使得燃料电池汽车的性能已接近传统内燃机汽车的水平。然而,由于实际车况下燃料电池会经历复杂的燃料供应、湿度、温度、电流、电压等循环过程,造成车用燃料电池的关键材料衰减加速。通过燃料电池汽车的大量示范运行,人们发现车用燃料电池的关键材料和部件的劣化工况主要有六种:(1)频繁的启动停止引起的高电位造成催化剂碳载体的腐蚀;(2)低温循环所伴随的胀缩造成膜电极机械损伤;(3)低负荷运行导致质子交换膜分解;(4)反复加减速引起的电位循环造成催化剂铂颗粒粗大化;(5)深功率放电引起质子交换膜、催化剂以及载体的衰减加速;(6)杂质引起电池催化剂毒化以及膜质子传导能力衰减。为全面系统地认识启停工况下燃料电池性能衰减与应对技术的研究进展,本文通过大量文献调研分析,首先总结出具有代表性的模拟实际启停工况的实验方案,分析采用这些启停实验方案的启停加速衰减研究;其次,总结研究启停过程产生高电位的衰减机理、实验论证和建模分析;再次,通过启停过程中衰减机理的深入探讨,从PEMFC系统运行管理角度,归纳了一系列能够有效降低启停过程对燃料电池造成衰减的优化运行条件及其缓解策略;最后,通过对上述这些已有研究的分析梳理,提出了本文的观点、存疑、分析和解释,希望能为PEMFC启停衰减的进一步深入研究提供有益的参考。
在PEMFC启停老化的研究中,很大一部分是通过老化加速实验来进行启停老化机理研究,进而提出解决策略。为了实现稳定的启停循环,必须人为地制造氢氧界面,这对实验条件的控制提出了很高的要求;同时,老化加速实验通常要经过成百上千次的循环,实验的花费很高、耗时很长,所以科学合理地进行老化加速实验,从实验中观测到更多的现象,获取更多的信息,是非常必要的。下文对文献中已有的启停老化加速实验研究,尤其是学术价值较高的几篇文献,进行了总结和梳理。
2007至2012年间,Cho等通过一系列控制不同因素的老化加速实验研究了阴极湿度[4, 5]、电池温度[6]、模拟负载(dummy load)[7]、供气顺序[8]、阳极铂载量[9]等因素对燃料电池启停老化的影响。他们加速老化的基本方法是:电池正常启动一段时间后,在阳极和阴极同时吹扫空气,以此创造氢氧界面,来模拟启停过程。以文献[6]为例,实验过程如图 1所示:首先将氢气和空气分别通入阳极和阴极,保持17s,模拟燃料电池正常工作的过程;然后停止空气供给,并保持氢气供给,将模拟负载接入保持10s,消耗剩余的氧;之后停止氢气供给保持10s,这一阶段模拟燃料电池停机的过程;接着用空气同时吹扫燃料电池的阴阳极20s,模拟长时间的停机工况;最后阳极通入氢气,断开模拟负载,模拟启动的过程,完成一个实验循环。他们的其他研究中的实验流程均与此类似。
Cho等[9]于2012年还研究了降低阳极铂载量对燃料电池启停老化的影响。燃料电池启停衰减机理如图 2所示。通过降低阳极的铂载量,可以显著减缓B区域内发生的氧还原反应,进而减缓整个衰减过程,同时又可以做到基本不降低燃料电池的性能。
通过Cho等的这一系列研究,可得出以下结论:在低湿、低温并且带有模拟负载的条件下,启停衰减速率最慢;适当降低阳极的铂载量,可以减慢燃料电池启停老化的过程,同时又可以基本不影响燃料电池的性能;通过快速吹扫,使得氢氧界面尽快消除,是减缓启停老化的有效手段。
Takagi等[10]于2006年通过老化加速实验研究了停机过程中停止供气的顺序对燃料电池老化的影响。如图 3所示,在恒定电流下正常工作1.5min后,切断负载电流,停止供给氢气或空气中的一种;当电池电压下降到0.2V时,停止供给另一种气体;保持一定的温度,电池关机5min后,继续供给氢气和氧气并接通负载,回到燃料电池正常工作的工况。
通过Takagi等的研究,得出燃料电池启停过程中由于阴极电势升高而引发阴极碳腐蚀的主要因素是阳极中进入了氧气而形成氢氧界面。因而,燃料电池在启停循环中先停止氢气供给再停止氧气供给是一种可能的缓解启停老化的策略。Yu等[11]在2012年也开展了类似的研究,得出了相似的结论,在此不再赘述。
日本山梨大学的Ishigami等[12]通过在阳极交替通入氢气和空气来研究启停老化过程。该研究通过喷涂对氧敏感的染色卟啉([Tetrakis (pentafluorophenyl) porphyrinato] platinum,PtPP)薄膜,实现空间可视化而观测阳极氧分压的分布,进而清晰地分辨出阳极流场中的富氢区和富氧区的变化情况。可视化燃料电池的示意图如图 4所示,氧浓度可视化主要通过图中的Dye-Coated PFA Sheet实现。通过观测可以发现,受气体在扩散层和催化层中的扩散以及电化学反应的影响,氢、氧共存时间比交替通入氢气与氧气的周期要更长一些。此外,停机过程比启动过程对燃料电池的老化有更严重的影响,且膜电极的老化主要发生在靠近流场出口和进口的部位。
Yu等[13]研究了停机过程中排气口阀门开闭对燃料电池老化的影响。实验循环过程如下:首先,两个单体电池保持在OCV状态30s后阳极和阴极分别通入氢气和氧气;其次,切断空气的供给,接入模拟负载,当电池电压下降到0.05V时,切断氢气供给;之后,其中一个电池的阴极排气口打开暴露在空气中,另一个电池的阴极排气口保持关闭;10s后移除模拟负载,两极恢复氢气和氧气供给。实验过程中两个电池阴极排气阀打开、关闭情况示意图和加速老化实验的流程分别如图 5和图 6所示。
另外,有文献[13]研究指出,当质子交换膜燃料电池经历启停循环过程时,电池排气阀打开容易导入空气形成氢氧界面。因此,一个封闭的电池(关闭排气阀)能够有效减少性能衰减,是一种缓解启停衰减的策略。
将上述文献中涉及到的老化加速循环实验的控制因素、循环次数、衰减率等进行总结,如表 1所示。
表 1
Table 1
表 1(Table 1)
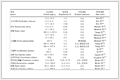
表 1 文献中的老化加速实验总结
Table 1 Summary of accelerated stress test
|
Factors | Cycles | Rate of degradation | References
|
|
Cathode gas humidity | 1500 | (0%RH 0.6V) 0.186 mA·cm-2 every cycle
(50%RH 0.6V) 0.240 mA·cm-2 every cycle
(100%RH 0.6V) 0.266 mA·cm-2 every cycle | [4, 5] | |
Cell temperature | 1200 | (40℃400mA·cm-2) 0.13mV every cycle
(65℃400mA·cm-2) 0.24mV every cycle
(80℃400mA·cm-2) 0.31mV every cycle | [6] | |
Virtual load or not | 1200 |
(Virtual load 0.6V) 0.299 mA·cm-2 every cycle
(No virtual load 0.6V) 0.678 mA·cm-2 every cycle | [7] | |
Gas supply sequence | 1200 | (Hydrogen and air simultaneously 0.6V) 0.68 mA·cm-2 every cycle
(Hydrogen first 0.6V) 0.47 mA·cm-2 every cycle | [8] | |
Anode Pt loading | 1000 | (Anode Pt loading 0.4 mg·cm-2 1A·cm-2) 0.21mV every cycle
(Anode Pt loading 0.1 mg·cm-2 1A·cm-2) 0.09mV every cycle | [9] | |
Stop gas sequence | 40 | (Stop hydrogen first 80 ℃ 1A·cm-2) Voltage decay 17%
(Stop air first 80 ℃ 1A·cm-2) Voltage decay 2% | [10] | |
Anode hydrogen and air supply alternately
Visualization of oxygen concentration | 500 | (200 mA·cm-2) 0.9mV every cycle | [12] | |
Stop gas sequence | 1500 | (Stop hydrogen first 1A·cm-2) 0.045mV every cycle
(Stop air first 1A·cm-2) 0.024mV every cycle | [11] | |
Cathode exhaust valve open and close | 1500 | (Close 1000 mA·cm-2 ) 0.024mV every cycle
(Open 1000 mA·cm-2 ) 0.093mV every cycle | [13] |
|
表 1 文献中的老化加速实验总结
Table 1 Summary of accelerated stress test
|
这些老化加速实验不仅展示了启停引起的衰减以及衰减速率,更重要的是探讨了不同工况(湿度、温度、虚拟负载等)下燃料电池的衰减程度,为如何减轻启停衰减提供了指导和建议。
根据以上讨论我们知道,降低电池温度、降低阴极气体湿度、接入虚拟负载、适当降低阳极铂载量、关闭阴极排气阀门以及首先停止供氧等措施能够有效减轻启停的衰减。但是,这些条件在实际使用中往往很难达到理想效果,所以想要有效减少燃料电池启停带来的衰减影响,还需要更多系统层面的改进。
PEMFC关闭时,由于两极气体分压不同和密封原因,氧气会同时出现在阳极和阴极;在电池启动时,氢气不断注入阳极,一个浮动的氢氧界面会在阳极形成,直到阳极全部被氢气占据。此外实验表明,PEMFC在多次启停后,会发生阴极催化层变薄、铂颗粒团聚以及碳载体减少。于是,人们试图在氢氧界面与实验现象之间建立联系,由此开始了对启停过程中老化机理的探索。
早在2000年,美国联合技术公司(UTC)的科学家就在专利中最早提出了氢氧界面的存在。之后于2005年,Reiser等[14]首次提出了氢氧界面会引发阴极高电位,从而导致阴极催化层内部的碳腐蚀及铂颗粒团聚等反应,并将该机理命名为“逆电流衰减机理”(Reverse-current decay mechanism)。这项机理在氢氧界面的客观存在与碳腐蚀等客观事实之间架起了理论的桥梁,加深了人们对启停过程的认识,推动了减轻及避免启停过程老化现象应对措施的发展,成为启停衰减问题研究的基础。
PEMFC正常工作时,阳极发生氢气的氧化反应:H2→2H++2e-,其平衡电势VH2eq≈0V(vs. RHE)。氢气氧化反应的速率大,过电势小,如图 7所示,实际反应电势Vma-φe,1a≈0.002V,其中Vma表示阳极铂金属相电势,φe,1a表示该区域电解质的液相电势。阴极发生氧还原反应生成水:O2+4H++4e-→2H2O,平衡电势为VO2eq≈1.23V。氧气还原反应的动力学速率很慢,过电势大,如图 7所示,实际反应电势Vmc-φe,1c≈0.836V,其中Vmc表示阴极金属相电势,φe,1c表示电解质的液相电势。于是电池的开路电压为U=Vmc-Vma=0.834V。
阳极存在氢氧界面时,阳极的局部区域存在氧还原反应,该区域的反应电势为:Vma-φe,2a≈0.593V。值得注意的是,若不考虑阳极金属相的电压损失,那么阳极区域的氢气氧化反应与氧还原反应的金属相电势是一样的,结果就是,氧气还原反应造成了该区域电解质液相电势的下降,即:φe,1a-φe,2a=0.591V。如果忽略液相电势在膜厚度方向的变化,那么φe,1c-φe,2c=0.591V,于是,阳极氧气还原区域对应的阴极区域的金属相与电解质相的电势差为:Vmc-φe,2c≈1.527V。由于质子交换膜的有限质子传导率,实际上使得液相电势在厚度方向存在变化,因此模拟计算的结果为:Vmc-φe,2c≈1.443V。至此,在启停过程中,阳极的氧气会导致阴极高电位,而在此高电位下,水会发生分解,而碳发生氧化反应生成二氧化碳,即“碳腐蚀”:
C+2H2O→CO2+4H++4e-
Shao等[15]报道碳腐蚀反应的平衡电势VCeq≈0.207V(vs. RHE),但是PEMFC在正常工作状态下该反应速率非常慢,然而,启停过程中的高电位及Pt颗粒的存在大大加速了该反应的速率,从而使得阴极碳载体被腐蚀,催化层变薄,如图 8所示。
在图 8中,TS-1、TS-2、BS-1、BS-2对应同一单体PEMFC阴极的4个不同区域。该单体PEMFC的阴极全部通氧气,TS-1、TS-2对应的阳极区域通氢气,而BS-1、BS-2对应的阳极区域通4% O2和氮气混合气体,人为制造氢氧界面。图 8显示的是6h后,这4个区域的横截面图的电镜图,可以看出,阳极存在氢氧界面的BS-1、BS-2区域的阴极催化层厚度严重变薄,这一实验现象与理论推测相吻合。
虽然Reiser等提出了“逆电流衰减机理”,但作为一个仿真模拟研究,并没有给出阴极高电位、逆向电流的实验依据。此外,尽管通过实验观测到了阴极变薄,但是并没有直接给出碳氧化(碳腐蚀)的实验依据。因此,后续研究分别从高电位、逆电流、碳腐蚀的直接实验验证出发,论证“逆电流衰减机理”。
为捕捉启停过程中阴极出现的高电位,Baumgartner等[16]在单体PEMFC上布置了4个外置式参考电极,如图 9、图 10所示。
在实验过程中,电池均恒流工作在5A左右。如图 11所示,在1100-1280 s时间段PEMFC单体处于欠气状态,导致阳极局部存在氧气形成氢氧界面,而在1280s时大量氢气瞬间涌入阳极,在阴极检测到瞬间的1.5V高电位。该项研究的疑问在于:为什么在1100-1280 s这段时间内没有检测到高电位?按照“逆电流衰减机理”,在这段阳极欠气的时间段氢氧界面会导致阴极的高电位。一个可能的解释是:在欠气阶段该传感器对应的阳极区域并不存在氢氧界面,而当重新供入大量氢气时,新涌入的氢气的挤压使得该传感器对应的阳极区域也存在氧气,从而导致了高电位的瞬间出现。
Kim等[17]于2009年通过引入一个动态氢电极(Dynamic hydrogen electrode,DHE)方法,明确捕捉到了稳定的阴极高电位。在实验中,阴极持续通入30 mL/min的空气(20.9% O2),而阳极则交替供气,在0-t1时间段,阳极通入充足的氢气,而在t1-t2时间段,阳极通入空气(20.9% O2)。整个过程中,PEMFC的阳极、阴极及全电池的电压变化如图 13所示。该图清晰地显示出在阳极改为供入空气后,氢氧界面的存在导致阴极1.5V左右的高电位。此外,阳极的电位稳定在0.8V左右。随着空气的持续通入,氢气被逐渐排出阳极,阴极的电位逐渐下降,最终接近阳极电势(两极都几乎是氧气)。在t2时刻,氢气再次通入,在阳极内部再次形成氢氧界面,从而再次检测到了高电位。但是由于氢气通入速率极快,阳极在短时间内被氢气全部占据,阴极高电位回落至正常电势。
此外,大连化物所的Yi等[18]也于2009年报道了通过三电极捕捉阴极高电位的现象,这里不再细述。
Reiser等[14]命名“逆电流衰减机理”的出发点是在氢氧界面下,阴极碳腐蚀或水分解形成的质子被阳极的氧还原反应消耗,形成了从阴极流向阳极的局部内部逆向电流。然而,内部逆电流的测量很难实现,一个等价的方法是将内部过程外部化,即通过测量同一电极内部不同区域之间的电荷交换(即电子流),来佐证内部逆电流(即质子流)。
2006年,Tang等[19]通过一个双电池体系(Dual cell configuration)首次实验验证了同一电极不同区域的电子交换,该实验体系如图 14所示。
双电池体系的初始状态是两个电池的阴极全部通入空气,阳极全部通入重整气(Reformate gas,组成为:0.01 ‰ CO,49% H2,17% CO2,其余为N2)。然后,关闭阀1,打开阀2,让空气以3mL/min的速度进入电池1的阳极。从图 15可以看到电池1的端电压持续下降,原因是在阴极内部高电压下水电解生成了H2,从而形成混合电势。此外,检测到了电流从电池1的阳极流向电池2的阳极,即有电子从电池2的阳极流向电池1的阳极,这说明在电池1的阳极局部存在氧还原反应。
该实验存在以下几个疑问:(1)空气刚刚进入电池1的阳极时,电流为什么会从电池2的阳极流向电池1的阳极?按照“逆电流衰减机理”,空气一旦进入电池1的阳极,就会在电池1的阳极内部形成氢氧界面(此时,电池2的阳极还全部是重整气),局部发生氧还原反应,进而发生电子从氢气氧化反应的阳极区域到氧还原反应的阳极区域的转移。从而,电子应从电池2的阳极流入电池1的阳极(电流为从电池1的阳极流向电池2的阳极)。一个可能的解释是,阳极局部发生氧还原反应加速了其他区域的氢气氧化反应,导致生成的大量电子除了供给电池1阳极的氧还原反应外,还从电池1的阳极流向了电池2的阳极。(2)当电池1的阳极全部被空气占据,空气开始进入电池2的阳极时,为什么两个电池之间不存在电子流?可能原文献作者解释有误,应该是当电池1和2的阳极交换电流为0时,电池1和2的阳极已经全部被空气所占据了,空气进入电池2的时刻比作者图示的时刻更加靠前,从而空气刚进入电池2的时刻为电池1和2的阳极交换电流的峰值时刻点。
Reiser等[14]在实验中观测到了阴极催化层厚度变薄,但并未直接证明这是因为碳腐蚀造成的。Kim等[17]于2009年定量地分析了启停过程中阴极电位及阴极排气的成分分析。如图 16所示,启停过程中的高电位同时伴随着CO2、CO的大量生成,这一实验结果直接论证了阴极高电位导致了阴极催化层内部的碳腐蚀。
2009年,Yousfi-Steiner等[20]的一篇综述中提出,除“逆电流衰减机理”外,还存在另一种机理可能导致阴极高电位。他们认为,双电池体系的一个致命弱点在于:两个电池仅仅由一根导线连接,而不是等电位仪控制,因此,不能将二者看作并联的两个原电池,而应该是一个原电池(Generator)和一个电解池(Electrolysis cell)的串联关系,如图 17所示。进而推导出:
|
${U_1} = {U_2} + i{r_{wiring}}$
|
(1)
|
其中,U1、U2分别表示电池1、电池2的端电压,i为导线中的电流(定义电池1的阳极流向电池2的阳极为正),rwiring为导线的电阻。
电池1的阴极供空气,阳极供氢气,是能够输出电流的原电池,其端电压满足:
|
${U_1} = ({E^1}_{eq,c} - {E^1}_{eq,a}) - {\eta ^1}_a - |{\eta ^1}_c| - i{r_1}$
|
(2)
|
其中,Eeq,c1为氧还原反应的平衡电势,Eeq,a1为氢气氧化反应的平衡电势,|ηa1|、|ηc1|分别为阳极、阴极的过电势的绝对值,r1为电池1内部的欧姆阻抗。
电池2的阳极与阴极都是空气,是电解池,其端电压满足:
|
${U_2} = ({E^1}_{eq,a} - {E^1}_{eq,c}) + {\eta ^2}_a + |{\eta ^2}_c| + i{r_2}$
|
(3)
|
其中,Eeq,a2为碳腐蚀的平衡电势,Eeq,c2为氧还原的平衡电势,|ηa2|、|ηc2|分别为阳极、阴极的过电势的绝对值,r2为电池2内部的欧姆阻抗。
通过联立(2),(3)式,得到:
|
$\eqalign{
&{U_2} = ({E^2}_{eq,a} - {E^2}_{eq,c}) + {\eta ^2}_a + |{\eta ^2}_c| + {{({E^1}_{eq,c} - {E^1}_{eq,a}) - {U_1} - {\eta ^1}_a - |{\eta ^1}_c|} \over {{r_1}}}{r_2} \cr
& = {U_{2,eq}} + {\eta ^2}_a + |{\eta ^2}_c| + {{({E^1}_{eq,c} - {E^1}_{eq,a}) - {U_1} - {\eta ^1}_a - |{\eta ^1}_c|} \over {{r_1}}}{r_2} \cr} $
|
(4)
|
根据式(4),作者得出结论:电池2的阴极能达到足够高的电位来使载体碳与Pt发生氧化腐蚀,如图 18所示。
这里存在以下几个疑问:首先式(4)表达的是电池2的端电压,并不能反映电池2的阴极的高电位。另外,尽管式(4)表明电池2的端电压是四项之和,但是并不意味着U2会很大,因为:
|
${U_{2,eq}} = {E^2}_{eq,a} - {E^2}_{eq,c} = 0.207V - 1.23V = - 1.023V$
|
|
此外,通过式(1)可知,U2<U1。其次,图 18作为解释原电池和电解池的端电压的差别,但是不能用来解释电池2的阴极的高电位。电池2的阴极电位是一个半反应(碳氧化、或者水分解)的电池,而不是如图 18所示的全反应的电势,它等于电池2的阴极金属相电势与电解质液相电势之差。最后,如图 19,本文对双电池体系各个部位的电势、各个部分的电势差做了一个详细的分析,结果表明,电池2的确是一个电解池,其端电压满足:
|
$\eqalign{
&{U_2} = \phi {^c}_{m,2} - \phi {^a}_{m,2} = (\phi {^c}_{m,2} - {^c}_{m,1}) - (\phi {^a}_{m,2} - \phi {^a}_{m,1}) + \cr
&({\phi ^c}_{m,1} - \phi {^a}_{m,1} = {U_1} - i\left( {{r_{wiring,1}} + {r_{wiring,2}}} \right) \cr} $
|
|
其中,rwiring,1+rwiring,2表示外电路导线的总电阻。
此外,电池2的阴极处金属相电势与电解质液相电势之差满足:
|
${V^c}_2 = {U_2} + {V^a}_2 - i{r_2} = {U_1} + {V^a}_2 - ({r_{wiring,1}} + {r_{wiring,2}} + {r_2})$
|
|
由于U1≈0.8V,V2a≈0.8V,i(rwiring,1+rwiring,2+r2) ≈0V,所以电池2的阴极反应电势可以高达1.6V。
根据上面的分析可知,“原电池-电解池衰减机理”与“逆电流衰减机理”并不矛盾,Yousfi-Steiner等[20]提出的“原电池-电解池衰减机理”,进一步指出了电池2作为电解池这一事实。但是,作者对阴极高电位的解释存在问题。
Reiser等[14]于2005年发表的文章中提出了一个解释阴极高电位的沿流道方向的一维稳态模型。该模型以电解质中的液相电势为唯一变量,以沿流道方向的质子守恒作为唯一控制方程,模拟了氢氧界面情形下液相电势沿流道的变化,指出液相电势在氢氧界面处急剧下降,导致对应阴极区域的高电位,从而引发碳腐蚀以及性能衰退反应。
随后,Meyers等[21]提出了一个更为详细的一维瞬态模型,该模型继承了沿流道方向一维的简化,但不同于Reiser等[14],该模型具有以下几个特点:(1)基于稳态的扩散方程,简单考虑了气体在膜电极内部厚度方向的传输;(2)在碳腐蚀的建模上,考虑了朗格缪尔等温吸附;(3)是一个瞬态模型,考虑了沿流道氢气氧气浓度随时间变化。该模型详尽地描述了在缺气工况下,流道内部的气体分布不均、氧气扩散到阳极发生还原反应,导致阴极高电位与相应的碳腐蚀反应。
Meyers等[21]模型的最大不足在于过于简化了气体在气体扩散层、催化层内部的传输过程,此外,应用界面模型来考虑催化层内部的电荷交换反应,偏离了实际。对此,德国学者Ohs等[22]于2009年提出了一个2D的稳态模型,多孔介质内部的气体扩散采用Maxwell-Stefan方程描述,催化层内部的电荷交换反应采用团聚体模型来表征,更为贴切地描述了阳极欠气工况下,阴极局部区域高电位的形成(>1.2V)和其导致的碳腐蚀和水分解反应。
综上所述,Reiser等[14]于2005年发表的先锋文献,引领了人们对启停过程中氢氧界面、高电位、碳腐蚀等关键科学问题的不断探索。时至今日,“逆电流衰减机理”所描述的阳极氢氧界面引起阴极高电位从而诱发碳腐蚀这一机制,不断地被后来者通过实验事实验证、理论模拟论证,作为出发点与落脚点,指导人们从材料改性、系统策略等多个方面抑制启停过程所伴随的老化。
PEMFC启停衰减抑制相关技术基本都是从消除阳极的氢空界面和降低阴极的高电位入手。International Fuel Cells(UTC前身)、UTC、Nissan、Ballard等公司系统深入研究了燃料电池在启停过程中出现的问题,从系统层面提出了诸多解决方案,总结如图 20所示。
车用燃料电池启停问题的研究需要追溯到磷酸燃料电池。1989年,研究人员发现,在其磷酸燃料电池电堆的启停过程中会出现阴极高电位,从而造成碳载体腐蚀分解、催化剂脱落、失去活性[23, 24]。他们的解决方案为:阴极通氮气和氧气的混合气(氮气占99.5(vol)%,氧气占0.5(vol)%),阳极通氮气并将阴极电位控制在0.3-0.7 V之间。Sederquist等[25]的策略为:停止氢气的供应,将空气引入一个循环装置中用于消耗氧气,然后将剩余的惰性气体引入阴极。
在解决PEMFC启停过程中老化问题的早
期,人们主要借鉴磷酸燃料电池的经验。但是PEMFC作为汽车的动力电源,出于移动应用考虑,惰性气体吹扫策略不合适。有研究人员[26-28]提出,可以在流场板外加一层冷却板(内部充满冷却液-水),当PEMFC停机后,流场板内气体不断被消耗,导致压力减小,从而使水流入流场板内,实现自钝化过程。另外,Bednarz等[29]提出通过施加一个外部电压使得水在阳极电解产生一个还原性气氛,达到钝化燃料电池阳极的目的。
如上文所述,由于在燃料电池启停过程中阴极会产生较高的电位,从而造成催化层载体腐蚀,催化剂脱落等老化现象,因此,大量专利聚焦在如何降低阴极电位上。Bekkedahl等[30]提出一种“短路”的解决策略。该策略通过在电堆中的每个单电池之间设置一个分路器,从而提高每个单电池承受阴极高电位的能力。例如通过旋转的或者热控制的弹簧致动短路机构可以仅在燃料电池堆的启动和关闭期间“短路”燃料电池堆中的每个单电池。Dine等[31]提出,通过部分关闭阳极排气回收系统,切断外部电路的主要负载,停止阴极的空气供给,用外加负载减少或限制电池电压,从而降低阴极电位。当停止燃料供应时,继续阳极气体循环,利用存在的氧气将氢气转化为水。一直持续到将所有氢气移除。现代汽车公司[32]提出关闭进气阀,外加负载,消耗残留氧气,从而降低阴极电位,起到保护电堆的目的。
从消除氢空界面入手,Condit 等[33, 34]提出通过断开主负载,切断气流并往两极通平衡气体。平衡气体组成包含至少0.0001的氢气(以体积计,且介于1.0%和小于4.0%氢气之间较佳),其余气体为氮气和其他对电堆呈惰性无害的气体,所有氧气通过在电池内与氢气反应而被消耗。另外还可以通过强制对流的方式,例如,Margiott等[35]在关闭电堆的时候采用空气清除阳极残留的氢气。具体为:采用鼓风机串联或并联的方式,使空气进入组件通过一个低入口,空气自然循环上升通过组件高出口排除(带有残留的氢气)。Reiser等[36]的另外一种方案提出,先断开主要用电设备,然后停止阳极含氢燃料供应,向阳极燃料流场鼓入空气迅速地将剩余氢气排出。Balliet等[37]提出电堆在启动时先用氢气吹扫阴极和阳极,然后用氧气吹扫阴极后再使用。Reiser提出[38]在电堆启动时,先用氢气快速吹扫阳极,然后再连接负载。Margiott等[39]提出电堆关闭时,先关掉氧气进气阀门,在阴极流场消耗氧气。然后打开氢气阀门,让氢气进入阴极流场。当阴极和阳极流场充满约100%氢气时,关闭氢气和氧气排气阀。在关闭期间,大气中的氧气会渗透进入燃料电池,当氢气浓度下降时,再次打开氢气阀补充燃料。Goto等[40]提出在电堆启动阶段,先给阳极通氢气,阴极通氧气(考虑到阴极残留的氢气,空气量要加上预设的增量)。Reiser等[41]在这些专利基础上提出:电堆关闭时用空气快速吹扫阳极;下次启动前先用氢气吹扫阳极,再投入使用。
基于上述启停衰减的缓解策略,本文将专利中有关应对启停带来的性能下降的缓解策略做了较系统的归纳,如表 2所示,列出了有关质子交换膜燃料电池在启停过程中系统应对策略的专利。
表 2
Table 2
表 2(Table 2)

表 2 专利提出的缓解策略总结
Table 2 Summary of mitigation strategy in patents
|
Patent holder | Application time | Mitigation strategy | No.
|
| UTC | 1998 | Flow field filled by liquid coolant | [27] | |
2000 | Flow field filled by liquid coolant | [26] | |
2001 | External connect‘short circuit’component | [30] | |
2001 | Stop oxygen and consumed remained oxygen by hydrogen | [31] | |
2001 | Fed balance gas into system | [33] | |
2001 | Fed balance gas into system | [34] | |
2001 | Swept anode hydrogen by air | [35] | |
2001 | Swept anode hydrogen by air | [36] | |
2002 | Swept anode and cathode by hydrogen and then swept cathode by air | [37] | |
2002 | When turned on,swept anode by hydrogen | [38] | |
2003 | Stop oxygen and consumed remained oxygen by hydrogen | [39] | |
2005 | When turned off,swept anode by air; when turned on swept by hydrogen | [41] | |
2009 | Inactived fuel cell stack by water before turned off | [28] |
| Ballard |
2001 | Consumed oxygen (cycle device),inert gases supplied to cathode circularly | [25] |
| Nissan |
2004 | In start stage,fed hydrogen in anode and then fed oxygen to cathode | [40] |
| Hyundai |
2002 | Closed air inlet valve,external load on,consumed remained oxygen | [32] |
| MTU |
2002 | Applying an external voltage for water electrolysis,reducing atmosphere generated at anode and inactived fuel cell anode | [29] |
|
表 2 专利提出的缓解策略总结
Table 2 Summary of mitigation strategy in patents
|
通过上述文献梳理归纳分析,Reiser等率先开展PEMFC启停过程的机理研究,并引领氢氧界面、高电位、碳腐蚀等关键科学问题的不断探索,使得“逆电流衰减机理”所描述的阳极氢氧界面引起阴极高电位从而诱发碳腐蚀这一机制,不断地被后续研究通过实验验证和理论模拟论证。在系统管理层面,通过改进优化燃料电池运行机制,如降低电池温度、降低阴极气体湿度、接入虚
拟负载、适当降低阳极铂载量、关闭阴极排气阀门,以及停机先停止供氧等可以有效缓解启停工况造成的衰减。然而,某些系统应对策略在实际使用中往往很难达到理想效果,还需要开展从材料改性、集成技术、系统控制策略等多个方面抑制启停过程所伴随的老化的深入研究。
 2016,
Vol. 79
2016,
Vol. 79 Issue (11): 1001-1011
Issue (11): 1001-1011 2016,
Vol. 79
2016,
Vol. 79 Issue (11): 1001-1011
Issue (11): 1001-1011