Research Progress in the Syntheses and Applications of Silafluorene-Containing Compounds
硅芴,即二苯并噻咯,是芴的衍生物,噻咯环位于硅芴中心,硅原子的两个环外σ*轨道与丁二烯部分的π*轨道产生σ*-π*共轭,有效降低了最低未占有轨道(LUMO)的能量,提高了电子亲和性和导电性[1],有利于电子的传输。硅芴结构分子将主族元素的电子效应引入共轭结构中,并以硅做桥联原子来构建刚性梯形共轭分子。两种效应的结合使得硅芴分子热稳定性良好,且可调谐其光物理性质,具有高的荧光效率,在有机发光二极管(OLED)[2]、聚合物太阳能电池(PSC)[3]、有机场效应晶体管(OFET)[4]、爆炸性微粒检测[5]等方面具有很大的应用前景。已有研究者针对硅芴类研究进展作了综述,但是侧重点各有不同,如李良春等[6]根据母体结构的不同,对硅桥联并环π共轭分子(其中包括二苯并硅杂环戊二烯,即硅芴)的研究进展进行了综述;曲红梅等[7]对母体结构仅含苯环和噻咯环的硅杂环戊二烯并苯小分子(其中包括二苯并噻咯)的合成和性能方面的研究作了综述;Holmes等[8]报道了应用于有机电子的聚硅芴的研究进展。本文主要介绍近几年最新的硅芴类化合物(包括小分子和聚合物)的合成方法、结构修饰、性能及应用研究现状。
目前报道的硅芴类化合物的合成方法主要有4种,包括双锂化-硅烷化反应、过渡金属催化反应、分子内sila-Friedel-Crafts反应、Si-H和C-H双活化反应。在此基础上,研究者们丰富并改进了此类化合物的合成方法体系。
Nozaki等[9]发现铑同样可催化无手性硅桥联炔烃和烷基炔烃的[2+2+2]环加成反应(图式1),可得到非对称的手性硅芴类衍生物,产率和对映选择性高。该反应对配体具有选择性,当配体为(R)-L单膦配体时,产率最高,原料结构中的基团对反应的产率及对映选择性均有影响。
Breunig等[10]报道了Ni催化C-C键和Si-H键活化脱氢反应,以联苯烯和二乙基硅烷为原料,以Ni (PPhMe2)4为催化剂,以甲苯为溶剂110℃下反应4h,得到9, 9-二乙基硅芴,产率为37.5%,反应过程如图式2所示。该反应溶剂可为THF、甲苯、苯或二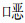 烷。但是当原料为2, 7-二叔丁基-亚联苯时,反应无选择性,得到3, 6-二叔丁基-9-硅芴和2, 7-二叔丁基-9-硅芴两种异构体的混合物,说明该反应对原料的选择是有要求的。
烷。但是当原料为2, 7-二叔丁基-亚联苯时,反应无选择性,得到3, 6-二叔丁基-9-硅芴和2, 7-二叔丁基-9-硅芴两种异构体的混合物,说明该反应对原料的选择是有要求的。
Xu等[11]报道了含氢硅烷联苯体系的分子内自由基环化反应合成硅芴和硅茚(图式3),该反应原料为易得的含氢硅烷,无需过渡金属催化剂、碱或酸,只需Si-H键和C-H键之间反应一步便可得到产物。同时不同于过渡金属催化的C-H活化反应,自由基硅烷化反应遵循电子效应,选择性地发生在位阻较大的位置,是已知合成方法的补充。当溶剂为三氟甲苯、自由基引发剂为二叔丁基过氧化物时产率较高,为84%。
类似地,Leifert等[12]通过2-二苯基硅烷取代的联苯衍生物的基质促进均裂芳香取代反应,合成了具有不同取代基的9-硅芴(图式4)。该反应以电子作催化剂,无需过渡金属催化剂,当氧化剂为叔丁基过氧化氢、引发剂为四丁基碘化铵时,产物的产率较高。
笔者课题组参照Huang等的方法合成了6, 6′-二碘-4, 4′-二溴-3, 3′二甲氧基联苯,在通过先锂化再硅烷化合成官能化的2, 7-二溴-9-硅芴的过程中,通过控制锂化反应的时间,在用位阻比较大的二苯基二氯硅烷进行成键关环反应时提高了反应温度,目标化合物产率得到很大提高,反应过程如图式5所示。
随后,通过Sonogashira反应制备了4种新型的荧光化合物(6a~6d),目标化合物的量子产率高达0.89,且发光及热稳定性好[13]。
笔者课题组进一步对亲电试剂诱导芳乙炔基取代硅芴衍生物的分子内关环反应进行了研究,通过亲电双环化反应第一次将呋喃环接到二苯并噻咯核上,成功合成了二呋喃并苯并噻咯衍生物7和8。研究发现只有以末端为供电子基团取代基的硅芴作为原料时,呋喃环的关环反应才可进行,且取代基的差异能引起化合物固态聚集行为的很大改变。这些化合物荧光量子效率最高可达99%,热稳定性好。化合物8在不同溶剂中可自组装成不同尺寸的微米线,这些微米线在溶液中或固态下均非常稳定,有望应用于有机微纳米器件、场效应晶体管等方面[14]。
此外,我们还利用硅芴的结构设计合成了具有立体空间构型结构的分子,把硅芴类分子通过中心螺硅原子连接合成了双螺硅杂双芴聚合物9,该聚合物发蓝光,量子效率为0.59,热稳定性良好[15]。
为了揭示聚硅芴分子的结构、光电性质以及结构-性能之间的关系,Chen等[16]利用量子化学计算方法,系统地研究了硅芴间的连接模式对聚硅芴光电性质的影响。他们发现,硅芴单元间以邻位相连接(化合物10)能形成非共平面几何结构,具有最高的单重态和三重态能量、最低的最高占有轨道(HOMO)、最高的未占有轨道(LUMO),并有最高的电子注入能力、空穴电子传输性能和最强的圆二色谱信号。与被广泛研究的2, 7-硅芴和3, 6-硅芴相比,聚(1, 8-硅芴)各类性能最优越,可做蓝光或深蓝光OLED、蓝色磷光发射器的双极主体材料及螺旋手性共轭化合物。
Yin等[17]对π堆积聚硅芴的电荷传输性质作了理论研究,发现π堆积的硅芴取代基及Si-Si骨架的σ共轭为聚(1, 1-硅芴)的电荷传输提供双通道(化合物11和12),作为n型半导体材料,其空穴及电子移动性能比聚二苯并富瓦烯高出1个数量级。
笔者课题组[18]利用Sonogashira反应合成了2, 7位乙炔基官能化的硅芴与芳基化合物的共聚物13~16,此类新型π共轭荧光聚合物含硅芴单元在溶液中荧光量子效率最高可达0.92,且发光稳定性好。
Shimizu[19]研究了9-位Si原子上取代基、3, 6-位及2, 7-位取代基对硅芴光物理性质的影响。在2-位和7-位分别引入不同的给电子基团和吸电子基团,制备不同的D-π-A型硅芴,可调节此类π体系化合物基态和激发态的电子性质和HOMO-LUMO能隙;而且发现吸电子基团和溶剂极性的增强都可导致发射峰红移,得到不同发光颜色的化合物。研究人员创造性地将其中发蓝光的化合物17和发橙光的化合物18在聚丙烯酰胺膜中以19:1相混合,得到了量子效率为0.81的具有强烈白光的聚合物薄膜。Wang等[20]通过Yamamoto反应合成了聚(9, 9′-二癸氧基苯基-2, 7-硅芴)(19)。该聚合物玻璃化温度为120℃,外部量子效率达75%,发光效率为2.1~2.3 cd/A。
在Et3N存在下,Cai等[21]将9, 9′-二氯-9-硅芴与二氯硅烷在Et2O/THF-H2O的两相溶液中共水解,合成了4种环状硅芴衍生物20~23。这些化合物固态时的量子效率比溶液中高,最高达0.54,具有弱的聚集诱导发光增强(AEE)行为。他们从晶体结构、紫外可见吸收光谱及分子轨道理论计算来研究及解释荧光机理及量子效率的差异,发现晶胞中的部分π-π相互作用导致π电子耦合和较大红移,可降低其量子效率。而在环形化合物中引入非荧光基团可增加荧光团之间的距离,阻止荧光团π-π堆积,使固态荧光效率更高。
他们还通过环水解和缩聚反应合成了3种分别含硅芴、1, 3-二苯基-9, 9′-硅芴及四苯基噻咯的环四硅氧烷(化合物24~26),并研究了它们在溶液中和晶体状态下的光学性质。这些化合物在溶液中量子产率低,而其固态量子效率最高可达0.78。他们还通过对这些化合物的晶体结构、分子轨道和激发态计算来研究它们的发光机理[22]。
Pusztai等[23]合成了4种1, 3-二苯基取代的不对称硅芴类化合物27~30。与没有取代基的硅芴同系物相比,在1位和3位引入苯基,使得发光光谱明显红移、荧光强度增加、溶液和固态荧光量子效率提高,最高达42%。硅芴9位Si原子上的苯取代基可增强荧光强度,而有机硅基团会导致荧光强度和量子效率的降低。化合物29和30具有典型的AEE效应。这些化合物都可做蓝光OLED材料,其中化合物28效果最好。通过对人体皮肤纤维母细胞的毒性测试证明这些化合物也可作为生物成像的潜在应用材料。
McDowell等[1]合成了一系列硅原子上含不同侧基的2, 7-二溴-3, 6-二甲氧基-9, 9′-硅芴单体31~36,进而开发了一条有效的室温聚合路线,探索了反应溶剂对聚合物反应的影响。聚合物数均分子量Mn>50kg/mol,发蓝光,固体量子效率>80%,聚合物膜透明,热稳定性好。用循环伏安法测得其HOMO能级为-5.62eV,LUMO能级为-2.62eV。
Yang等[24]将四苯基乙烯和硅芴通过Suzuki偶联以共价单键形式连接起来,合成了3种新型的具有AEE效应的化合物37~39。通过共用一个苯环,改变四苯乙烯与硅芴核的连接方式,发光颜色从绿色向天蓝、深蓝变化,其中以化合物38Si-tPE制成的未经掺杂的OLED器件发天蓝色的光,电流效率为8.04cd/A,能量效率为6.17lm/W,外量子效率为3.38%。
Wang等[25]合成了一种新型的基于硅芴的蓝色磷光OLED主体材料1, 3-二(9-甲基-9-硅芴)苯(Me-DBSiB,化合物40)。通过sp3杂化的硅原子将9-甲基-9-硅芴连接到苯环骨架上从而保持此化合物较高的单重态和三重态能量,提高了化合物热力学和发光稳定性。由于苯环对化合物的HOMO及LUMO无贡献,其能隙宽为4.1eV。当以Me-DBSiB为主体材料,双(4, 6-二氟苯基吡啶-N, C2)吡啶甲酰合铱(Ⅲ)为客体材料,最大电流效率为14.8cd/A。
Chen等[26]合成了二苯胺或咔唑封端的硅芴衍生物41~44,这些化合物能隙宽、荧光量子产率高,稳定性好。基于此类硅芴衍生物的非掺杂双层OLED的电致发光效率均比基于N, N′-双萘基-N, N′-二苯基-2, 7-二胺-9, 9′-二苯基-芴的器件性能好,其中以化合物42为发光层的OLED性能最好,CIE (commission internationale de L'Eclairage)指数为(0.175,0.144),在蓝光区,最大电流效率为1.62cd/A,外量子效率(external quantum efficiency,EQE)为1.36%。用化合物42作为掺杂剂,溶液法制成的OLED器件,EQE为2.48%,开关电压低至4V。实验结果表明,与芴相比,硅芴稳定性更好,能隙低。封端的芳胺基团及硅芴9位的有机基团均对OLED的性能有影响。
Keyworth等[4]通过Suzuki偶联反应分别将咔唑、三苯胺、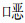 二唑和三唑单体连接到2, 7-硅芴或3, 6-硅芴单体上,成功合成了一系列能级可调的交替共聚物,并研究了硅芴上取代基位置对其电荷传输性质的影响。他们发现含2, 7-硅芴重复单元的聚合物比含3, 6-硅芴重复单元的聚合物的能隙小。这些化合物光致发光性能好,但是聚合物的分子量不高,成膜能力差。其中以含三苯胺和2, 7-硅芴单体的共聚物(聚合物45)制成的OFET的空穴迁移率最大,为3×10-4cm2·V-1·m-1,电流开关率为105。
二唑和三唑单体连接到2, 7-硅芴或3, 6-硅芴单体上,成功合成了一系列能级可调的交替共聚物,并研究了硅芴上取代基位置对其电荷传输性质的影响。他们发现含2, 7-硅芴重复单元的聚合物比含3, 6-硅芴重复单元的聚合物的能隙小。这些化合物光致发光性能好,但是聚合物的分子量不高,成膜能力差。其中以含三苯胺和2, 7-硅芴单体的共聚物(聚合物45)制成的OFET的空穴迁移率最大,为3×10-4cm2·V-1·m-1,电流开关率为105。
Song等[27]合成了两种以二苯并噻咯-噻吩-苯并噻二唑-噻吩为主链的低能隙化合物46a和46b,这类化合物的分子量高,溶解性好。分别以这两种化合物和(6, 6)-苯基-C71-丁酸甲酯(PC71BM)的掺杂物为激发层制成太阳能电池,在100mW/cm2的光照条件下,能量转化效率分别为2.72%和5.08%。当以TiOx为阻挡层时,开路电压、短路电流、填充系数、能量转化效率最高可分别达0.91V、11.50mA·cm-2、0.58、6.05%。这表明46b是一种具有很大潜在应用价值的太阳能电池给体材料。
Lin等[28]合成了一种可作为太阳能电池电子受体的二苯并噻咯-二吡咯并吡咯二酮分子(化合物47)。该化合物热稳定性好、吸收谱宽而强,与聚(3-己基噻吩)(P3HT)能量水平相匹配,电子迁移率适中。获得的P3HT:DBS-2DPP混合膜具有良好的纳米级互穿网络,有利于电荷分离及提高有机太阳能电池(OSCs)的效率。基于P3HT和DBS-2DPP混合膜通过溶剂退火及溶液加工的OSCs的能量转化效率高达2.05%,是无富勒烯类受体的小分子体系,溶液加工的OSCs能量转化效率最高值表明DBS-2DPP是一种很有潜在应用价值的OSCs材料。
Song等[29]通过Suzuki偶联反应合成了两种新型的以硅芴为电子给体的D-A型聚合物:聚(二苯并噻咯-二苯并喹啉)48和聚(二苯并噻咯-二苯并吩嗪)49,它们在有机溶剂中溶解性良好并具有较高的热稳定性。聚合物48和49分别以1:3和1:6的比率与PC71BM混合,作为太阳能电池的激发层,开路电压、短路电流、填充系数、能量转化效率分别为0.89V、5.1mA·cm-2、30.2%、1.4%和0.98V、3mA·cm-2、52.8%、1.6%。
Li等[30]通过Suzuki偶联反应合成了3种以硅芴为电子给体单元、5-烷氧基-6-氟苯并噻二唑为电子受体单元、噻吩为间隔基的D-A型交替共轭聚合物50a~50c,并将其作为给体材料应用于聚合物太阳能电池中。氟原子的引入可降低聚合物HOMO和LUMO的能级进而提高开路电压,而柔性的烷氧基链单元的引入则可提高其溶解性,同时不影响聚合物链在固态时的密堆积。以这些化合物与PC71BM做成的聚合物太阳能电池开路电压和能量转化率最高可分别达0.98V、6.41%。
Yang等[31]通过将硅芴与芴的共聚物聚(硅芴-(9, 9′-二甲基-芴)-二乙烯) PSFF 51a及51b附着到100nm的中空SiO2纳米球上,用于检测溶液中的三硝基甲苯(TNT)和环三亚甲基三硝铵(RDX),检测限分别为2×10-7和8×10-7。他们发现,硅烷改性的PSFF包裹的SiO2纳米球与未经改性的PSFF包裹的纳米球及十八基改性的纳米球相比,荧光量子效率最高。虽然检测限不高,但吸附在SiO2纳米球上的荧光团对爆炸物的敏感度仍高于用环糊精封装的荧光团。
Dedeoğl等[32]通过建立硅芴-苯二乙烯和四苯基噻咯-苯二乙烯的单体及二聚体模型,研究了这些聚合物和一系列爆炸物及非爆炸的硝基苯(NB)形成的复合物(见下图)的稳定性及检测灵敏度,用分子内原子、量子理论的方法研究电子密度的拓扑学,他们发现分析物和聚合物间的非共价相互作用的实质是π-π堆积和氢键作用。复合物的稳定性与计算得到的HOMO-LUMO带隙相符合;同时发现,含硅芴聚合物对爆炸物的检测具有选择性,而含噻咯的聚合物只可检测芳香TNT却不能检测RDX。
他们用时变密度泛函理论研究了化合物53~56在探测硝基类爆炸物时的荧光猝灭效应,发现硅芴和噻咯分子中硅原子形成的共轭桥键结构离域性增强,使得这些聚合物的光电性能得以提升,静态猝灭机理可能是硅芴类聚合物和爆炸物之间的电荷转移。该研究证明硅芴类聚合物可作为硝基类爆炸物的化学传感器材料[33]。
此外,Li等[34]基于一种π堆积硅芴聚合物聚乙烯硅芴PVMSiF 57,首次成功组装成了一种分子纳米保险丝器件,开关率高达4×106,证明了聚合物结构和类保险丝阻抗转换行为的基本关系。硅原子的引入可能控制π堆积聚合物的电荷传输及易破碎的荷电状态下π-π堆积易断裂,形成硅原子刺激下的类保险丝机理。
硅芴类化合物与芴类化合物具有相似的结构,已受到研究者们广泛关注,围绕硅芴类化合物的合成、结构修饰及性能研究,人们开展了许多工作。硅芴类化合物由于其刚性共轭结构而具有较好的热稳定性,而且刚性分子结构可以提高分子的量子效率。将硅元素的电子效应与桥联刚性梯形结构结合在一起,在此基础之上,通过设计和改性硅芴类化合物来改变它们在溶液中和固态下的光物理性能,发展具有良好的热性能硅芴类化合物化合物;探索反应条件温和、产率高、能普遍使用的合成方法,拓展硅芴类化合物的应用范围;在有机光电材料领域,利用硅芴的刚性共轭结构来发展分子导线,分子开关等分子器件;刚性结构与柔性基团相结合来发展刚柔并济的功能光电材料,等等,都是该领域未来的发展方向。
 2016,
Vol. 79
2016,
Vol. 79 Issue (6): 483-489
Issue (6): 483-489 2016,
Vol. 79
2016,
Vol. 79 Issue (6): 483-489
Issue (6): 483-489