1. 华中师范大学第一附属中学 湖北武汉 430223;;
2. 华中师范大学化学教育研究所 湖北武汉 430079;;
3. 湖北省荆州中学 湖北荆州 434020
Improvement on Experiment of Laboratory Preparation and Property Test of Ethylene
1. No. 1 Middle School Affiliated to Central China Normal University, Wuhan 430223, China;;
2. Chemical Education Institution, Central China Normal University, Wuhan 430079, China;;
3. Hubei Jingzhou High School, Jingzhou 434020, China
Abstract:
On the basis of references about improvement of laboratory preparation of ethylene, this study showed the improvement of laboratory preparation and property test of ethylene from the selection of chemical reagents, experiment operation and optimization of device.
Key Words:
preparation of ethylene
ethephon
property test
improvement of experiment
在《普通高中化学课程标准(实验)》化学II的主题3中的“活动与探究建议”[1]部分指出,通过实验探究乙烯的主要化学性质。同时,在人教版《化学2》[2]中第68页设置了2个关于乙烯性质探究的实验,因此,在教学中教师倾向于采用实验探究的方式向学生展示乙烯的化学性质。然而,在进行乙烯性质探究之前,制备较为纯净的乙烯气体是必不可少的步骤。
1 研究现状
在传统的课堂教学中,通常采用加热乙醇和浓硫酸的方法制备乙烯气体[3],这种制法存在包括反应原料、实验装置和实验过程等诸多不足之处。虽然,有许多研究者曾尝试从调节原料浓度[4]、控制反应温度[4]、加入催化剂[4-5]、改变脱水剂[6]、改进实验装置[7]等方面对传统实验进行改进,但是,仍旧存在许多难以避免的问题。于是,有研究者从改变反应原料入手,采用乙烯利和氢氧化钠制备乙烯[8](以下称为“参考实验”),取得了很好的效果,但是仍然存在一些有待改进的地方。在参考文献的基础上,从药品配置、装置优化和实验操作等方面对乙烯的实验室制法进行实验方案优化。
2 实验原理
在参考文献[8]中,反应原理部分所给出的反应方程式中的乙烯利结构式有误,结构式中少1个氢原子,正确的反应方程式如下:
根据产物鉴定及机理分析,初步推断乙烯利制备乙烯的反应机理如图 1所示:
氢氧根离子进攻乙烯利中的P原子,得到氧负离子中间体2。随后形成P=O 键,氯代烷基作为离去基团离去,得到中间体3 及磷酸4。中间体3中氯原子离去形成乙烯。而生成的磷酸与氢氧化钠发生中和反应得到磷酸钠。
3 实验优化
尽管参考实验具有非常理想的效果,但是通过实验验证发现仍旧存在一些不足:(1) 参考实验中采用的40%的乙烯利溶液,浓度过大,反应速率过快,不利于实验现象的观察;(2) 实验操作中没有注明所使用的仪器规格,对于直径较小的橡皮塞不容易打成双孔,因此,圆底烧瓶难以匹配到合适的双孔橡皮塞;而使用规格较大的圆底烧瓶易造成药品浪费,既不经济也不环保;(3) 实验装置中没有设计气体干燥、检测和收集装置,无法知道是否产生乙烯气体;(4) 实验装置中没有设计防倒吸装置,容易造成倒吸现象;(5) 实验装置中没有设计尾气吸收装置,容易造成大气污染。
根据以上分析,实验研究小组进行了一系列的实验改进,具体改进方案如表 1所示。
表 1
Table 1
表 1(Table 1)
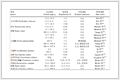
表 1 参考实验与改进实验对比细目表
Table 1 Comparison between reference experiment and improved experiment
| 类别 | 参考实验 | 改进实验 |
| 实验药品 | 质量分数为40%的乙烯利溶液、氢氧化钠固体 | 质量分数为25%的乙烯利溶液、氢氧化钠固体、酸性高锰酸钾溶液、碱石灰 |
| 实验仪器 | 圆底烧瓶(带双孔塞)、分液漏斗、铁架台、导管 | 三颈烧瓶(带单孔塞)、滴液漏斗、铁架台、导管、漏斗、气囊、烧杯、球型干燥管 |
| 实验装置 | 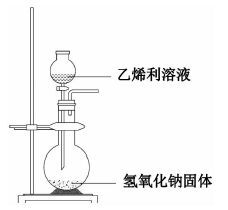
| 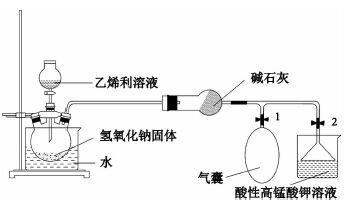 |
| 实验操作 | 实验时,先在圆底烧瓶或者锥形瓶中加入少量的氢氧化钠固体,塞上带分液漏斗的双孔塞,通过分液漏斗向试管中滴加40%左右的乙烯利溶液,即有乙烯产生。反应过程中,可以通过调节滴加乙烯利的快慢,控制产生乙烯的速度 | (1) 按照装置图所示连接好实验装置,检查装置气密性;(2) 将10 g乙烯利固体配制成质量分数为25%的溶液,备用;用天平称取5 g的氢氧化钠固体于三颈烧瓶中,塞紧瓶塞;
(3) 打开滴液漏斗的玻璃塞,加适量乙烯利溶液于滴液漏斗中;(4) 打开滴液漏斗的开关活塞,反应开始进行。挤压气囊,让气体充满导管通道,排尽装置中的空气,调节滴液漏斗活塞控制反应的快慢。控制活动夹1和2,调节乙烯气体的收集和检验 |
| 注:高纯度的乙烯利晶体较贵,在实验中可以选择市场上出售的乙烯利农药配制相关浓度的乙烯利溶液。 |
|
表 1 参考实验与改进实验对比细目表
Table 1 Comparison between reference experiment and improved experiment
|
与参照实验相比,改进后的实验有如下优点:(1) 反应物质量分数改为25%时,反应速率更为适宜;(2) 反应装置改为三颈烧瓶,则不需要多孔橡皮塞,使得反应装置更易组装;(3) 由于反应放出大量的热,将三颈烧瓶放在水浴里,可以降低反应装置的温度,防止烫伤;(4) 反应装置、收集装置和检验装置齐全,可及时观察产物的生成、收集和检验情况,实验现象非常明显;(5) 在反应装置和收集装置之间加入1个干燥装置,使得收集到的乙烯更为纯净;(6) 将传统的倒立漏斗式防倒吸装置中的溶液改为能够检测产物性质并吸收尾气的酸性高锰酸钾溶液,使得该部分装置既是性质检验装置,又是尾气吸收装置,同时还能防止倒吸,既保证整个实验装置简易化又保证了其安全性。漏斗口部分浸入在溶液中,保证了气体的充分吸收,避免气体泄漏污染大气。
4 实验现象
打开滴液漏斗后,反应装置中的乙烯利溶液与氢氧化钠固体剧烈反应,有大量气泡产生,同时放出大量的热;打开活动夹1后,收集装置的气囊逐渐膨胀变大;打开活动夹2后,检验装置中的酸性高锰酸钾溶液逐渐褪色。经过多次重复实验,发现改进后的实验方案具有很好的重现性和很高的产率。
5 实验启示
首先,在进行教学实验设计时,要有以生为本的思想,所有实验的设计要在实际验证的情况下保证其良好的安全性、简洁性、重现性和可视化等特点。另外,在科研过程中,探索是永无止境的。研究者要有不断开拓创新精神,不能屈服于传统,认为传统的东西一定是最好的。最重要的是,研究者一定要保证研究过程的科学性和研究结果的准确性,否则,其对科学事业发展的负面影响将是无法估计的。
 2016, Vol. 37
2016, Vol. 37  Issue(13): 50-52
Issue(13): 50-52  2016, Vol. 37
2016, Vol. 37  Issue(13): 50-52
Issue(13): 50-52